目前,乳腺癌已超过肺癌成为全球范围内发病率第一的恶性肿瘤。近年来,随着临床医学的不断发展,靶向治疗、内分泌治疗在晚期乳腺癌领域得到了长足发展,化疗作为晚期乳腺癌治疗基石亦有所突破。本期特别分享一例雌激素受体(ER)阳性、人表皮生长因子受体2(HER2)阳性晚期乳腺癌的病例。抗HER2治疗已成为HER2阳性晚期乳腺癌一线标准治疗,临床首先给予抗HER2靶向治疗联合化疗方案进行治疗,为患者带来了部分缓解(PR)的良好疗效,但治疗6周期后,患者因化疗不耐受而更换治疗方案。后续进行的7周期双靶联合内分泌治疗效果不佳,加用抗HER2治疗,病情仍未得到控制。考虑到患者既往治疗的反应情况及目前存在的问题,换用口服长春瑞滨联合靶向治疗方案,在保障疗效的同时,降低毒性,为患者带来了稳定的疗效。可见,在抗HER2治疗中寻找更佳配伍化疗药物的重要性。
浙江省肿瘤医院乳腺肿瘤内科
浙江大学临床医学本硕七年制专业毕业
主要从事乳腺癌内科的临床工作,具有丰富的国内和国际多中心新药临床试验经验,擅长乳腺癌术后辅助规范化治疗和晚期乳腺癌的内分泌和靶向治疗以及化疗。发表国内核心期刊及SCI论文数篇,主持厅级课题2项
2016年10月-2017年03月 在国家食品药品监督管理总局药品审评中心(CDE) 挂职担任审评员工作
中国健康促进基金会乳腺疾病专业委员会委员
浙江省康复医学会肿瘤康复专业委员会青年委员
浙江省细胞生物学学会理事
病例介绍
基本信息:女,53岁。
主诉:右乳腺癌伴双肺转移2年余。
个人史、既往史、家族史:无特殊。
月经史:已绝经。
现病史:患者于2021年10月因“发现右乳肿块1月余”就诊于某三甲医院,2021年10月1日行超声,提示右乳外上象限低回声区伴多发细小钙化 BI-RADS:5类,右侧腋下肿大淋巴结转移考虑。2021年10月11日行胸部CT,提示两肺多发结节灶,考虑转移瘤。
2021年10月27日右乳及右腋下淋巴结穿刺病理提示(右乳)结合免疫组化,导管内癌,小灶浸润;IHC:(右乳肿物) C-erbB-2(3+)(浸润性癌成分), ER-, PR-;(右腋下淋巴结):ER-, PR-。FISH检测:右乳肿块HER-2基因扩增呈阳性;右腋下淋巴结HER-2基因扩增呈阳性。
2021年10月27日 CT引导下左肺结节穿刺活检,病理示浸润性癌,结合临床病史及免疫组化考虑乳腺癌转移;免疫组化结果: ER (50%,1-2+), PR( 8%,1-2+),Ki-67(35%), c-erbB-2(BC) (3+)。
临床诊断:右乳癌右腋下淋巴结肺转移
治疗经过:
一、 一线治疗
2021年10月29日至2022年2月11日,予THP方案(紫杉类化疗联合曲妥珠单抗、帕妥珠单抗)治疗6周期。治疗后复查右乳肿块及右腋窝淋巴结、两肺结节缩小,疗效评价:PR。由于化疗耐受性下降,2022年3月7日至2022年6月21日予曲帕双靶联合OFS+AI(依西美坦)内分泌治疗6周期。
二、 二线治疗
2022年6月2日,外院查乳房MR示:右乳癌化疗后,右乳上象限团块影,右侧乳腺乳晕区稍增厚,右乳上象限部分结节较前2022年3月4日新发,BI-RADS 6。
2022年6月8日起加用吡咯替尼抗肿瘤治疗。
2022年7月13日,1.本院乳房复查MR提示:右乳上方环形强化及局灶性非肿块样异常强化,请对照老片,BI-RADS:6;2.右侧腋下增大淋巴结,考虑转移可能大。
2022年7月28日,更换治疗方案:伊尼妥单抗静滴(2mg/kg/w,首次负荷量)+长春瑞滨软胶囊 60mg 口服 d1、8,q3w+吡咯替尼 320mg qd。
2022年7月28日至2023年12月4日共用药23周期。
用药后于2022年9月8日起规律复查乳房MR。
2023年11月3日复查乳房MR示:右乳上方及外上象限段样分布非肿块样异常强化较前相仿,BI-RADS:6;右侧腋下增大淋巴结,较前大致相仿,左乳未见明显异常,BI-RADS:1。
2023年11月3日复查肺部CT示两肺多发类结节灶及条索状影,较前大致相仿。
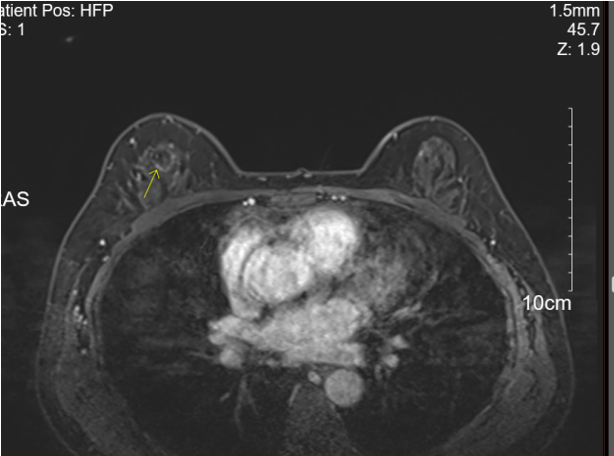
图1 乳房MR 2022-7-13
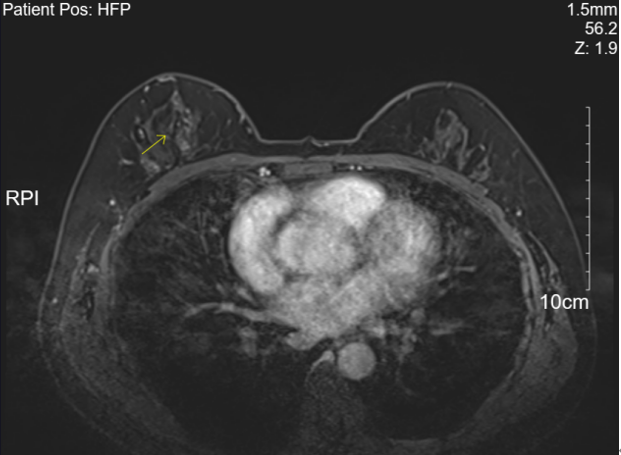
图2 乳房MR 2023-11-03
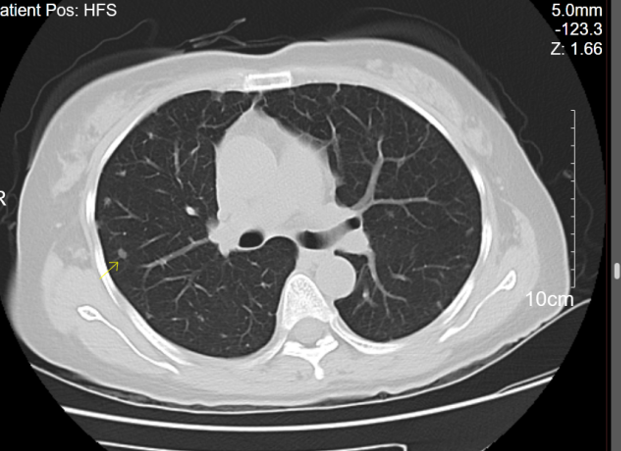
图3 胸部CT2022-7-13
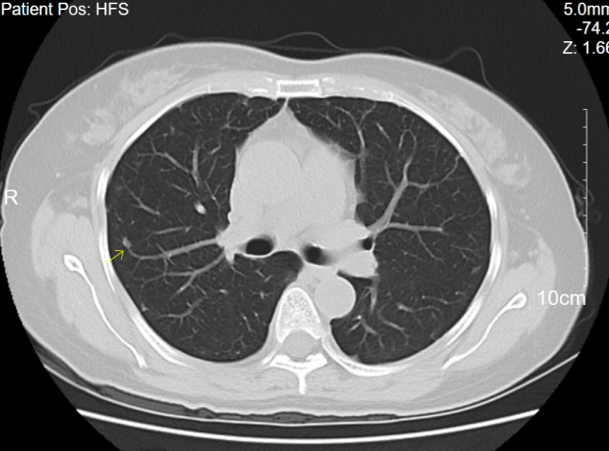
图4 胸部CT 2023-11-03
疗效稳定。
点评专家简介
浙江省肿瘤医院乳腺内科副主任兼病区主任
国家抗肿瘤药物临床应用检测专家委员会乳腺癌组专家
中国抗癌协会整合肿瘤心脏病学分会常务委员
中国女医师协会乳腺专业委员会常务委员
中国健康促进基金会乳腺疾病专家委员会常务委员
中国临床肿瘤学会乳腺癌专家委员会委员/CSCO-BC指南编委
中国医师协会肿瘤医师分会第二届委员会乳腺癌学组委员
浙江省数理医学学会乳腺肿瘤诊疗专业委员会主任委员
浙江省数理医学学会乳腺临床试验专业委员会候任主任委员
浙江省免疫学会肿瘤免疫与生物治疗专业委员会副主任委员
专家点评
HER2阳性乳腺癌约占整体乳腺癌发病的15%~20%[1],是最具侵袭性的乳腺癌亚型之一。近年来,随着抗HER2药物的不断发展,HER2阳性晚期乳腺癌患者的预后得到显著改善。CLEOPATRA研究结果显示[2],THP方案治疗可以为HER2阳性晚期乳腺癌患者带来18.7个月的中位无进展生存期(PFS)和57.1个月的中位总生存期(OS),成为既往曲妥珠单抗和紫杉类治疗未失败的HER2阳性乳腺癌患者的首选治疗方案。本例患者入院即给予THP方案进行治疗,病情得到了良好控制。但治疗6周期后,患者因不能耐受化疗而更换治疗方案。虽然双靶联合内分泌治疗的耐受性好于双靶联合化疗,但本例患者换用靶向联合内分泌治疗方案后,病情并未得到控制,再次出现进展。那么,如何在保证靶向治疗联合化疗的疗效的同时,降低其毒副反应?
长春瑞滨作为经典的抗微管类乳腺癌化疗药物,在临床前研究中已表现出与曲妥珠单抗在多种HER2阳性乳腺癌细胞系中的协同抗肿瘤作用[3]。HERNATA研究显示[4],曲妥珠单抗联合多西他赛或长春瑞滨治疗疗效相似(中位OS分别为35.7个月 vs 38.8个月,HR = 1.01;95% CI,0.71-1.42;P=0.98),但长春瑞滨组具有更少的3~4级骨髓抑制、感染、神经病、指甲改变和水肿等治疗相关不良事件(TRAE),且至治疗失败时间(TTF)显著延长(7.7个月 vs 5.6个月,HR = 0.50, 95% Cl,0.38-0.64,P<0.0001)。因此,对于HER2阳性晚期乳腺癌患者,长春瑞滨联合靶向治疗能够更好地平衡临床获益与风险,尤其是对于紫杉类不可耐受的患者。
除了曲妥珠单抗,长春瑞滨联合其他靶向治疗亦展现出了良好的疗效和安全性。在接受过曲妥珠单抗或曲妥珠单抗+帕妥珠单抗方案治疗的HER2阳性晚期二线乳腺癌患者中,长春瑞滨联合吡咯替尼治疗的客观缓解率(ORR)达43.6%,疾病控制率(DCR)为84.6%[5]。HOPES研究结果显示,长春瑞滨联合伊尼妥单抗治疗能够显著延长患者的中位PFS达39.1周,显著提高ORR和DCR,且安全性良好,成为紫杉类治疗后的HER2阳性晚期乳腺癌的优选方案[6]。VELVET研究中,长春瑞滨联合双靶抗HER2治疗的ORR达74.2%,中位PFS为14.3个月,且患者耐受性良好[7],再证了长春瑞滨联合靶向治疗的疗效及安全性。
既往研究显示,77%的晚期乳腺癌、肺癌患者认为口服药物更具优势,会更倾向于选择口服化疗药物[8]。口服和静脉注射长春瑞滨的药代动力学行为和疗效相似,但口服给药可以减少对患者生活的影响,减轻患者的心理负担。在疗效相当的情况下,89%的曾接受过口服化疗的患者会继续选择口服化疗,而接受过静脉化疗的患者中有67%会转而选择口服化疗[9],可见相对而言,口服用药患者的治疗依从性更佳,为疾病的长期控制奠定基础。长春瑞滨联合吡咯替尼用于HER2阳性乳腺癌晚期二线治疗的研究亚组分析显示[5],相比静脉注射,口服长春瑞滨联合吡咯替尼治疗的患者PFS绝对值较高,虽然无统计学差异,但亦提示口服用药可能为患者带来更久获益。
考虑到本例患者采用THP方案治疗耐受性差,而靶向联合内分泌治疗未能取得疗效的情况,临床换用长春瑞滨联合靶向治疗方案进行治疗。至2023年12月4日,共治疗23周期,患者病情控制良好,疗效稳定,且耐受性良好。可见,更为高效、低毒的长春瑞滨联合抗HER2治疗可以为患者带来更佳疗效、更长疾病控制、更高生存质量,或为临床治疗的更优选择。
[1] Gion M, Trapani D, Cortés A, et al. Systemic Therapy for HER2-Positive Metastatic Breast Cancer: Moving Into a New Era. Am Soc Clin Oncol Educ Book. 2022 Apr;42:1-11.
[2] Sandra M Swain, David Miles, Sung-Bae Kim, et al. Pertuzumab, trastuzumab, and docetaxel for HER2-positive metastatic breast cancer (CLEOPATRA): end-of-study results from a double-blind, randomised, placebo-controlled, phase 3 study. Lancet Oncol. 2020 Apr;21(4):519-530.
[3] Pegram MD, et al. Rational combinations of trastuzumab with chemotherapeutic drugs used in the treatment of breast cancer. J Natl Cancer Inst. 2004;96(10):739-749.
[4] Andersson M, et al. Phase III randomized study comparing docetaxel plus trastuzumab with vinorelbine plus trastuzumab as first-line therapy of metastatic or locally advanced human epidermal growth factor receptor 2-positive breast cancer: the HERNATA study. J Clin Oncol. 2011;29(3):264–271.
[5] Jiang K, Hong R, Xia W, et al. Pyrotinib Combined with Vinorelbine in Patients with Previously Treated HER2-Positive Metastatic Breast Cancer: A Multicenter, Single-arm, Prospective Study [published online ahead of print, 2023 Oct 12]. Cancer Res Treat. 2023;10.4143/crt.2023.786. doi:10.4143/crt.2023.786
[6] 边莉,徐兵河,邸立军,等.重组抗HER2人源化单克隆抗体联合长春瑞滨治疗HER2阳性转移性乳腺癌随机对照Ⅲ期临床研究[J].[2023-12-04].
[7]Perez E A ,López-Vega, José Manuel, Petit T ,et al.Safety and efficacy of vinorelbine in combination with pertuzumab and trastuzumab for first-line treatment of patients with HER2-positive locally advanced or metastatic breast cancer: VELVET Cohort 1 final results[J].Breast Cancer Research : BCR, 2016, 18.
[8] Eva María Ciruelos, et al. Eur J Cancer Care. 2019;00:e13164.
[9] Schott S, Schneeweiss A, Reinhardt J, Bruckner T, Domschke C, Sohn C, et al. Acceptancemof oral chemotherapy in breast cancer patients - a survey study. BMC Cancer. 2011;11:129.
排版编辑:肿瘤资讯-Tracy











 苏公网安备32059002004080号
苏公网安备32059002004080号


