
近年来乳腺癌领域进展迅速,但更多是针对晚期治疗的新药研究,而早期治疗进展相对较少。很高兴在ASCO能看到早期HR阳性乳腺癌的进展,在这里和大家分享可能真正影响临床决策的一些研究。既往内分泌治疗虽然一直存在“加减法”的讨论,但因为内分泌治疗的不良反应特别少,所以我们更多关注HR+领域加法的进展,一个是传统内分泌治疗的加法,一个是靶向内分泌治疗的加法。
专家简介
博士,副主任医师,硕士研究生导师
四川省肿瘤医院,乳腺外科副主任(主持工作)
毕业于中南大学湘雅医学院
加拿大麦吉尔大学 访问学者
中国抗癌协会乳腺癌专委会 青年专家
中国医师协会乳腺外科医师专委会 青年委员
中华医学会肿瘤学分会乳腺肿瘤学组 青年委员
成都市抗癌协会临床科研与转化医学专委会 主任委员
JCO中文版乳腺肿瘤专刊 青年编委
传统内分泌治疗的加法
1
传统内分泌治疗的加法是卵巢功能抑制对乳腺癌复发和生存的影响,这是EBCTCG的荟萃分析。EBCTCG的荟萃分析向来是属于重磅的权威研究,研究纳入了25项随机临床试验,一共入组了接近15000例绝经前的患者,这些患者是ER+或者ER未知状态的早期乳腺癌女性(对PR无要求),通过EBCTCG方法去分析复发和特定原因的死亡。A组分为两个小组,A1组不化疗,A2组是随机前进行化疗,也就是化疗后确定没有绝经的患者。B组是随机化疗,可能会在化疗中经历卵巢的损伤之后造成了绝经。
试验结果显示,在A组和B组的人群中都可以看到卵巢切除或者抑制可以降低乳腺癌的复发风险。相对来说,未化疗或者化疗后没有绝经的A组人群获益更加明显,15年复发率获得了12.1%的绝对改善,而B组人群(化疗前未绝经但化疗后不确定)有获益,但比较少,15年复发率获得1.3%的绝对改善。这体现了我们在临床研究中经常面临的一个问题,统计学意义和临床意义如何理解。像B组人群,从统计学上讲,确实达到了统计学差异,P=0.02,可是实际上每年的复发风险降低不足0.1%,所以对于这类患者,如何去使用卵巢切除/抑制,就需要更慎重的权衡。不过两组间的差异比较明显,但没有给出交互检验的P值,我们期待原文正式发布后给我更多的细节。

大家比较关心一个问题,是不是卵巢抑制对年轻的患者比较有用、接近围绝经期的患者没用?分析按年龄分的复发率即回答了这样一个问题。对于A组人群,不管是小于35岁还是50岁左右的围绝经人群,都可以看到使用卵巢切除/抑制的获益。我们也可以看到,在未化疗和化疗后未绝经的这部分人群中,无论是小于45岁还是45-50岁的人群都可以获益,不同年龄组的获益水平略有些差别,年纪大一点的患者获益少一点。
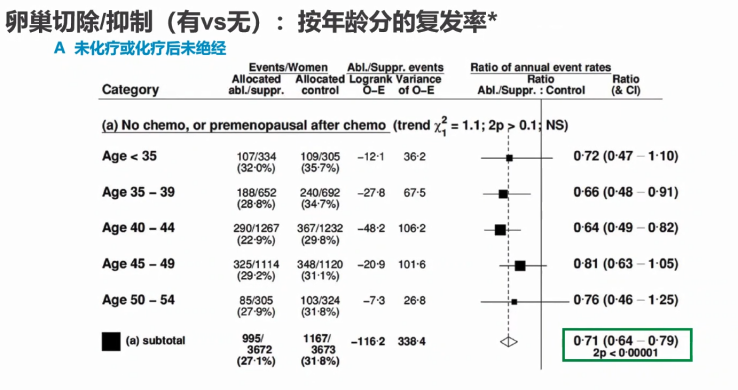
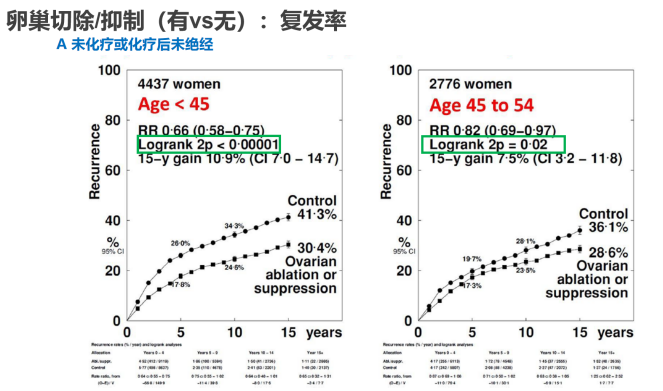
有趣的是,在化疗前未绝经但化疗后不确定月经状态的人群中,年龄的影响就会更加明显。整体来讲,获益还是有的(P=0.03),但看亚组分析会发现,40岁以下人群可以确定获益,但45岁以上这部分人群,从森林图来看获益不太确定。期待原文发表后交互检验的结果揭示这三个年龄组之间是否有差别。
 死亡率也是这篇研究的主要终点之一。在确定未绝经的A组人群中,乳腺癌死亡率和全因死亡率是明显降低的,但无复发死亡没有差别,也就是说,治疗并没有为患者造成其他额外的负担,整体死亡率的降低来自于乳腺癌。而这次ASCO报告并没有给出另一个亚组的死亡率。B组复发风险HR值仅为0.91,15年只降低了1.3%,这样的值是否能转化为死亡率的降低,我对原文的发表拭目以待。
死亡率也是这篇研究的主要终点之一。在确定未绝经的A组人群中,乳腺癌死亡率和全因死亡率是明显降低的,但无复发死亡没有差别,也就是说,治疗并没有为患者造成其他额外的负担,整体死亡率的降低来自于乳腺癌。而这次ASCO报告并没有给出另一个亚组的死亡率。B组复发风险HR值仅为0.91,15年只降低了1.3%,这样的值是否能转化为死亡率的降低,我对原文的发表拭目以待。
对于A组来说,淋巴结阳/阴都可以降低复发风险。似乎加入他莫昔芬后,OFS的获益水平降低,这比较好理解,内分泌治疗的获益就那么多,再加一样药会减少组间差异,但有无他莫昔芬都可以获益。
报告还对比了卵巢切除和卵巢抑制两种方法。卵巢切除的复发率获益更好,15年获益为15.3%,卵巢抑制的15年获益6.4%。两组HR相差大(0.65 vs 0.76),但同样没有给出交互检验的P值。对年轻患者来说,现在似乎都已经习惯了卵巢抑制。但如果这篇文章发表会不会给出卵巢切除更佳的提示。
整体来讲,卵巢切除和抑制的方式对ER+绝经前乳腺癌患者有很好的益处,这种益处更集中表现在内分泌治疗前确定没有绝经的这部分患者。而他莫昔芬的加入可能会让获益变得差别不那么大,但还可以看到获益趋势。这篇研究也留下了两个疑问,一个是如果患者已经到了50岁且经过化疗,是不是就不必测激素水平,不用OFS了?另一个是卵巢切除和卵巢抑制是两种不同的方法,是否疗效不同、适用于不同的患者?回顾性研究存在一定的偏倚,但其结果对未来的治疗选择有一定的指引作用。
2
第二个传统内分泌的强化治疗的研究来自于SOFT研究。SOFT研究非常经典,十多年来结果被反复应用。这次报告评价了绝经前早期HR+乳腺癌女性PAM内在亚型和ROR评分能否确定OFS获益。
ROR是一个结合50个基因检测、肿瘤大小和淋巴结状态进行的风险分级,如果淋巴结阴性,低风险定义是0-40,如果淋巴结阳性的话,0-15是低风险,16开始就算中风险了。相对来说淋巴结阳性中高风险的比例会更高。这个研究的主要目的是评估绝经前HR+/HER2-乳腺癌女性PAM50 ROR评分和远处复发之间的预后关系。次要目标是评估非常年轻的和年轻的女性ROR评分和内在亚型是否有差别。还有一个是非常有临床意义的,评估ROR高分是否预示着EXE+OFS对比单药他莫昔芬有更大获益。如果ROR确实可以预测OFS+EXE效果更好,可以指导用药,就会对临床更有意义,所以我更关注这个次要指标。研究终点通过DDFI和BCFI进行分析。
研究的队列中非常年轻的女性和年轻的女性占比不低,小于40岁的女性有接近30%,足够进行分析。此外这个研究入组时,ASCO/CAP指南要求的激素受体阳性的界值是ER或者PR表达需要大于10%。
研究结果表明,ROR HIGH的人群预后比较差,明显低于低风险人群。研究的主要终点达到了,ROR确实可以预测患者的预后。在年轻和非常年轻人群的亚组中,ROR HIGH人群的复发风险比较高,但无论是哪组,中风险和低风险人群的预后区分度都不好。在不同的淋巴结状态和化疗状态亚组中,淋巴结阴性患者的ROR和更高的远处转移风险相关,淋巴结阳性的患者大部分都为高风险评分,所以低风险10年DRFI无法确定。整体上讲,无论患者是否接受化疗,高ROR与高远处复发风险相关。

第二个终点是年轻患者和非常年轻的患者预后有没有差别。在内在亚型上,非常年轻的以及淋巴结阳性的患者有更明显的侵袭性疾病特征,也就是说淋巴结阳性的患者ROR的评分高风险的比例较多,内在亚型Luminal B占比更高。整体来讲,如果患者非常年轻,本身就代表她内在基因亚型可能比较不良。小于40岁的人群预后更差,虽然年龄和很多其他预后不良因素相关,但无论是Luminal A还是Luminal B型,预后都劣于40岁以上人群,年龄本身就是一个明确的预后不良因素。

但我们比较关心的预测指标这一终点没有达到显著性差异,ROR评分对绝经前女性患者的OFS获益没有预测作用。

总结:ROR评分确实有提示预后的作用,但并没有很好的预测作用。
3
既然讲了内分泌治疗,不得不提到对患者生活质量的影响。辅助内分泌治疗期间加入卵巢功能抑制,我们希望患者能够持续用药,让患者能够得到最好的获益。但现实是,SOFT研究中一半患者伴有抑郁的不良反应,很多患者没有办法持续治疗,所以我们应该在治疗的同时关注患者的生活质量,在不影响生活质量影响的情况下药物才可以持续使用下去。这个研究的目的是探索绝经前女性接受辅助内分泌联合或不联合GnRHa的生活质量以及内分泌症状的差异。这是一个横断面研究,采用内分泌症状功能评估量表。患者用药包括他莫昔芬、GnRHa+AI和接近1/4的GnRHa+他莫昔芬的人群,这也几乎代表了所有早期HR+患者采用的内分泌治疗的方案。结果发现与接受他莫昔芬,或者GnRHa+他莫昔芬治疗的患者相比,GnRHa+AI导致的内分泌症状负担更重,以及会有更低的生活质量。在他莫昔芬的基础上,加入GnRHa并没有显著影响患者生活质量,有点温水煮青蛙的感觉。但是一旦从他莫昔芬+GnRHa换成了AI+GnRHa,患者的身体健康评分就降低,内分泌量表评分也会降低,表明绝经前妇女接受AI+GnRHa治疗后内分泌症状增加了。通过生活质量评估,我们发现AI+GnRHa方案会让患者更加抵触,可能会导致更多的停药,如何进行更好的干预是一个亟待解决的问题。

靶向内分泌治疗的加法
1
靶向内分泌是最近的研究亮点,的确为高危的患者带来了很好的获益。NATALEE研究结果的汇报,是今年ASCO在乳腺癌领域最重磅,或者说万众期待的结果,即瑞波西利联合内分泌治疗方案用于HR+/HER2-早期乳腺癌辅助强化治疗。这个研究说了很多年,放了两次鸽子,这次终于公布了,报告的是预设的第二次中期分析的主要终点,而第一次没有报告。
首先重点看一下它的入组人群,NATALEE研究共入组5101例患者,实际上最初入组计划4000例,后续增加到了5000例。入组人群中IIB和III期的人群并不特别有争议,在MonarchE研究中也有相似的人群,大家比较关注的是IIA期患者也入组了,比如N0+G2+高危因素(Ki67≥20%、RS高风险)或者N0+G3。最终在整体患者中N0患者占比28%,这也是大家比较关注疗效的一个群体。试验组用药是瑞波西利联合AI类药物,剂量选择了400mg,用药时长是三年,主要研究终点是IDFS,以及其他疗效和安全性的评估。NATALEE还有比较特殊的一点是允许在辅助治疗12月内入组,而Monarch E研究是3个月,也即NATALEE研究实际上入组的人群会比较分散,可能会筛掉一些早期复发的人群。不同既往辅助治疗时长(3个月内、3个月后入组)对结局有没有影响,我也期待将来NATALEE出一个结果。

中位随访34个月后,主要研究终点 3年iDFS获益是3.3%,HR 0.748,是一个不错的水平,与MonarchE研究3年iDFS获益HR差距不是特别大。我们比较关注的低危人群怎么样呢?森林图上2期和3期患者获益没有差别,而淋巴结阴性的患者更偏左一点,至少从统计学来讲不会有差异,告诉我们淋巴结阴性的人群似乎也可以从CDK4/6抑制剂中获益。

DDFS同样获益,OS方面没有统计学差别,但OS数据受到后线治疗的影响,目前数据也尚不成熟。在安全性方面,晚期患者使用瑞波西利可能会出现QT间期延长的现象,但是在早期还可接受。整个研究中仅有19%的人因为AE停用了瑞波西利,MonarchE研究中共有17%的人停用,两者停药率差不多。相对晚期600mg来讲,400mg安全性良好,但也得到了一个阳性的结果。NATALEE和MonarchE都是阳性的结果。MonarchE主要研究终点是两年,终点后的随访分析3年iDFS获益HR值是0.664,NATALEE是0.748。这样一个非头对头的比较并没有发现特别明显的差异。实际上我们发现这两个研究入组人群相差还是蛮大的,特别是在相对低危的人群中。根据入组标准,I期人群中部分在MonarchE可以入组(T1N1mi+G3/Ki67≥20%),但在临床中我们很少遇到这样的患者,这是它唯一比NATALEE多的人群,其他方面NATALEE的人群要更广。

这段时间我也参加了一些会议,讨论CDK4/6抑制剂目前有很多研究,结果有阴性有阳性,而CDK4/6抑制剂是否真的有用、到底用哪个药、要不要筛高危人群?我觉得这个药物是否有效更多来自于药物本身的特征,而不在于是高危还是低危的人群。我们看结果阳性的研究中,MonarchE所有人群都是高危人群,而亚组分析没有表现出任何不同的获益趋势,并没有因为淋巴结4个及以上或者淋巴结1-3个产生不同的获益水平。即在MonarchE这样结果阳性的研究中,高低危并不影响获益。而结果阴性的PALLAS研究中,有58%人群是临床高危人群,在高危人群同样没有看到任何获益趋势。而NATALEE研究人群混合了高危和相对低危的人群,该有效的还是有效。所以我觉得对于符合临床实验入组条件的患者都可以用药。如果患者同时满足两个研究的入组条件,则更多依据不良反应、药物经济学和可及性进行选择。
2
今年MonarchE研究也进行了汇报,报的是按照年龄分层的疗效和安全性,研究人群主要是分为两组,<65岁和≥65岁的人群。基线上可以看到≥65岁人群更少使用新辅助化疗,这符合我们临床的认知。≥65岁人群ECOG评分1级稍多,有更多的合并症,以及初始内分泌更多使用芳香化酶抑制剂,因为65岁以上绝经后的患者比较多。
虽然老年患者(≥65岁)绝对获益稍微低一点,但都未通过交互检验,也就是说老年患者获益与整体人群是一致的,老年患者并不是使用阿贝西利的禁忌。因为AE调整剂量或者减量并没有影响老年患者的获益,所以我们要规范治疗,而不是因为年龄和AE让患者直接失去治疗的机会。

总结
除了HR低表达的人群或者通过一系列模型筛查出的不适合延长内分泌的人群,整体来讲内分泌治疗还是在往强化的方向走。这种强化内分泌治疗获益相对于持续20年的复发风险来讲还是有意义的。
传统内分泌的强化有两个方向,一个是OFS,一个是治疗时间的延长。OFS研究了很多年,确实是一个非常好的治疗方式,只是我们目前还没有发现特别好的模型或者精准的个体化治疗方案预测患者能否从OFS中获益,特别是今年EBCTCG荟萃分析中提出的化疗前未绝经但化疗后不确定的这部分人群,以及卵巢切除或抑制是不是有差别,是不是要改变现在似乎已经很先进的非手术的观念。
到了靶向内分泌治疗的时代,既往已经有了MonarchE研究,但MonarchE受众人群相对比较窄,NATALEE又填补了大量的中危患者,并报道了阳性结果,而且森林图没有显示高危和中危的获益差异,我相信如果可及的话,很乐意给患者尝试,当然也要关注它的不良反应。
Richard Gray, et al. 2023 ASCO Abstract 503.
Lauren Claire Brown et al. ASCO 2023. Abstract 504.
Natalija Dedic Plavetic, et al. 2023 ASCO Poster 560.
Dennis J, et al. 2023 ASCO Abstract LBA500.
Hamilton, et al. 2023 ASCO Abstract 501.
排版编辑:肿瘤资讯-ZZ












 苏公网安备32059002004080号
苏公网安备32059002004080号


