共识 1:对三代 EGFR-TKI进展,脑部增强MRI来排除脑转移;血清学肿瘤标志物如CEA、SCCA和CYFRA21-1 等可用于辅助评估疾病进展,NSE和 ProGRP可用于辅助评估NSCLC是否发生SCLC转化;ctDNA 或CTC动态监测可辅助提前预判NSCLC进展可能 (共识级别:1A)
共识 2:原发性耐药主要与治疗初始已存在对TKI治疗不敏感的其他EGFR突变或相关信号通路 激活等有关,二代测序能够鉴别这些分子异常,从而有助于判断肿瘤潜在耐药分子机制(共识级别:1A,见表 2、3)
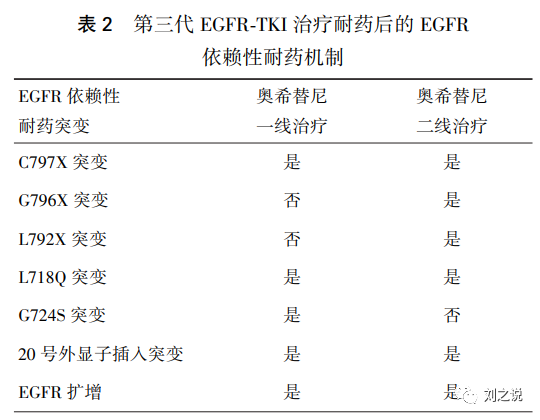
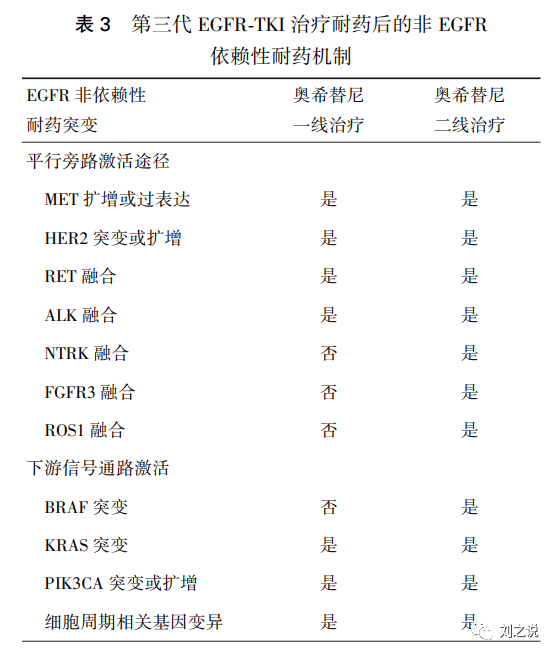
共识 3:获得性耐药在第三代EGFR-TKI 一线和二线治疗后均可发生,两者耐药谱有所差异,主要包括EGFR依赖性、非EGFR依赖性、组织学及表型转化及未知耐药机制。其中,C797X 突变是最主要的EGFR依赖性耐药机制,而MET扩增是最主要的非EGFR依赖性耐药机制(共识级别:1A)
共识 4:对于第三代EGFR-TKI治疗耐药后广泛进展的患者,强烈推荐使用一种或多种方法联合进行广谱分子检测,以明确耐药机制;首选组织样本进行检测,组织样本不可及时可采用外周血 ctDNA或其他体液样本作为补充。除了分子检测之外,建议同步行组织活检以排除SCLC 等组织学转化(共识级别:1A)
共识 5:对于经第三代EGFR-TKI 治疗耐药后出现寡进展的患者,推荐在先前EGFR-TKI 基础上联合局部治疗,如手术或立体定向放疗(SBRT) (共识级别:1A)
共识 6:对于经第三代EGFR-TKI 治疗耐药后出现颅内进展的患者,推荐在原先EGFR-TKI 基础上,基于肿瘤的位置、大小和患者身体情况等综合评估后联合手术和/或放疗治疗;对于进展累及脑膜的患者,可考虑第三代 EGFR-TKI加倍剂量治疗 (共识
级别:1A)
共识 7:对于经第三代EGFR-TKI治疗耐药后出现广泛进展的患者,针对不同耐药机制,推荐给予相应的联合治疗如双靶联合治疗、靶向联合化疗/ 抗血管治疗或免疫联合化疗/抗血管等治疗手段,同时鼓励符合条件的患者积极参加新一代EGFR-TKI及新型疗法如ADC药物等正在进行的临床试验 (共识 级别:1A)
联合或换用第一代EGFR-TKI 或 EGFR 单克隆抗体
对于经三代EGFR-TKI二线治疗耐药后出现T790M/C797S反式构象突变的患者,尝试三代EGFR-TKI联合第一代EGFR-TKI;
出现 T790M/C797S顺式构象突变时,尝试布格替尼联合西妥昔单抗治疗;
对于经三代EGFR-TKI 一线治疗出现C797S单独突变,可直接换用一代/ 二代EGFR-TKI进行治疗;
病例结果显示,1例经奥希替尼治疗后进展出现T790M/C797S 反式突变的患者,接受奥希替尼联合一代EGFR-TKI厄洛替尼治疗1周后获得PR,但 3个月后该患者因出现T790M/C797S 顺式突变而再次进展。一项回顾性病例分析中,布格替尼联合EGFR单抗西妥昔单抗治疗奥希替尼耐药后出现 T790M/C797S 顺式突变患者的客观缓解率可达60%,提示布格替尼联合西妥昔单抗可作为经三代EGFR-TKI治疗耐药后出现T790M/C797S顺式突变患者的潜在治疗选择
双靶联合
对于既往经三代EGFR-TKI 治疗耐药后出现可靶向分子耐药机制的患者,首选推荐在先前EGFR-TKI 基础上联合耐药分子对应靶向药物进行双靶联合治疗。目前对于该研究较多的是针对奥希替尼耐药后出现 MET异常患者的治疗
对于经奥希替尼治疗后出现 MET基因扩增和/蛋白过表达的患者,MET 抑制剂联合奥希替尼可作为有效的治疗策略。Ⅱ期SAVANNAH报道显示,奥 希替尼联合MET抑制剂赛沃替尼用于治疗既往接受过奥希替尼耐药后经FISH或IHC检测存在MET基因扩增和/或蛋白过表达的晚期NSCLC 患者, ORR可达 32%,尤其在MET基因高扩增和/或蛋白高水平表达( IHC90+和/或FISH 10+)的患者中, ORR可达 49%,中位DoR为9.3个月,中位 PFS达7.1个月,显示出良好的临床疗效及安全性。另一项Ⅱ期ORCHARD 报道显示,奥希替尼联合赛沃替尼用于既往经奥希替尼一线治疗后经NGS检测存在MET基因扩增的患者,17例可评估疗效患者的ORR 达 41%。Ⅱ期INSIGHT2 研究初步结果显示,奥希替尼一线治疗耐药后经组织FISH确认存在MET扩增的患者接受奥希替尼联合另一MET抑制剂特泊替尼可获得约50%的ORR。一项Ⅰ/Ib 期研究(NCT02099058),探索了c-MET 抗体偶联药物Teliso-V (ABBV⁃399) 联合奥希替尼用于治疗奥希替尼治疗失败后 c-MET 过表达的非鳞NSCLC 的安全性和初步疗效,19例可评估疗效患者的ORR为58%。针对三代EGFR-TKI 治疗耐药后出现其他如Her-2突变/扩增、KRAS G12C 突变、ALK融合等可靶向分子机制的患者,经临床综合评估,也可尝试三代EGFR-TKI 联合耐药分子改变对应的靶向药物如DS-8201、AMG-510、洛拉替尼等双靶联合治疗策略
联合化疗
一项回顾性分析纳入44例既往经EGFR-TKI 治疗后进展的患者,其中98%患者既往接受过奥希替尼单药治疗,接受奥希替尼联合化疗(≥3线治疗)治疗,中位OS达到10.4个月。另一项单中心回顾性分析,评估在奥希替尼治疗后进展的EGFRm+ NSCLC 中,继续奥希替尼联合化疗治疗的疗效,结果显示,继续接受奥希替尼联合化疗的患者的mPFS( 7个月vs. 4个月,P=0.032) 和mOS(52.0个月 vs. 40.5个月,P=0.234)高于不再接受奥希替尼的患者。评估化疗联合/不联合奥希替尼用于奥希替尼一线治疗后病情进展(非CNS进展)EGFR突变阳性晚期NSCLC患者中疗效和安全 性的Ⅲ期 COMPEL 报道正在进行中
联合抗血管生成药物
尽管贝伐珠单抗联合奥希替尼在多项研究中显示阴性结果,但抗血管生成药物,特别是小分子靶向药物,如安罗替尼、阿帕替尼等也是奥希替尼耐药后可选的联合策略之一。一项回顾性分析,纳入39例经奥希替尼治疗耐药的EGFR突变NSCLC患者,接受奥希替尼联合阿帕替尼治疗的ORR为 12.8%、DCR为79.5%, PFS达 4个月,36%的患者用药时间超过6个月
免疫治疗
目前已有文献数据不支持对靶治疗后疾病进展的EGFR突变的患者常规应用免疫检查点抑制剂单药治疗,ICIs单药在EGFR突变的NSCLC 患者中疗效不佳与肿瘤突变负荷较低,及肿瘤组织中 浸润淋巴细胞水平较低有关,但 EGFR突变的肿瘤细胞组成性增强原癌基因信号转导使PD-L1表达上调,从而介导免疫逃逸,提示EGFR-TKI耐药后应 用免疫治疗存在潜在获益可能。
免疫治疗联合化疗和/或抗血管治疗
ICIs与化疗和/或抗血管生成治疗联用在EGFR-TKI治疗后耐药患者中的疗效已被初步证实。Ⅲ期ORIENT-31临床研究,评估了抗PD-1单抗(信迪利单抗)联合贝伐珠单抗类似物 IBI305和含铂双药化疗(培美曲塞和顺铂) 在 EGFR突变NSCLC耐药患者中的疗效和安全性。约36%的患者既往接受过三代EGFR-TKI治疗,中期结果显示,与含铂化疗对照组相比,信迪利单抗联合 IBI305和 化疗组6.9个月vs. 4.3个月,HR=0.464(P<0.001)以及信迪利单抗联合化疗组(5.5个月vs. 4.3个月,HR=0.723,P=0.0181)可改善患者 mPFS。
NEJ043是一项阿替利珠单抗联合贝伐珠单抗和化疗(紫杉醇和卡铂) (ABCP)治疗EGFR突变经治的NSCLC Ⅱ期临床研究。未达到既定随访时间,但观察到了良好的客观缓解:ORR 达 56%,mPFS 为 7.4个 月,mOS 为18.9个月, 且联合治疗耐受性良好
CheckMate722是一项纳武利尤单抗联合化疗对比单纯化疗用于EGFR 突变晚期 NSCLC经 EGFR-TKI治疗后疾病进展患者的Ⅲ期临床研究,两组分别纳入了 22%和 24%既往经奥希替尼治疗的患者,结果显示,相比单纯化疗,免疫联合化疗并未显著改善患者 mPFS (5.6个月vs. 5.4个月HR=0.75,P=0.0528) 和 mOS( 19.4个月vs. 15.9个月,HR=0.82)
第三代EGFR-TKI耐药的EGFR突变的NSCLC患者可能从ICIs与化疗和/或抗血管生成联合治疗中获益。目前对于经三代EGFR-TKI治疗耐药后机制不明的患者,免疫联合治疗可能是一种潜在治疗的选择,但该联合治疗方案的最佳模式、获益人群筛选及安全性尚需进一步探索
新药临床研究
细胞毒性药物⁃抗体偶联制剂(ADCs) 是一种将可靶向肿瘤抗原的特异性单抗和具有高效细胞毒性的小分子化疗药物通过连接子偶联而成的新型药物,可 利用抗体与肿瘤抗原间的特异性结合,将小分子化 疗药物输送到肿瘤细胞,发挥肿瘤杀伤作用。ADCs可克服多种三代EGFR-TKI 耐药分子机制,在三代EGFR-TKI耐药患者显示出良好的疗效和安全 性。
DS-1062 是一种ADC,由人源化抗TROP2 IgG1 单克隆抗体,通过含四肽的可裂解连接 子,偶联至拓扑异构酶Ⅰ抑制剂有效载荷(exatecan衍生物)TROPION-PanTumor01 研究结果显示,Dato-DXd 在34例后线的晚期 NSCLC 患者(其中69%为经奥希替尼治疗耐药的患者)中,显示出令人鼓舞的抗肿瘤活性:ORR达 到 35%。Patritumab derutecan是一 种携带拓扑异构酶Ⅰ抑制剂的HER3 ADC,Ⅰ期结果显示,44例既往接受过奥希替尼和铂基化疗的患者接受Patritumab derutecan获得39%的ORR和 68%的DCR,mPFS为8.2个月
双特异性抗体
双特异性抗体在EGFR-TKI治疗耐药后多项分析展现出不错的疗效。Amivantamab是一类可靶向EGFR/cMET的双特异性抗体,一项Ⅱ期研究共入组 45例未接受过化疗的奥希替尼耐药的EGFR突变NSCLC患者,接受 Amivantamab联合第三代EGFR-TKI Lazertinib 治疗后的ORR为36%,mPFS为4.9个月,其中EGFR或MET生物标志物阳性的患者中的ORR 为 47%。
新型免疫治疗药物研发方面,由康方生物完全独立自主研发的全球首创双特 异性抗体新药依沃西(PD-1/VEGF双抗,AK112),拟被纳入突破性治疗品种名单,联合化疗用于治疗EGFR-TKI治疗耐药的EGFR突变的局部 晚期或转移性SCLC ( nsq⁃NSCLC),Ⅱ期研究结果显示,依沃西联合化疗用于经EGFR-TKI治疗失败后患者的ORR 为68.4%, DCR为94.7%,mPFS为8.2个月
第四代靶向药
为克服第三代EGFR-TKIs靶向耐药,多种第四代EGFR也处于早期临床研究阶段。JBJ-04-125-02是一种变构EGFR抑制剂,在细胞及动物水平均已观察到抑制 L858R/T790M/C797S 型EGFR突变的作用。BLU-945和BLU-701是另外两种均可穿透血脑屏障且不与野生型EGFR结合的第四代 EGFR-TKIs。临床前研究中,BLU-945能抑制三联EGFR突变亚型( L858R/T790M/C797S及 19del/T790M/C797S)。BLU-701在临床前研究中也显示出良好的肿瘤抑制活性,目前BLU-701联合或不联合奥希替尼或化疗用于经EGFR-TKIs治疗耐药后NSCLC患者的全球I/Ⅱ期临床研 究正在进行中 ( HARMONY,NCT05153408)
共识 8:第三代EGFR-TKI 治疗耐药后进展的晚期EGFR突变NSCLC患者经积极治疗后无临床症状或症状稳定,应定期接受血清学肿瘤标志物及胸腹部增强CT等检查;伴有脑、骨转移者需要复查脑MRI 和/或全身骨扫描。对于再次获得完全缓解的患者进行ctDNA、CTC动态监测有助于判断预后和
制定进一步的治疗策略(共识级别:2A)
文献来源
李咏生,孙建国,李梦侠.第三代EGFR-TKI耐药后诊疗策略专家共识[J].中华肺部疾病杂志(电子版),2023,16(02):145-155.
免责声明本文仅供专业人士参看,文中内容仅代表刘之说立场与观点,不代表肿瘤资讯平台意见,且肿瘤资讯并不承担任何连带责任。若有任何侵权问题,请联系删除。
排版编辑:肿瘤资讯-Kate











 苏公网安备32059002004080号
苏公网安备32059002004080号


