医路曼话,百家畅谈。2023年4月18日17:00良医汇【肿瘤资讯】携手大连医科大学附属第二医院肿瘤内科李曼教授开展的系列乳腺癌线上培训课程——“半月曼谈”第二十六期如约举行。

“半月曼谈”精品云课堂聚焦乳腺癌前沿研究、病理、影像、临床诊治等方面,以乳腺癌疑难病例讨论、诊疗经验分享、规范化指南解读等形式进行专题培训,整个系列课程邀请乳腺领域知名专家深入剖析、集思广益,广大中青年医师共同参与、全面提高乳腺癌的诊治水平,为难治性乳腺癌患者献计献策。同时,云课堂采用线上直播+课程制作的形式,让讨论更有参与感、传播度更广。
本期4月18日17:00的精品云课堂名家齐聚,特邀福建省肿瘤医院刘健教授担任特邀顾问,中国科学院大学附属肿瘤医院陈占红教授、哈尔滨医科大学附属第二医院路丹教授及吉林省肿瘤医院陈飞教授担任指导嘉宾。

课程伊始,李曼教授介绍了“半月曼谈”栏目开设的主旨,诚邀各位专家教授针对相关议题各抒己见,开展深入对话。

畅叙医情——病例分享
在“畅叙医情”环节,大连医科大学附属第二医院宋晨博士分享了一例晚期HR+/HER2-病例。专家们围绕该例患者的后续治疗方案进行了探讨。

病例资料
基本情况:
患者,女,59岁,已绝经,无特殊既往病史家族。
现病史:
2015-4因“发现左乳肿”就诊。
完善乳腺乳腺超声检查提示左乳腺实性占位病变并钙化(3.0×2.5cm,BI-RADS 5级)。
完善CT及ECT检查,脑、肝、肺、骨无转移。
外科手术治疗:
2015-5-15 行左乳癌肿物扩大切除+淋巴结清扫术。
术后病理:左乳腺浸润性导管癌(II级),3.5×3.0×2.5cm,脉管内见癌栓;左侧锁骨下淋巴结1/2枚,I组15/18枚,II组0/1枚,III组1/1枚转移癌;乳头、皮肤、筋膜未见癌累及。
免疫组化:ER(80%强+),PR(70%强+),HER2(1+),Ki-67(55%)。
术后诊断:左乳腺浸润性导管癌改良根治术后 IIIC期 pT2N3aM0
术后辅助治疗:
2015-6至2015-11,行EC-T治疗8周期
2015-11-18起行左胸壁及锁骨上下区放疗
2015-12起行来曲唑+戈舍瑞林内分泌治疗
2016-12-15行卵巢切除手术,后继续服用来曲唑,至2020-3-4
病情进展:
2020-3 全身骨显像提示较2019-7-18全身骨显像对比,左侧骶髂关节、右侧髂骨放射性浓聚灶,较前新发,考虑骨转移可能大,请结合其他相关检查随诊;骶椎小片状放射性增强灶,较前相仿,随诊观察。如下图所示:
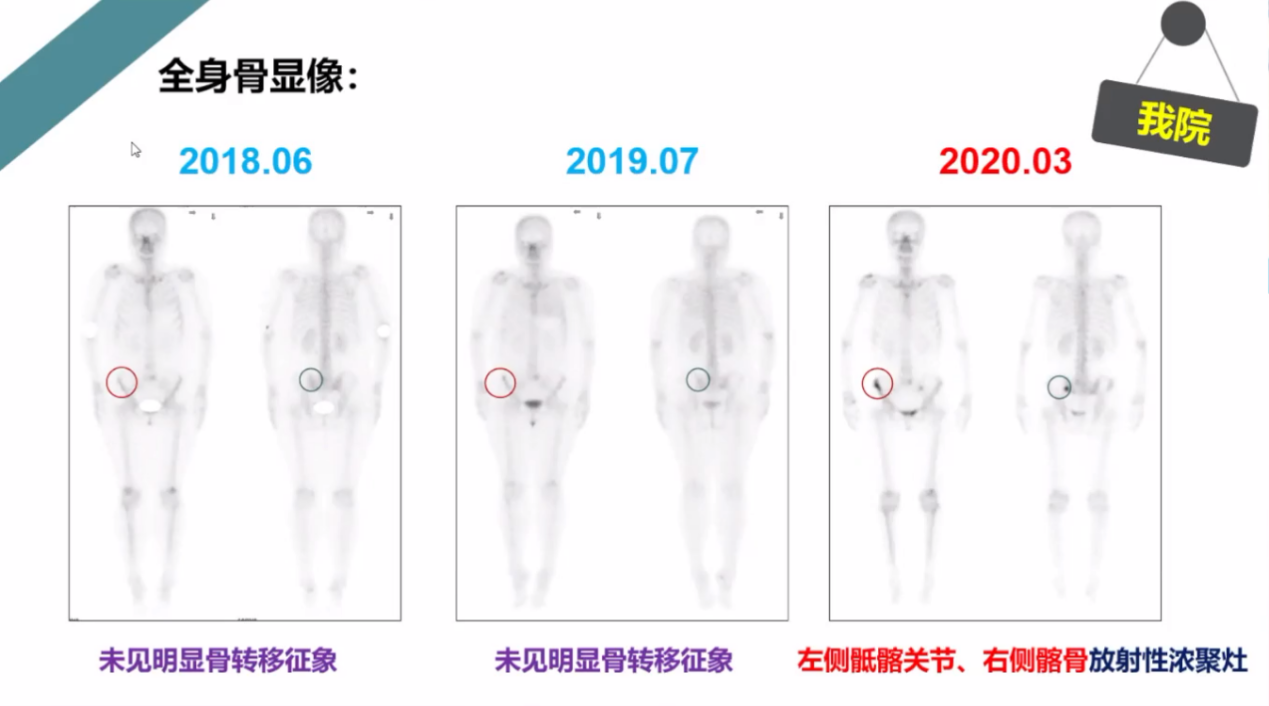
图一
完善骨窗CT提示左侧髂骨出现骨转移,如下图:
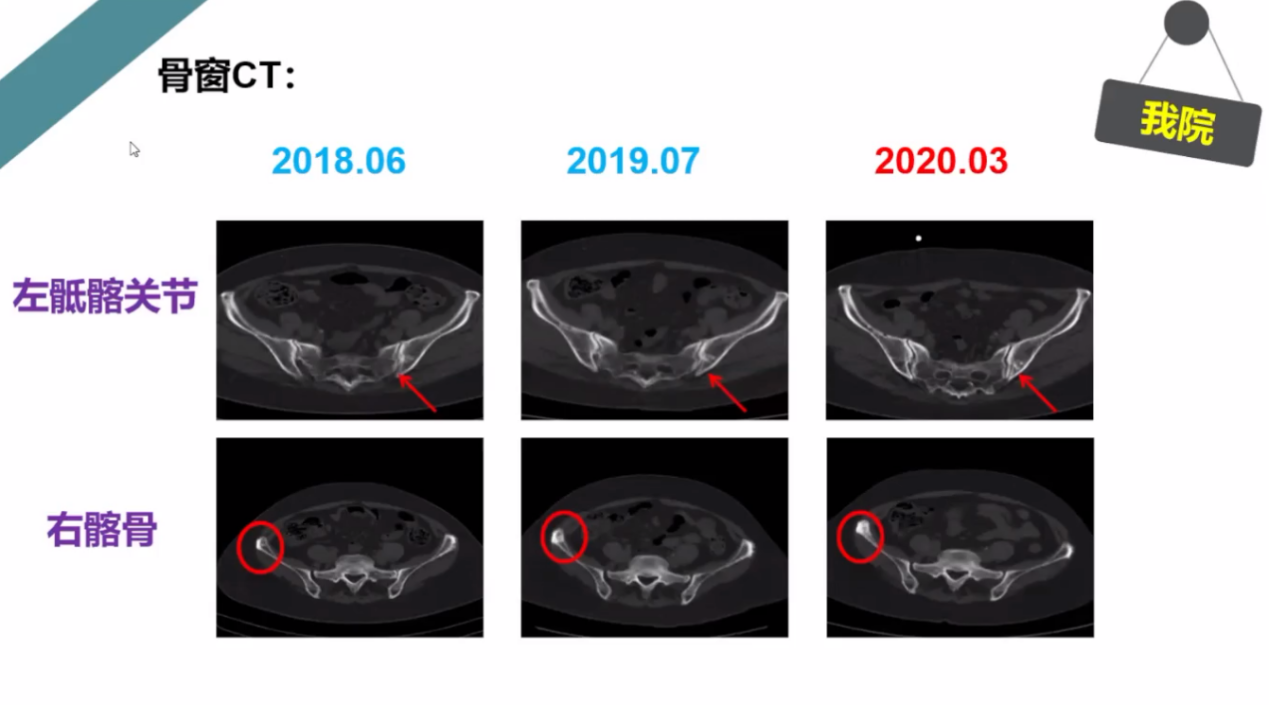
2020-3腹部超声提示:肝右叶异常回声。完善肝胆脾胰增强核磁,示肝右叶内异常信号,结合病史,考虑转移瘤可能性大,如下图。肝脑CT无病灶。
2020-3-13行肝脏穿刺活检术,结果如下图,(肝脏穿刺组织)可见癌组织,结合免疫组化,符合乳腺癌转移。
免疫组化:ER(90%+),PR(-),HER2(1+),Ki67(45%+),EGFR(-),CK5/6(-);BRCA1(90%强+),P53(60%弱+),AR(1%弱+),TOPII(Ⅱ级)。9 行右乳腺癌改良根治手术。
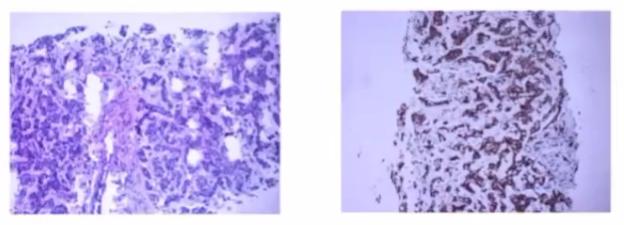
补充诊断:左乳腺癌术后 骨转移 肝转移
左乳腺浸润性导管癌改良根治术后 IIIC期 pT2N3aM0
双侧卵巢切除术后
晚期一线治疗:
2020-3至2020-5行哌柏西利+氟维司群内分泌治疗2周期,伊班膦酸钠骨保护治疗。
2020-5疗效评价,上腹部磁共振示患者肝转移灶增多,增大,如下图:
骨窗CT如下图,示新发胸椎、腰椎转移灶:
 疗效评估:肝脏病灶PD,骨转移病灶PD,总体疗效评价PD,疾病进展时间(TTP)2个月。
疗效评估:肝脏病灶PD,骨转移病灶PD,总体疗效评价PD,疾病进展时间(TTP)2个月。
晚期二线治疗:
2020-5至2020-9 行白蛋白紫杉醇+卡培他滨化疗6周期。
2020-9至2022-4 行卡培他滨维持治疗21周期。
同时针对骨转移继续伊班膦酸钠骨保护治疗。
2022-1,维持治疗18周期时患者出现腰痛,骨窗CT示髂骨骨转移范围增大,如下图所示:
胸椎、腰椎转移病灶增大、增多,如下图所示:
完善PET-CT如: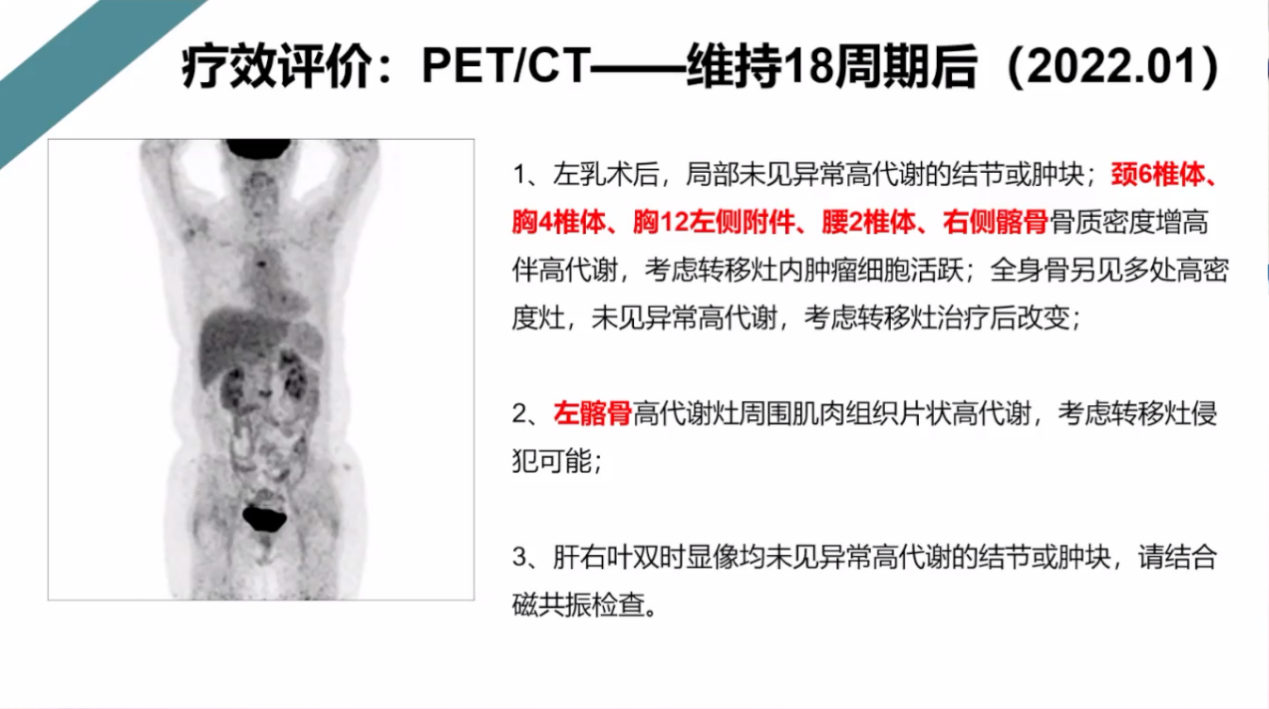
腹部增强磁共振如下图所示,肝脏病灶持续缩小、减少:
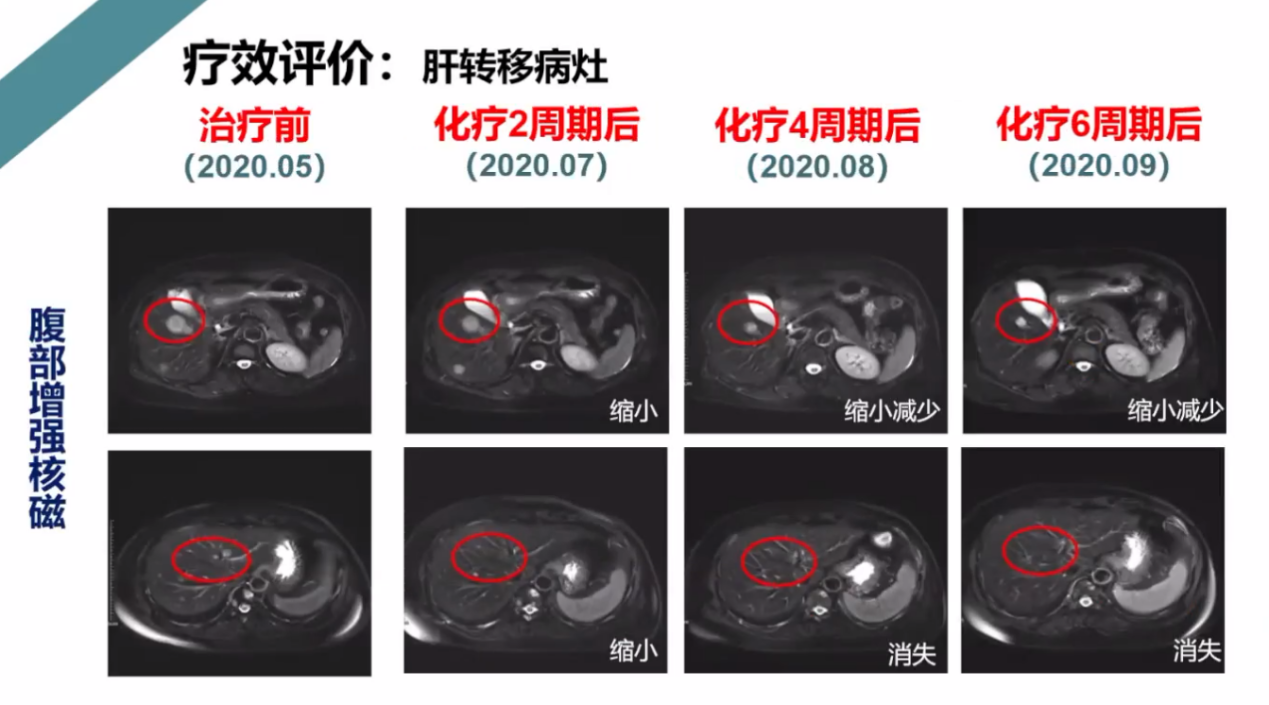

疗效评价:骨转移 PD,肝转移 CR。
2022-1行姑息放疗,具体部位:颈6椎体、胸4椎体、腰2椎体、骶椎、双侧髂骨及髋臼。
剂量:DT 30Gy/10f
2022-4 卡培他滨维持治疗21周后,患者腰痛获得缓解,肝部病灶增多、增大,如下图所示:
疗效评价:骨转移病灶PD(TTP 20个月),肝转移病灶 PD(TTP 23个月),总体疗效评价 PD(TTP 20个月)。
晚期三线治疗:
2022-4至2022-9 行艾立布林治疗6周期,同时针对骨转移行伊班膦酸钠骨保护治疗
疗效评价:骨转移病灶保持稳定,如下所示: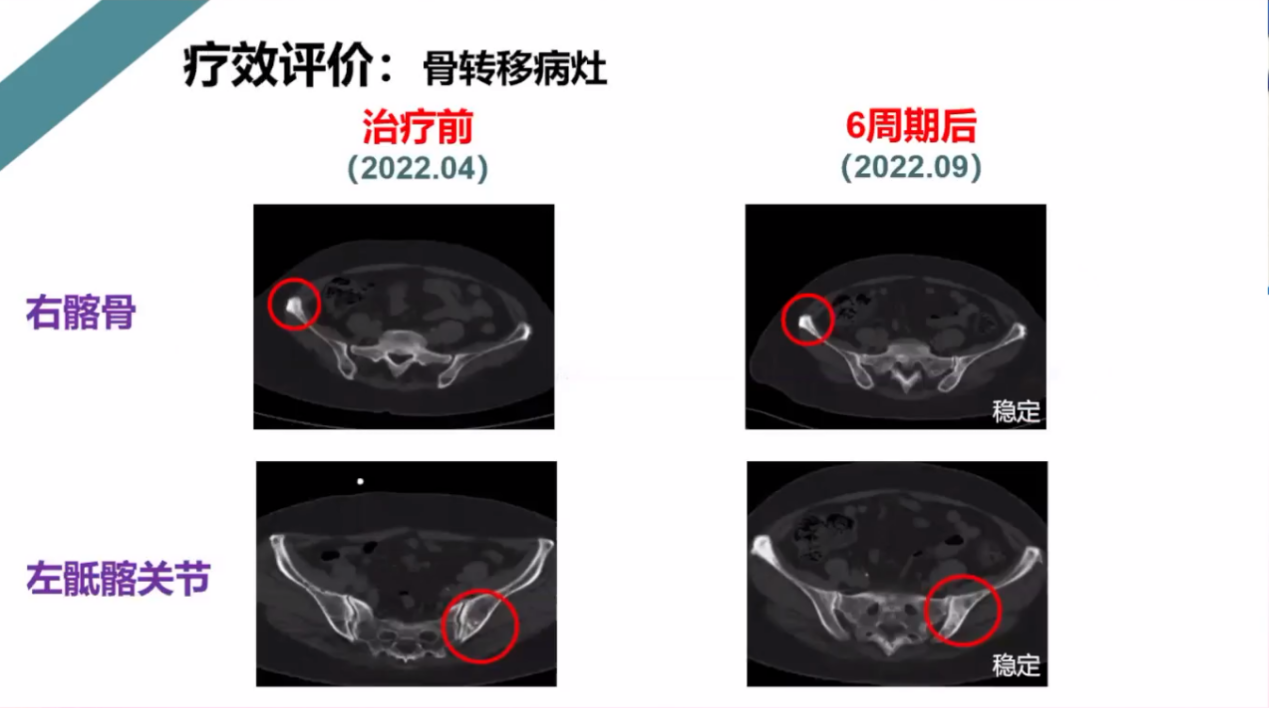
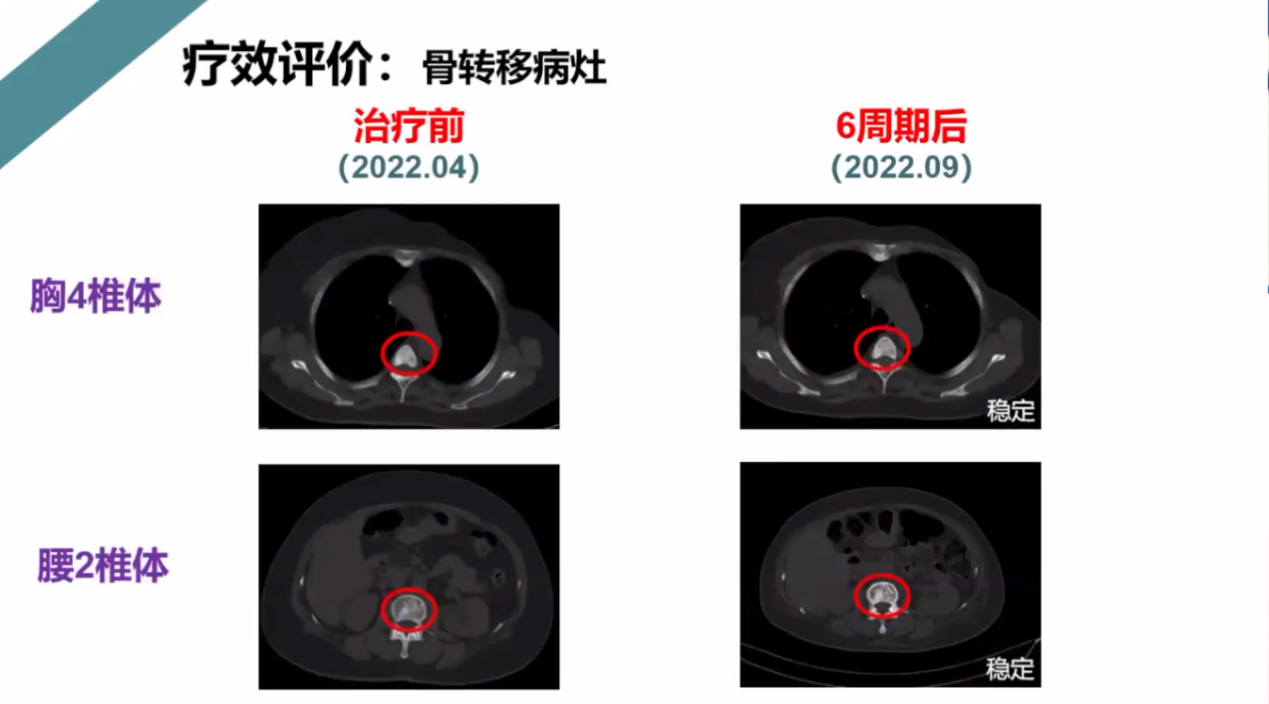
肝转移病灶2周期,4周期后缓解,6周期后进展,如下图所示: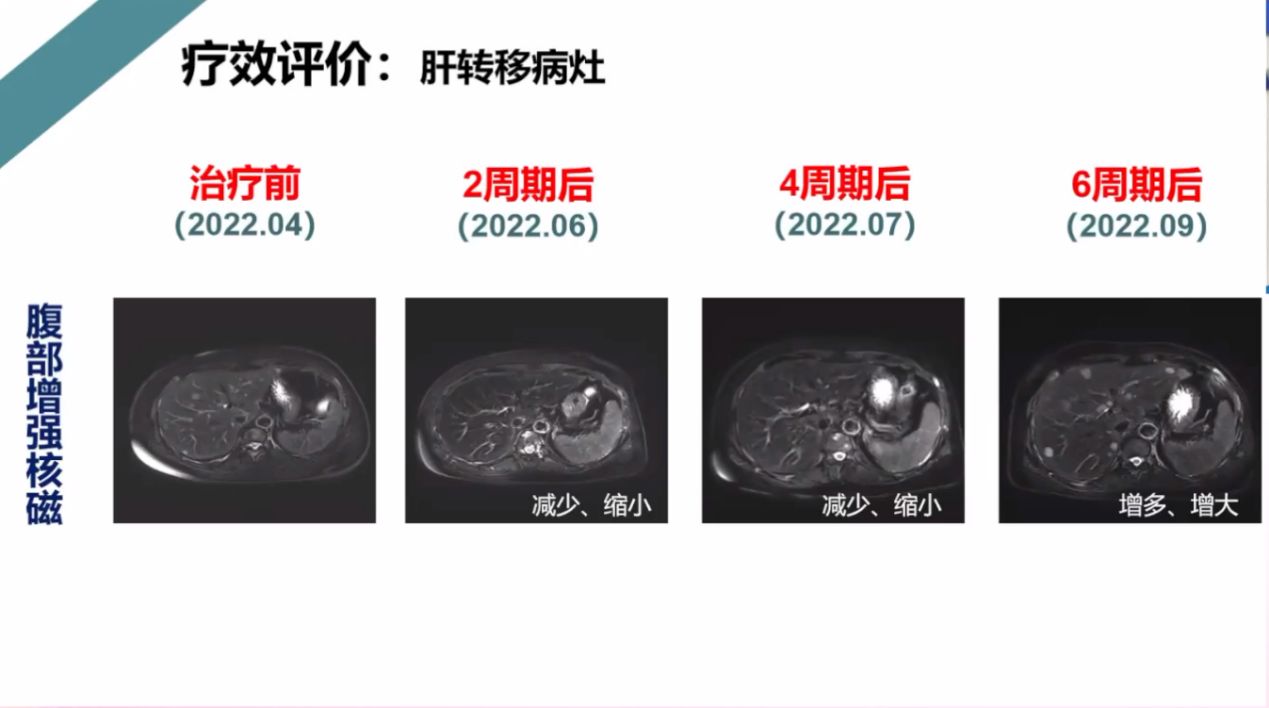
疗效评价:骨转移 nonCR nonPD,肝转移 PD ,总体疗效评价 PD (TTP 5个月)。
晚期四线治疗:
2022-9至2022-11行吉西他滨+顺铂治疗2周期,同时行伊班膦酸钠骨保护治疗。
疗效评价:骨转移病灶保持稳定,如下图所示:

肝转移病灶进展,如下图所示: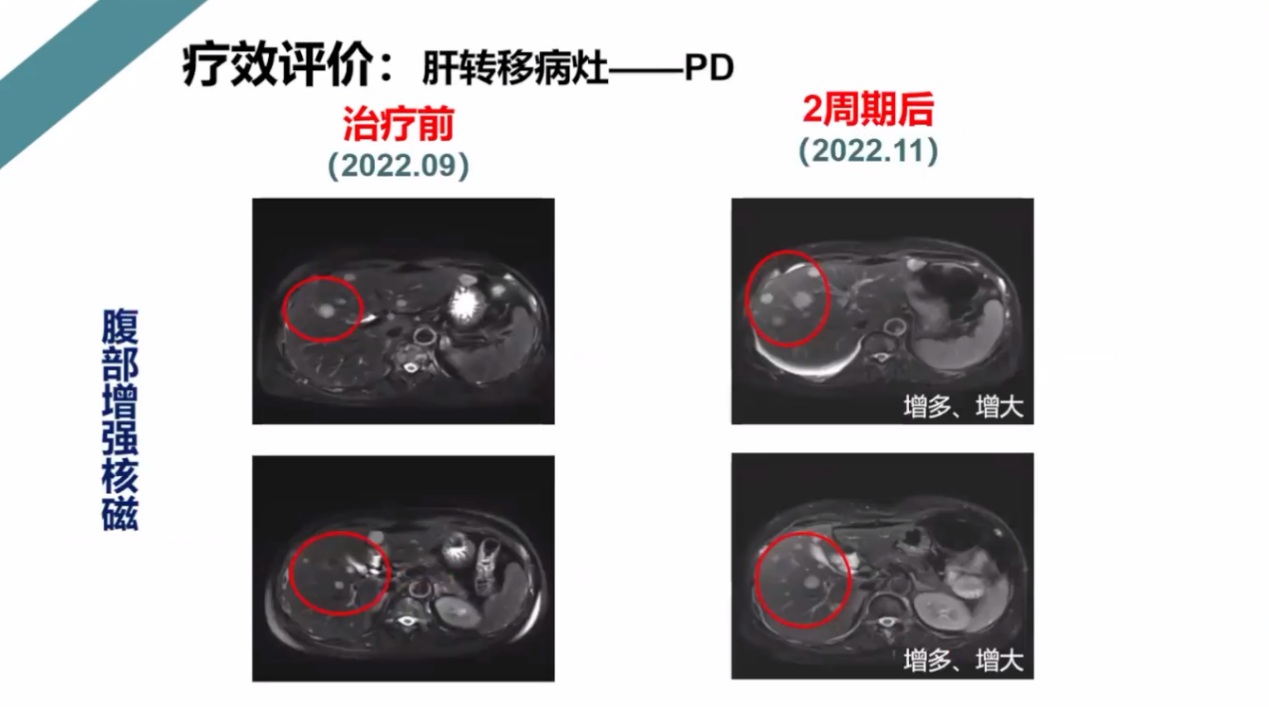
疗效评价:骨转移 nonCR nonPD,肝转移 PD,总体疗效评价 PD(TTP 2个月)
基因检测:BRCA2移码突变。
晚期五线治疗:
2022-11至2023-3 行奥拉帕利治疗4个月(患者3个月起自行因不良反应由300mg bid po减量至150mg bid po),同时行伊班膦酸钠骨保护治疗。
疗效评价:骨转移病灶保持稳定,如下图所示: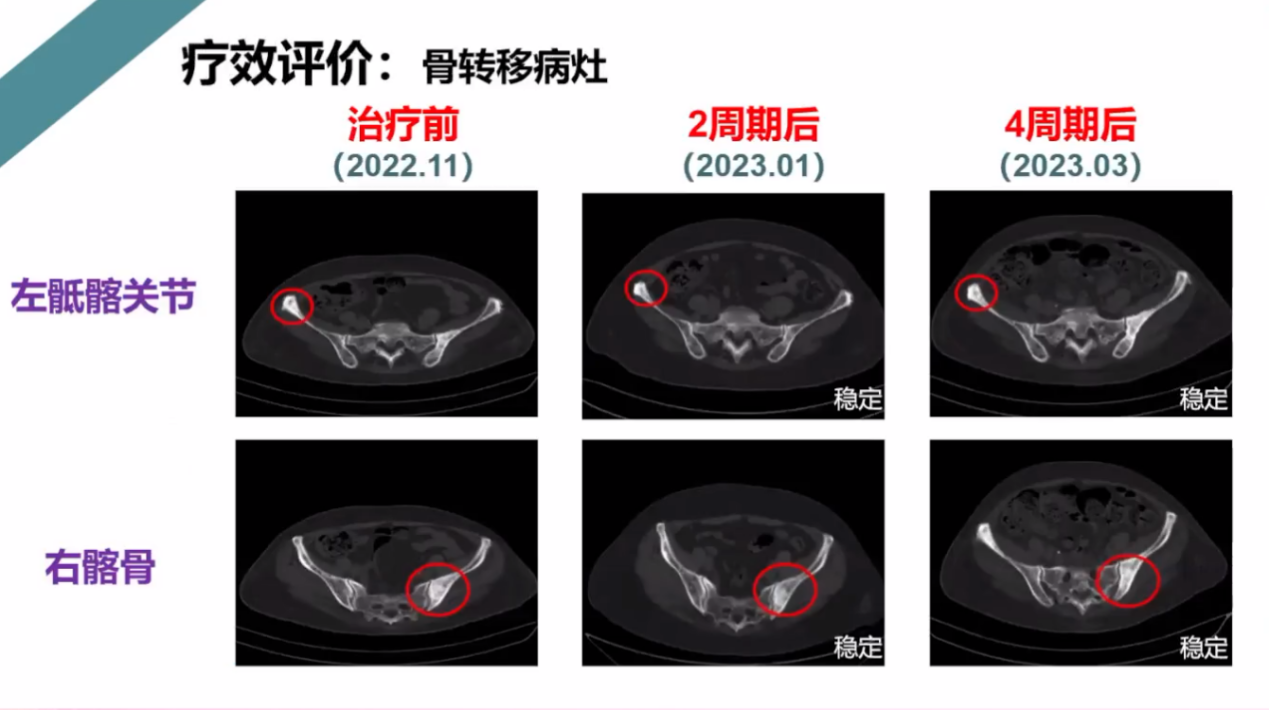
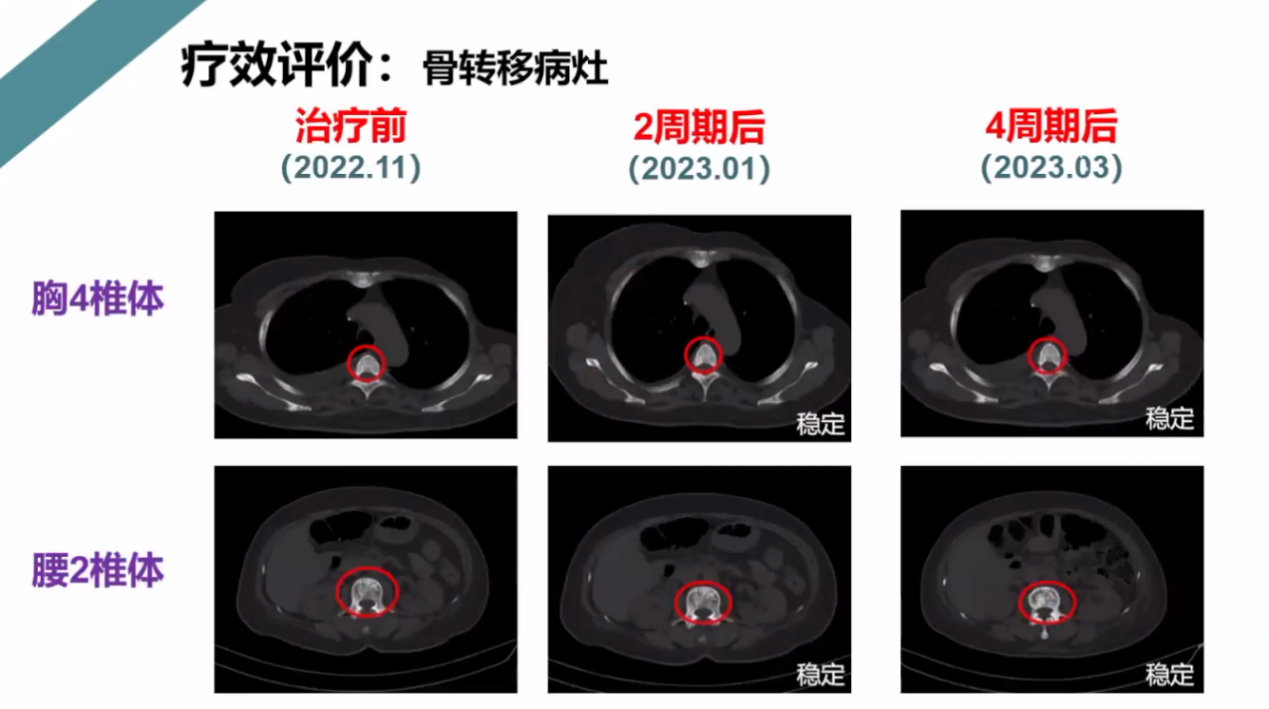
肝转移病灶,2周期后减少,4周期后进展,如下图所示: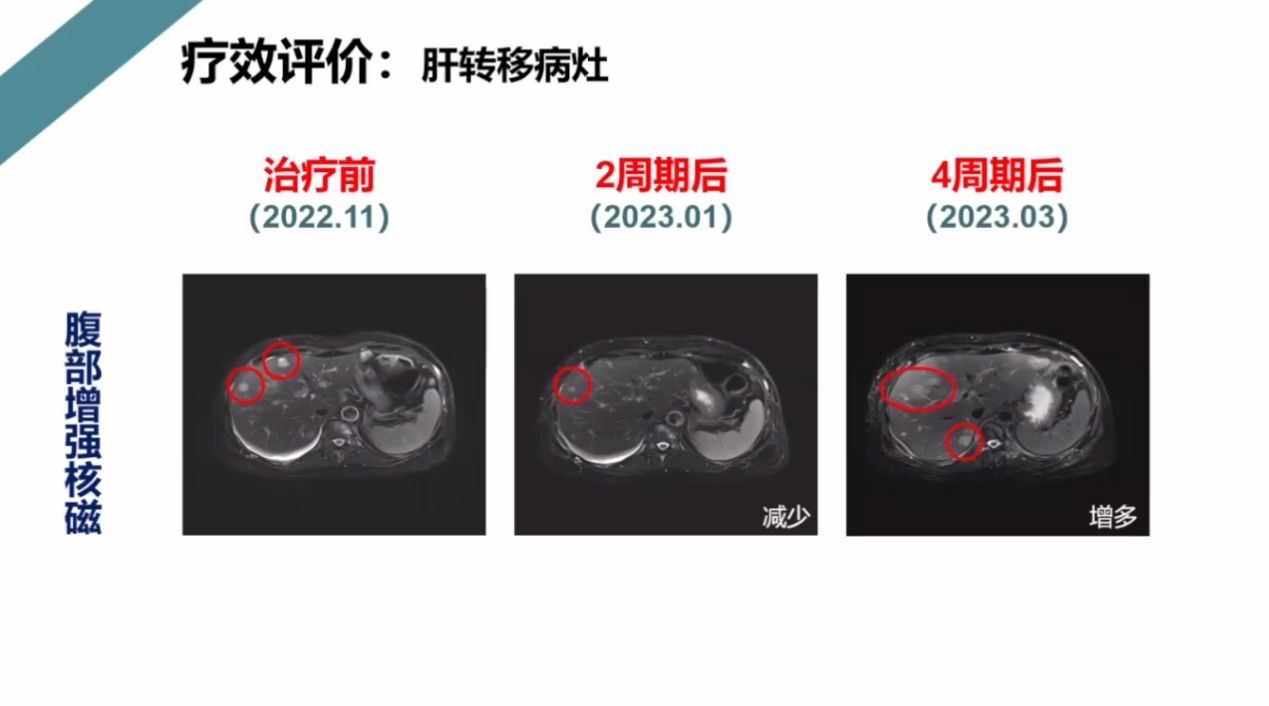
患者截止2023-3小结如下图所示: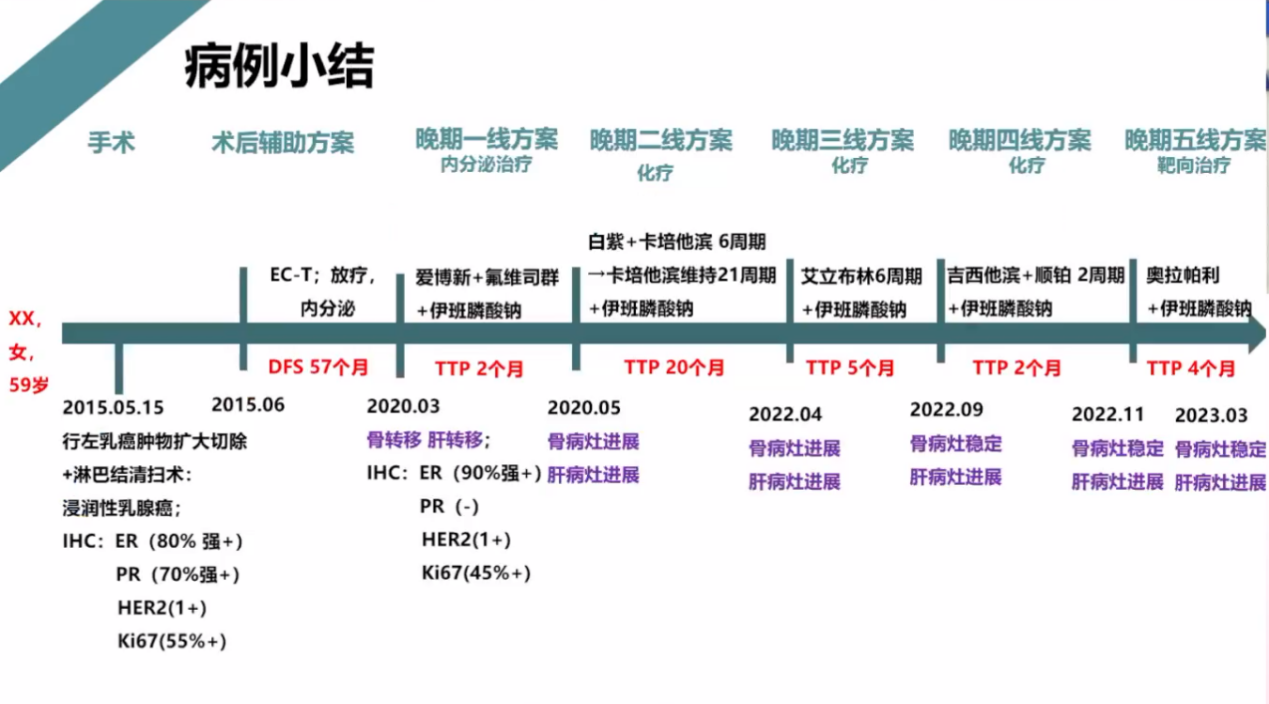
病情变化:
2023-4-13 患者突发截瘫,胸腰骶椎增强核磁如下,考虑胸段脊膜新发转移:
问题讨论:
1) 患者为已绝经,59岁,术后约4年复发转移,肝转移,骨转移,晚期内分泌一线治疗后耐药,下一步应如何治疗?应更换内分泌治疗方案还是选择化疗?
2)患者接受晚期二线治疗后,骨转移病灶进展,肝转移病灶缓解至CR,下一步治疗方案应如何选择?PET-CT是否可作为判断肝脏疗效的金标准?
3)患者五线接受奥拉帕利后进展,并于近期出现截瘫,下一步治疗应如何选择?
集思广医—众专家各抒己见
在讨论环节中陈占红教授、路丹教授及陈飞教授各自分享了对该病例的见解。
陈占红教授:该患者为Luminal型,术后已接受来曲唑内分泌治疗接近5年,为继发性耐药。患者复发后选择CDK4/6抑制剂+氟维司群的内分泌治疗的方案正确,但考虑患者已经继发耐药,疗效可能不如首次接受内分泌治疗的晚期一线患者。2个月后患者出现疾病进展,考虑患者此时为原发耐药,接下来可选择以紫杉类为主的化疗方案。患者晚期二线治疗后,不必立刻应用创新药物,考虑其骨转移进展而肝转移完全缓解,可考虑在完善评估后选择针对骨转移的治疗,如放疗,固定等。本病例中,PET-CT在磁共振已使用的前提下可作为重要影像学评估参考,用以评估骨转移和肝转移的疗效。结合循证医学证据,该患者或可尝试更早尝试PARP抑制剂。后续治疗方面,可尝试从不同角度进行治疗,从内分泌治疗角度,可选mTOR抑制剂依维莫司、HDAC抑制剂如西达本胺+依西美坦,从化疗角度看,可选长春瑞滨,从抗血管生成角度看,可选安罗替尼,ADC类药物可尝试DS-8201。
 陈占红教授
陈占红教授
路丹教授:该患者接受辅助内分泌治疗超2年,考虑应为继发性耐药,虽然晚期一线接受CDK4/6抑制剂+氟维司群的内分泌治疗,但从内分泌治疗角度考虑此时实际为二线内分泌治疗。治疗方案选择正确,可能由于患者肿瘤分期较晚,导致辅助治疗未结束时出现进展。考虑患者接受CDK4/6抑制剂仅2月出现进展,接受其他靶向治疗获益可能性不大,结合药物可及性考量,化疗是后续首选治疗方案。该患者骨转移为成骨性改变,乳腺癌骨转移通常为溶骨性,溶骨性改变在治疗过程中需警惕假性进展,而结合该患者影像学及临床症状,符合骨转移病灶进展。对于肝转移的诊断,增强核磁是主要手段,PET-CT的诊断意义虽然高,但难以认定为金标准,该患者肝脏病灶可认为CR。该患者肿瘤呈现出嗜器官性,在骨骼上进展较为明显。该患者突发截瘫后,可先尝试放疗。由于后线治疗方案TTP较短,难以决断最佳治疗方案。建议重新活检以明确病理状况及基因表达,对后续治疗方案选择进行指导,可考虑尝试DS-8201。内分泌治疗在晚期一线治疗效果较后,后线治疗则难以令人满意。
 路丹教授
路丹教授
陈飞教授:该患者初诊时分期已较晚,辅助内分泌治疗接近5年后出现复发,对于其为原发性耐药或继发性耐药存在争议。从辅助治疗角度考虑,患者为继发性耐药,从晚期治疗角度考虑,患者则倾向于原发性耐药。后续治疗不建议继续内分泌治疗,对于后CDK4/6抑制剂用药选择,PI3K抑制剂、mTOR抑制剂等暂时不可及,可进行BRCA基因检测以考虑是否可尝试PARP抑制剂,否则则应选择化疗,可选紫杉醇+卡培他滨以使得后续维持治疗有药可选择。该患者骨病灶进展,肝病灶完全缓解。对于椎体骨病灶的评估,磁共振评估效果可能更好。PET-CT虽然特异性较高,但仍不可作为影像学评估的金标准。后续治疗考虑患者多发骨转移,应以内科药物为主,考虑增加骨保护治疗可考虑ADC类药物,如DS-8201,也可考虑核素治疗。患者后期经基因检测发现BRCA2突变,奥拉帕利提供约4个月的PFS,但因血液学毒性而减量,该患者经历提示尽早接受基因检测的重要性。目前除BRCA基因突变外未观察到其他通路突变,可尝试HDAC抑制剂或ADC类药物如DS-8201、戈沙妥珠单抗。
 陈飞教授
陈飞教授
名医点睛——刘健教授一锤定音
刘健教授:该患者为恶性程度较高的Luminal B型,既往内分泌治疗总体令人满意,在接近5年时才出现复发转移,应考虑为继发性耐药。临床上对于原发耐药与继发耐药的判断标准为复发时间节点,该方法实用但科学性稍微欠缺。患者接受CDK4/6抑制剂联合氟维司群内分泌治疗2个月后,表现为晚期复发转移乳腺癌原发性耐药。内分泌治疗耐药机制复杂,下游通路中的信号改变都可能导致耐药发生。后续治疗方案可选化疗,对于已经原发性耐药的患者,采取CDK4/6抑制剂跨线使用或其他靶向治疗药物可能疗效欠佳。
PET-CT在专家共识中不作为标准检测方法,主要原因为性价比太低,以及对富含血流的部位(如肝脏、脑部)的判断不如CT或核磁共振,如今随着PET-MRI的发展,或可弥补PET-CT的缺陷。PET-CT的优点在于评估骨转移的疗效,可评估骨密度的变化,较传统X射线、CT可更灵敏地判断SUV的变化,不过对于肝转移的评估还需结合肝脏MRI检查。该患者为微进展,在疾病稳定(SD)至PD的过度,此时不宜立刻更改治疗方案,可尝试微调或增加局部补充治疗,以最大化发挥现有治疗方案的效果,待PD后再更改治疗方案。
患者出现截瘫提示病情已至终末期,预期生存较短,或可尝试外科介入以取得较放疗更好的效果,改善生活质量。从患者病情发展看来,后期肿瘤异质性较强,骨病灶对于化疗效果较好,肝脏则产生化疗原发性耐药,TTP极短。BRCA基因检测提示胚系突变,本应在肝脏转移后第一时间进行活检,了解其肿瘤异质性。该患者难以从PARP抑制剂后线单药治疗中获益,在后线使用应考虑联合方案,可增加铂类、紫杉类以取得更好的效果。目前也可尝试ADC类药物,如DS-8201。
 刘健教授
刘健教授
本次云课堂以一例HR+/HER2-晚期骨转移、肝转移疑难病例为引,从晚期化疗与内分泌治疗的选择、骨转移及肝转移的治疗等全角度讨论了该患者的疗效评价和后续治疗方案,讨论过程可谓畅所欲言。相信本次课程也让大家对此类晚期乳腺癌的规范化诊治有了更深入的了解。“半月曼谈”更多精品课程将继续呈现,精彩不断,欢迎持续关注!
排版编辑:肿瘤资讯-xiaodong











 苏公网安备32059002004080号
苏公网安备32059002004080号


