我国是胃癌高发国家,既往一线标准化疗对晚期患者获益有限,且诊疗进展相对滞后。在此背景下,经典研究CheckMate-649开创了免疫联合化疗这一全新治疗模式,树立了晚期胃癌一线治疗新标准。在年初举行的ASCO GI 大会上,CheckMate-649研究公布了迄今该领域最长的3年随访数据,进一步证实了纳武利尤单抗联合化疗为中国晚期胃癌患者带来的前所未有的长期获益。
在研究不段取得突破的同时,广大临床医师同样关注CheckMate-649方案在真实临床中的获益,两者如同硬币正反两面,互为表里、相互促进。为此,【肿瘤资讯】特邀CheckMate-649研究中国主要研究者、北京大学肿瘤医院沈琳教授,以及北京协和医院赵林教授接受此次【经典回“胃”AB面】专题采访,对CheckMate-649中国亚组3年随访数据进行深度解读,并带来真实临床中的免疫治疗精彩病例,分享经验和体会。

A面: CheckMate-649中国亚组近1/3患者长期生存,OS、PFS获益超越全球人群
沈琳教授介绍道,CheckMate-649是开胃癌免疫治疗之先河的里程碑式研究,首次证实与单纯化疗相比,化疗基础上联合免疫治疗(纳武利尤单抗)用于一线治疗的生存获益显著。中国亚组3年随访数据进一步验证了研究结果,全人群3年OS率接近30%,这在整个胃癌研究历史上都非常罕见;尤其是PD-L1 CPS≥5人群,3年OS率达到31%,较单纯化疗(11%)几乎提升了三倍。也就是说,纳武利尤单抗联合化疗一线治疗不仅为HER2阴性晚期胃癌患者整体带来生存获益,还能使近1/3的患者实现长期生存,获益力度非常大。
 CheckMate-649中国亚组3年随访OS结果
CheckMate-649中国亚组3年随访OS结果
沈琳教授还指出,除了OS外,CheckMate-649研究的另一大特点在于获益全面。中国亚组3年随访数据显示,无论是全人群还是PD-L1 CPS≥5人群,纳武利尤单抗联合化疗的ORR均较化疗提高20个百分点,持续缓解时间(DOR)超过一年,较化疗近翻倍;另外中国亚组全人群中位PFS较化疗延长近1.5倍(8.3个月 vs 5.6个月)、CPS≥5人群中位PFS则较化疗近翻倍(8.5个月 vs 4.3个月)。沈琳教授认为,这反映出CheckMate-649方案良好的疾病控制效果,不仅可改善生活质量,且可能转化成患者的长期获益:从3年随访数据中也可以看到,治疗18周内达到CR/PR的患者中位OS可长达21.5个月,提示肿瘤深度缩小的患者恰恰是长期生存获益的人群。
此外,沈琳教授提到,对比全球人群3年随访数据,中国人群有获益更大的趋势,尤其是PD-L1 CPS≥5人群,OS HR为0.56(全球人群:0.70),PFS HR为0.51(全球人群:0.70),风险下降达到近50%,可见中国人群的获益非常明显,这些随访结果给中国患者选择纳武利尤单抗联合化疗方案提供了更多的数据支撑和更强的信心。
最后,沈琳教授认为,未来或可继续关注CheckMate-649研究更长期随访数据,例如5年生存率;另外探索哪些患者可能从免疫治疗中长期获益,包括对患者的肿瘤突变负荷(TMB)和基因特征等方面的分析,CheckMate-649研究在这方面做了很多表率,这对于促进基础转化研究、实现精准治疗具有重要意义。
B 面:真实世界中,超高龄IV期患者经一线纳武利尤单抗联合化疗达到完全缓解、长期获益
除了临床研究,CheckMate-649开创的治疗模式也在实践中为中国患者带来了切实获益。本次采访,赵林教授分享了北京协和医院诊治的一例超高龄晚期胃癌免疫治疗病例;沈琳教授也给予了点评。
赵林教授介绍,患者85岁,因“呕吐、体重下降”于2021年3月来医院就诊。患者既往只有高血压病史,无其他特殊疾病。胃镜检查发现胃食管结合部(GEJ)环周溃疡性病变,病理学结果为中低分化腺癌(Lauren分型:肠型);免疫组化结果为HER2(1+),MSS,PD-L1 CPS=10,EBER(-)。影像学检查发现胸腹部、胃周多处可疑淋巴结转移。经MDT评估,判断右上食管沟旁淋巴结为远处转移,为IV期胃食管结合部癌(cT3N2M1)。
MDT讨论后认为,该患者虽然仅有单一远处转移,但综合考虑年龄等基础情况,应以全身系统治疗为主。赵林教授指出,在患者就诊时,CheckMate-649研究结果已经正式公布,是当时唯一在晚期胃癌一线免疫治疗中获得阳性结果的III期临床研究,证实纳武利尤单抗联合化疗获益显著优于化疗,特别是对PD-L1表达阳性的人群;随后的中国亚组结果与全球结果一致。此外,该患者存在PD-L1高表达(CPS=10),为免疫治疗潜在优势人群,应选择免疫治疗联合化疗作为首选。
对于具体药物和用药方案的决策,赵林教授表示,在免疫治疗药物方面,选择了当时唯一获得阳性结果的纳武利尤单抗;在化疗方面,选择了在国内胃癌临床实践中常用的一线方案奥沙利铂联合替吉奥(SOX),且考虑到患者为超高龄,对化疗药物进行了减量(奥沙利铂100 mg,替吉奥40 mg bid)。
使用该方案治疗1个周期后,患者进食哽咽感基本消失。经过8个周期治疗后,患者原发肿瘤、转移淋巴结明显缩小,评价为部分缓解(PR),随后改为使用纳武利尤单抗联合替吉奥维持治疗;三个月后,因患者口腔不适,改为纳武利尤单抗单药维持治疗。在维持治疗过程中再次进行了胃镜等全面检查,病理结果显示仅为慢性炎症,已无残存肿瘤细胞,经MDT评估为临床完全缓解(cCR)。该患者从2021年就诊,至今已近两年时间,目前还在接受纳武利尤单抗单药维持治疗,近期疗效评价仍为cCR。
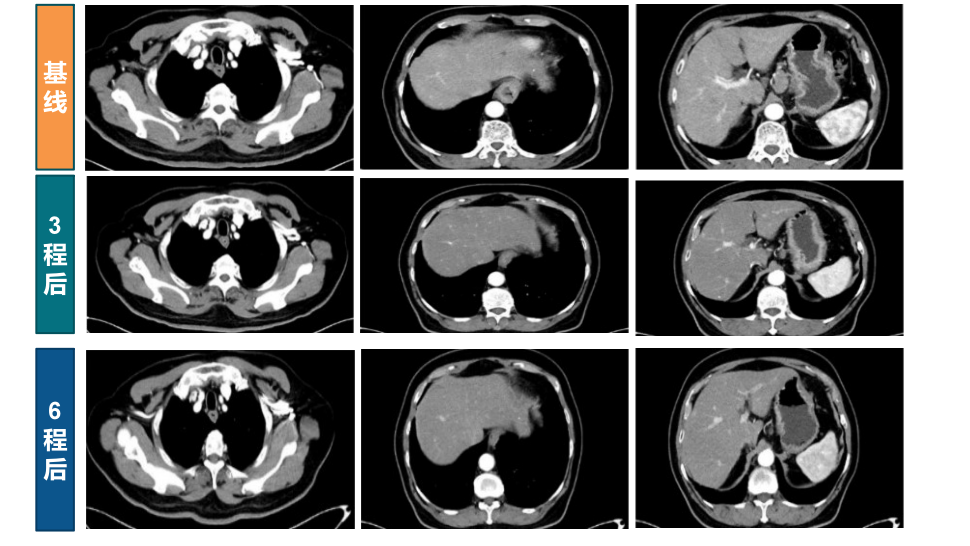
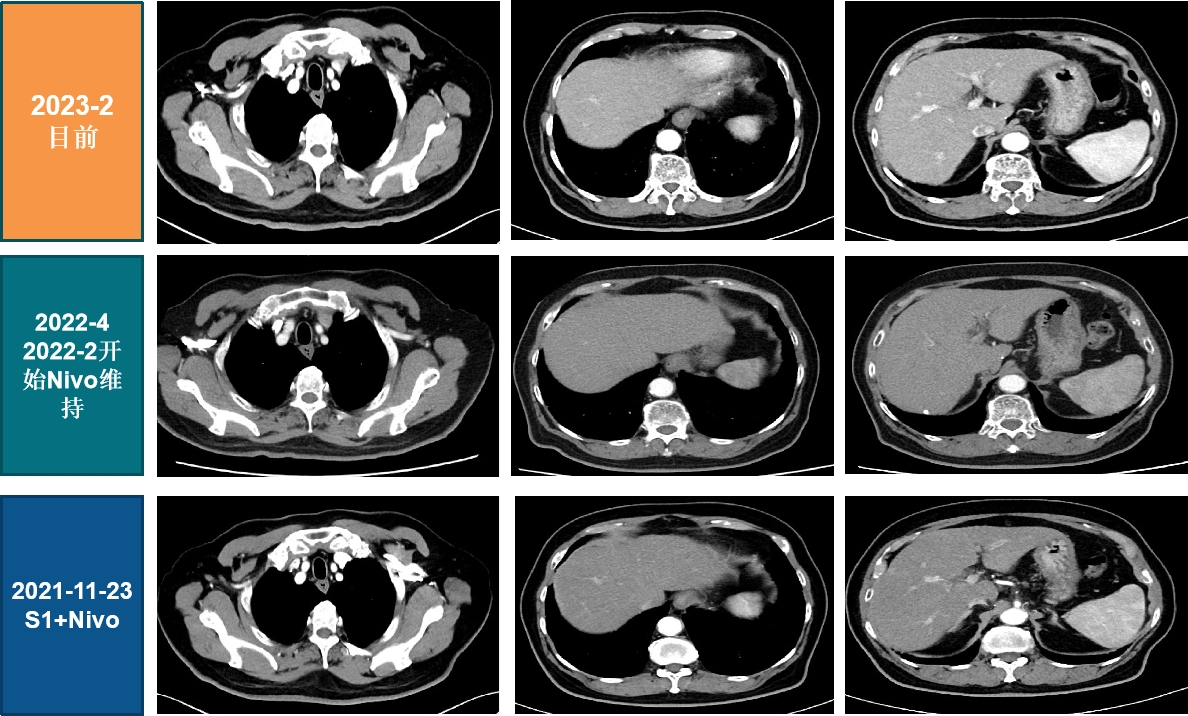 病例患者接受纳武利尤单抗+化疗过程中的影像学检查结果
病例患者接受纳武利尤单抗+化疗过程中的影像学检查结果
赵林教授认为,该病例充分体现了免疫治疗所带来的深度缓解和持久疗效,也再次反映了CheckMate-649研究的3年随访结果:免疫治疗组的生存曲线后续已出现了“平台化”的趋势,与真实世界治疗效果互相印证,提示未来该患者可能真正实现临床治愈。
谈及该病例的启示及临床中用药的体会,赵林教授表示,自2021年纳武利尤单抗联合化疗在中国获批以来,免疫联合化疗已经成为晚期胃癌一线治疗的新标准,且CheckMate-649研究数据的不断更新反复验证了这一模式在晚期胃癌中的地位;近期中国亚组3年随访数据的公布也再次强烈提示,中国人群从免疫治疗中的获益比西方人群更多,可能与不同人种之间的免疫微环境和分子特征差别有关,值得深入研究。赵林教授还指出,在免疫治疗疗效越来越好的今天,对于晚期胃癌甚至伴有转移的患者,能否通过一线免疫联合化疗争取到更多局部治疗机会,或可成为未来重要的研究方向。此外,虽然现在对免疫治疗的经验越来越多,安全性越来越有把握,但仍需重视免疫治疗相关不良反应管理,在实践过程中密切随访。
对于该病例,沈琳教授也点评道,这一85岁超高龄IV期胃食管结合部癌患者有很大的代表性,因为胃癌在我国高发,且随着人口老龄化,超高龄的患者日益增多。不仅如此,该例患者属于胃食管结合部肿瘤,同时又是HER2阴性,甲胎蛋白(AFP)升高,这类患者通常预后较差;赵教授选择使用纳武利尤单抗单抗联合化疗,并对化疗方案进行了减量,决策符合当时最新的临床证据,也契合当前的治疗理念:国际上已有研究结果提示,对于老年、身体状况较好的患者,给予减量联合治疗,结局往往好于不治疗或单药治疗。
沈琳教授总结道,该例患者通过纳武利尤单抗单抗联合化疗达到cCR,且已随访了两年以上,获得了长期生存,可以说实现了获益最大化;总之,近年来已免疫治疗的出现对于老年以及超高龄胃癌患者有非常大的意义,该例患者带给了我们很多启示,也大大增强了我们对于老年胃癌患者治疗的信心。相信伴随免疫治疗的不断发展,未来更多胃癌患者有望实现长期生存乃至治愈。
历任北京大学肿瘤医院副院长、北京市肿瘤防治研究所副所长
北京学者
中国抗癌协会肿瘤精准治疗专业委员会主任委员
中国抗癌协会肿瘤药物临床研究专业委员会首届主任委员
中国临床肿瘤学会临床研究专家委员会主任委员
中国临床肿瘤学会胃癌专家委员会候任主任委员
中国抗癌协会大肠癌专业委员会副主任委员
北京癌症防治学会理事会轮值理事长
博士、硕士生导师
任北京肿瘤防治研究会消化肿瘤专家委员会主任委员
北京抗癌协会食管癌专业委员会副主任委员
北京肿瘤病理精准诊断研究会副会长
CSCO结直肠癌专家委员会委员
CSCO食管癌癌专家委员会委员
CSCO抗肿瘤药物安全委员会委员
国家远程医疗与互联网医学中心胃肠肿瘤专家委员会副主任委员
排版编辑:肿瘤资讯-Rethyu











 苏公网安备32059002004080号
苏公网安备32059002004080号


