广泛期小细胞肺癌(ES-SCLC)患者预后较差,且长期以来,其治疗手段未能有重大突破。铂类化疗药物(卡铂或顺铂)联合依托泊苷是ES-SCLC的标准治疗方案。2002年,日本的一项Ⅲ期研究(JCOG 9511)在174例日本患者中发现,相较于依托泊苷联合顺铂(EP),伊立替康联合顺铂(IP)方案可改善ES-SCLC疗效反应,并延长患者生存时间。然而,2009年,在北美人群开展的SWOG S0124研究未发现IP方案能给ES-SCLC患者带来更多的生存获益。
随着免疫治疗时代的到来,Ⅲ期CASPIAN研究证实在EP方案的基础上,联合度伐利尤单抗虽然只能将ES-SCLC患者中位总生存期(OS)延长2.4个月(12.9个月 vs 10.5个月,HR=0.71,P=0.0003),但可显著提升其3年生存率(17.6% vs 5.8%),且具有“免疫治疗长拖尾效应”,提示ES-SCLC患者仍有长期生存的希望。
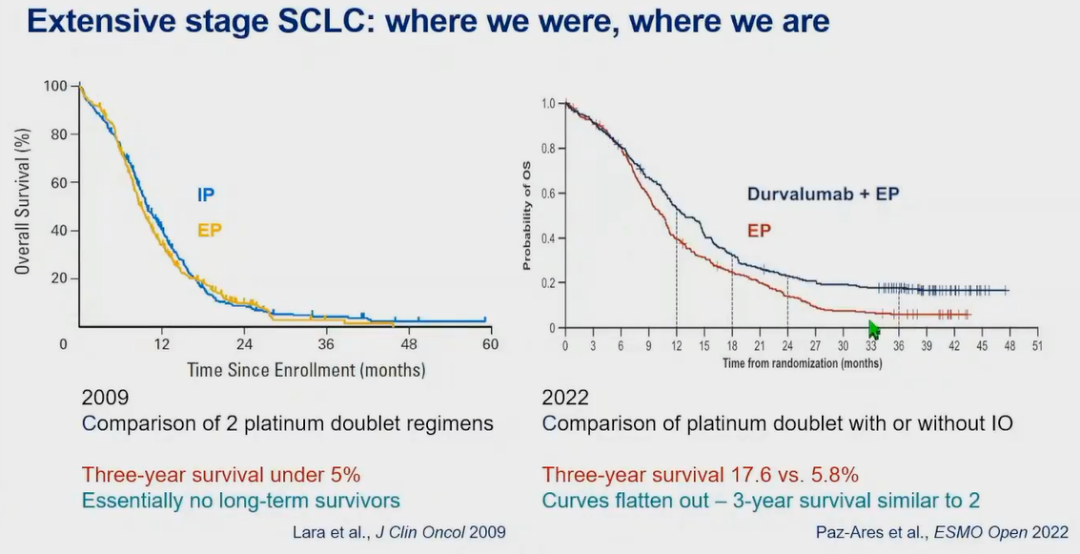
改善SCLC免疫治疗效果的探索
有学者基于转录组学对SCLC患者进行分群,Rudin等人提出可基于4种关键的转录因子(ASCL1、NeuroD1、YAP1和POU2F3)表达水平,将SCLC患者分为4个亚群,并以此预测患者预后和免疫治疗反应,但仍需要开发更有效的治疗药物,以改善SCLC患者预后。
除了PD-1/PD-L1抑制剂,联合其他免疫检查点抑制剂(ICI)或许可改善SCLC患者生存。然而,CASPIAN以及SKYSCRAPER2研究分别证实,在化疗的基础上联合CTLA-4或TIGIT抑制剂未能延长患者生存时间。
除此以外,Tarlatamab是新近研发的一种双特异性T细胞募集调节剂,可结合SCLC细胞表面DLL3和T细胞表面CD3,诱发T细胞介导的肿瘤细胞裂解,在Ⅰ期临床研究中展现出改善患者预后的潜力。联合靶向DNA损伤修复通路和表观遗传修饰药物或许也是改善SCLC预后的潜在方法。
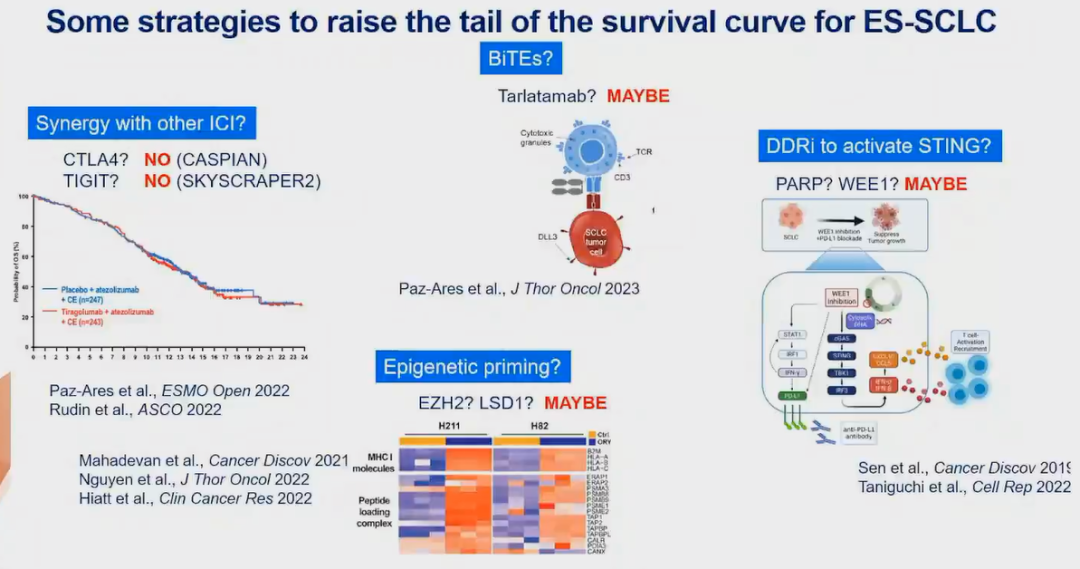
抗原递呈和T细胞募集
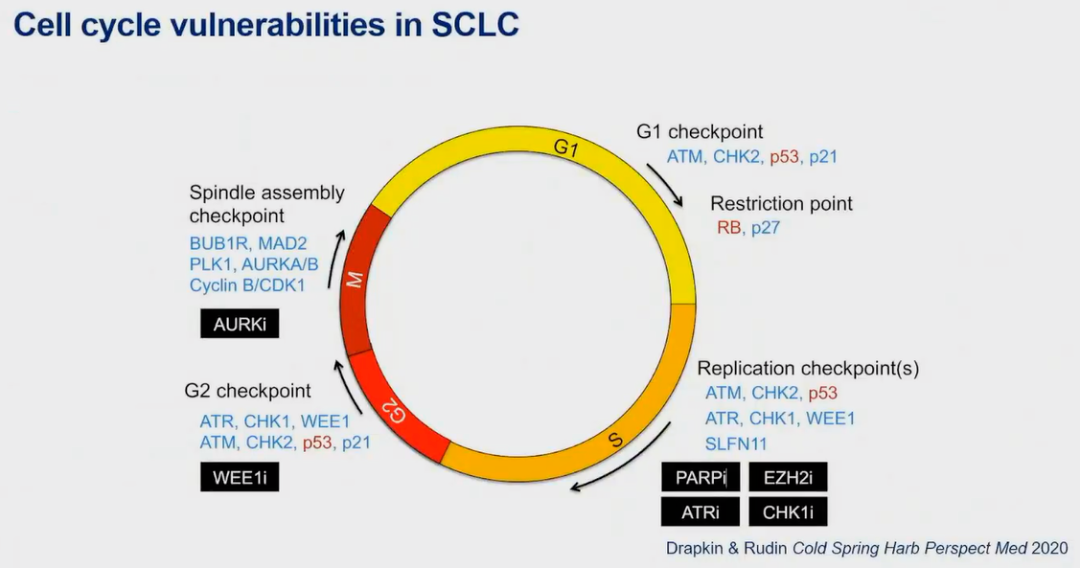
细胞周期调控
SCLC通常因为基因突变等原因,丢失细胞周期关键调节蛋白P53和RB1的表达。因此,SCLC或许对细胞周期控制有不错的疗效反应,许多相关药物如PARP抑制剂、WEE1抑制剂等正在进行抗肿瘤活性评估。有基础研究发现,WEE1抑制剂(AZD1775)可导致SCLC细胞发生G2/M期阻滞,激活cGAS/STING、Ⅰ型和Ⅱ型干扰素通路,并通过促进CD8+细胞毒性T细胞浸润诱导免疫应答,提示细胞周期调控类药物可与免疫治疗发挥协同抗肿瘤作用。
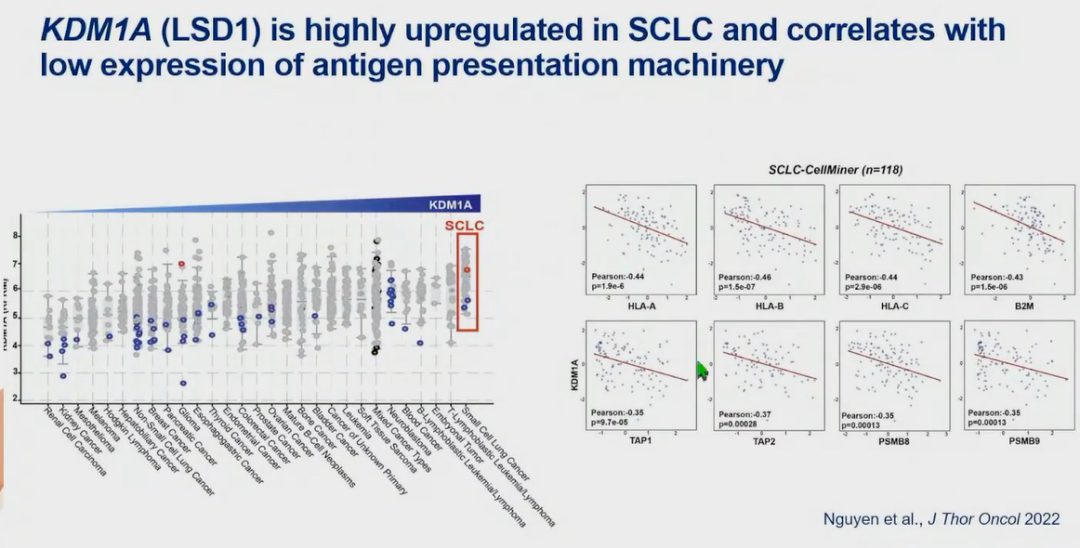
表观遗传修饰学修饰
SCLC中赖氨酸特异性脱甲基酶1(LSD1)高表达,并与MHC-I表达下调及免疫抵抗相关。靶向抑制LSD1可激活干扰素信号通路,诱导肿瘤的固有免疫原性,恢复MHC-I表达,并改善SCLC免疫反应性,证实了表观遗传学修饰在SCLC MHC-I表达及免疫治疗反应中的重要性。
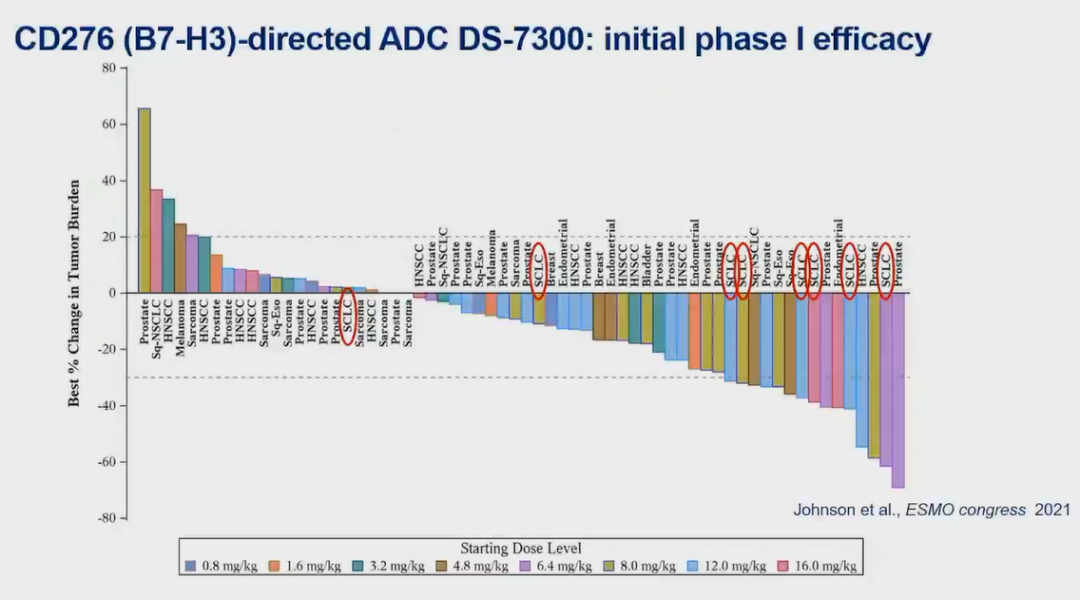
抗体偶联药物曙光初现
免疫治疗可改善SCLC患者预后,但仅有一小部分患者对免疫治疗有疗效反应,肿瘤细胞表面缺失MHC-I表达可能是SCLC患者免疫抵抗的重要原因。
Tarlatamab、细胞周期调控及表观遗传修饰靶向药物可通过促进SCLC抗原递呈,激活抗肿瘤免疫,与免疫治疗发挥协同抗肿瘤作用。
其他治疗策略如ADC类药物可能也是改善SCLC患者预后的潜在手段。

1. Noda K, Nishiwaki Y, Kawahara M, Negoro S, Sugiura T, Yokoyama A, et al. Irinotecan plus cisplatin compared with etoposide plus cisplatin for extensive small-cell lung cancer. N Engl J Med. 2002;346(2):85-91. doi: 10.1056/NEJMoa003034.
2. Lara PN, Jr., Natale R, Crowley J, Lenz HJ, Redman MW, Carleton JE, et al. Phase III trial of irinotecan/cisplatin compared with etoposide/cisplatin in extensive-stage small-cell lung cancer: clinical and pharmacogenomic results from SWOG S0124. J Clin Oncol. 2009;27(15):2530-2535. doi: 10.1200/jco.2008.20.1061.
3. Paz-Ares L, Chen Y, Reinmuth N, Hotta K, Trukhin D, Statsenko G, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer: 3-year overall survival update from CASPIAN. ESMO Open. 2022;7(2):100408. doi: 10.1016/j.esmoop.2022.100408.
4. Rudin CM, Poirier JT, Byers LA, Dive C, Dowlati A, George J, et al. Molecular subtypes of small cell lung cancer: a synthesis of human and mouse model data. Nat Rev Cancer. 2019;19(5):289-297. doi: 10.1038/s41568-019-0133-9.
5. Rudin CM, Liu SV, Lu S, Soo RA, Hong MH, Lee JS, et al. SKYSCRAPER-02: Primary results of a phase III, randomized, double-blind, placebocontrolled study of atezolizumab (atezo) + carboplatin + etoposide (CE) with or without tiragolumab (tira) in patients (pts) with untreated extensive-stage small cell lung cancer (ES-SCLC). Journal of Clinical Oncology. 2022;40(17). doi: 10.1200/JCO.2022.40.17_suppl.LBA8507.
6. Paz-Ares L, Champiat S, Lai WV, Izumi H, Govindan R, Boyer M, et al. Tarlatamab, a First-In-Class DLL3-Targeted Bispecific T-Cell Engager, in Recurrent Small Cell Lung Cancer: An Open-Label, Phase I Study. J Clin Oncol. 2023:Jco2202823. doi: 10.1200/jco.22.02823.
7. Mahadevan NR, Knelson EH, Wolff JO, Vajdi A, Saigí M, Campisi M, et al. Intrinsic Immunogenicity of Small Cell Lung Carcinoma Revealed by Its Cellular Plasticity. Cancer Discov. 2021;11(8):1952-1969. doi: 10.1158/2159-8290.Cd-20-0913.
8. Taniguchi H, Caeser R, Chavan SS, Zhan YA, Chow A, Manoj P, et al. WEE1 inhibition enhances the antitumor immune response to PD-L1 blockade by the concomitant activation of STING and STAT1 pathways in SCLC. Cell Rep. 2022;39(7):110814. doi: 10.1016/j.celrep.2022.110814.
9. Nguyen EM, Taniguchi H, Chan JM, Zhan YA, Chen X, Qiu J, et al. Targeting Lysine-Specific Demethylase 1 Rescues Major Histocompatibility Complex Class I Antigen Presentation and Overcomes Programmed Death-Ligand 1 Blockade Resistance in SCLC. J Thorac Oncol. 2022;17(8):1014-1031. doi: 10.1016/j.jtho.2022.05.014.
10. Rudin CM, Pietanza MC, Bauer TM, Ready N, Morgensztern D, Glisson BS, et al. Rovalpituzumab tesirine, a DLL3-targeted antibody-drug conjugate, in recurrent small-cell lung cancer: a first-in-human, first-in-class, open-label, phase 1 study. Lancet Oncol. 2017;18(1):42-51. doi: 10.1016/s1470-2045(16)30565.
排版编辑:肿瘤资讯-晴天











 苏公网安备32059002004080号
苏公网安备32059002004080号


