医路曼话,百家畅谈。一路走来,良医汇【肿瘤资讯】携手大连医科大学附属第二医院肿瘤内科李曼教授开展的系列乳腺癌线上培训课程——“半月曼谈”迎来了一周年。一年来,“半月曼谈”怀揣着对学术的无限追求,共同完成了对二十三个病例的探讨与交流,在此,“半月曼谈”诚挚感谢一直以来给予支持的各位专家与同道。

“半月曼谈”精品云课堂聚焦乳腺癌前沿研究、病理、影像、临床诊治等方面,以乳腺癌疑难病例讨论、诊疗经验分享、规范化指南解读等形式进行专题培训,整个系列课程邀请乳腺领域知名专家深入剖析、集思广益,广大中青年医师共同参与、全面提高乳腺癌的诊治水平,为难治性乳腺癌患者献计献策。同时,云课堂采用线上直播+课程制作的形式,让讨论更有参与感、传播度更广。
本期3月21日17:00,我们迎来了“半月曼谈”年度总结,特邀解放军总医院江泽飞教授、江苏省人民医院殷咏梅教授、中国医学科学院肿瘤医院袁芃教授、西安国际医学中心薛妍教授及复旦大学附属肿瘤医院范蕾教授担任客座嘉宾,并在会前作开幕致辞。





江泽飞教授表示,祝贺“半月曼谈”圆满走过一周年,一年以来,“半月曼谈”奉献了精彩的学术报告与深入的病例分析。期待未来在类似活动的引导下,各区域间加强医疗交流合作,共同提高诊疗水平,为患者提供更好的服务。
殷咏梅教授表示,“半月曼谈”作为一档每半月一次的优质学术交流平台,为患者带来了丰富的规范化诊疗帮助,希望未来该平台可以越做越好,开展更多类似的学术交流活动。
袁芃教授表示,很荣幸再次参加“半月曼谈”,一年以来,“半月曼谈”保持着稳定的更新,参与者收获颇丰。期待本次总结会后继续保持,未来带来更多精彩的病例分享,与各位同道在学习中共同提高进步。
薛妍教授表示,希望在李曼教授的带领下,“半月曼谈”可以越来越好,打造广受肯定的精品学术栏目,帮助广大医务工作者共同学习、进步。
范蕾教授表示,“半月曼谈”在疫情期间如一阵春风带来新鲜的气息,对临床疑难病例提供了专家视角解读,为患者带来更好的医学支持,期待“半月曼谈”越做越好。
周年回首——病例总结


本期“半月曼谈”周年特辑的学术研讨首先由大连医科大学附属第二医院徐岭植博士带来既往节目中的病例总结。一年以来,“半月曼谈”分享了二十三例疑难病例,邀请来自全国的乳腺专家提供指导,徐博士介绍了过往病例的病例特征,并从影像/病理疑难问题,IV期原发灶局部处理、转移灶局部处理以及全身治疗方案等四方面进行了深入总结与汇报。总体而言,“半月曼谈”涵盖了不同类型、不同分型乳腺肿瘤,涵盖了运行病例临床诊治的疑点和难点,总体9个月无进展生存(PFS)率达60%,总体一年总生存(OS)率达80%,尤其对于早线病情变化的患者,专家研讨带来的获益更加明显,晚期一/二线9个月PFS率和一年OS率均达到了100%,体现了“半月曼谈”举办的初衷和目的,切实为广大疑难重症患者带来了有效临床获益。
开启新生——前沿速递
 随后,殷咏梅教授分享了HER2阳性晚期乳腺癌治疗的排兵布阵。殷教授首先回顾了2022年HER2阳性乳腺癌治疗的重要进展,介绍了一线治疗中基于双靶的多项临床探索,以及二线治疗中创新抗体偶联药物(ADC)和酪氨酸激酶抑制剂(TKI)取得的最新数据,并基于临床研究就热点关注的T-DXd在临床使用中的疑问作出解答,指出更加前线的使用可带来更好的疗效。此外,针对脑转移和多线治疗进展后的用药策略,殷教授指出新型ADC药物同样是优选方案。
随后,殷咏梅教授分享了HER2阳性晚期乳腺癌治疗的排兵布阵。殷教授首先回顾了2022年HER2阳性乳腺癌治疗的重要进展,介绍了一线治疗中基于双靶的多项临床探索,以及二线治疗中创新抗体偶联药物(ADC)和酪氨酸激酶抑制剂(TKI)取得的最新数据,并基于临床研究就热点关注的T-DXd在临床使用中的疑问作出解答,指出更加前线的使用可带来更好的疗效。此外,针对脑转移和多线治疗进展后的用药策略,殷教授指出新型ADC药物同样是优选方案。

畅叙医情——病例分享
“畅叙医情”环节,大连医科大学附属第二医院赵姗姗博士分享了多处转移的三阳型晚期乳腺癌病例,患者在骨髓、全身多发骨及淋巴结转移的情况下,于晚期二线接受T-DXd治疗后取得接近CR疗效。专家们围绕该例患者的后续治疗方案进行了探讨。
病例资料
基本情况:
患者,女,37岁,未绝经。
现病史:
2019年4月因右乳肿物就诊。患者核磁共振如下图所示,可见乳腺占位及腋窝肿大淋巴结:(图一):
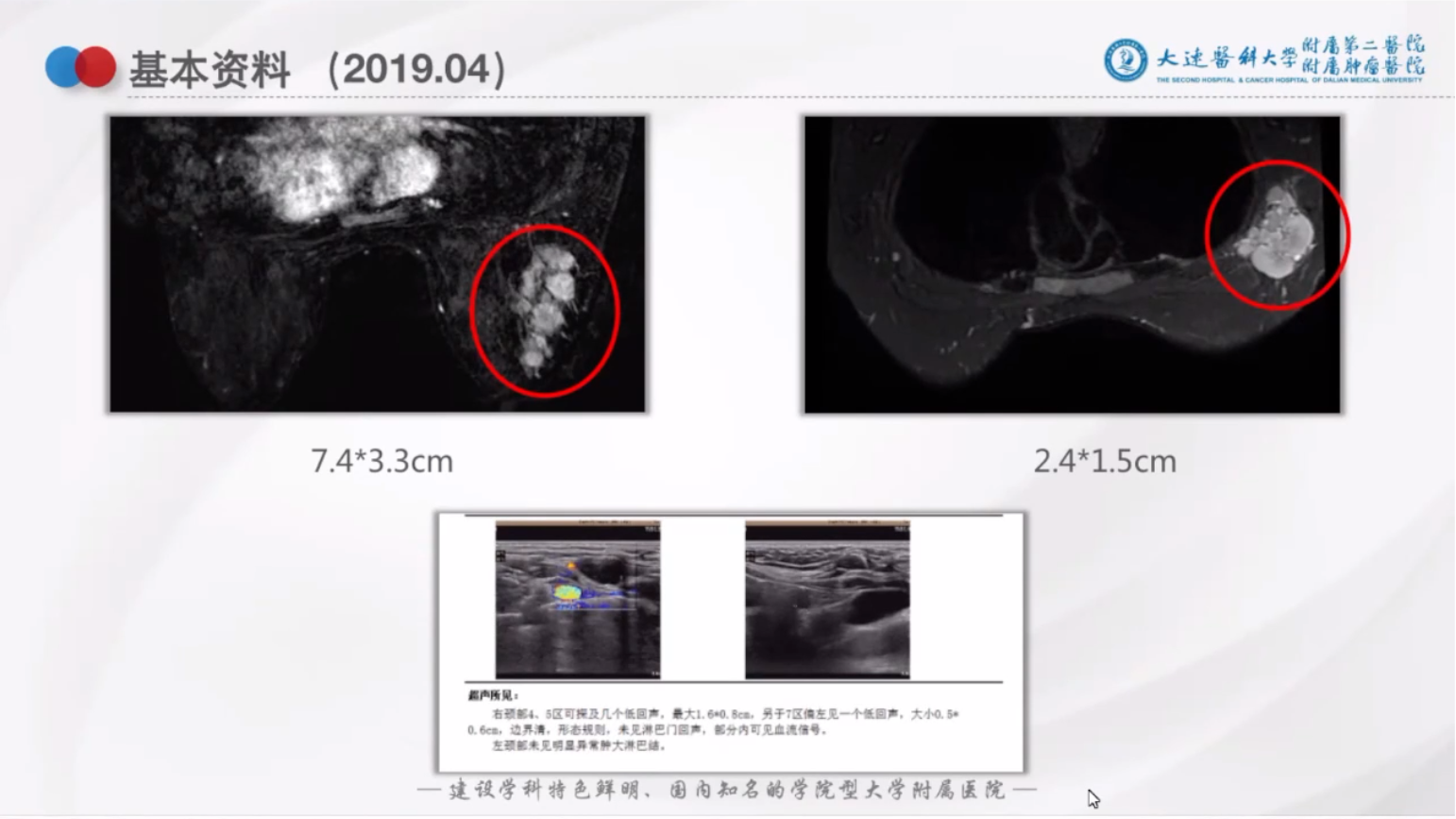
图一
穿刺活检病理如下:
(右乳肿物)腺癌;
(右腋窝淋巴结)纤维组织中可见腺癌;
(右颈部淋巴结)细胞学:可见成团的癌细胞
免疫组化:
乳腺:
ER(90%中等强度+),PR(<1%中等强度+),HER2(2+),Ki67(30%+)
FISH检测:阳性
腋窝:
ER(80%中等强度+),PR(1%中等强度+),HER2(2+),Ki67(30%+)
FISH检测:阳性
初步诊断:
右乳腺癌IIIC期 cT3N3M0
右腋窝、右锁骨上淋巴结转移
新辅助治疗:
EC-TH 8周期
疗效评估:
8周期后,患者乳腺病灶、腋窝淋巴结及颈部淋巴结出现明显缩小,最佳疗效评价达到持续PR。(图二)

图二
手术治疗:
2019-9-22行右侧保留乳头乳晕的乳腺癌改良根治术+I期乳房重建术
术后病理:
(右乳全腺体)乳腺癌新辅助化疗后标本:非特殊型浸润性乳腺癌2级,Miller-Payne(MP)评分3级,肿物大小1×0.7×0.8cm;
(腋窝淋巴结)未见癌转移 0/12;
免疫组化:ER(80%强+),PR(1%弱+),HER2(2+),Ki-67(3%+);
FISH检测:阳性
辅助治疗:
2019-11-13起行辅助放疗,剂量:PTV:50Gy/2.0Gy/25F,锁骨上加DT:10Gy。
放疗后行托瑞米芬内分泌治疗,继续曲妥珠单抗靶向治疗至2020-6。
2021-4 患者因背部疼痛就诊外院,胸椎MRI示:T6椎体及椎体根异常信号,肿瘤病变可能性大,后就诊我院,行ECT示第6胸椎小片状核素分布浓度,考虑骨转移。(图三)

图三
穿刺活检病理:
(骨 胸6椎)腺癌,结合免疫组化结果,符合乳腺癌来源;
免疫组化:GATA-3(+),Mamgb(乳球)(大部分+),ER(60%弱-中等强度+),PR(≤1%弱+),HER2(2+),Ki-67(20%+);
FISH检测:阳性。
修订诊断:
右乳癌术后 骨转移(胸6椎体)
右乳癌改良根治术后 IA期 ypT1N0M0
右乳腺癌IIIC期 cT3N3M0 右腋窝、右锁骨上淋巴结转移
病例特点:
年轻女性;
DFS:19个月;
胸椎单发骨转移;
其余脏器无转移病灶;
分子分型:三阳型。
曲妥珠单抗停药10个月。
手术干预:
2021-5-17 全麻下行胸椎后经皮胸5,7椎供根螺钉置入、钉棒系统内固定术+胸6椎体后凸成形术。
2021-6行局部放疗:PTV 40Gy/2.0Gy/20F。
完善检查:
2021-6行PET/CT示:胸6,7,12椎体、腰3椎体棘突、右髂骨、右坐骨、右侧耻骨联合、左股骨颈多发糖代谢异常增高灶,考虑转移,如下图所示如下图所示:(图四)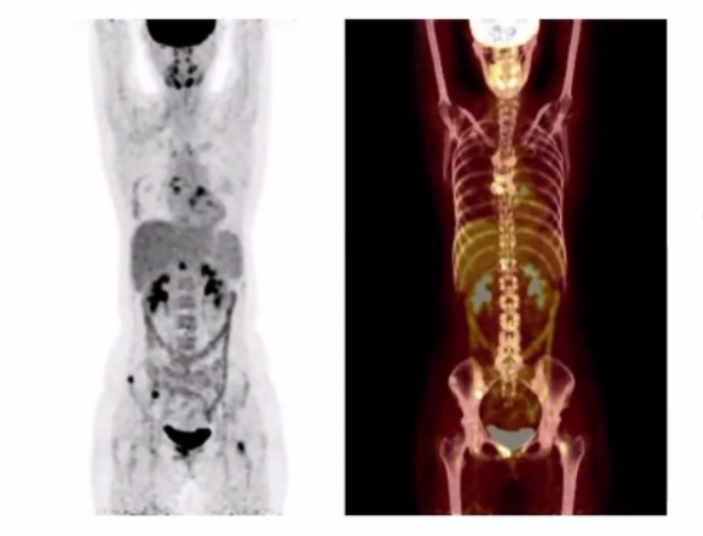
图四
CT辅助检查:
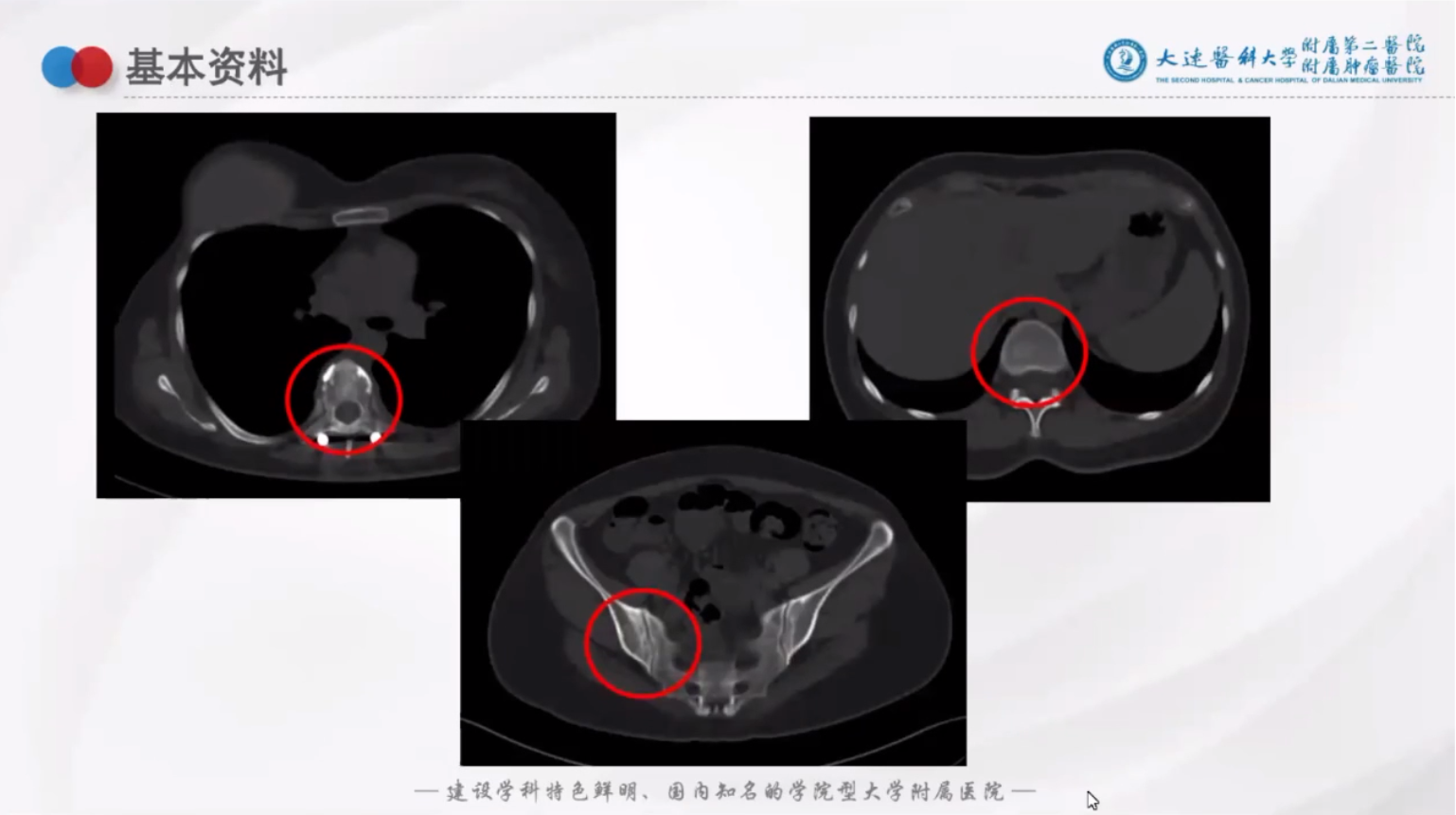
修订诊断:
右乳癌术后 多发骨转移
右乳癌改良根治术后IA期ypT1N0M0
右乳腺癌IIIC期cT3N3M0 右腋窝、右锁骨上淋巴结转移
晚期一线治疗:
吡咯替尼+卡培他滨
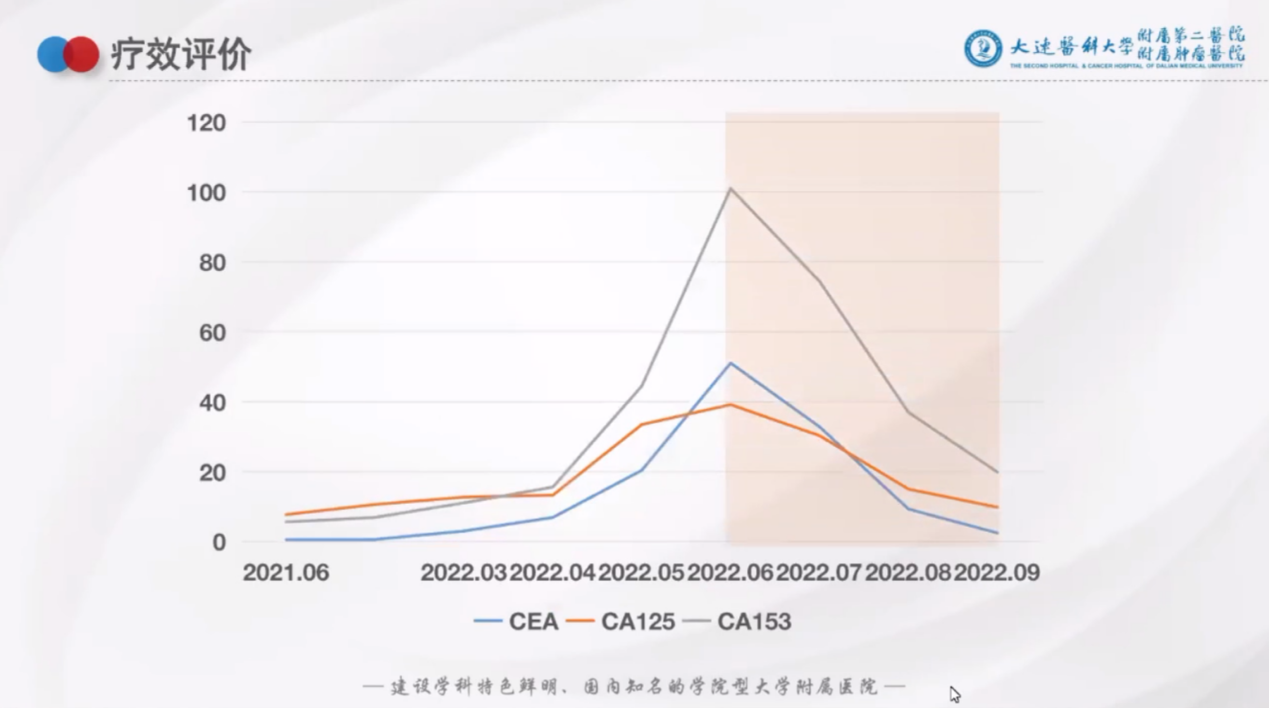
疗效评估:骨病灶逐渐修复,但治疗9个月时肿瘤标志物开始出现升高趋势并且患者出现周身疼痛的症状,如下图:
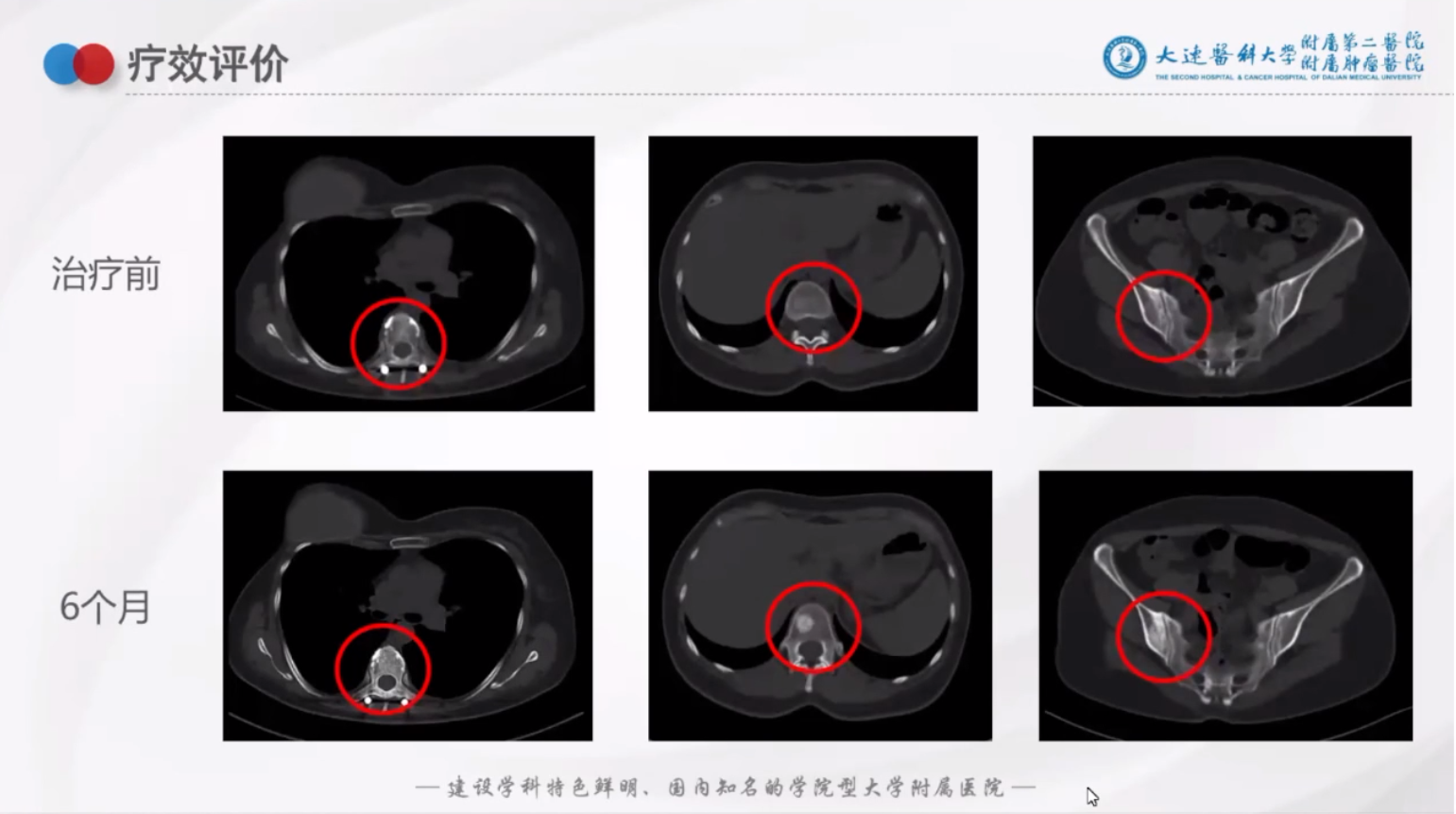
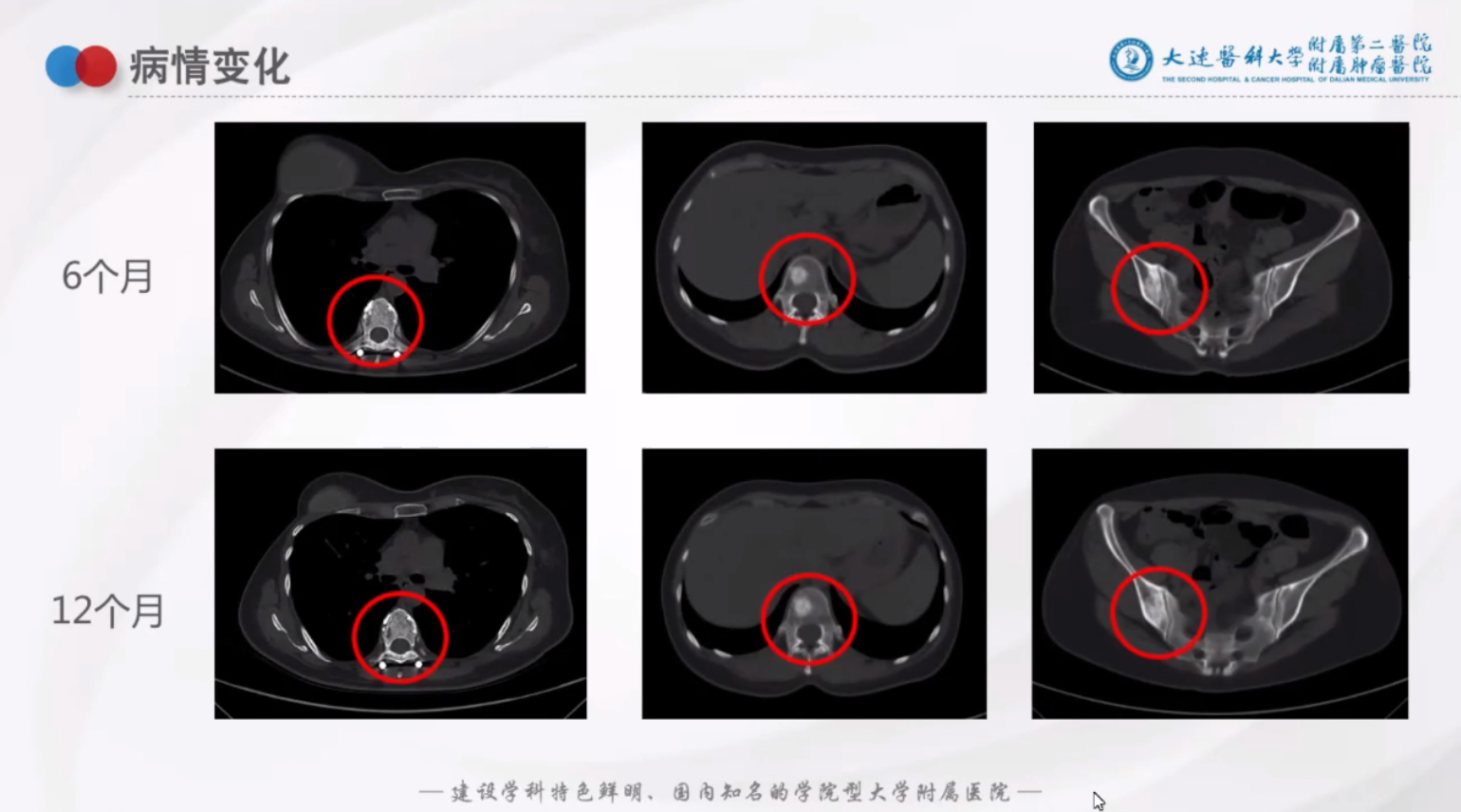
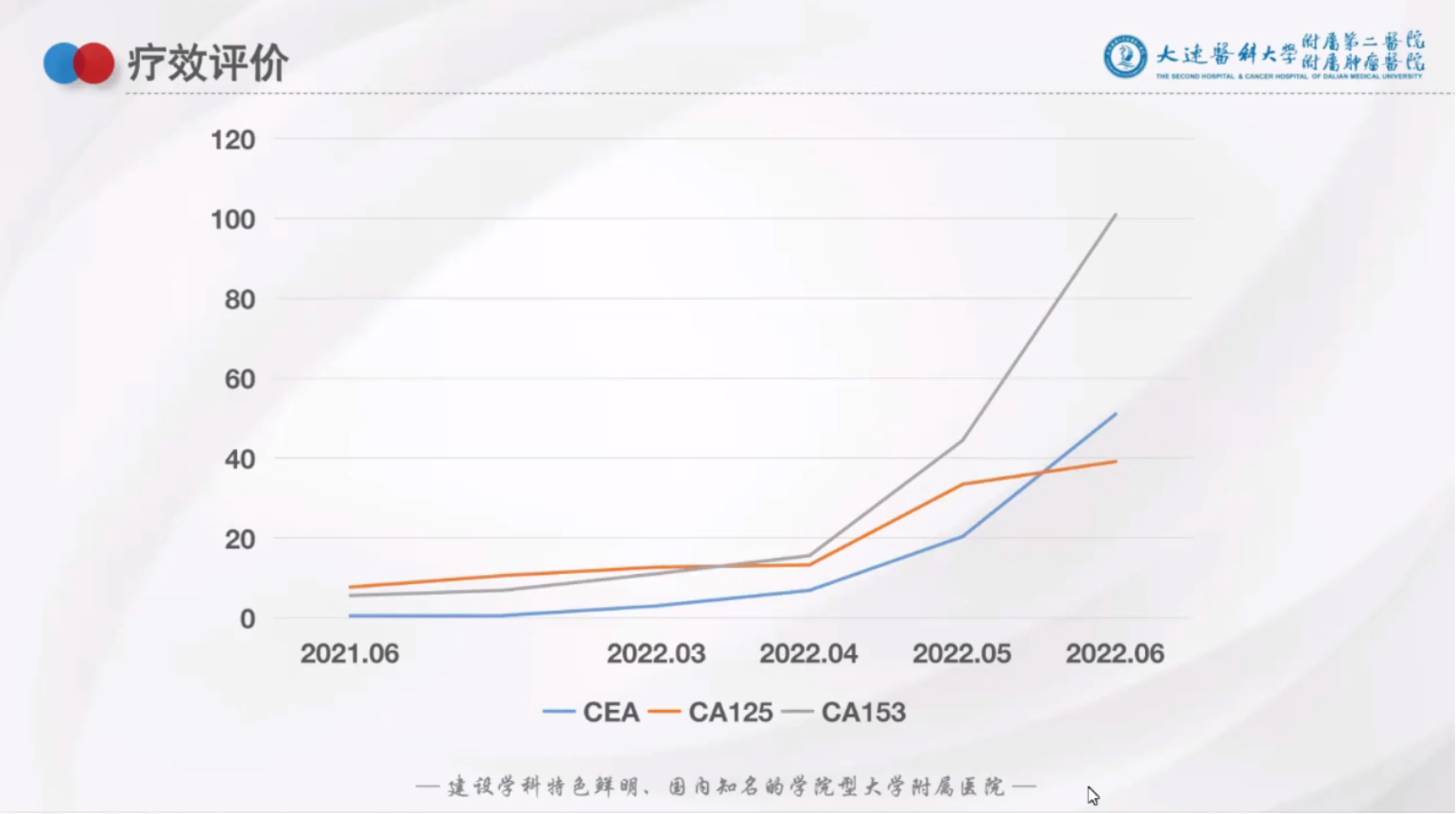
完善检查:
2022-6 患者行ECT检查,提示骨病灶进展:(图五)
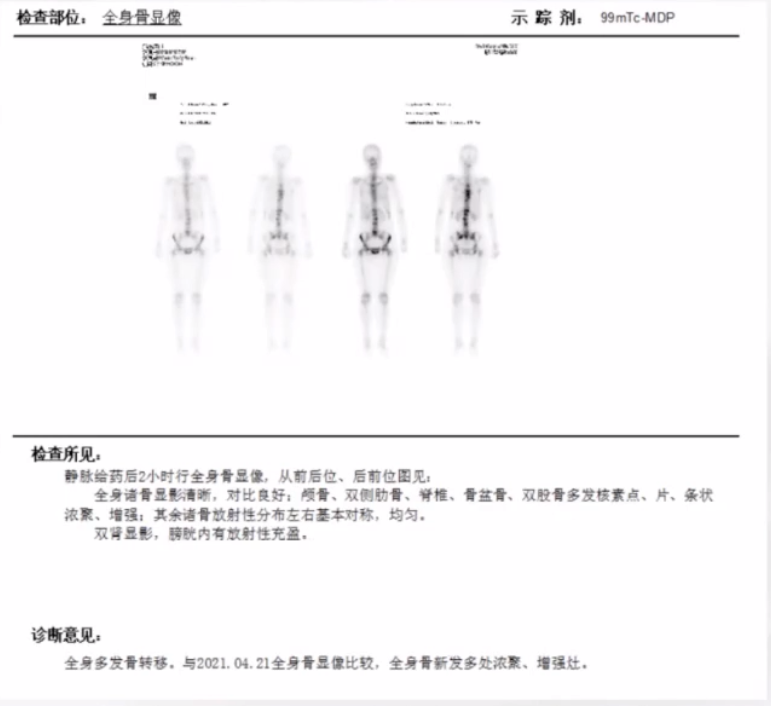
图五
2022-6 完善PET/CT检查显示:
 2022-6 完善骨髓穿刺细胞学检查,结果示:转移癌骨髓象。
2022-6 完善骨髓穿刺细胞学检查,结果示:转移癌骨髓象。
修订诊断:
右乳癌术后 骨髓转移 多发骨转移 多发淋巴结转移
右乳癌改良根治术后IA期ypT1N0M0
右乳腺癌IIIC期cT3N3M0 右腋窝、右锁骨上淋巴结转移
更新病例特点:
年轻女性;
DFS:19个月;
PFS1:12个月;
骨髓、骨、淋巴结转移;
分子分型:三阳型
既往应用曲妥珠单抗、吡咯替尼。
晚期二线治疗:
T-DXd
疗效评估:
患者骨痛缓解;CT提示骨病灶修复;肿瘤标志物下降,如下图: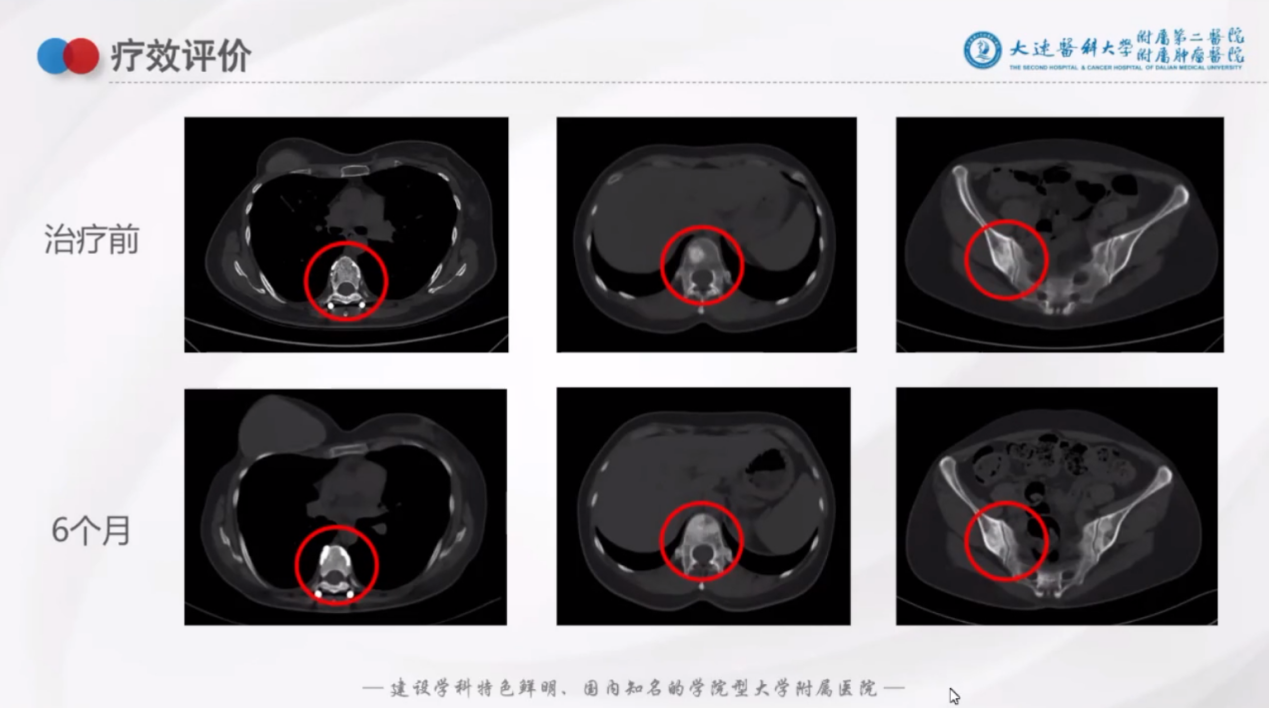
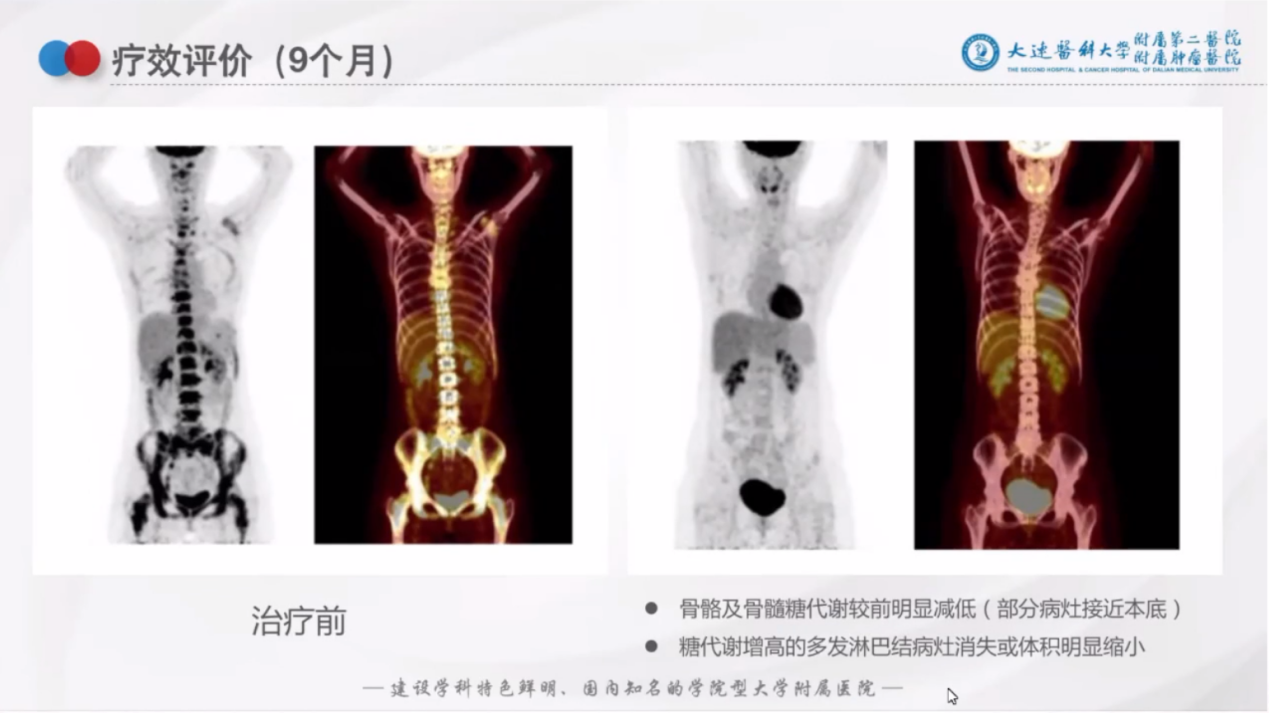
治疗9个月后,复查PET/CT,如下图所示:
 完善骨髓穿刺细胞检查,结果示:未见肿瘤细胞。
完善骨髓穿刺细胞检查,结果示:未见肿瘤细胞。
疗效评价:接近CR。
问题讨论:
1)患者术后复发,仅有第6胸椎骨转移,其他脏器无转移病灶,应当如何治疗?应当首先全身治疗还是首先局部治疗?
2)患者经过晚期一线系统治疗后,骨髓、全身多发骨及淋巴结转移,下一步应如何治疗?
3)患者经T-DXd晚期二线治疗后,接近CR疗效,但因经济条件受限无法继续接受T-DXd治疗,下一步治疗方案应如何选择?应停药观察还是换药维持治疗??
集思广医—众专家各抒己见
在讨论环节中,薛妍教授、范蕾教授及袁芃教授各自分享了对该病例的见解。
薛妍教授:患者初诊时已达到IIIC期,存在锁骨上淋巴结转移,新辅助治疗取得了不错的疗效,虽然术后曲妥珠单抗辅助治疗结束10个月后复发,但可能并不是对曲妥珠单抗完全耐药。患者单发骨转移时,由于未存在椎体压迫、骨折等问题,因此全身治疗与局部治疗的取舍并无明确矛盾,可根据局部治疗方式的选择进行全身+局部的治疗。应与骨科进行会诊,判断手术紧迫度,如手术迫切性较强,应优先考虑局部治疗,否则可考虑在全身治疗兼顾的前提下考虑结合局部治疗手段。患者晚期一线接受吡咯替尼+卡培他滨治疗后出现骨髓转移、多发骨转移,骨髓转移可能为造血功能带来障碍,影响后续治疗,因此后续应考虑抗体偶联药物(ADC)如T-DXd,如患者经济条件受限,也可考虑双靶+化疗。T-DXd的晚期二线治疗取得了良好的疗效,患者因经济条件无法接受T-DXd治疗,后续可选双靶+内分泌治疗(OFS、AI或氟维司群)维持治疗,暂不考虑增加CDK4/6抑制剂。
 薛妍教授
薛妍教授
范蕾教授:该患者无瘤间期较短,根据不同临床研究中可能有不同判断,因此很难判断是否对曲妥珠单抗耐药。患者接受病理活检明确新发的单发骨转移病灶为转移病灶,且分型为三阳型,考虑其分期,治疗应以全身治疗为主,而且针对单发骨转移的局部治疗并不会影响全身治疗,特别是患者骨转移瘤位于承重骨,可能带来骨相关事件的风险,因此可以考虑手术干预。患者在吡咯替尼联合卡培他滨晚期一线治疗后发生耐药,后续治疗可考虑ADC如T-DXd。患者在接受T-DXd治疗后取得很好的疗效,疗效评价接近CR,在患者因经济原因暂停治疗后,由于缺乏可评估病灶,可选择较为温和的内分泌治疗联合双靶治疗。T-DXd在临床研究中,也有部分患者未持续用药至进展,具体用药周期有待进一步研究。 范蕾教授
范蕾教授
袁芃教授:对于该患者而言,再出现肿瘤复发之后,全身治疗优先级更高。如因骨转移出现症状,或有迫切需求防止骨相关事件的发生,再考虑优先局部治疗。所以整体而言,应以全身治疗为主。目前看来,应继续采取内分泌联合双靶抗HER2治疗,部分研究可能推荐采取化疗联合内分泌治疗,但考虑患者仅为单发病灶,更推荐抗HER2治疗联合内分泌治疗。患者晚期一线治疗后骨髓受侵,应通过检查明确造血功能是否受到影响,ADC类药物T-DM1或T-DXd都有导致骨髓抑制的风险,可依据患者造血功能的状态考虑双靶联合内分泌治疗。考虑患者未出现危及生命的内脏转移,可暂不考虑化疗。当双靶联合内分泌治疗一段时间后,如患者造血功能正常,也可尝试调整至ADC类药物。晚期二线T-DXd治疗后,患者肿瘤负荷较低,PET/CT显示了全身多处转移病灶的缓解,取得了很好的治疗效果,继续坚持下去或可取得更好的疗效。但患者因经济原因无法继续接受治疗,可选择双靶联合内分泌治疗,可依据患者个体情况尝试增加不良反应较轻的CDK4/6抑制剂以取得更好的疗效。

袁芃教授
名医点睛——殷咏梅教授总评
殷咏梅教授:临床实践中,对于HER2阳性乳腺癌患者,随着越来越多的抗HER2靶向治疗药物问世,患者有了更多的用药选择。对于HER2+/HR+患者,可在无法耐受化疗的前提下,或在化疗耐药后,可以考虑使用抗HER2靶向治疗联合内分泌治疗。但当下对于抗HER2治疗的选择,仍存在很多问题。例如ADC药物与TKI药物皆可在患者对另一种治疗方式耐药后作为后线选择,但TKI与ADC的优先级暂无定论,临床上很难解答这一难题。疗效更好的创新药物上市后究竟应尽量推向前线还是在后线使用,目前尚无答案。每个创新药物都在试图向前线推进,甚至在新辅助治疗、辅助治疗中取进行应用,但若将创新药物应用于前线,那么在患者新辅助治疗未达pCR,或晚期一线治疗进展后应如何用药?对于创新药物的排兵布阵,临床上仍需大量研究以给出答案,我们希望通过合理用药为患者取得最长的生存,达到最好的生活质量。
 殷咏梅教授
殷咏梅教授
本次云课堂周年回顾云集多位国内乳腺癌专家,不仅回顾了“半月曼谈”二十三期的过往病例,还分享了抗HER2靶向治疗前沿进展,并围绕一例三阳型乳腺癌病例展开了抗HER2治疗用药序贯的讨论。讨论过程中各位专家谓畅所欲言,分享了各自的真知灼见。相信本次课程也让大家对HER2阳性乳腺癌的诊疗有了更深入的了解。走过一年,“半月曼谈”与你相伴学习,未来日子里,更多精品课程将继续呈现,精彩不断,欢迎持续关注!
排版编辑:肿瘤资讯-xiaodong











 苏公网安备32059002004080号
苏公网安备32059002004080号


