手术是可切除非小细胞肺癌(NSCLC)达到根治的最佳手段,然而术后复发依旧是常见临床难题。新辅助免疫联合化疗可改善此类患者的近期和远期结局,而对于不能化疗的患者,尚无有效新辅助治疗方案。近日,中国医学科学院肿瘤医院赫捷院士团队的一项Ⅱ期研究显示卡瑞利珠单抗+阿帕替尼新辅助治疗方案具有良好活性和安全性,该研究结果已发表在J Thorac Oncol(IF=20.121)上。

研究背景
30%~77%仅行手术的NSCLC患者会发生术后复发,微转移灶可能是复发的主要原因。新辅助治疗可能有助于降低肿瘤大小,增加手术切除机会,消除微转移灶。新辅助化疗并未显著改善患者结局,需要更为有效的新辅助治疗策略。
免疫治疗为NSCLC的治疗带来了突破性变革。CheckMate 816研究显示和单纯化疗相比,新辅助纳武利尤单抗联合化疗具有更高的病理完全缓解率(pCR)(24.0% vs 2.2%),并可显著延长无事件生存(EFS)。而对于不能耐受或拒绝化疗的患者,还需要积极探索有效新型治疗方案。因此进行Ⅱ期研究评估卡瑞利珠单抗联合阿帕替尼新辅助治疗可切除NSCLC患者的活性和安全性。
研究方法
这是一项前瞻性单臂Ⅱ期研究。纳入的是初治ⅡA~ⅢB期NSCLC患者(ⅢB期仅T3N2,AJCC第8版)。除外已知EGFR突变患者。患者接受3周期卡瑞利珠单抗+阿帕替尼治疗,完成新辅助治疗后3~4周手术。术后4~8周行卡瑞利珠单抗单药辅助治疗12周期,研究者决定是否行其他辅助治疗。主要研究终点是疗效分析集(EAS)的主要病理缓解(MPR)率。次要终点包括病理完全缓解(pCR)率、客观缓解率(ORR)、疾病控制率(DCR)、无病生存期(DFS)、EFS和安全性。
研究结果
患者和治疗
78例患者入组。51%患者为Ⅲ期,其中14%为可切除ⅢB期。76%患者为鳞状细胞癌,35%为N2淋巴结受累,14%患者PD-L1 TPS≥50%。
手术总结
65例(83%)患者行手术切除,纳入EAS。65例患者中,57%行胸腔镜手术,5%初始为胸腔镜手术,转为开胸手术。中位手术持续时间143分钟。100%患者为R0切除。5例(8%)患者延迟手术,其中2例是因为不良事件(AE),3例因为新冠影响。
手术并发症发生率为11%,最常见是肺炎(5%)。1例(2%)患者术后30天内因呼吸衰竭死亡,1例(2%)在术后30~90天不明原因死亡。中位术后住院时间是8天。
疗效
EAS中,MPR率为57%,其中3例(25%)为腺癌,34例(64%)为鳞癌。pCR率为23%,均为鳞癌患者。鳞癌患者的pCR率为28%。新辅助治疗后,2例(3%)患者达到影像学完全缓解(CR),32例(49%)患者为部分缓解(PR),影像学ORR为52%。
全分析集(FAS)中,MPR率为47%,pCR率为19%。59例鳞癌患者中,MPR率为58%,pCR率为25%;19例腺癌患者中,MPR率为16%,pCR率为0。影像学ORR为47%,包括2例(3%)CR和35例(45%)PR。3例(4%)患者在新辅助治疗期间疾病进展(表1,图1)。
表1 肿瘤反应
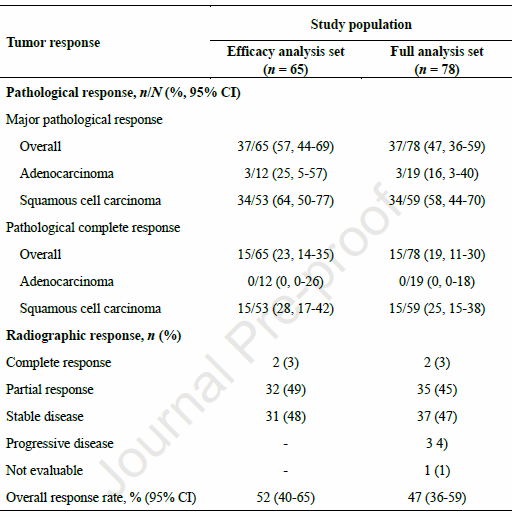
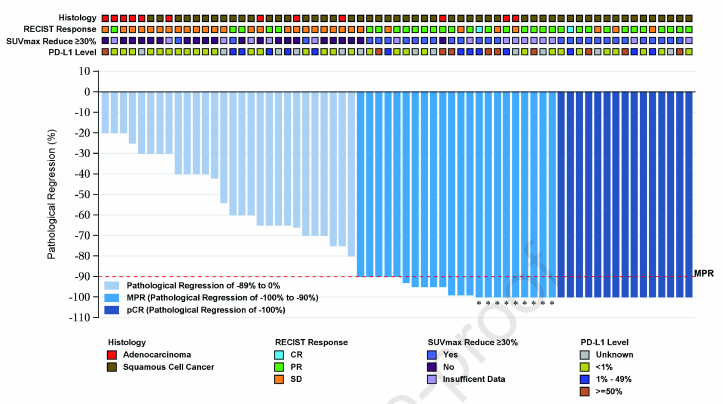
图1 肿瘤反应情况
安全性
新辅助治疗期间,78%患者发生治疗相关AE(TRAE),最常见的是低蛋白血症(24%)、蛋白尿(23%)和天冬氨酸氨基转移酶升高(23%)。免疫介导AE中,最常见的是1~2级甲状腺功能亢进(13%)和甲状腺功能减退(6%)。4例(5%)患者发生3级TRAE,高血压、肌酸激酶升高、食欲减退和自身免疫性胰腺炎各1例(1%)。
8%的患者因蛋白尿、咳嗽、咯血、肌酸激酶升高、自身免疫性胰腺炎和自身免疫性心肌炎延迟新辅助治疗。没有治疗相关死亡报道。1例患者在2周期卡瑞利珠单抗治疗后死于急性心肌梗死,认为和新辅助治疗无关。
PET-CT影像学参数和MPR的相关性
61例(78%)患者术前具有PET-CT评估,其中50例(82%)行手术切除。术前PET-CT评估显示26例(52%)患者具有部分代谢反应(PMR),1例(2%)患者具有完全代谢反应(CMR),其中25例(93%)为MPR。此外,SUVmax降低和病理退缩具有显著相关性(R=0.619,P<0.0001,图2)。根据受试者工作特征(ROC)曲线,预测MPR的最高敏感性(93%)和特异性(91%)见于SUVmax降低32%。37例接受手术具有MRP的患者中,28例(76%)术前SUVmax≤6。ROC分析显示预测MPR的最佳术前SUVmax界值是6.9,最高敏感性是81%,特异性是93%。
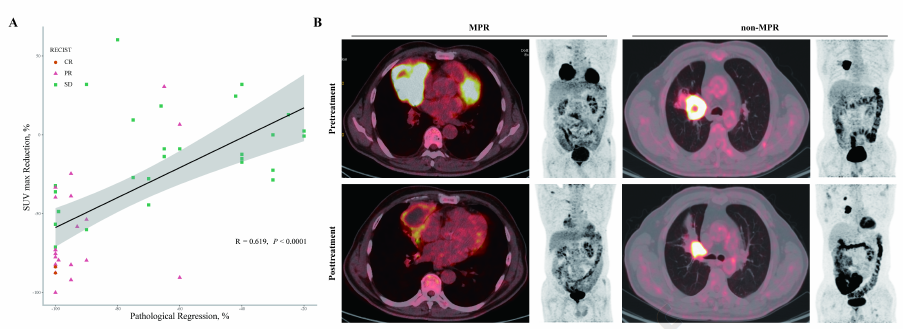
图2 PET-CT和反应相关性
新辅助治疗病理反应的生物标志物分析
30例PD-L1<1%的患者中,13例(43%)达到MPR,其中7例(23%)达到pCR。PD-L1≥50%的患者具有更多肿瘤退缩,MPR率为90%,pCR率为30%。此外,和疾病稳定(SD)/进展(PD)(P=0.05)和未达到MPR(P=0.0088)的患者相比,影像学CR/PR和MPR患者具有更高的治疗前PD-L1表达(图3)。
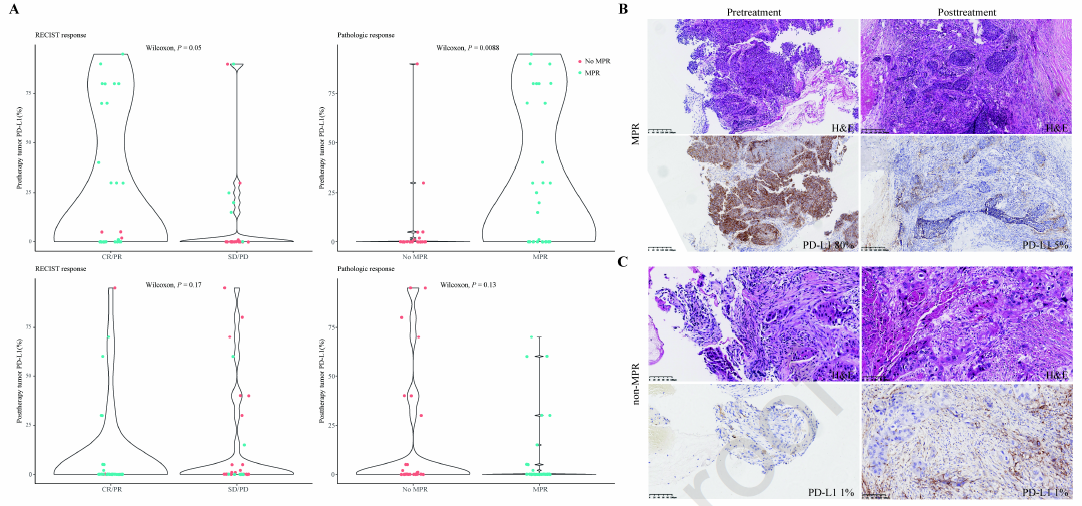
图3 PD-L1和反应相关性
65例手术患者行二代测序(NGS)。MRP患者中,TP53是最常见的异常基因,而MCL1是未达到MPR患者中最常见的异常基因。pCR患者中,5种最常见的异常基因包括PTEN、DHD8、AXL、NTRK2和INPP4B。此外,具有高肿瘤突变负荷(TMB)的患者具有更佳MRP和pCR的趋势,尽管未达到显著性。
对比病理反应患者和无反应患者的ctDNA浓度和不同时间点(治疗前[TP0],新辅助治疗第2周期前[TP1],第3周期前[TP2]和术前[TP3])动态变化。未达到pCR/MPR的患者具有更高的术前ctDNA浓度。和未达到MRP/pCR患者相比,MPR/pCR患者在TP2和TP3的ctDNA阳性比例明显降低。13例TP3 ctDNA阳性患者,100%术后具有残留病,31%达到MPR。33例ctDNA阴性患者中,45%达到pCR,55%为MPR。结果表明术前ctDNA状态可能是新辅助治疗病理反应的潜在预测因子。
筛选出18个具有预后意义的分化甲基化区域(DMRs),这些DMRs在MRP和未达到MPR患者中具有显著差异。MPR组HOXA9和SEPT9的治疗前CpG部位甲基化水平显著低于非MPR组。15例HOXA9和SEPT9甲基化水平低于中位值的患者中,14例(93%)获益于新辅助治疗,而高于中位值患者中仅20%获益。结果提示治疗前HOXA9和SEPT9甲基化可能是新辅助治疗的独立预后预测因素。
讨论
这是第一个用于可切除NSCLC患者的“去化疗”新辅助治疗方案。研究达到主要终点,MPR率为57%,pCR率为23%。治疗相关毒性可控,未报道新的安全性信号。预测病理反应的生物标志物有助于发现潜在获益人群。
大多数新辅助临床研究中,MPR和pCR被认为是生存的替代终点。小型单臂新辅助化疗免疫治疗研究显示可切除Ⅰ~Ⅲ期肿瘤中MPR为26.9%~58.6%,pCR率为19.2%~34.5%。该研究中,对于可切除ⅡA~ⅢB期NSCLC患者,新辅助卡瑞利珠单抗+阿帕替尼具有良好病理结果。但是由于研究设计和入组人群的不同,研究间应谨慎对比。
腺癌和鳞癌患者间的新辅助免疫治疗反应存在矛盾。NADIM研究显示纳武利尤单抗+化疗在腺癌患者中具有更高的MPR和pCR率,而其他研究显示出相反结果。该研究中鳞癌患者具有更高的MPR和pCR率。PET-CT在免疫治疗中的预测作用还不成熟。当前研究中,代谢反应和MPR之间观察到相同的预测效应,SUVmax降低和病理反应之间的显著相关性。生物标志物方面,研究发现随着PD-L1表达增加,MPR率增加;ctDNA浓度和状态可早期预测病理反应;HOXA9和SEPT9甲基化水平具有MPR的潜在预测价值。这些结论还需要在大样本量研究中证实。
研究局限性在于研究为单中心小样本量研究,缺乏对照组,生存随访时间不足,主要终点MPR仅是替代终点,生物标志物结果是探索性。但是研究初步证实新辅助卡瑞利珠单抗+阿帕替尼在可切除NSCLC患者中具有良好MPR,毒性可控。病理反应潜在预测生物标志物可初步发现不需要新辅助化疗的患者。需要继续进行随机研究验证这些结果。
Zhao J, et al. Efficacy, Safety, and Biomarker Analysis of Neoadjuvant Camrelizumab and Apatinib in Patients with Resectable Non-Small-Cell Lung Cancer: A Phase 2 Clinical Trial. J Thorac Oncol. 2023;S1556-0864(23)00161-2.
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


