医路曼话,百家畅谈。01月10日17:00良医汇【肿瘤资讯】携手大连医科大学附属第二医院肿瘤内科李曼教授开展的系列乳腺癌线上培训课程——“半月曼谈”第二十期如期举行。

“半月曼谈”精品云课堂聚焦乳腺癌前沿研究、病理、影像、临床诊治等方面,以乳腺癌疑难病例讨论、诊疗经验分享、规范化指南解读等形式进行专题培训,整个系列课程邀请乳腺领域知名专家深入剖析、集思广益,广大中青年医师共同参与、全面提高乳腺癌的诊治水平。同时,云课堂采用线上直播+课程制作的形式,让讨论更有参与感、传播度更广。
本期01月10日17:00的精品云课堂可谓菁英云集,邀请了中国医学科学院肿瘤医院马飞教授担任特邀顾问,中国人民解放军总医院赵卫红教授、中国科学院大学附属肿瘤医院郑亚兵教授、北京大学肿瘤医院严颖博士担任指导嘉宾。


 课程伊始,李曼教授介绍了“半月曼谈”栏目开设的主旨,并由大连医科大学附属第二医院李曼教授和孙思文博士进行病例分享和讨论,各位专家教授针对相关议题各抒己见,开展深入对话。
课程伊始,李曼教授介绍了“半月曼谈”栏目开设的主旨,并由大连医科大学附属第二医院李曼教授和孙思文博士进行病例分享和讨论,各位专家教授针对相关议题各抒己见,开展深入对话。

畅叙医情——病例分享
在接下来的“畅叙医情”环节,大连医科大学附属第二医院孙思文博士为大家分享了一例激素受体阳性HER2低表达的右乳腺癌伴全身多发转移患者,在经过两线化疗和两线内分泌治疗以及T-DXd治疗后均进展的病例,专家们围绕该例患者的治疗抉择进行了探讨。

基本情况:
患者某某,46岁,月经规律,无特殊既往病史及家族史。
现病史:
2018.8.21患者因“腰背部疼痛、行走困难”就诊血液科。
CT检查:
CT提示多发溶骨性骨质破坏,脑、肺、腹部未见异常。
胸11椎体穿刺活检:
肿瘤细胞ER(90%中-强阳),PR(1%弱阳性),HER2(2+),ki67指数为15%。
右乳超声:
右乳实性结节(BI-RADS 4C 级,癌?),右腋下肿大淋巴结,最大3.1*1.7cm。
右乳MRI:
右乳肿物(29mm*28mm)BI-RADS 5,右腋下多发肿大淋巴结,考虑转移(图1)。
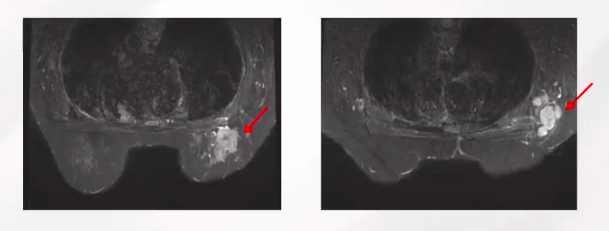
图1: 右乳MRI
骨扫描ECT:
第8、9、11胸椎,左后第11肋、第3、4腰椎、骶骨多发点、片状核素浓聚,诊断意见,考虑为恶性肿瘤多发骨转移(图2)。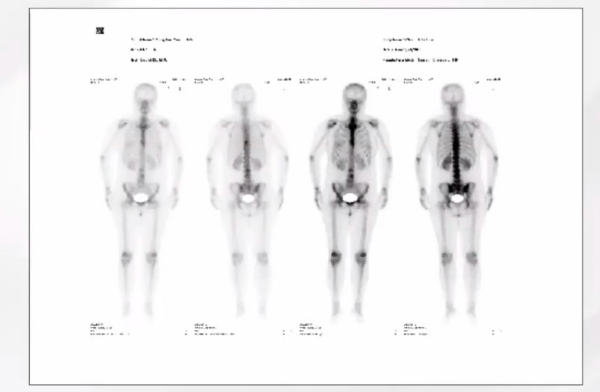
图2: 骨扫描ECT
诊断:
右乳腺癌 右腋窝淋巴结转移 骨转移 Ⅳ期 cT2N2M1
一线治疗:
多西他赛+卡培他滨6个周期序贯卡培他滨单药维持,同时,予双膦酸盐
一线疗效评估:
右乳结节:多西他赛+卡培他滨2个周期达到部分缓解(PR),维持治疗阶段达到完全缓解(CR)(图3)。
 图3: 右乳结节一线治疗后疗效评估
图3: 右乳结节一线治疗后疗效评估
右腋窝淋巴结:
右腋窝淋巴结:2个周期治疗后出现显著退缩,在维持治疗阶段仅有微小残留(图4)。
 图4: 右腋窝淋巴结一线治疗后疗效评估
图4: 右腋窝淋巴结一线治疗后疗效评估
骨扫描ECT:
2周期治疗后,骨转移的软组织病灶显著缩小,在维持治疗阶段,向成骨进一步转换(图5)。
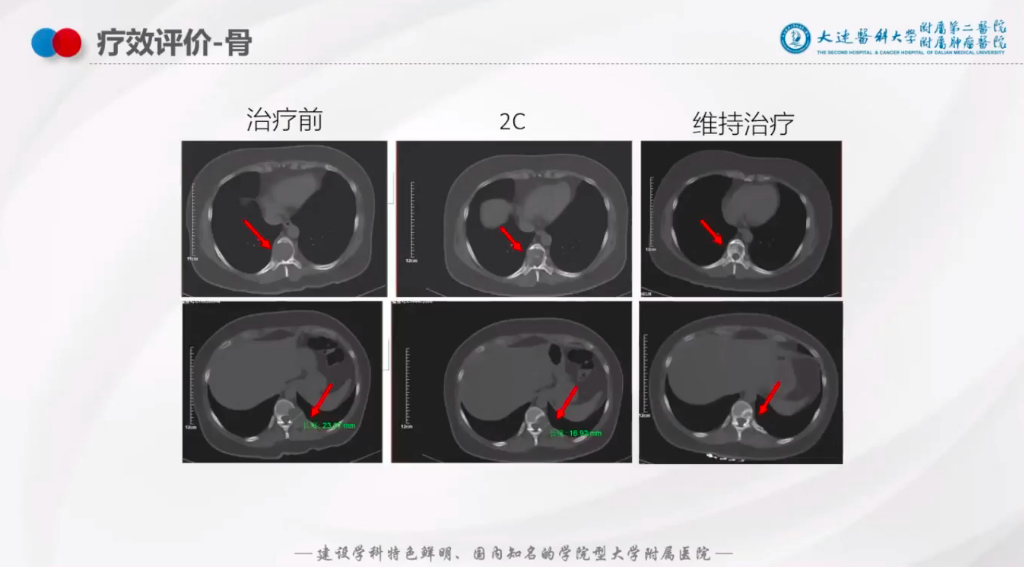
图5: 骨一线治疗后疗效评估
病情首次复发:
2019.11超声提示右乳再次出现实性结节(BI-RADS 5),大小约为1.2*0.7cm,形态欠规则;
2019.11 胸部CT提示右腋窝淋巴结较前增大,同时,溶骨性骨质破坏略有加重;
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 Ⅳ期 cT2N2M1,病情进展,TTP1:15个月。
二线治疗:
哌柏西利+来曲唑+卵巢功能抑制(OFS)
二线治疗疗效评估:
右乳肿物:治疗4个月之后缩小,评估为疾病稳定(SD),治疗1年后评估为CR(图6);
 图6: 右乳肿物二线治疗后疗效评估
图6: 右乳肿物二线治疗后疗效评估
右腋窝淋巴结:
在治疗1年后,仅有微小残留(图7);
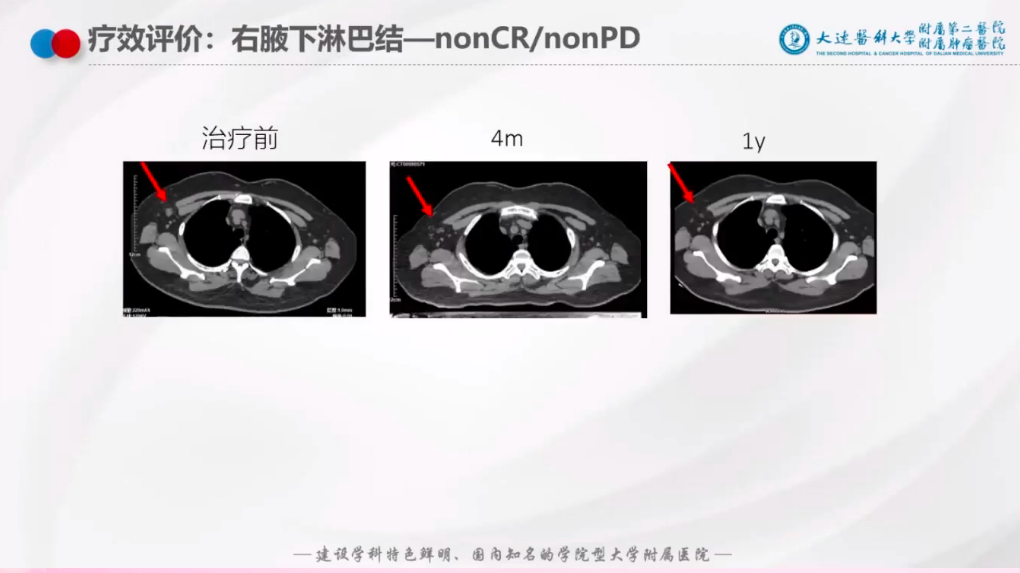
图7: 右腋窝淋巴结二线治疗后疗效评估
骨扫描ECT:
在内分泌治疗阶段以成骨改变为主,呈现稳定状态(图8);
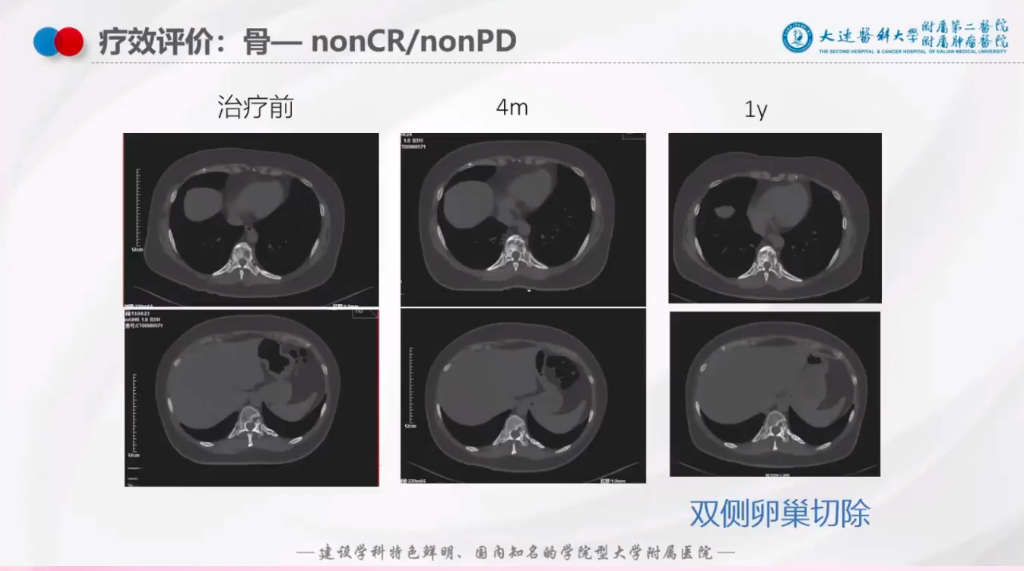
图8: 骨二线治疗后疗效评估
手术:
患者在二线治疗1年后,接受了双侧卵巢切除。
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 Ⅳ期 cT2N2M1,乳腺病灶CR,腋窝淋巴结微小残留(nonCR/nonPD),骨病灶向成骨转化 (nonCR/nonPD);
病情二次复发:
2022.2乳腺、骨病灶稳定,但是,胸部CT提示双肺多发转移瘤,右腋窝淋巴结增大。
肺穿刺活检:
可见腺癌,符合乳腺癌来源。
免疫组化结果:
ER( >90%弱-中等强度阳),PR(约5%弱阳性),HER2(1+),ki67指数为30%+,GATA-3(+)、Mamgb(乳球)(-),雄激素受体(AR)(-);
基因检测:
未见PIK3CA突变。
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 肺转移,病情进展,TTP2:27个月。
三线治疗:
依维莫司+氟维司群
三线治疗疗效评估:
右腋窝淋巴结:治疗后3个月时较前缩小,但是,第5个月时,较前增大(图9);
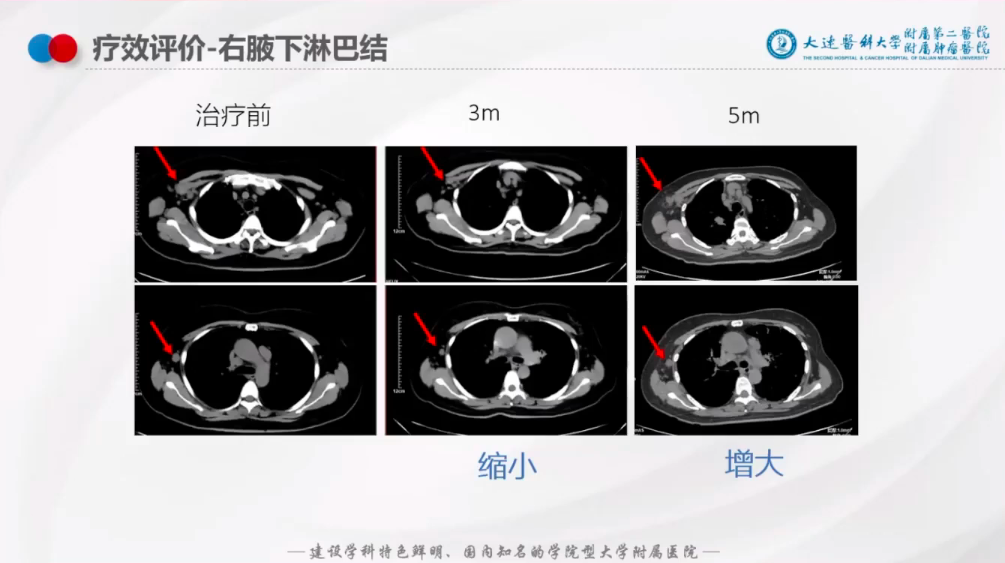
图9: 右腋窝淋巴结三线治疗后疗效评估
肺:治疗后3个月较前缩小,疗效评估SD,但是,第5个月时,疾病进展(图10);
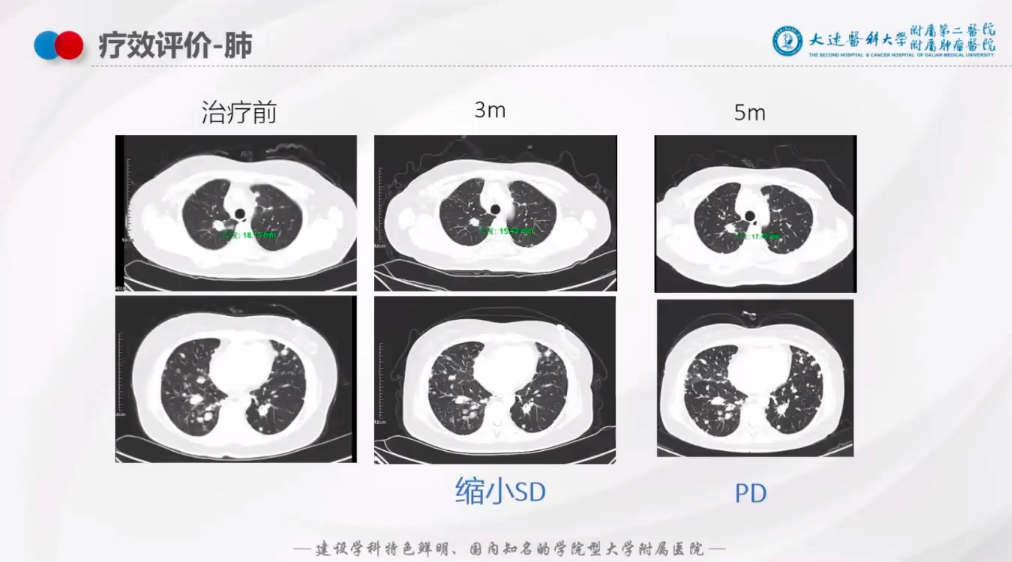
图10: 肺三线治疗后疗效评估
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 肺转移,病情进展,TTP3:5个月。
四线治疗:
艾立布林
四线治疗疗效评估:
肺:治疗后2个周期,呈现PD(图11);
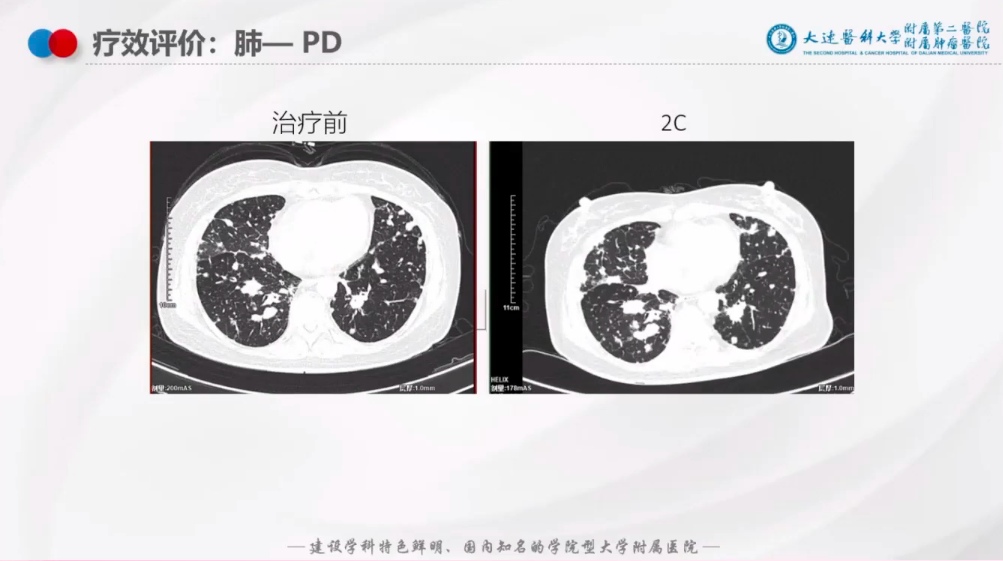
图11: 肺四线治疗后疗效评估
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 肺转移,乳腺、左腋窝淋巴结、骨病灶稳定,肺病灶进展,TTP4:2个月;
五线治疗:
T-Dxd;
五线治疗疗效评估:
肺:治疗4个周期之后呈现缩小的SD,但是,在6个周期之后出现疾病进展(图12);

图12: 肺五线治疗后疗效评估
右侧腋窝:腋窝淋巴结呈现增大的趋势(图13);
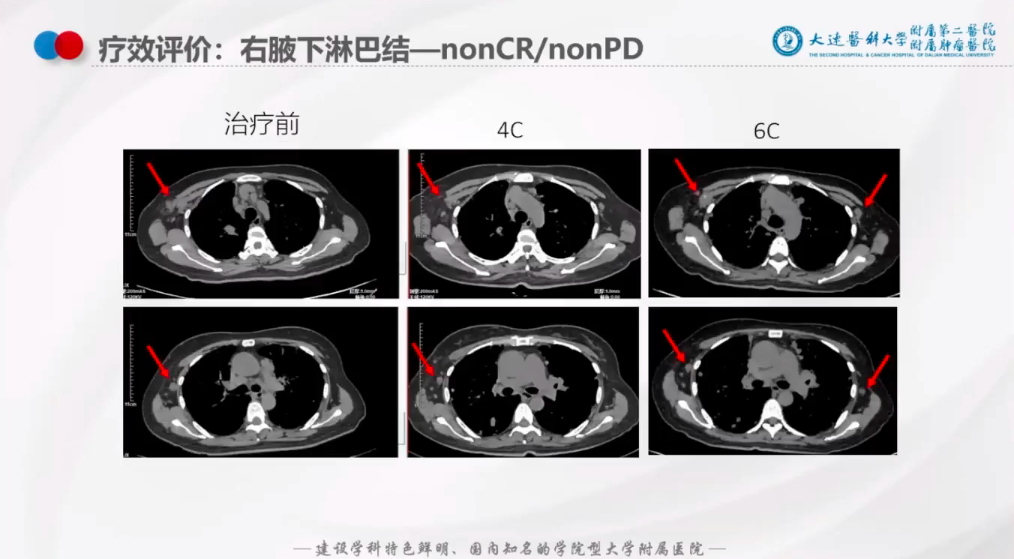
图13: 腋窝淋巴结五线治疗后疗效评估
诊断:
右乳腺癌 右腋下淋巴结转移 骨转移 肺转移,肺部病灶进展,TTP5: 5个月;
问题讨论:
1) 患者在二线治疗达到乳腺病灶CR,腋窝淋巴结微小残留(nonCR/nonPD),骨病灶向成骨转化 (nonCR/nonPD)疗效之后,可否行乳腺局部治疗?
2) 患者四线治疗之后,肺内病灶呈现进展状态,下一步治疗方案是什么?
3)患者5线治疗进展之后,后续治疗方案是什么?
集思广医—众专家各抒己见
在讨论环节中,赵卫红教授、郑亚兵教授、严颖博士分别分享了自己的观点。
赵卫红教授:该例患者不论是化疗还是内分泌治疗,都取得了不错的疗效。对于该例患者在二线治疗达到乳腺病灶CR,腋窝淋巴结微小残留(nonCR/nonPD),骨病灶向成骨转化 (nonCR/nonPD)疗效之后是否需要局部治疗,个人所在单位会进行多学科讨论。当然,现在亦有临床研究证实,该种局部治疗并不延长患者生存,但是,一般而言,对于肿块有破溃情况的患者,我们会考虑局部治疗。该例患者肿块距离皮肤尚有一段距离,破溃的几率较小,因此,对于该例患者的局部治疗,可能会持一种谨慎的态度对待。根据患者在二线治疗选择内分泌治疗之后所获得的长期疾病控制,还有患者在出现肺部新发病灶之后所做的免疫组化结果,提示患者在三线治疗也应该选择内分泌治疗,所以患者后来采取依维莫司+氟维司群治疗,亦是非常规范的治疗选择。当然,也可以考虑进行CDK4/6抑制剂的再挑战,不过患者所获得的PFS依旧有限。患者在四线治疗使用艾立布林也没有获得满意的获益,可能可以考虑使用紫杉、蒽环、长春瑞滨、吉西他滨、铂类等药物。个人可能更倾向于后续使用白蛋白紫杉醇进行挑战。T-DXd对于HER2过表达的患者更具有效性,而该例患者为HER2低表达的患者,能够在6个周期治疗后再出现进展已属不易。由于患者在五线治疗后,病情处于加速期的状态,后续需要根据患者耐受程度选择治疗方案,个人可能会选择白蛋白紫杉醇周疗的方式,如果患者不能耐受化疗,则可以考虑选择阿贝西利+依西美坦的方案。
 赵卫红教授
赵卫红教授
郑亚兵教授:该例患者并不存在肿块破溃的风险,同时,亦不存在因疾病影响生活质量的问题。因此,对于该例患者手术的意义并不大。因为对于Ⅳ期的患者而言,手术并不能改善患者的总生存,在该阶段主要治疗目的是改善患者生活质量。至于该例患者在一线治疗时,优先使用化疗还是“CDK4/6抑制剂+”的治疗方案?在以前CDK4/6抑制剂上市之前,会优先使用化疗,而现在大家的理念已经有所改变。当然,该例患者在接受一线治疗时的时间尚早,因此,多西他赛+卡培他滨,序贯卡培他滨维持亦是正确选择。患者在二线内分泌治疗选择依维莫司+氟维司群具备可行性,因为该方案不仅国内可及,而且,具有逆转耐药的作用。患者在五线治疗之后,肺内病灶已经较为广泛,症状亦明显,由于患者既往已经用过了诸多的内分泌药物,后续可能优先考虑予以化疗。由于患者既往使用多西他赛获得了较长的疾病控制,因此,后续可以考虑再使用紫杉类药物,优先考虑白蛋白紫杉醇单药治疗。此外,在经济条件许可的情况下,也可以考虑白蛋白紫杉醇联合贝伐珠单抗治疗。
 郑亚兵教授
郑亚兵教授
严颖博士:患者在二线治疗出现成骨性改变之后,不论从脊柱稳定性的角度,还是疼痛控制方面,都暂时没有骨转移放疗的指征。患者在初诊入院时,如果对于骨转移病灶能够进行核磁检查,有助于帮助我们了解患者的疼痛是由于骨质破坏还是脊髓压迫所致。患者在二线治疗选择哌柏西利+来曲唑+卵巢功能抑制(OFS)获得了较长的疾病控制时间,而在该治疗方案治疗进展之后,一个是PI3K抑制剂,然而该药目前国内不可及,因此,还是考虑选用依维莫司。在系列临床研究中显示,在CDK4/6抑制剂治疗进展之后,再选用内分泌治疗,中位PFS时间仅为6~7个月,很难达到特别长的时间。该例患者在CDK4/6抑制剂治疗进展之后,主要出现了新发的肺转移,而免疫组化亦提示激素受体强阳,HER2阴性的结果,因此,个人同意在患者肿瘤负荷不太重时,再给予患者一次内分泌治疗的机会。虽然,患者在使用依维莫司+氟维司群治疗之后,TTP时间仅为5个月,但与真实世界的数据具有相似性。针对HER2低表达的治疗,现在主要是T-Dxd/DS-8201,对于HR阳性HER2阴性乳腺癌,最主要的驱动基因还是在HR,患者在经过两线内分泌和两线化疗之后,再选择T-Dxd,具有合理性。当然,患者后续治疗不论选择化疗还是内分泌,再有效的概率均较低,而个人更关注患者对于后续治疗的耐受程度。如果患者还能耐受化疗,则个人会再尝试化疗。由于患者经过多线治疗失败,而且,目前状态较差,个人可能会选择单药化疗,甚至是长春瑞滨一类的口服节拍化疗。反之,则只有内分泌治疗。对于患者能否耐受内分泌+靶向治疗,还得具体问题具体分析,实在难以耐受,则只能单药内分泌治疗。
严颖博士
马飞教授: 对于该例患者初始治疗方案,在今天看来更倾向于选择内分泌或“内分泌+”,但是,在患者症状较重,肿瘤负荷较大的时候,亦可以选择化疗,尤其是彼时CDK4/6抑制剂尚未上市之时,这是完全正确的选择。在患者系统治疗取得愈来愈好疗效的今天,通过局部治疗来补救的依赖亦会越来越少,所以,同意大家对于该例患者是否进行局部治疗的看法。当然,未来亦可以探索在系统治疗取得令人满意疗效的时候,加入局部治疗对于患者生活质量、生存是否有提升作用。在骨转移的诊断方面,骨扫描的敏感性较高,但是,特异性低,而且,骨扫描难以区分是溶骨还是成骨改变,因此,一般还需要通过X线或CT对于患者的骨质破坏情况进行判断。此外,核磁共振对于诊断骨转移的敏感性较高,尤其是椎体的骨转移,核磁共振诊断的效果更好。虽然PET-CT诊断骨转移的敏感性、特异性都较高,但是,在应用过程中存在诸多阻碍,所以,目前不将其作为常规推荐。骨活检是诊断骨转移的金标准,但是,通过骨活检进行分子分型可能受到脱钙的影响,因此,对于分子分型结果的判读需要谨慎。在骨转移的疗效评估方面,为了避免判断失误,建议联合骨转移周围连带的软组织病灶以及标记物的状态,进行综合判断,可能结果更加准确。依维莫司是mTOR抑制剂,与PAM通路相关,可能在PI3K突变人群中的疗效更优,但是,在使用时并未要求患者的PI3K一定呈现突变状态,所以,患者在三线治疗选择依维莫司亦可行。患者后续治疗可以选用蒽环、白蛋白紫杉醇、吉西他滨、铂类等,同时,由于患者属于HER2-low的状态,因此,如果可及的情况下,DS-8201、RC48等带有旁观者效应的抗体偶联药物(ADC)亦可选择。此外,即将上市的戈沙妥珠单抗,对于激素受体(HR)阳性、HER2阴性人群亦具有一定疗效,只是尚未获批适应症。当然,还可以给患者进行下一代测序(NGS)检测,以明确导致内分泌耐药的原因,进而指导后续的内分泌联合治疗。对于患者五线治疗之后的后续治疗,个人同意各位教授的选择,单药化疗对于患者生活质量的影响较低,优先考虑。
 马飞教授
马飞教授
以多线治疗失败的HR+HER2低表达右乳癌伴全身多发转移患者的病例为例,专家们从前沿进展探讨、个人经验分享等各个维度,对于患者最佳的治疗方案进行了梳理,达成了诸多诊疗上的共识,相信未来也定会给大家的乳腺癌诊疗提供借鉴。“半月曼谈”更多精品课程即将呈现,精彩不断,欢迎关注!
排版编辑:肿瘤资讯-xiaodong











 苏公网安备32059002004080号
苏公网安备32059002004080号


