探寻更为高效、安全的EGFR突变非小细胞肺癌(NSCLC)治疗方案,是我们始终不懈追求的方向。近年来,聚焦于EGFR突变的药物研发和应用势头强劲,不仅极大地提高了肿瘤患者的生存率,也对临床治疗格局产生了深远的影响。药物的研发进展和临床疗效成为不同层级学术会议持续关注和探讨的热点。本平台关注到2022年ESMO亚洲年会(ESMO ASIA 2022)上的相关报道,选取和整理了一些代表性药物的新研究、新进展和新数据,特邀中国医学科学院肿瘤医院王洁教授加以点评,以飨读者。
中国医学科学院肿瘤医院内科主任
主任医师,协和医学院长聘教授,博士生导师
2021年何梁何利基金科学技术与进步奖获得者
国家〃杰出青年〃基金获得者
教育部创新团队带头人
第七届中国青年女科学家奖获得者
入选国家百千万人才工程并获有突出贡献中青年专家称号
中国临床肿瘤学会(CSCO)副理事长
CSCO小细胞肺癌专家委员会副主任委员
CSCO非小细胞肺癌专家委员会候选主任委员
中国医师协会肿瘤多学科专委会主任委员
中国抗癌协会肺癌专业委员会副主任委员
北京医学会肿瘤分会副主任委员
北京慢性病防治与健康教育研究会副会长
精准施策 获益显著:EGFR常见突变一线治疗
Lazertinib(LBA7)
B.C. Cho等[1]报告了随机双盲对照Ⅲ期LASER-301研究(NCT04248829)结果,比较了lazertinib(240 mg/d,n=196)和吉非替尼(250 mg/d,n=197)治疗Exon 19 del/Exon 21 L858R等常见突变且未经治NSCLC患者的疗效和安全性,在lazertinib适应症上做出了新的探索。研究的主要终点是无进展生存期(PFS),次要终点是客观缓解率(ORR)、缓解持续时间(DoR)、总生存期(OS)、治疗相关不良事件(TRAEs)等。
疗效方面,①两组药物中位PFS(mPFS)分别是20.6和9.7个月,HR=0.45(P<0.001);DoR分别是19.4和8.3个月。lazertinib组的ORR和DCR分别达76%和94%。两药物组中位OS(mOS)均未达到,lazertinib组18个月生存率高于吉非替尼(80% vs 72%),HR=0.74(P=0.116)。②在不同人种、Exon 19 del/ Exon 21 L858R突变等亚组分析中,lazertinib治疗后mPFS均达吉非替尼组一倍;其中,亚裔组mPFS分别是20.6和9.7个月。(见表)
 表1 lazertinib与吉非替尼疗效数据比较(截至2022年7月29日)
表1 lazertinib与吉非替尼疗效数据比较(截至2022年7月29日)

安全性方面,lazertinib引起的TRAEs与其他TKIs相似。总体来看(n=196),大多数为1或2级轻度TRAEs,最常报告的(≥10%)是触觉异常(39%)、皮疹(36%)、瘙痒(27%)和腹泻(26%);3级少见,最常见的为贫血(4%)、腹泻(3%)等;未出现4级TRAEs。(见表)

阿美替尼(370P)
F.S. Cun等[2]回顾分析了南京脑科医院2020年4月~2022年6月期间阿美替尼单药或联合治疗52例EGFR共突变患者后的疗效和安全性。主要终点是ORR,次要终点包括PFS、OS、疾病控制率(DCR)和安全性。中位年龄为65岁(32~84岁),61.5%为女性,5.8%的患者接受阿美替尼+贝伐珠单抗治疗,9.6%接受阿美替尼+培美曲塞治疗。
疗效方面,①阿美替尼单药治疗后患者的ORR和DCR分别为65.9%和95.5%。研究人员分析了不同共突变亚组的ORR和DCR(见表)。②阿美替尼+贝伐珠单抗或培美曲塞也显示出抗瘤活性,ORR为87.5%,DCR为100%。PFS和OS尚未达到。安全性方面,5.8%(3/52)和7.7%(4/52)的患者出现皮疹和腹泻(1~2级),3.8%(2/52)的患者出现≥3级TRAEs。

QL1706(332P)
W. Fang等[3]报告了Ⅱ期试验(NCT05329025)突变队列数据,探讨了QL1706(5.0 mg/kg)+贝伐珠单抗+化疗(培美曲塞+卡铂)一线治疗晚期T790M耐药突变患者的疗效和安全性。在维持阶段,患者接受QL1706+贝伐珠单抗+培美曲塞治疗延长至24个月。纳入的31例T790M突变患者为进展期或不能耐受第三代TKI治疗。中位年龄为55岁(39~74岁)。其中,19例(61.3%)此前接受过第三代EGFR TKI,16例(51.6%)曾接受过抗血管生成治疗。
疗效方面,截至2022年5月31日,经治后患者ORR为64.5%(20/31),DCR为93.5%(29/31)。PFS尚不成熟。6个月PFS率为61.3%。mOS为5.75个月(4.86~7.10个月)。安全性方面,30例(96.8%)出现TRAEs,最常见的(>40%)是贫血(77.4%)、食欲下降(61.3%)、AST升高(45.2%)、便秘(41.9%)。其中10例(32.3%)出现≥3级TRAEs,最常见的是血小板数减少(9.7%)和贫血(9.7%)。8例(25.8%)出现严重TRAEs。

在ESMO ASIA2022上,上述几个研究值得我们特别关注。
Lazertinib是一款血脑屏障穿透率高的第三代EGFR TKI,此前在韩国获批用于既往接受过TKI治疗的EGFR T790M突变局部晚期或转移性NSCLC患者。从ESMO ASIA 2022公布的LASER-301研究数据来看,该药对Exon 19 del/Exon 21 L858R等常见突变患者,无论是否有脑转移,均有着较好的疗效。Lazertinib作为三代EGFR TKI较一代TKI能显著提高患者生存,并且亚组分析中在L858R亚型中,lazertinib显示更高获益趋势。在安全性上可见其在皮疹和心脏毒性(Q-T间期延长)上不良反应发生率相对较低,延续了在临床前研究中观察到的安全谱优势。
另外,ESMO ASIA 2022上公布了研究人员探索EGFR共突变患者的治疗策略。例如,国产口服第三代EGFR TKI阿美替尼在单药、联合抗血管生成药物或化疗对共突变患者中,表现出较好的抗瘤活性。需要强调的是,EGFR共突变的发生,不会因为EGFR突变类型(Exon 19del,20ins,21 L858R突变)的不同而有所不同。我们在临床治疗中,不仅要关注到EGFR突变,也要注意如TP53、RB1、CTNNB1、PIK3CA突变,还有EGFR、NKX2-1、CDK4、CDK6和CCNE1扩增。因为共突变的存在可能会影响到药物选择和最终疗效;对于共突变患者,药物选择不能顾此失彼,要两相兼顾。
QL1706为国产PD-1/CTLA-4双抗。QL1706+贝伐珠单抗+铂基化疗在小样本(n=31)EGFR TKI治疗失败的T790M耐药突变型NSCLC患者中显示出较有前景的抗瘤活性,患者耐受性较好。作为国产新药,需要我们予以关注。
聚焦痛点 强强联合:EGFR常见突变二线治疗
Amivantamab+Lazertinib+卡铂+培美曲塞四联方案(398TiP)
目前奥希替尼耐药进展后的标准治疗是含铂化疗,但获益有限。此前CHRYSALIS-2研究队列A证明一线/二线奥希替尼及铂基化疗耐药后 amivantamab+lazertinib对Exon 19 del/Exon 21 L858R的疗效。此后,研究人员进一步探索该方案联合铂基化疗是否能为患者提供更好的临床获益。
ESMO ASIA 2022上,J. Wang等[4]报告了随机开放标签Ⅲ期MARIPOSA-2研究方案(NCT04988295),以评估疾病进展期或奥希替尼耐药后,联合治疗方案amivantamab+ lazertinib+卡铂+培美曲塞(LACP,A组) vs 卡铂+培美曲塞(CP,B组)对EGFR常见突变的局部晚期或转移性非鳞NSCLC的疗效和安全性。另设amivantamab+卡铂+培美曲塞组(ACP,C组)以评估lazertinib在LACP中的作用。
研究人员在该方案中,将500例符合条件的患者按2:2:1(A:B:C)随机分配,按lazertinib治疗线数(一线或二线)、是否有脑转移和亚裔人群等进行分层。主要终点是PFS;关键次要终点包括ORR、OS、安全性和健康相关生活质量。研究尚在入组中,数据有待揭晓。
奥希替尼+necitumumab治疗方案(329P)
J.W. Riess等[5]报告了Ⅱ期ORCHARD平台研究(NCT03944772)期中分析结果,探讨了奥希替尼+necitumumab(一款封闭EGFR配体结合位点的单抗)对奥希替尼一线治疗后疾病进展的继发EGFR突变晚期NSCLC患者的疗效和安全性,以期建立二线新型联合治疗方案。纳入奥希替尼一线治疗后16例继发EGFR扩增、L718/G724突变等突变患者,接受奥希替尼(80mg/d,口服)+necitumumab(800mg,每3周第1+8天,静注)。主要终点:ORR,其他终点:安全性。无效性标准被定义为ORR≥45%的概率<10%。
疗效方面,截至2022年2月11日,11例(69%)已停止治疗,13例可评估确认的反应。ORR为15%,均为部分缓解(PR)。5例(39%)疾病稳定(SD),5例(39%)疾病进展(PD),1例(8%)无法评估。安全性方面,7例(44%)出现一个或多个≥3级的TRAEs,5例(31%)出现严重不良事件,2例(13%)出现不良事件并导致死亡,1例可能与necitumumab有关。未见间质性肺炎病例。
研究人员认为,虽然未出现新的安全信号;然而,由于试验符合无效标准,目前已停止入组;联合方案可能无法向耐药患者提供更为有效的临床疗效。
纳武利尤单抗+化疗治疗方案(LBA8)
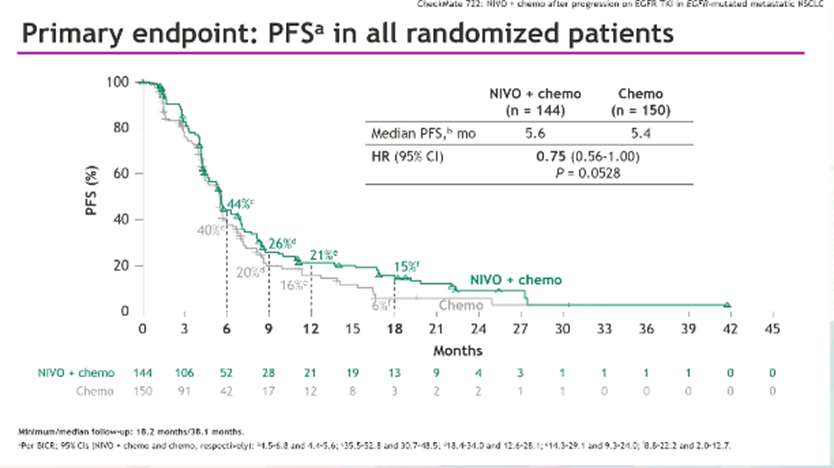
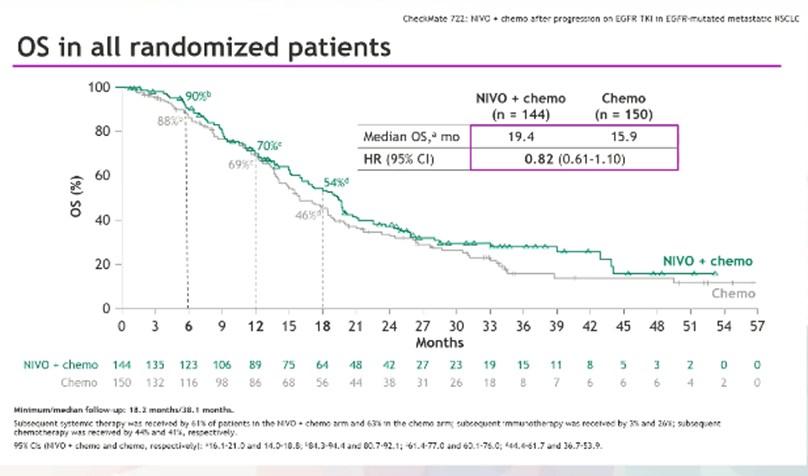
T.S.K. Mok等[6]报告了Ⅲ期随机CheckMate722(NCT02864251)研究结果,旨在探讨免疫联合化疗对TKIs治疗后疾病进展的NSCLC的疗效和安全性。纳入294例经第一或二代TKIs治疗后进展患者。主要研究终点:PFS,次要研究终点:OS、ORR、DOR、9个月PFS率和12个月PFS率。
疗效方面,在最终分析中(最短随访18.2个月,中位随访38.2个月),纳武利尤单抗(360 mg)+化疗组(n=144)相比单纯化疗组(n=150)在mPFS改善上并无显著性差异(5.6 vs 5.4 个月,P=0.0528)。mOS分别是19.4 vs 15.9个月(HR=0.82)。亚组分析中,在EGFR敏感突变患者(n=269)和一线TKIs经治后(n=248),PFS有显著性差异(见表)。安全性方面,45%接受纳武利尤单抗+化疗的患者出现3~4级TRAEs,29%接受化疗的患者出现3~4级TRAEs。
研究人员认为,虽然未发现新的安全信号,纳武利尤单抗+化疗对突变患者PFS的改善并无显著性意义,OS方面的改善表现为数据上的差异(numerical difference);仅在EGFR敏感突变和TKI一线经治患者中可观察到获益趋势。


左右滑动可查看图片
EGFR突变NSCLC靶向治疗后耐药不可避免,后续单纯化疗疗效有限,如何进一步提高疗效,克服耐药是很大的挑战。多靶点联合治疗,如双特异性抗体的四药联合方案,有可能为患者带来更好的预后。
ESMO ASIA 2022上的MARIPOSA-2研究方案值得关注,即四联方案amivantamab + lazertinib +卡铂+培美曲塞(LACP方案)相比单纯卡铂+培美曲塞(CP方案)对耐药后突变患者具有显著的疗效。LACP方案的目的是在amivantamab +lazertinib治疗模式基础上,再联合含铂化疗,期望给耐药患者提供更为有效的治疗策略。MARIPOSA-2研究目前还在进行中,期待相关数据能够尽快揭晓。
其他联合治疗方案,如靶向联合或免疫联合化疗也都在探索耐药后肺癌治疗策略,有特点的是ORCHARD研究(奥希替尼+necitumumab治疗)和CheckMate722研究(纳武利尤单抗+化疗治疗)。Checkmate722研究是将免疫治疗引入耐药后基因突变患者治疗策略中来,需要解决两个问题:①奥希替尼耐药后免疫治疗效果如何?②驱动基因阳性患者免疫治疗效果如何?另外,ORCHARD研究是探索“个体化”治疗的尝试,此前分析过EGFR C797S突变的奥希替尼+吉非替尼方案;RET融合突变的奥希替尼+selpercatinib方案,而这次ESMO ASIA 2022上报道的是EGFR扩增、L718/G724突变的奥希替尼+necitumumab方案。
目前,针对奥希替尼耐药后治疗方案的各类研究非常丰富,进展各不相同。奥希替尼确实创造了一个EGFR突变治疗的“奥希替尼时代”。上述三个新疗法、新方案将成为“后奥希替尼时代”的开拓者和引领者,为患者打开全新的治疗局面。
前沿探索 积累经验:EGFR非经典突变治疗
Amivantamab+Lazertinib(322MO)
B.C. Cho等[7]报告了开放标签CHRYSALIS-2研究(NCT04077463)队列C期中分析结果,探讨了amivantamab(1050/1400mg,静注)+lazertinib(240 mg,口服)在非经典突变(如S768I、L861Q、G719X等,排除Exon 20ins),且未经治或一代或二代TKIs经治进展后的晚期NSCLC患者中的治疗效果。
截至2022年6月8日,评估了40例患者治疗反应(≥1次基线后评估或因任何原因终止)。中位年龄为64岁,47.5%为女性。19/40例患者接受过治疗(期中17/40例接受过一线治疗,2/40例接受过2线治疗)。Exon 19 G719X突变占比较大(60.0%),其中存在复合突变。疗效方面,60.0%(24/40)的患者观察到PR。在30例患者(≥3次基线后评估或因任何原因终止)中,总ORR为53%(34%~72%),其中阿法替尼经治后的患者,ORR为50%(12%~88%);初治患者,ORR为59%(33%~82%)。在参与反应评估的40例患者中,21例出现治疗应答,中位持续治疗时间为5.95个月,mDoR未达到(2.86~未达到),4例应答超过6个月。

安全性方面,皮疹相关的不良反应39例(75%),其中3级为7例。≥3级的静脉血栓栓塞症(VTE)为14例;1级间质性肺病(ILD)为2例。不良反应导致的剂量减少病例数分别为:amivantamab 8例(15%)和lazertinib 10例(19%),不良反应导致的治疗中断为3例(6%)。

阿美替尼(373P)
研究人员探讨了阿美替尼单药治疗(165 mg/d,口服)治疗局部晚期或转移性EGFR突变(Exon19del、Exon21 L858R除外)NSCLC的疗效和安全性,40例患者被分为20ins突变队列(队列1,n=20)和20 ins以外的非经典突变队列(队列2,n=20)。此次ESMO ASIA2022上,W. Fang等[8]报告了2021年2月~2022年5月期间队列2治疗数据(见表)。主要研究终点是ORR。
疗效方面,经治后队列2患者的ORR为50%,DCR为100%。在不同突变型亚组分析中,G719X/L861Q/S768I和其他突变型(Exon 20ins除外)的ORR分别为53.8%和33.3%。G719X、L861Q和S768I突变分别出现8、6和1例,其他突变包括L747P/S、V774M、H773M等。安全性方面,18.75%(3/16)患者发生严重AEs。11例患者肌酸激酶升高。在肌酸激酶亚组分析中,0级、1~2级和≥3级ORR分别为40%、50%和57.1%。

EGFR非经典突变的NSCLC患者群体,目前尚没有更好的治疗选择,需要更多的研究进行探索。
ESMO ASIA2022上报告的CHRYSALIS-2研究队列C聚焦Exon18 G719X、Exon21 L861Q、Exon20 S7681、L833V、L861R、Ex18 E709K、V744M(Ex20ins除外)等非经典突变晚期患者群体,报告了amivantamab+lazertinib联合用药对非经典突变患者有效的抗癌活性(ORR=53%,78%的患者正在接受治疗),在初治和阿美替尼经治后患者中都观察到了良好的抗肿瘤活性。更为重要的一点是,在经过多重治疗的患者中,联合方案依旧显示出良好的疗效,证实了方案的获益。本研究中amivantamab+lazertinib的总体安全性与先前报告一致。当然,CHRYSALS-2队列C入组尚未结束,研究需要深入,一些关键性指标还有待揭晓。
阿美替尼是一款口服第三代EGFR TKI。ESMO ASIA 2022公布的队列2的新数据表明,一方面,在165 mg/d高剂量情况下,与其他非经典突变型相比,阿美替尼对G719X和L861Q和S768I这3个非经典突变具有抗肿瘤活性。另一方面,肌酸激酶增加与阿美替尼的疗效呈正相关。此外,EGFR Exon20ins突变的治疗是一个难点,药物研发呈现出多发发力的态势,阿美替尼队列1也在进行这方面的临床试验,结果值得期待,为非经典突变患者提供更多的药物选择。
[1] B.C. Cho, M-J. Ahn, J.H. Kang, et al. A randomized, double-blind, multinational phase III study to assess the efficacy and safety of lazertinib versus gefitinib in the first-line treatment of patients with EGFR mutation (EGFRm), advanced NSCLC (LASER301; NCT04248829). ESMO ASIA 2022, LBA7
[2] F.S. Cun, H. Zhang. Outcomes in patients with EGFR-mutant locally advanced or metastatic NSCLC co-mutations receiving aumolertinib as first-line treatment: A retrospective study. ESMO ASIA 2022, 370P
[3] W. Fang, Y. Yang, Y. Zhao,et al. A phase II, open-label, single-center study of QL1706 plus latinum doublet chemotherapy with bevacizumab as firstline treatment in patients with advanced NSCLC: Data from EGFR mutant cohort. ESMO ASIA 2022, 332P
[4] J. Wang, R. Garcia Campelo,N. Girard, et al. MARIPOSA-2: Randomized phase III study of amivantamab + lazertinib + chemotherapy vs chemotherapy alone in EGFRmutant NSCLC after osimertinib failure. ESMO ASIA 2022, 398TiP
[5] J.W. Riess, J.A. De Langen, Z. Piotrowska, et al. ORCHARD: Osimertinib + necitumumab in patients (pts) with advanced NSCLC whose disease progressed on first-line (1L) osimertinib. ESMO ASIA 2022, 329P
[6] T.S.K. Mok, K. Nakagawa, K. Park, et al. Nivolumab (NIVO) + chemotherapy (chemo) vs chemo in patients (pts) with EGFR-mutated metastatic non-small cell lung cancer (mNSCLC) with disease progression after EGFR tyrosine kinase inhibitors (TKIs) in CheckMate 722. ESMO ASIA 2022, LBA8
[7] B.C. Cho, Y. Wang, Y. Li, et al. Amivantamab in combination with lazertinib in patients with atypical epidermal growth factor receptor (EGFR) mutations excluding exon 20 insertion mutations: Initial results from CHRYSALIS-2. ESMO ASIA 2022, 322MO
[8] W. Fang, Q. Bu, Q.Wang, et al. Safety and efficacy of aumolertinib treatment in patients with advanced NSCLC harboring uncommon EGFR mutations: Cohort 2. ESMO ASIA 2022, 373P
CRC code: EM-118822,Approved Date: 2024-07-03
往期回顾
1、【2022 CSCO】破茧成蝶 向森而生 | 亚洲数据公布!Amivantamab开启晚期肺癌EGFR靶向治疗新纪元!
2、【2022 WCLC】破茧成蝶 向新而生|Amivantamab联合方案一线治疗EGFR敏感突变肺癌患者PFS或超28个月!
3、【2022 ASCO速递】破茧成蝶 向新而生 | 吴一龙教授解读非小细胞肺癌EGFR和MET通路靶向治疗新进展
4、【2022ELCC&AACR】破茧成蝶 向新而生| 赵军教授:EGFR exon 20ins NSCLC靶向治疗新突破
5、【2022 ELCC】破茧成蝶 向新而生| EGFR 20ins非小细胞肺癌治疗前沿进展盘点
6、ESMO2021|囊括EGFR/MET途径,克服奥希替尼耐药,Amivantamab联合Lazertinib研究数据闪耀ESMO
7、【2021 ASCO】陆舜教授分享肺癌靶向治疗最新进展,创新组合疗法有望克服EGFR TKI耐药
8、吴一龙教授谈EGFR 20外显子插入突变NSCLC诊疗现状与进展,Amivantamab(JNJ-61186372)机制独特或可带来突破
9、周彩存教授:WCLC重磅来袭!NSCLC EGFR Exon 20ins难治突变靶向治疗迎来重大突破!EGFR经典突变靶向治疗新组合惊艳全场!
排版编辑:肿瘤资讯-DND












 苏公网安备32059002004080号
苏公网安备32059002004080号


