精准治疗,诊断先行。随着二代测序(NGS)检测技术的不断发展,三阴性乳腺癌(TNBC)潜在的可干预靶点日渐明朗,且随着FDA近期获批数个针对晚期乳腺癌的全面基因组测序(Comprehensive Genomic Profiling)后的靶向疗法,TNBC患者的精准治疗可见希望。那么基于NGS检测指导下的晚期TNBC治疗有哪些新进展?又带来了哪些治疗新思路?【肿瘤资讯】有幸邀请到袁芃教授就该话题进行了梳理与分享,现整理如下,供肿瘤学界同行参考学习。

国家癌症中心中国医学科学院肿瘤医院
中国抗癌协会乳腺癌专业委员会 常委
北京癌症防治学会 理事长
中国临床肿瘤学会(CSCO) 乳腺癌专家委员会 常委
中国抗癌协会 理事
中国医师学会肿瘤医师分会 委员
国家自然科学基金 评审专家
国家科学技术奖 评审专家
TNBC是一类预后较差的乳腺癌类型,化疗一直是其主要治疗手段。随着检测技术的进步,乳腺癌分子表达图谱日渐清晰,一项纳入8654例晚期乳腺癌患者的研究中,使用FoundationOne®CDx进行检测,结果发现6959例患者(80.4%)至少携带一种基因突变,且存在相应的靶向治疗(图1)。
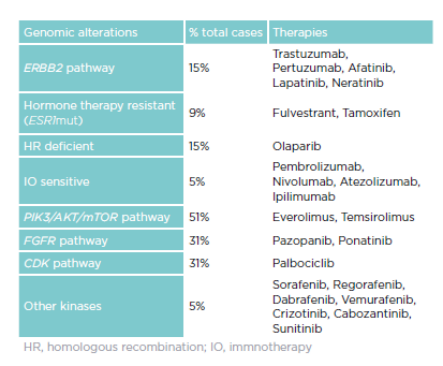
图1. 晚期乳腺癌患者使用FoundationOne®CDx检测发现的基因突变及其相应靶向治疗
其中TNBC潜在的治疗靶点有PI3K/AKT/mTOR、BRCA1/2、FGFR等,为TNBC的治疗指引了新的方向。以下将主要介绍NGS对几种常见肿瘤发生途径或基因改变的检测以及其对TNBC治疗的指导意义。
PI3K/AKT/PTEN通路活化与AKT抑制剂
LOTUS Ⅱ期研究中,将口服AKT抑制剂Ipatasertib联合紫杉醇作为转移性TNBC的一线治疗,结果显示无进展生存(PFS)明显优于对照组紫杉醇(图2)。这项研究中PI3K/AKT活化肿瘤定义为存在PTEN基因失活改变或PIK3CA/AKT1途径存在活化突变。
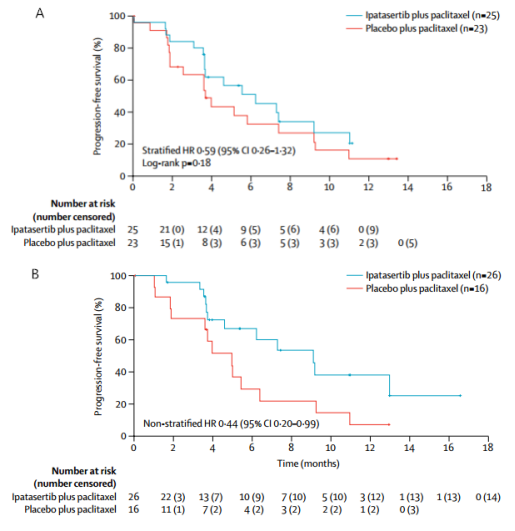
图2. PTEN低水平亚组(A)和PIK3CA/AKT1/PTEN突变亚组(B)的PFS
研究中采用免疫组化(Ventana IHC)和FoundationOne®CDx两种方法进行检测,结果显示,采用NGS检测的103例TNBC标本中, 42例(41%)携带与PIK3CA/AKT1/PTEN通路相关突变,而采用IHC检测中的21例患者,只有6例(29%)发现PTEN缺失--NGS较IHC能更全面地发现PIK3CA/AKT1/PTEN通路相关突变。更重要的是,只有PIK3CA/AKT1/PTEN突变患者在应用Ipatasertib治疗时才有显著获益,而IHC虽然检测到更多PTEN低表达肿瘤,但与非PTEN低表达肿瘤相比较,Ipatasertib治疗并不具有更多优势,表明分子遗传学改变较蛋白表达改变对靶向治疗更具指导意义。可以说,NGS将有望作为Ipatasertib伴随诊断用于指导治疗。
目前正在进行的IPATunity130研究,是一项国际性双盲安慰剂对照的双臂随机Ⅲ期研究,评估Ipatasertib+紫杉醇一线治疗PIK3CA/AKT1/PTEN改变的晚期TNBC或HR+/HER2-乳腺癌,研究中采用的就是FoundationOne®CDx检测PIK3CA/AKT/PTEN变异,该研究预计在2021年12月公布结果。
ERBB2变异与抗HER2治疗
一直以来,对乳腺癌治疗最具指导意义的HER2改变主要是扩增,临床常规检测方法是IHC和FISH。但实际上HER2除了扩增改变外,还存在点突变、插入/缺失和重排。约1.6%~2.0%的乳腺癌携带HER2活化突变,多数发生在激酶结构域(第19-20外显子)和细胞外区域(第8外显子),最常见改变为19外显子的p.L755S错义突变(43%),这些变异发生率低,采用常规IHC检测无法获得,只能通过NGS或数字PCR的方法才能明确变异的情况。
Neratinib是不可逆抑制EGFR、HER2、HER4的口服酪氨酸激酶抑制剂,体外可有效抑制携带HER2突变和扩增的乳腺癌细胞株的细胞内信号传导。2015年首例报告Neratinib成功治疗HER2 L755S突变晚期乳腺癌,肿瘤缓解时间超过1年。Neratinib治疗HER2突变转移性乳腺癌的临床研究目前正在招募患者。
此外SUMMIT篮式研究亦正在评估Neratinib在HER2突变的多种实体瘤中的安全性和有效性。采用HER2抑制剂治疗HER2突变乳腺癌的病例报道很多,有报道一例三阴性炎性乳腺癌经肿瘤组织NGS检测发现ERBB2 V777L与S310F 位点突变,给予拉帕替尼+曲妥珠单抗+化疗,病情缓解(图3)。以上数据表明,NGS可以改善传统IHC/FISH检测ERBB2变异的局限性,能够检出ERBB2非扩增型变异。

图3. 拉帕替尼+曲妥珠单抗+化疗治疗后病情缓解
NTRK融合与NTRK 抑制剂
Entrectinib和Larotrectinib 治疗NTRK融合实体瘤超高的治疗反应率,使FDA批准其泛瘤种NTRK融合适应证。总体而言,乳腺癌是发生NTRK融合的低频瘤种,发生率不足5%,但分泌性乳腺癌的NTRK融合发病率超过90%。一项Entrectinib的汇总分析中,所有NGS检测携带NTRK阳性实体瘤的治疗反应率为57%,中位缓解持续时间(DoR)10个月,中位PFS 11个月,中位总生存(OS)21个月,其中6例NTRK阳性乳腺癌中的5例对治疗有反应(83%; 95%CI 36-100,图4)。因此在临床实践中对于晚期乳腺癌,尤其是缺少治疗手段的TNBC可考虑进行NGS检测NTRK融合基因,一旦证实存在该变异,患者获得治疗缓解的机会明显增加。
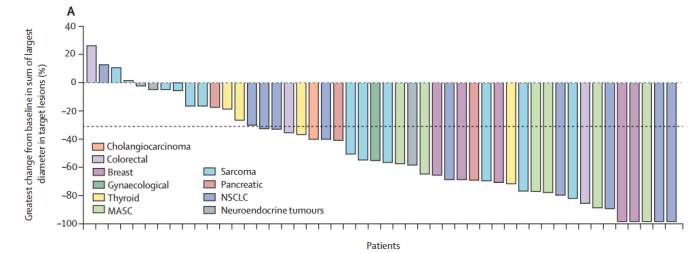
图4. 采用NGS检测的NTRK融合阳性不同肿瘤中患者对Entrectinib的个体应答
免疫标志物的检测与免疫治疗
免疫治疗在乳腺癌尤其是晚期TNBC中的疗效崭露头角。通过IMpassion130研究的阳性结果,使得阿特珠单抗成功获批治疗PD-L1阳性不可切除的局部晚期或转移性TNBC。但在适合人群方面,除了PD-L1表达之外,是否还存在其他预测疗效的免疫治疗生物标志物?近年的研究显示, CD274(PD-L1)扩增(1%~3%)、BRAF GA(1%~4%)、TMB突变负荷、MSI-H(0.1%~0.4%)、PBRM1 GA(1%)等,可能将成为预测免疫治疗疗效的标志物,这些标志物均依赖NGS检测,其中以聚焦TMB的研究较多。
TMB独立于PD-L1的表达,一些研究表明,与PD-L1表达相比,TMB与免疫治疗反应率的相关性更高。TAPUR研究是帕博利珠单抗后线治疗高TMB转移性乳腺癌的Ⅱ期篮子研究,结果显示,晚期TNBC患者的肿瘤控制率37%,治疗反应率21%,中位PFS 10.6个周,中位OS 31.6个周(表1),这些数据表明TMB在乳腺癌的免疫治疗中极具应用前景。
表1. TAPUR研究结果

总之,TNBC是一组高度异质性的疾病,以TNBC异质性为基础探究疾病个体化治疗策略尤为重要,针对TNBC的可干预的治疗靶点(如AKT、ERBB2、NTRK、免疫检查点等)及相关药物像一颗颗璀璨的星星点亮了患者治疗的道路,通过NGS检测发现上述变异并将其应用于临床实践中,将为晚期TNBC患者带来新的希望。
排版编辑:肿瘤资讯-frank














 苏公网安备32059002004080号
苏公网安备32059002004080号


