目前针对微卫星高度不稳定性(MSI-H)的结直肠癌,国内外的指南均推荐免疫检查点抑制剂用于晚期患者的系统治疗。对于其在局部晚期患者的围手术期治疗中的价值则是近期临床研究的热点。NICHE研究即针对MSI-H的结直肠癌新辅助治疗做了相应的探索,其结果让人印象深刻。此文介绍一例拒绝手术治疗的直肠腺癌(cT3aN0M0,ⅡA期)患者,经过5个周期XELOX方案化疗和5个周期特瑞普利单抗免疫治疗后,达到临床完全缓解。

重庆医科大学附属第一医院肿瘤科主治医师,助教
中国抗癌协会肿瘤放射治疗专业委员会会员
中国抗癌协会肉瘤专业委员会会员
中国抗癌协会肿瘤心理学专业委员会会员
中国抗癌协会重庆市抗癌协会会员
基本情况
性别:女
年龄:43岁
职业:办公室职员
入院日期:2019年5月13日
主诉:便血,直肠腺癌 7+月,肛门坠胀2月
现病史
7+月前,患者无明显诱因出现便血,呈鲜血,初量少,未予重视,后便血量增加,自诉最多时约60mL,呈鲜红色,伴头昏,无腹痛、腹泻,无里急后重等,遂于重庆某三甲医院就诊,查肠镜:距肛门4~10cm可见一大小约6cm×4cm巨大盘状隆起新生物,表面呈菜花状,可见糜烂及渗血。病理活检提示腺癌。诊断为“直肠腺癌”,完善相关检查未见远处转移,予以止血等对症治疗后出血好转,建议进一步手术治疗。患者拒绝手术治疗,并要求出院,出院后长期口服“中药”(具体不详)治疗,未行手术、放化疗等治疗,未再复查。2个月前患者出现肛门坠胀,排便后为甚,未进一步治疗。患者自觉肛门坠胀感进行性加重,现偶有便血,量少,无明显腹痛、腹泻,为求进一步治疗入院。
既往史
患者平素健康状况良好。否认高血压、糖尿病、冠心病、传染病史,否认食物、药物过敏史,否认手术外伤、输血史,预防接种史按规定。
家族史
父亲去世,原因不详,母亲体健,否认家族传染病史。否认精神病、肿瘤、糖尿病、血友病家族遗传病史。
体格检查
入院查体:KPS评分90分,神清,心肺未见明显异常,腹平,未见胃肠型及蠕动波,腹软,无肌紧张,无压痛、反跳痛,全腹未扪及包块,肝、脾脏肋下未触及,肝区无叩击痛,双肾区无叩击痛,腹部移动性浊音试验阴性。肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套染血。
入院后实验室检查
血常规、肝功、肾功、电解质、凝血象未见明显异常。
肿瘤标志物:糖类抗原19-9 3.7 U/mL,糖类抗原72-4 21.0 U/mL ↑,癌胚抗原 3.4 ng/mL ,甲胎蛋白 5.2 ng/mL 。
辅助检查
入院时复查肠镜并再次取活检病理复核,结果如下:
肠道清洁度欠佳,有较多粪液粪渣,整个结直肠黏膜呈“豹纹”样改变,距肛缘约3~5cm见溃疡性新生物,占管腔超过1/2,边缘隆起,中央粗糙、糜烂、出血,活检8块。诊断:直肠腺癌、大肠黑变病。(图1)
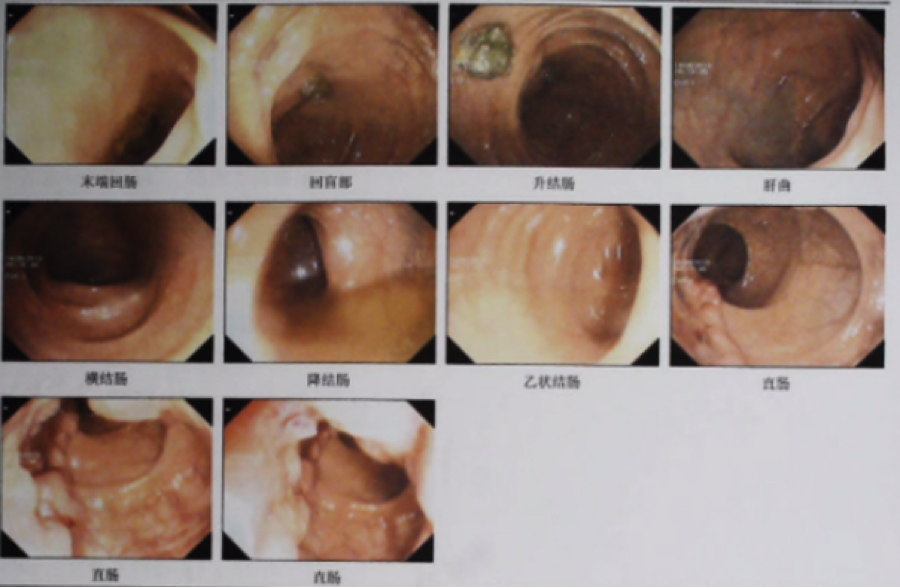
图1. 2019年5月14日电子结肠镜检查报告
胸腹CT:
直肠中下段肠壁不均匀增厚,外膜面稍毛糙,考虑肿瘤性病变可能。肝左叶多发小囊肿。子宫强化欠均匀,后壁可疑小结节,请结合MRI检查。右肺下叶前基底段浅淡小结节影,考虑为炎性肉芽肿可能性大。
直肠MRI:
直肠中下段肠壁增厚,考虑肿瘤性病变,直肠癌可能,MR分期为T3a N0 ,CRM(-),EMVI(-)。盆腔少许积液。子宫肌层信号不均匀,增强后强化不均。宫颈内多发小囊肿。(图2)
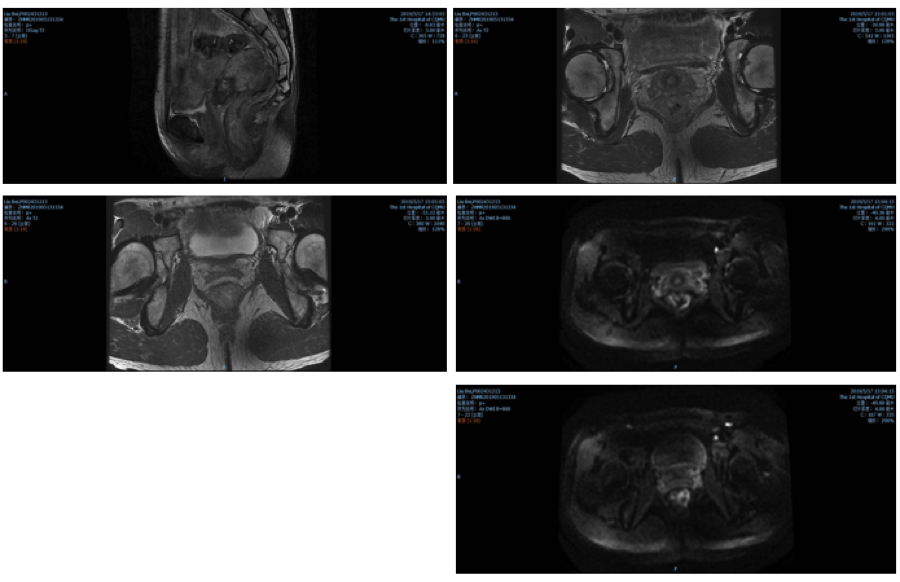
图2. 2019年5月17日直肠MRI结果
手术/活检病理:
免疫组化:MLH1(+),MSH2(+),MSH6(+),PMS(-),Ki67 60%,Braf(-),PD-1肿瘤内5%(+),PD-L1(-),EGFR(+)。
基因检测结果:
未检测到KRAS、NRAS、BRAF基因突变。MSI检测到微卫星高频不稳定(MSI-H)。(图3)

图3. 微卫星不稳定性(MSI)分析报告单
疾病诊断
直肠腺癌(cT3aN0M0,ⅡA期)
入院后治疗经过
手术治疗:再次向患者建议手术治疗,患者明确拒绝
放射治疗:患者拒绝手术后,向患者建议同步放化疗,但患者仍拒绝放疗。
因此,我们考虑全身系统治疗。
系统治疗:
据现有循证证据,结合患者意愿,推荐化疗基础上联合靶向治疗或免疫治疗,但患者拒绝靶向治疗及免疫治疗,要求仅行化疗。
2019年5月18日至2019年6月29日 行XELOX方案(奥沙利铂200mg d1+卡培他滨1500mg bid d1~14)化疗3周期,然后复查。第1周期化疗后,症状稍缓解。
(2019年7月13日)
查体:肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套无染血。
血常规、肝功、肾功、电解质、凝血象未见明显异常。
癌谱:糖类抗原19-9 7.5 U/mL ,糖类抗原72-4 21.0 U/mL ↑,癌胚抗原 2.1 ng/mL ,甲胎蛋白 5.4 ng/mL 。复查下腹部及盆腔MRI:直肠癌化疗后:直肠中下段肠壁稍显增厚,符合直肠癌表现,mr TRG分级约为3级。子宫肌层信号不均匀,增强后强化不均,较请结合临床。宫颈内多发小囊肿。盆腔少许积液。骨盆诸骨信号明显不均。疗效评价疾病稳定(SD)。(图4)
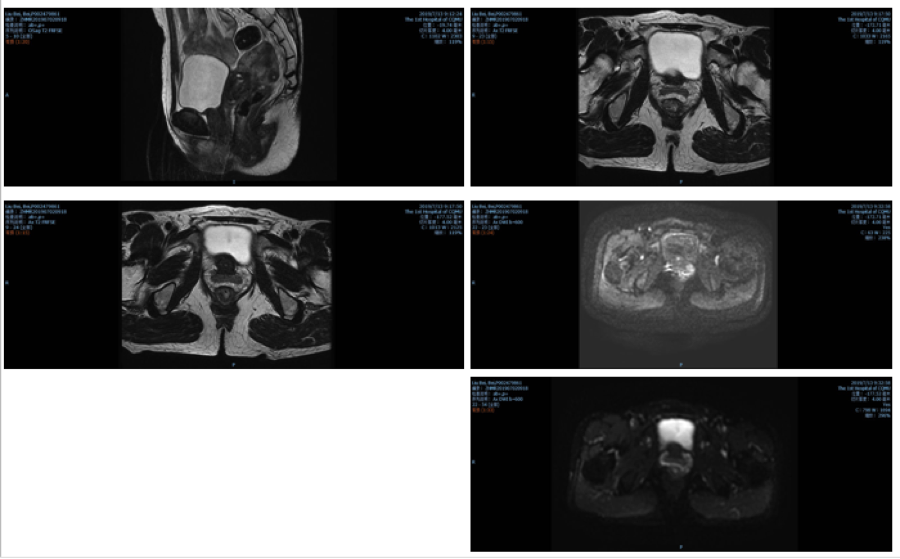
图4. 2019年07月13日经过3个周期化疗的MRI结果
复查后疗效欠佳,再次建议患者手术或同步放化疗,患者仍明确拒绝。
经沟通后,患者愿意尝试免疫治疗。
免疫治疗:
复查
2019年8月1日行第1次特瑞普利单抗免疫治疗(240mg ,Q3W),未行化疗。
(2019年08月21日返院)
患者偶感肛门轻微坠胀,已无便血等不适。
肿瘤标志物:糖类抗原19-9 7.2 U/mL ,糖类抗原72-4 22.6 U/mL ↑,癌胚抗原 1.9 ng/mL ,甲胎蛋白 4.3 ng/mL 。
查体:肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套无染血。
2019年08月22日行第2次特瑞普利单抗240mg免疫治疗,同时于2019年08月23日开始行第4周期XELOX方案(奥沙利铂200mg d1+卡培他滨1500mg bid d1~14)化疗。
(2019年09月11日返院)
肿瘤标志物:糖类抗原19-9 9.6 U/mL ,糖类抗原72-4 31.2 U/mL ↑,癌胚抗原 1.8 ng/mL ,甲胎蛋白 6.1 ng/mL 。
查体:肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套无染血。
2019年09月12日行第3次特瑞普利单抗240mg免疫治疗,同时于2019年09月13日开始行第五周期XELOX方案(奥沙利铂200mg d1+卡培他滨1500mg bid d1~14)化疗。
(2019年10月08日返院)
肿瘤标志物:糖类抗原19-9 8.7 U/mL ,糖类抗原72-4 24.8 U/mL ↑,癌胚抗原 2.0 ng/mL ,甲胎蛋白 5.4 ng/mL 。
2019年10月09日行第4次特瑞普利单抗240mg免疫治疗。此时患者再次拒绝化疗。
查体:肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套无染血。
(2019年10月29日返院)
2019年10月30日行第5次特瑞普利单抗240mg免疫治疗。
(2019年11月04日返院)
腹部及盆腔MRI,结果回示:直肠癌化疗后:直肠中下段肠壁稍显增厚,与2019年07月13日比较病变减轻,随访。肝S4小囊肿。子宫肌层信号不均匀,增强后强化不均,请结合临床。宫颈内多发小囊肿。盆腔少许积液。骨盆诸骨信号明显不均。(图5)
查体:肛门见皮赘,进指后于左侧后壁扪及菜花样组织,距肛门较近,约4cm,向上界限不清,退指后指套无染血。
此时行MDT讨论,拟定下一步治疗,但查阅影像未见肿瘤,查体未扪及肿块,建议患者复查肠镜。
复查肠镜:未见肿瘤。肠道清洁度尚可,病人取侧卧位,循环进镜达回肠末端约5cm,未见异常。见回盲瓣及阑尾口正常:反复进退镜观察,距肛门10cm直肠见多个直径约0.2cm~0.3cm扁平息肉,表面光滑。据肛门5cm见环形皱襞,于十点钟方向见黏膜发白,皱襞集中。肛门口见数枚红色痔核。(图6)
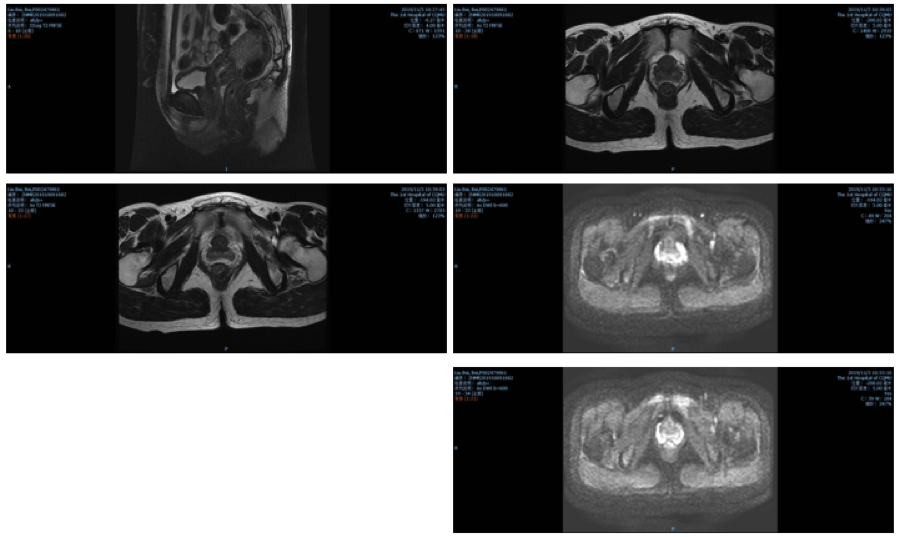
图5. 2019年11月4日经过5次特瑞普利单抗和5个周期化疗的MRI结果
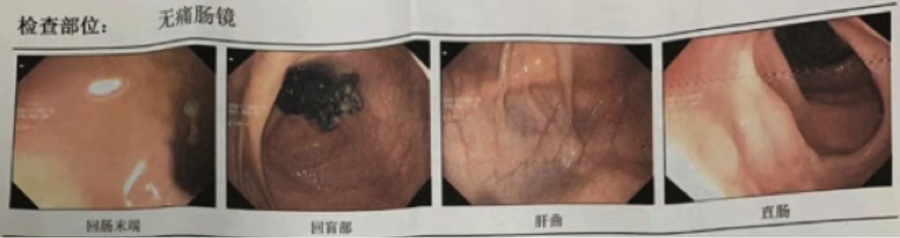
图6. 2019年11月8日经过5次特瑞普利单抗和5个周期化疗的
结直肠镜结果
疗效评估
再次行院内MDT讨论,查阅影像学未见肿瘤,查体:进指后未扪及肿块。复查肠镜:未见肿瘤。患者体征:感觉良好无异样。临床评估:完全缓解(CR)
小结
患者治疗历程如下:图7。

图7. 患者治疗历程图

重庆医科大学附属第一医院肿瘤科副主任;放射医学教研室副主任,医学影像技术教研室副主任。
国家卫健委肿瘤多学科诊疗(MDT)试点工作专家委员会成员
中国临床肿瘤学会(CSCO)结直肠癌专家委员会委员
中华医学会放射肿瘤学分会胃肠学组委员
中国医师协会放射肿瘤学医师分会委员
中国医师协会结直肠肿瘤医师分会MDT专委会委员
中国医师协会结直肠肿瘤医师分会放疗专委会委员
中国医师协会结直肠肿瘤医师分会内科专委会委员
中国抗癌协会肿瘤大数据与真实世界研究专委会委员
中国抗癌协会大肠癌专委会放疗学组委员
重庆医学会放射肿瘤学分会副主任委员
重庆医师协会放射肿瘤治疗医师分会副会长
重庆抗癌协会放射肿瘤专委会副主任委员
重庆抗癌协会肿瘤化疗专委会副主任委员
从病史可以看出该患者的治疗过程相对比较简单,但治疗策略及具体方案的选择是根据患者的临床病理特征,结合患者的个人意愿,做出的一些新的尝试。该患者入院时基于MRI分期,为cT3aN0M0,ⅡA期。对于局部晚期直肠癌患者,根据2019 CSCO指南,推荐行同步放化疗+经腹切除+辅助化疗(I级推荐,1A类证据)或短程放疗+经腹切除+辅助化疗(II级推荐,1B类证据),临床实践中,对于cT3aN0M0,且无局部高危复发风险因素的直肠癌患者也可采用手术+辅助化疗的治疗方案。该患者因自身原因拒绝局部治疗,包括手术及局部放疗。在全身系统治疗时,也因经济原因拒绝联合靶向治疗或免疫治疗。在尝试使用3个周期XELOX化疗,肿瘤退缩欠佳,疗效评估为疾病稳定后,患者愿意尝试使用免疫治疗,经过后续2个周期XELOX化疗和5周期免疫治疗后,患者在临床上达到了完全缓解。该例患者接受特瑞普利治疗1个周期后,肛门轻微坠胀,便血等不适症状明显改善,指检无染血,肿瘤标记物稳步下降,3月后复查影像学、肛门指检和肠镜都未见肿瘤,即达到cCR,且未出现明显的不良反应,生活质量良好,疗效颇佳,安全耐受性高。
免疫检查点抑制剂在晚期结直肠癌治疗领域取得的良好疗效,获得了NCCN、ESMO、CSCO等国内外各大指南认可,并推荐用于MSI-H/dMMR晚期结直肠癌患者的挽救治疗。另一方面,也推动了其在早期和局部晚期结直肠癌围手术期治疗领域相关研究的开展。NICHE研究:纳武利尤单抗 +Ipilimumab在早期结直肠癌新辅助双免疫治疗后,7例dMMR患者4例达到pCR(7例dMMR患者获得重大病理缓解)。VOLTAGE研究:局部进展期直肠癌新辅助放化疗后序贯纳武利尤单抗免疫治疗, 队列2最多纳入5例MSI-H的患者,术前放化疗后,接受5个周期的纳武利尤单抗,病理完全缓解(pCR)率达100%;以上研究结果均提示:针对MSI-H/dMMR的结直肠癌,免疫治疗的加入显著增加肿瘤退缩深度,肿瘤的病理完全缓解也明显高于既往的治疗方法。对于那些不可手术切除的局部晚期结直肠癌,或拒绝根治性手术的低位、早中期直肠癌,免疫检查点抑制剂的加入将可能获得令人惊喜的疗效。直肠癌术前放化疗以后临床完全缓解(cCR)患者“观察等待”的非手术治疗策略,将来也许会因免疫治疗而再次上演。正是基于上述研究结果的思考,结合患者的实际需求,我们尝试着加入免疫检查点抑制剂。
国内外指南推荐用于MSI-H/dMMR肠癌治疗的免疫检查点抑制剂是纳武利尤单抗和帕博利珠单抗,但价格昂贵,该例患者因经济原因拒绝上述两种标准推荐药物,选择了特瑞普利单抗,国产PD-1抑制剂最大的好处是性价比高,能承受其经济压力的患者更广。实际上,特瑞普利单抗也正在结直肠癌治疗领域进行应用探索。Clinical trial上注册有两项关于特瑞普利单抗治疗结直肠癌的研究,分别是中国医科院肿瘤医院发起的《立体定向放射治疗联合PD-1抑制剂治疗结直肠癌寡转移的II期研究》和中山大学第六医院发起的《特瑞普利单抗联合或不联合塞来昔布新辅助治疗可切除的伴错配修复蛋白缺陷或高度微卫星不稳定的非转移性结肠癌的初步研究》,结果将于2020年公布,希望上述研究的结果能够给我们的尝试提供更有力的证据。
此病例展示了免疫治疗针对MSI-H/dMMR局部晚期直肠癌治疗的疗效,同时也引发更多的思考和问题:1. 此例患者显著的疗效主要是来自免疫治疗联合化疗吗?单药免疫治疗是否足够?2. 完全缓解后下一步治疗是继续免疫治疗维持,还是手术?切除范围?3. 良好病理缓解能否转化为生存获益?4. 免疫治疗应用的时机,是否越早越好?期待进行更多的临床研究和临床探索来回答这些问题,为MSI-H/dMMR结直肠癌治疗带来新的革命。
排版编辑:GQ















 苏公网安备32059002004080号
苏公网安备32059002004080号


