2019年9月27日至10月1日,2019年欧洲肿瘤内科学会(ESMO)年会在西班牙巴塞罗那举行,该会议是欧洲最负盛名和最具影响力的肿瘤学会议,会议期间大量肿瘤临床治疗相关的研究结果公布,为推动肿瘤诊疗进步发挥巨大作用。乳腺癌诊疗通过分子分型,探寻更多的潜在治疗靶点,有望进一步改善晚期乳腺癌的预后。在本次大会上,两项研究采用Foundation Medicine Inc.(FMI)开发的全面基因组检测(CGP检测)平台,在转移性乳腺癌患者中检测PIK3CA和BRCA1/2突变状态,助力晚期乳腺癌精准诊疗。
(一)转移性乳腺癌中PIK3CA基因突变
306PD 探索PIK3CA在转移性乳腺癌中的突变率
随着第一个特异性PIK3CA抑制剂alpelisib的获批,探索PIK3CA突变率以及不同亚型乳腺癌患者中PIK3CA的突变形式成为研究热点。目前,对于转移性乳腺癌,PIK3CA突变检测已经列入NCCN指南。本研究纳入了4096例转移性乳腺癌患者,其中ER+/HER2-,HER2扩增和TNBC分别为1249、1922和925例。对所有患者进行FoundationOne CDx检测,分析基因变异谱、TMB和MSI状态。研究同时使用SP142 IHC检测PD-L1表达。
在不同亚型的晚期乳腺癌中,PIK3CA突变状态见下方(表1,图1)。其中,PIK3CA基因在ER+(39%)和HER2扩增(37%)患者中的变异率,高于TNBC患者(21%)。PIK3CA基因的变异形式主要表现为点突变和小片段插入突变,在所有乳腺癌亚型中,PIK3CA H1047R是最常见的变异形式。ESR1基因变异在ER+患者发生率更高。BRCA1基因变异在PIK3CA突变的TNBC中最常见。BRCA2基因变异在PIK3CA突变的ER阳性患者最常见。FGFR1基因变异在PIK3CA突变的ER阳性患者中最常见。EGFR和BRAF突变多见于PIK3CA突变的TNBC患者。与免疫治疗获益相关的生物标志物,如CD274扩增和PD-L1表达在TNBC乳腺癌中发生率最高。TMB在PIK3CA突变的队列中最高,无论患者是什么乳腺癌亚型。
表1. 在不同亚型的晚期乳腺癌中,PIK3CA突变状态分析
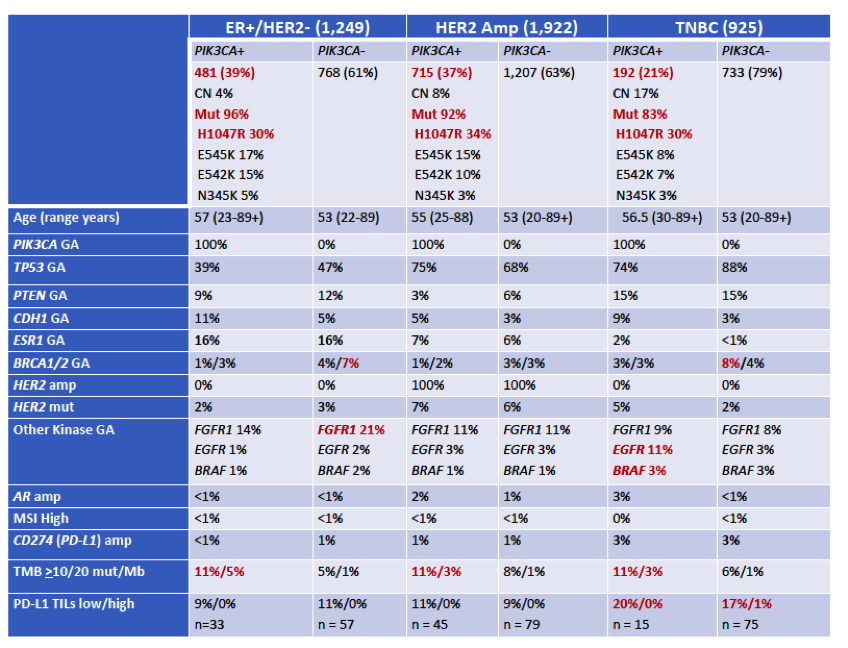
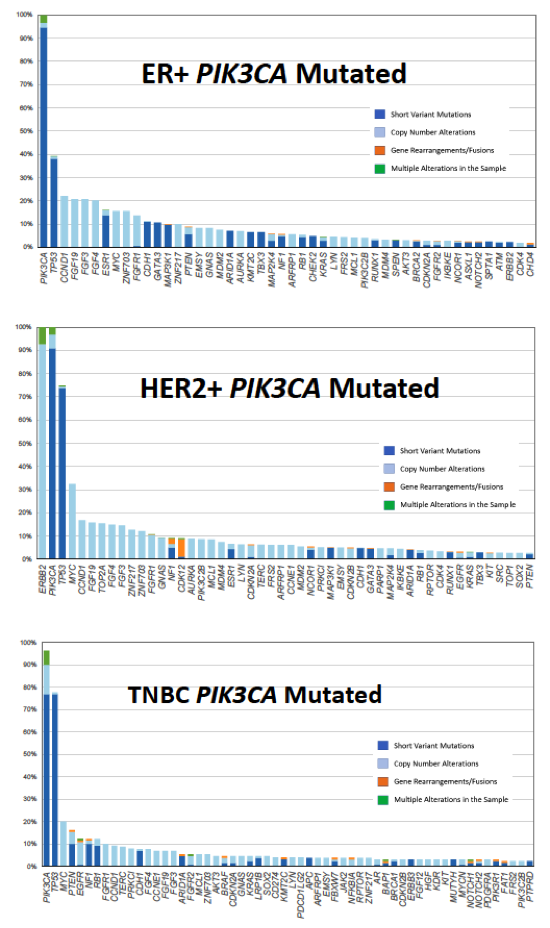
图1. 不同亚型PIK3CA突变的乳腺癌中,常见共存基因的长尾现象
会上同时报道了2例PIK3CA突变的患者:病例1(图2)为转移性ER+/HER2+复发性导管乳腺癌,合并肾上腺转移,67岁女性。患者已经接受了内分泌治疗(AI)和抗HER2曲妥珠单抗治疗。患者检测发现H1047R PIK3CA突变,ERBB2扩增(拷贝数18个)、ESR1 D538G突变和FGFR1扩增(拷贝数7个),以及TP53 K373fs* 49突变。TMB为19 mut/Mb,未进行PD-L1 IHC 检测。患者检测到PIK3CA突变提示患者可能对内分泌治疗和抗HER2治疗耐药。目前患者正在接受PIK3CA靶向治疗和免疫检查点抑制剂治疗。
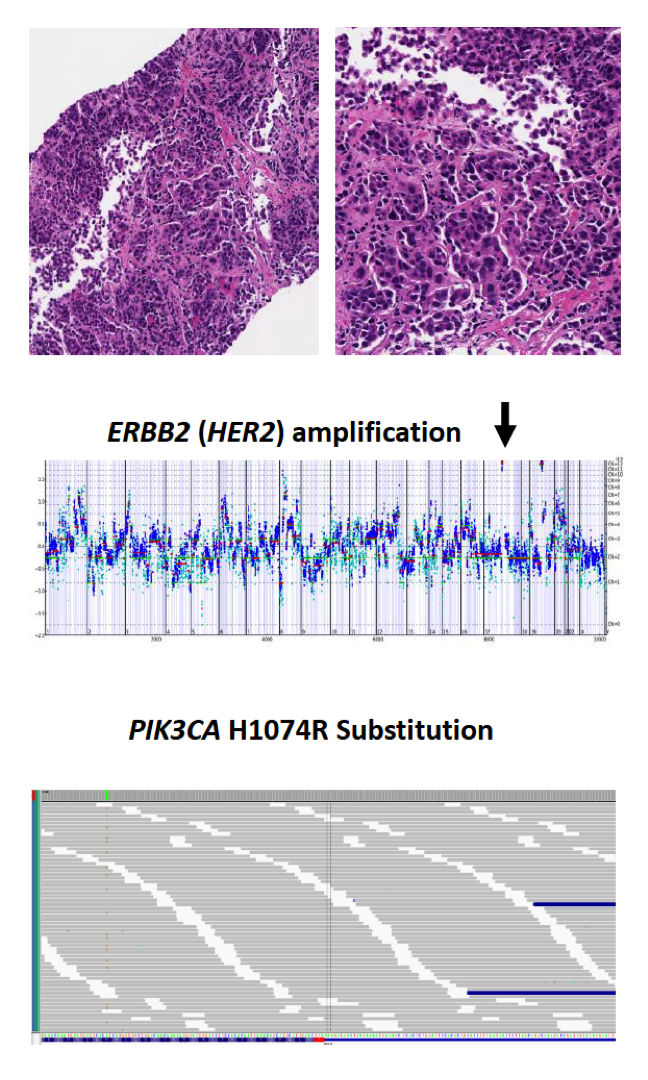
图2. 病例1
病例2(图3)为TNBC乳腺癌,转移至肝脏,67岁女性。患者既往接受过多线化疗后进展。FoundationOne CDx检测发现PIK3CA Q546K突变同时合并FGFR2扩增(拷贝数15个)以及FGFR2短片段突变 (C382R)。其他基因变异包括CTNNA 1缺失,JAK2扩增和TP53 Q144 *突变。患者为MSI稳定型,TMB为9 mut/Mb,未进行PD-L1 IHC检测。这例患者可以接受的潜在靶向治疗包括PIK3CA抑制剂、FGFR2抑制剂;考虑到患者的TMB中等,可以尝试接受免疫治疗。
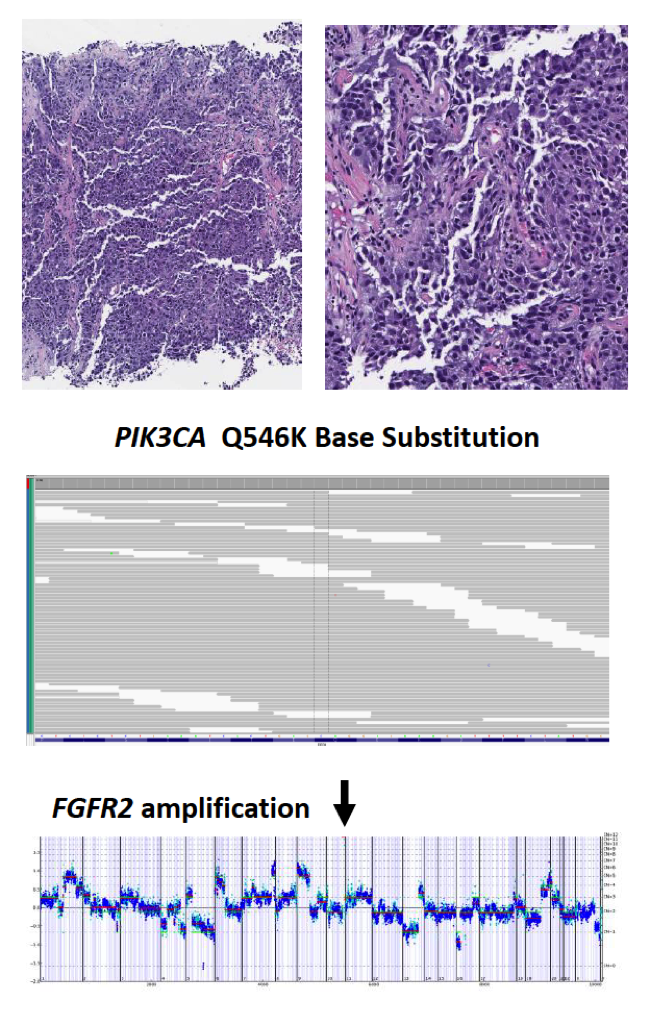
图3. 病例2
小结:本研究探索了转移性乳腺癌中PIK3CA变异状态。PIK3CA变异会影响其他标志物,如TMB相对更高等。PIK3CA基因变异形式在不同亚型乳腺癌中分布并不一致,这些发现可能指导PIK3CA抑制剂未来在转移性乳腺癌中的使用。
(二)转移性乳腺癌中BRCA1/2突变分析
314P 对II期ABRAZO研究中的患者进行NGS测序:评估Talazoparib用于既往接受过铂类或非铂类细胞毒性化疗进展的BRCA1/2突变型晚期乳腺癌
PARP1和PARP2在单链DNA损伤修复中扮演重要作用,PARP抑制剂可以阻断DNA损伤修复位点的PARP蛋白。携带BRCA1/2突变的癌细胞,不能通过同源重组修复断裂的双链DNA。PARP抑制剂可以引发肿瘤细胞的协同致死,进而实现杀伤肿瘤的作用。Talazoparib是一个有潜力的PARP抑制剂。目前,Talazoparib已在美国、欧洲等地区获批用于胚系BRCA1/2突变,HER2阴性的转移性乳腺癌。ABRAZO是一项两个队列、两个阶段的II期研究,队列1入组了对既往铂类治疗有响应,距离最后一次用药8周以内未进展的gBRCA1/2突变携带者;队列2入组了接受过≥3线不含铂细胞毒化疗的患者。在两个队列中,Talazoparib均显示出确认的疗效。
在HER2阴性、gBRCA1/2突变的局部晚期或晚期乳腺癌中,患者的基因突变谱是否影响其接受PARP抑制剂治疗的疗效,目前尚未明确。本研究纳入了ABRAZO研究中的患者,旨在检测BRCA1/2突变(包括胚系和体细胞突变)、其他参与同源重组修复(DDR)的基因、同源重组修复缺陷(HRD)状态(使用基因组杂合性缺失gLOH评估)以及这些基因突变谱与疗效的关系。
本研究对ABRAZO研究中入组患者基线肿瘤组织(原发或转移灶)进行FoundationOne CDx NGS检测。84例入组患者中,60例(71%)有足够的组织标本进行NGS测序。这些入组患者中,79例既往采用BRACAalysis CDx检测证实携带致死性或可疑致死性gBRCA突变,另外5位患者使用当地其它BRCA1/2检测。
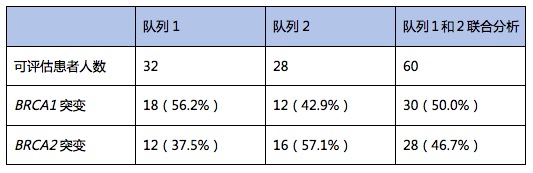
60例接受FoundationOne CDx检测的患者,58例(97%)检测到至少1个肿瘤BRCA1或BRCA2突变,没有患者同时合并BRCA1和BRCA2突变,见下表2。2例未检测到肿瘤BRCA1/2突变的患者,检测到BRCA2意义未知的突变体,与他们已知的gBRCA2突变不同。肿瘤BRCA1/2突变最常见的变体类型为单核苷酸变异、缺失或插入。58例患者中,1例检测到BRCA1拷贝数变异。
表2. 肿瘤BRCA1/2突变(可评估ITT人群)
55例患者参与评估胚系和肿瘤组织BRCA突变状态的一致性,结果显示,53例(96%)患者表现出胚系和肿瘤BRCA突变状态相似(图4)。
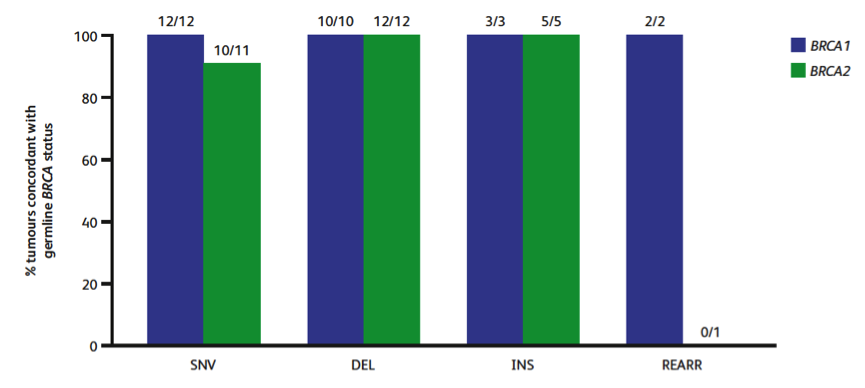
图4. 肿瘤组织FoundationOne CDx检测有较高的敏感性发现胚系BRCA1/2突变
47例可评估患者,40例(85%)表现为BRCA杂合性丢失(LOH),保留突变的BRCA等位基因。这40例患者中,37例患者,肿瘤组织检测到gBRCA突变,1例表现为肿瘤获得性BRCA突变,2例患者gBRCA突变状态未知。
肿瘤组织中非BRCA1/2突变谱:在BRCA突变肿瘤中,TP53和PIK3CA是最常见的非BRCA基因突变,排除拷贝数变异。在BRCA1突变患者中,TP53突变更常见,这一趋势在队列1中更明显;在BRCA2突变的患者中,PIK3CA突变更常见。在BRCA突变的肿瘤中,如果同时考虑拷贝数变化,RAD21和MYC是最常见变异基因。
基因突变谱和Talazoparib疗效的关系:
1. 肿瘤BRCA1/2突变相关性分析:在BRCA1和BRCA2突变的肿瘤中,Talazoparib的疗效相当:队列1临床响应与BRCA突变关系分别为4/17(24%)和8/12(67%);队列2分别为3/12(25%)和10/16(63%)。队列2中,在5例未携带BRCA1/2 LOH的患者和19例携带BRCA1/2 LOH的患者中,采用Cox比例风险模型评估BRCA1/2突变状态对PFS的影响,未观察到PFS显著差异 [HR (95% CI): 1.057 (0.384-2.904); P=0.915]。队列1由于BRCA1/2 LOH阴性人数太少,未开展这一分析。
2. DDR突变相关性分析:队列2中,DDR突变数(2 vs 1)和Talazoparib最佳疗效具有显著相关性,单个突变与更好的疗效相关,见下图5。但队列1中未观察这一现象。与这一现象一致,在BRCA突变队列中,非BRCA DDR突变并不会增加Talazoparib治疗的敏感性(见图2)。
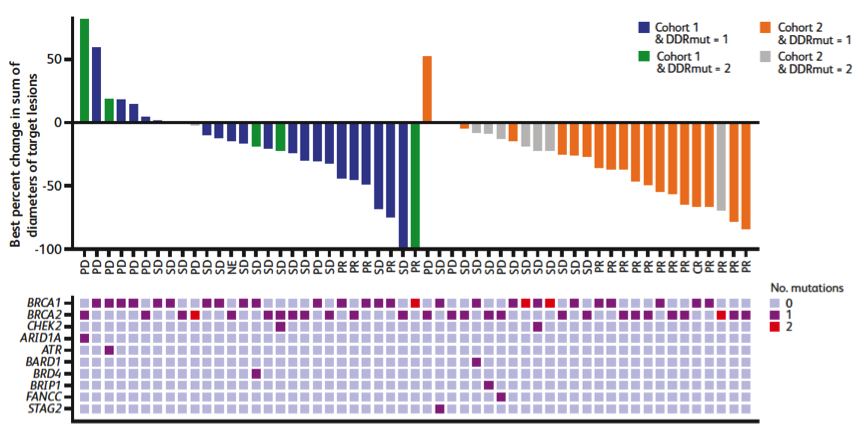
图5. 研究者评估自基线开始的最佳疗效:根据DDR突变数目分析
3. 非DDR突变的相关性分析:探索常见的非DDR突变与疗效的相关性,结果显示,队列1和队列2中,未观察到TP53、RAD21、MYC、PIK3CA和PTEN与Talazoparib PFS的关系。
4. gLOH评分的相关性分析:在队列2中观察到未取得临床获益的患者,gLOH评分有更高的趋势(非显著),在队列1中也观察到相似的现象,见图3。总体而言,基于本次分析,并不能明确gLOH评分和疗效的关系。
小结:本研究对ABRAZO研究中的患者进行FoundationOne CDx 检测,探讨CGP检测平台检测BRCA1/2突变的敏感性,同时评估其他分子突变谱对PARP抑制剂疗效的影响。结果显示——85%的可评估病人中,至少1个肿瘤BRCA状态表现为LOH;BRCA1和BRCA2突变的肿瘤其突变谱有所不同;BRCA1或BRCA2突变的患者临床获益相近;在BRCA1/2突变患者中,是否存在非BRCA1/2的DDR基因的突变,对Talazoparib敏感性并无影响。本研究证明,基于gBRCA突变状态来筛选从PRAP抑制剂中获益的人群是合适的。
(三)总结
上述两项研究均采用FoundationOne CDx 平台对晚期乳腺癌患者进行检测,第一个研究探索了转移性乳腺癌中PIK3CA变异状态;第二项研究分析了患者的BRCA突变状态,发现FoundationOne CDx检测平台与单基因检测平台的检测结果高度吻合。同时两项研究还探索了其他共存的基因突变,对靶向药物疗效的可能影响等,为患者靶向治疗选择提供重要参考。

中山大学肿瘤防治中心
中国临床肿瘤学会(CSCO)青委会委员
广东省胸部肿瘤防治委员会乳腺癌专业委员会委员兼秘书长
中国南方肿瘤临床研究协会(CSWOG)青委会常委
广东省医学教育协会肿瘤学专业委员会常委委员
广东省中西医结合学会乳腺病专业委员会委员
广东省药学会乳腺科用药专家委员会委员
乳腺癌主要根据临床病理和分子分型开展治疗,但三阴性乳腺癌(TNBC)和难治性多发耐药性乳腺癌(如内分泌治疗耐药后的激素受体阳性乳腺癌,或曲妥珠单抗等抗HER2靶向药耐药后的HER2阳性乳腺癌),仍然缺乏有效的治疗靶点。随着基因组学的研究进展,乳腺癌的分子生物学特征谱也逐渐清晰,而基因组学研究下的新靶点探寻,也成为乳腺癌个体化治疗研究的重要课题。此外,随着Atezolizumab在乳腺癌的获批,从分子层面探索免疫治疗优势人群也成为临床关注的热点。采用全面的基因组测序方法,如FMI的FoundationOne CDx检测,可一次检测324个基因,同时还可以提供TMB及MSI 信息,为探寻乳腺癌的潜在治疗靶点和评估免疫治疗获益的可能提供重要信息。
上述两项研究均采用FMI FoundationOne CDx检测对转移性乳腺癌患者的基因突变谱进行分析。第一项研究在大样本量的转移性乳腺癌患者中评估了不同亚型乳腺癌患者中PIK3CA基因突变状态,随着PIK3CA抑制剂的上市,探索不同亚型乳腺癌患者中这一基因的变异状态,为筛选PIK3CA抑制剂获益的人群提供重要思路。研究同时还分析了患者其他的基因分子特征以及免疫治疗相关的预测靶点情况。第二项研究采用FoundationOne CDx检测肿瘤组织中BRCA突变状态,结果与单基因检测具有较高的一致性。研究同时在BRCA突变患者中分析了DDR突变数、gLOH评分与患者接受PARP抑制剂疗效的关系,结果显示采用FoundationOne CDx对肿瘤组织进行BRCA1/2突变检测,作为筛选PARP抑制剂的适用人群是非常合理的。这一研究也证实了FMI CGP检测的准确性,提示该检测不仅能检测现有靶向治疗的目的基因,还能发现肿瘤的其他突变谱,进而预测其从相应靶向治疗中获益的可能性。
[1]PIK3CA Alterations in Metastatic Breast Cancer. 2019 ESMO, abs 306PD.
[2]Next-generation DNA Sequencing Results for Tumours From Phase 2 ABRAZO Study of Talazoparib After Platinum or Cytotoxic Non-platinum Regimens in Patients With Advanced Breast Cancer and Germline BRCA1/2 Mutations. 2019 ESMO, abs 314P.











 苏公网安备32059002004080号
苏公网安备32059002004080号


