本例为1例弥漫大B细胞淋巴瘤/高级别B细胞淋巴瘤伴有MYC和BCL-2重排(生发中心来源,IVA期,IPI4分)患者,2024年8月因下腹部疼痛就诊,经病理、影像学及分子检测确诊。病程中先后在北京,东北等多家医院接受多线治疗,疾病仍不断进展并出现中枢和骨髓浸润。徐州医科大学附属医院桑威主任团队和吉林大学第一医院白鸥主任国巍大夫团队经过多次讨论,为患者制定了“异基因造血干细胞移植及供者CD19 CAR-T”治疗方案,患者最终达到完全缓解。
徐州医科大学附属医院血液内科
2025级博士研究生
病例简介
患者:女,43岁。
主诉:2024年8月就诊时主诉下腹部疼痛,无发热、寒颤等症状,自发病来饮食睡眠尚可,体重未见明显变化。
辅助检查:
盆腔肿物穿刺活检(外院2024-09-13):穿刺肿瘤组织由中等偏大的淋巴样细胞排列,可见分裂象。免疫组化:CD56(-)、Ki-67(+90%)、BCL-2(+90%,强阳)、Bcl-6(-)、CD10(+)、CD20(+)、CD30(-)。
FISH检测:MYC及BCL-2断裂/分离。
基因突变筛查:MYC及BCL-2突变。
PET-CT(外院2024-9-12):双附件区囊实性肿物,代谢活性不均匀增高,伴腹膜增厚、代谢活性增高,盆腔积液,考虑腹膜转移:全身多处骨骼、淋巴结受累,包括颅底骨质、双侧肱骨等多部位,双侧胸腔积液、心包积液。
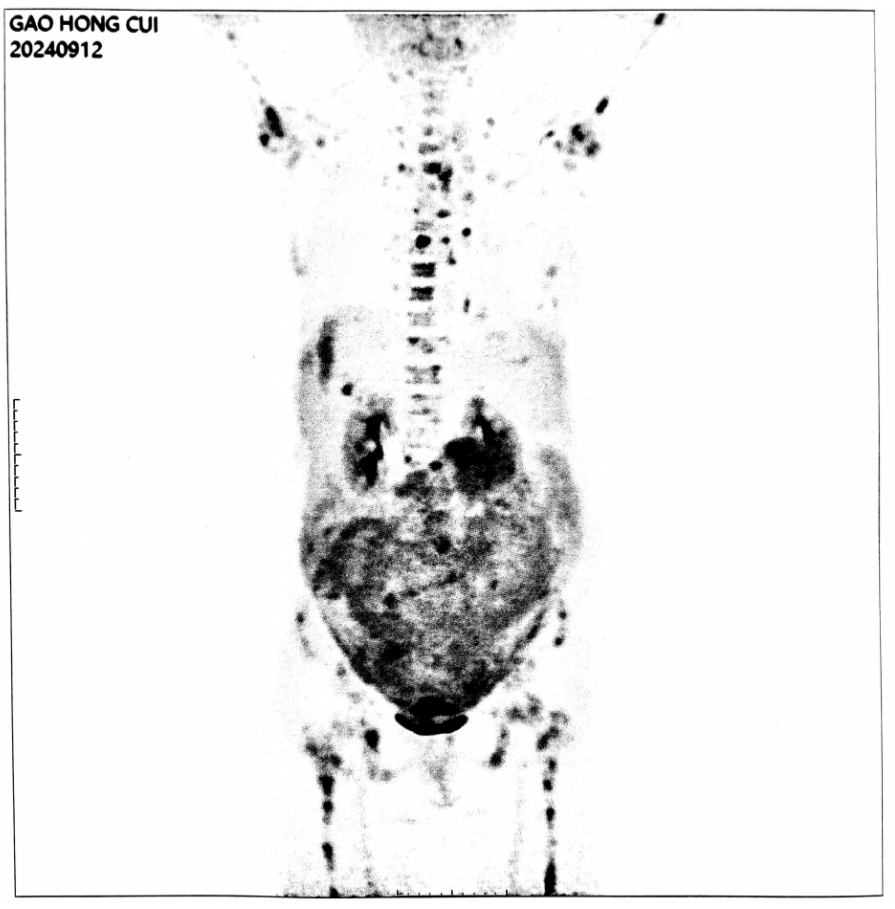
诊断:弥漫大B细胞淋巴瘤/高级别B细胞淋巴瘤伴有MYC和BCL-2重排(生发中心来源,IVA期,IPI4分)
外院治疗经过
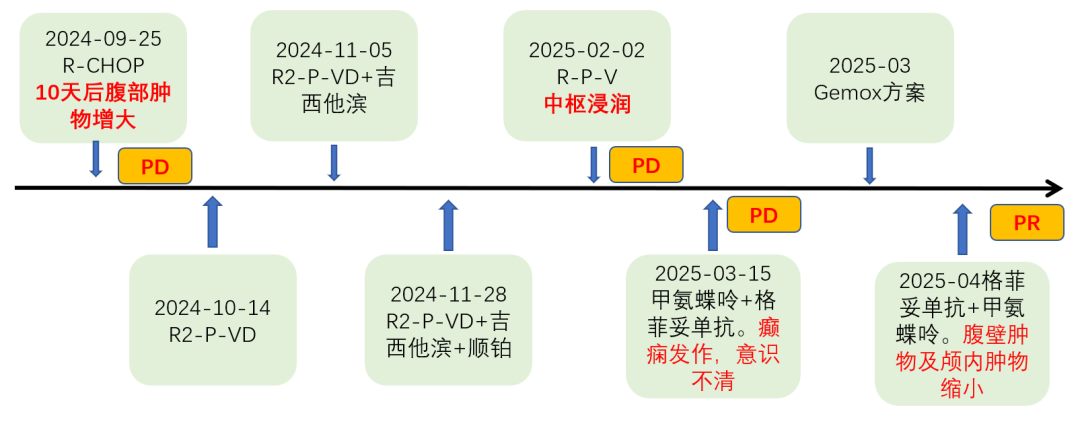
1、2024-09-25 予R-CHOP方案治疗,10天后腹部肿物增大。
2、2024-10-14 更改为R2-P-VD方案化疗。
3、2024-11-05 予R2-P-VD联合吉西他滨化疗。
4、2024-11-28 R2-P-VD联合吉西他滨、顺铂化疗。
5、2025-02-02 予R-P-V方案化疗。
6、2025-03-12 PET:患者出现中枢浸润。疾病进展。
7、2025-03-15 予甲氨蝶呤+格菲妥单抗治疗。患者出现癫痫发作,意识不清。
8、疾病进展,加用Gemox方案,口服泽布替尼继续治疗。
9、2025-04 予格菲妥单抗+甲氨蝶呤方案治疗。患者腹壁肿物及颅内肿物缩小,考虑疗效PR。
本院入院病情评估
1、骨髓流式细胞术:CD19 + B 淋巴细胞约占全部有核细胞 0.19%,表型为 CD19+,CD5+,CD20+, CD10-,CD56-,CD4-,CD8-,为异常表型单克隆 B 淋巴细胞。
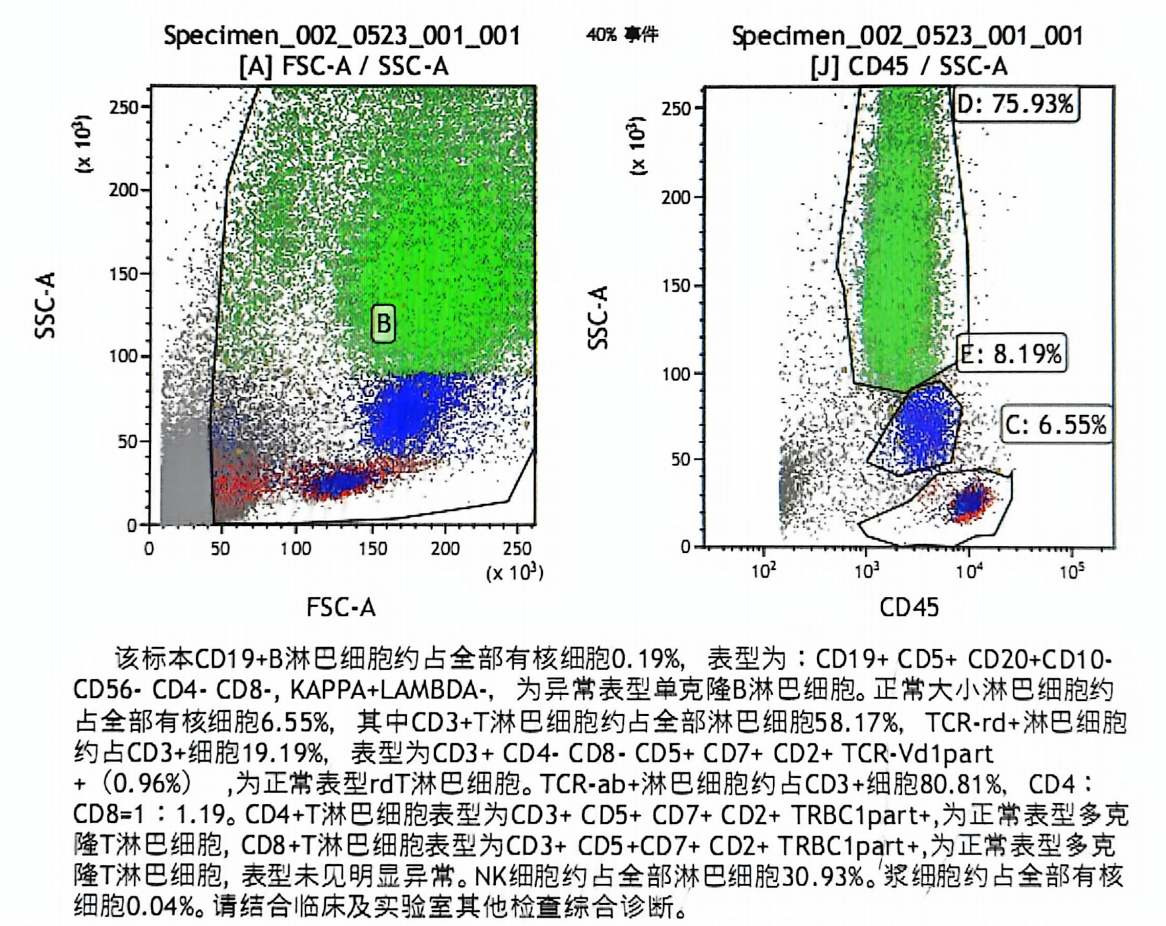
2、病理切片加做免疫组化:本院免疫组化:瘤细胞CD19(+)、CD22(弱+)、CD5(-)、PD1(-)、CD99(-)、P53零表达、TDT(-)。

3、PET-CT(本院2025-05-23):肠系膜局部壁增厚,PET 摄取稍增高,SUVmax 约为 4.4g/ml,右下腹壁皮下团片状软组织密度影,SUVmax 约为 3.6g/ml。
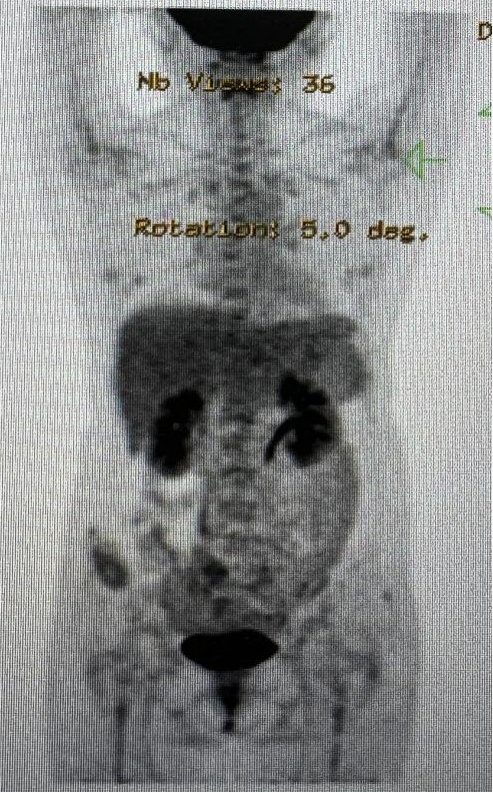
本院治疗经过
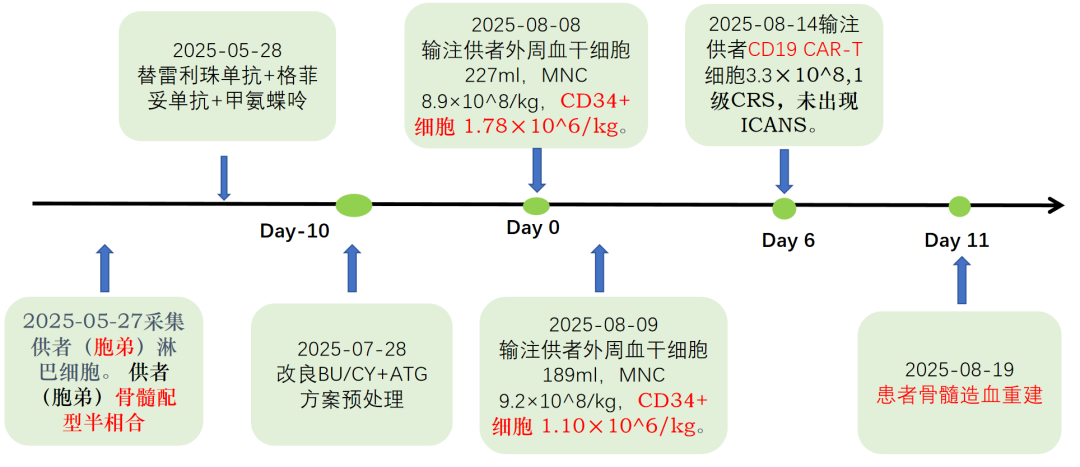
1、2025-05-27采集供者(胞弟)淋巴细胞。 供者(胞弟)骨髓配型半相合。
2、2025-05-28 替雷利珠单抗联合格菲妥单抗、甲氨蝶呤桥接化疗。
3、2025-07-28(-10天)改良BU/CY+ATG方案预处理。
2025-08-08 输注供者外周血干细胞227ml,MNC 8.9×108/kg,CD34+细胞 1.78×106/kg。
2025-08-09 输注供者外周血干细胞189ml,MNC 9.2×108/kg,CD34+细胞1.10×106/kg。
2025-08-14(+6天)输注供者CD19 CAR-T细胞3.3×108,1级CRS,未出现ICANS。
2025-08-19(+11天)患者骨髓造血重建。
疗效评估
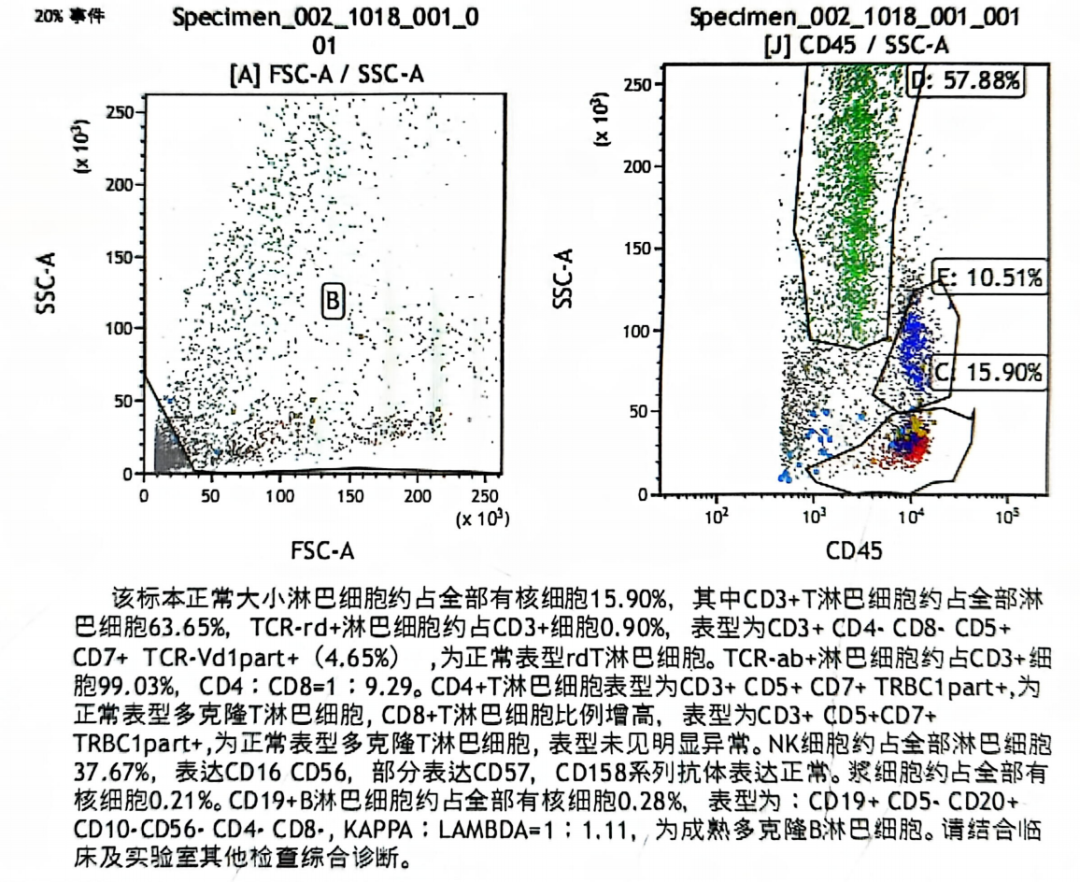
1、复查骨髓流式细胞术(2025-09-10):正常大小淋巴细胞约占全部有核细胞15.9%,CD19+B淋巴细胞约占全部有核细胞0.28%,表型为:CD19+ CD5-,CD20+,CD10-,CD56-,CD4-,CD8-,KAPPA : LAMBDA=1: 1.11,为成熟多克隆B淋巴细胞。
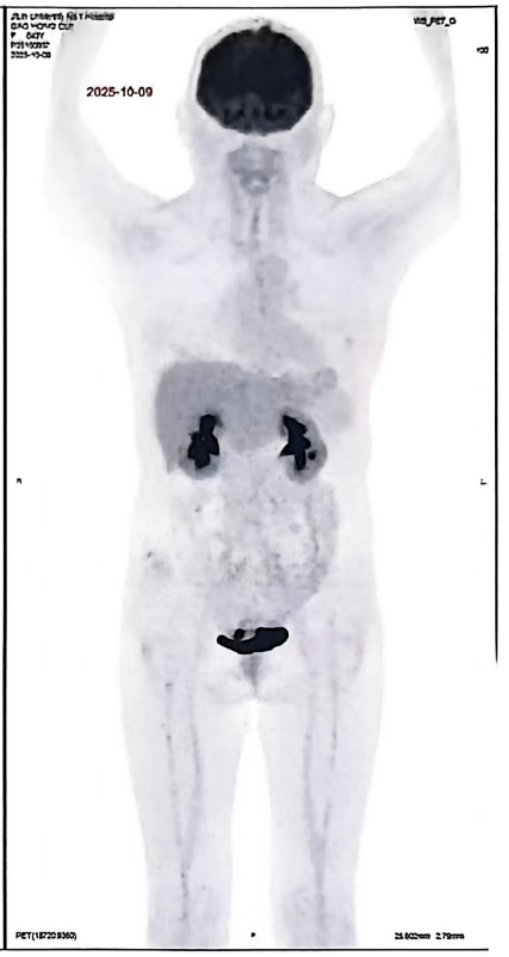
2、外院PET-CT(2025-10-09):完全缓解(CMR)
(1)前次所示右侧颞叶、右侧颞前区皮下、宫颈及盆腔肠管代谢病灶,均消失,考虑淋巴瘤活性受抑。(2)脾不大,代谢不高;全身所示骨骼及髓腔未见异常高代谢。
专家点评
徐医附院细胞研究和转化医学中心副主任
徐医附院血液科科副主任,淋巴瘤病区主任
中华医学会血液学分会淋巴细胞疾病学组委员
中国抗癌协会淋巴瘤专委会委员
中国临床肿瘤学会淋巴瘤专家委员会委员
中国EBV相关疾病工作组秘书长
中国老年医学会血液学分会淋巴瘤学组委员中国中国抗癌协会血液肿瘤专业委员会青年委员
中国抗癌协会血液肿瘤委员会委员
江苏省医学会血液学分会青年委员会副主任委员
江苏省淋巴瘤联盟副主席
江苏省医学会血液学分会淋巴瘤学组委员
江苏省“六大人才高峰”“333”人才培养对象
江苏省“科教强卫工程”青年医学人才
国家自然科学基金评审专家
异基因造血干细胞移植(allo-HSCT)联合供者CD19 CAR-T细胞治疗,是多线治疗暴露失败的复发难治B细胞淋巴瘤的终极治疗方案。本例43岁女性患者,确诊双打击DLBCL(生发中心来源,IVA期,IPI 4分),经多线化疗失败,伴全身多脏器转移及中枢浸润,疾病进展迅猛,经格菲妥单抗联合方案获部分缓解后,通过半相合allo-HSCT联合供者CD19 CAR-T治疗达到完全缓解,充分证实该联合方案的抗瘤价值。半相合allo-HSCT可重建供者免疫系统,发挥移植物抗淋巴瘤(GvL)效应,为CAR-T治疗奠定基础;供者来源CD19 CAR-T细胞则具备更强的靶向杀伤活性与持久性,与GvL效应协同,实现难治性病灶深度清除。
感染、细胞因子释放综合征(CRS)及移植物抗宿主病(GVHD)是该联合治疗的主要毒性风险,直接影响预后。感染防控需贯穿治疗全程,CRS与GVHD的早期识别和调控是治疗成功的关键。本例患者输注CAR-T后仅出现1级CRS,无ICANS,造血重建顺利,未发生严重GVHD,提示优化桥接化疗、预处理方案及严密监测可有效降低不良反应风险。患者前期化疗曾出现中枢毒性,警示临床需平衡疗效与毒性防控。本案例通过全程精细化管理(肿瘤负荷控制、功能监测、毒性干预、支持治疗),保障患者顺利完成治疗,凸显了全程管理的重要性。
综上,半相合allo-HSCT联合供者CD19 CAR-T,为多线治疗失败、合并中枢浸润的高危双打击DLBCL患者提供了“免疫重置+精准靶向”的挽救路径。尽管该方案仍面临预处理毒性、GVHD防控、长期复发监测等挑战,但对传统治疗无效的患者而言,仍是值得探索的重要选择。未来,需进一步优化治疗方案、个体化调控CAR-T输注策略、完善并发症预防与复发监测体系,以提升患者长期生存率及生命质量。
吉林大学第一医院
美国路易维尔大学 访问学者
中国老年医学学会血液学分会 常委
中国老年医学学会血液学分会 第二届 委员 青年学组 秘书
中国抗癌协会第一届淋巴瘤整合康复专业委员会 常委
CSCO抗白血病联盟&抗淋巴瘤联盟第一届青年委员会 委员
中国慢性淋巴细胞白血病工作组 青年学组 委员
中国人体健康科技促进会 中枢淋巴瘤多学科诊疗专业委员会 委员
中国北方慢性淋巴细胞白血病中青年协作组 委员
北京影像诊疗技术创新联盟 血液病数字诊疗专业委员会 委员
吉林省健康管理学会淋巴肿瘤专业委员会 秘书
患者青年女性,2024年8月,多处结外占位起病,确诊为高级别B细胞淋巴瘤(DHL)Ⅳ期,IPI 4分。2024.8~2025.3 先后就诊3家医院,经历2线,5疗程免疫化疗无效,疾病持续进展。2025.5就诊吉大一院血液科,就诊时患者再次进展并新发中枢浸润,ECOG 3分。
回顾诊治经历,患者为年轻,高度侵袭性,原发难治大B细胞淋巴瘤,且因多疗程治疗后,体能显著下降,治疗耐受性差,临床高危。治疗极具挑战,无标准方案,需进行高度个体化策略。出于快速控制病情的目的,就诊吉大一院血液科,给予CD20/CD3双抗联合MTX方案。入院后完善的NGS结果显示为EZB亚型,伴TP53突变。经3疗程治疗,虽然疗效达PR,但是骨髓抑制达4度,治疗难以如期进行。因此需寻求更加有效的治疗措施。
幸运的是患者有同胞全合供者。因此经会诊,患者及时的在徐医附院血液科(桑威教授团队)接受了CAR-T联合异基因造血干细胞移植治疗,获得完全缓解。
此患者是新型治疗方法对原发难治高危大B细胞淋巴瘤挽救治疗成功的范例,为高度难治DLBCL挽救治疗提供了新的临床实践依据。
排版编辑:肿瘤资讯-robin











 苏公网安备32059002004080号
苏公网安备32059002004080号


