CTS5是 一种简单的临床病理学工具,用以评估ER阳性乳腺癌患者经过5年内分泌治疗后的晚期远处转移(DR)残余风险。CTS5以ATAC研究为训练集创建的,并以BIG 1-98研究为验证集验证其有效性。主要研究终点是内分泌治疗5年后发生晚期远处转移的时间。此次2019ASCO会议发布了关于CTS5的最新研究结果,李俊杰教授将为我们解读这一结果。

复旦大学附属肿瘤医院乳腺外科
现任乳腺外科教学秘书
中国抗癌协会乳腺癌专业委员会青委
中华医学会乳腺肿瘤学组青委
上海市抗癌协会乳腺癌专业委员会青年委员及青委会秘书
JCO 中文版青年专家等职务
《中华乳腺病杂志》中青年编委
乳腺癌是全球女性高发癌症,在中国最新统计数据乳腺癌已跃居成为女性发病率第一的恶性肿瘤。2018年GLOBOCAN数据提示中国每年新发乳腺癌超过36万例。
大部分乳腺癌患者初诊时属于早期阶段。其中,80%左右为激素受体阳性(HR+)患者。 激素受体阳性患者术后存在长期复发风险, 5年的标准内分泌治疗可显著降低患者的近期疾病复发风险,但与激素受体阴性患者不同,HR+乳腺癌术后的远期复发风险持续存在,即使T1N0的患者5~20年的远期复发率仍达14%,因此5年标准内分泌治疗仍然无法避免患者的远期复发风险,对于接受标准5年内分泌治疗后的延长治疗,既往已有多项临床研究对此观点进行探讨,2018年SABCS公布的EBCTCG 荟萃分析结果提示,接受5年他莫昔芬(TAM)治疗后绝经的HR阳性早期患者,继续5年芳香化酶抑制剂(AI)延长治疗可降低35%的复发风险;接受5年TAM序贯AI或5年AI治疗后绝经期的HR阳性患者,继续3~5年AI延长治疗可降低20%的复发风险。绝对获益上,延长内分泌治疗与不延长相比,能够降低2.5%的乳腺复发事件;5~10年的TAM和AI联合或者序贯治疗能够降低2.1%的乳腺复发事件;单纯5年AI后再延长能够降低1.2%的乳腺复发事件。虽然延长内分泌治疗可以降低乳腺癌的远期复发风险,但可以看到这些数据绝对获益都是比较低的,提示并非所有患者都适合延长内分泌治疗。因此寻找哪些患者适合延长内分泌治疗,成为临床实践中的重要问题。如果有一种工具能评估5年内分泌治疗后ER阳性乳腺癌患者晚期远处转移残余风险,将为这些患者的治疗带来很大的获益。因此,英国皇家马斯登医院Ralph Lauren乳腺癌研究中心Mitch Dowsett教授领衔的多机构联合团队开发并验证了CTS5。
CTS5(Clinical Treatment Score post–5 years)是 一种简单的临床病理学工具,用以评估ER阳性乳腺癌患者经过5年内分泌治疗后的晚期远处转移残余风险。CTS5是以ATAC(阿那曲唑、他莫昔芬,单药或联合用药)研究为训练集创建的(n= 4735),并以BIG 1-98研究为验证集(n= 6711)验证其有效性。主要研究终点是内分泌治疗5年后发生晚期远处转移的时间。
CTS5(ATAC)=0.471×阳性淋巴结个数+0.980×(0.164×肿瘤大小-0.003×肿瘤大小平方+0.312×肿瘤分级+0.03×年龄)
在ATAC队列(HR=2.47; 95% CI 2.24~2.73; P< 0.001)和Big1-98验证队列( HR =2.07; 95% CI 1.88~2.28; P<0.001)显示出高度的一致性。 在训练集中定义的CTS5 (ATAC)风险分层为低(,第5~10年的远处转移风险< 5% )、 中(5%~10%)和高(>10%)风险,在验证集中发现43%患者为低风险,观察到的第5~10年远处转移率为3.6% (95%CI 2.7%~4.9%) ,第5~10年有63%的淋巴结阴性患者为低风险,远处转移率为3.9% (95%CI 2.9%~5.3%),有24%的1~3个淋巴结阳性的患者为低风险,远处转移率为1.5% (95%CI 0.5%~3.8%)。
最终的CTS5算法确定42%的女性每年有1%的远处转移风险,这些患者被认为是延长内分泌治疗潜在价值有限的低危患者。也就是说有48%的患者为中高危患者,需要接受内分泌延长治疗。
目前CTS5仅是在已经报道的III期研究中做了模型建立和验证,在非研究的真实世界中CTS5的有效性尚无报道,2019年ASCO报道了来自Mitch Dowsett及其团队的评估CTS5在非研究ER+早期乳腺癌人群的CTS5有效性验证的回顾性研究。
研究设计
对2000—2007年诊断为早期ER+乳腺癌的非临床试验患者的回顾性分析,验证CTS5的有效性。主要研究终点为远期远处转移 (5~10年)。Cox回归模型用于确定CTS5的预后价值,并生成与10年远处转移风险相关的Kaplan-Meier曲线(%)。
研究结果
研究共纳入2428名患者,平均随访时间为9.34年(表1)。CTS5对绝经后和绝经前的远期远处转移有显著的预测作用(表2)。绝经后队列的CTS5风险分层与之前的BIG1-98/ATAT训练队列比较。42.1%的绝经后妇女被归为低风险组,远期远处转移风险为4.9%,与中、高危组相比,这些患者远期远处转移风险显著降低(表2)。在绝经前人群中,41%被归为低风险,远期远处转移风险为4.9%(图1)。CTS5对化疗和未化疗患者的预后评估显示化疗(HR=2.26, 95%CI 1.68~3.03)和未化疗(HR=1.93, 95%CI 1.32~2.82),CTS5对绝经后远期远处转移的复发风险与观察结果高度一致(图2) 。
表1 入组患者基线特征
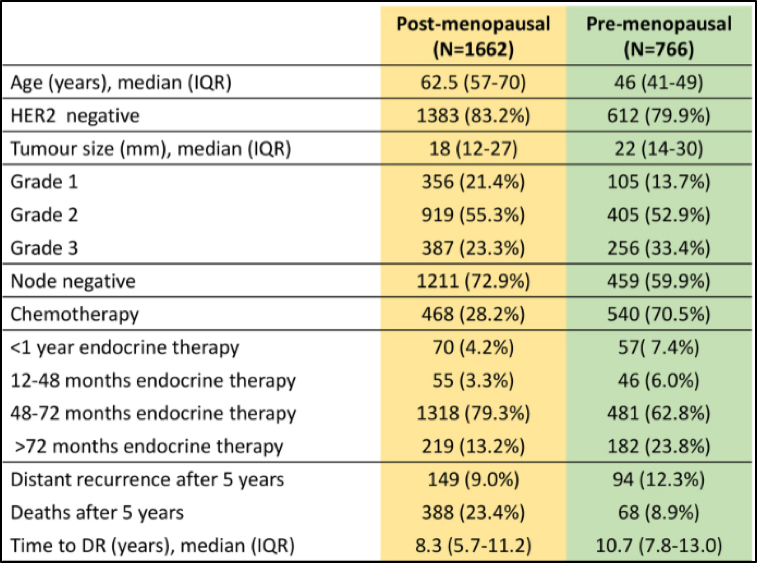
表2 CTS5对绝经后和绝经前的远期远处转移有显著的预测作用
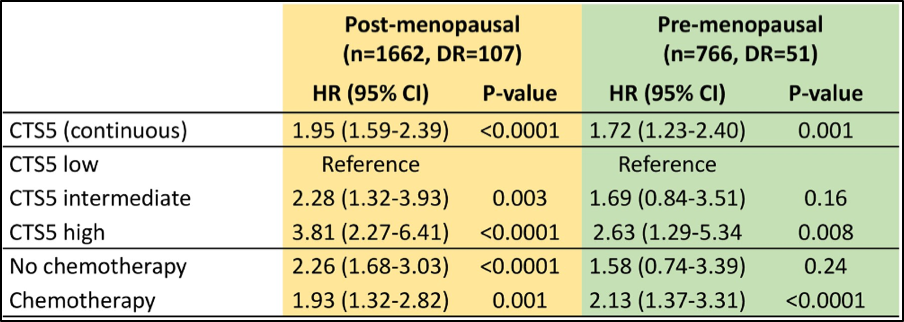
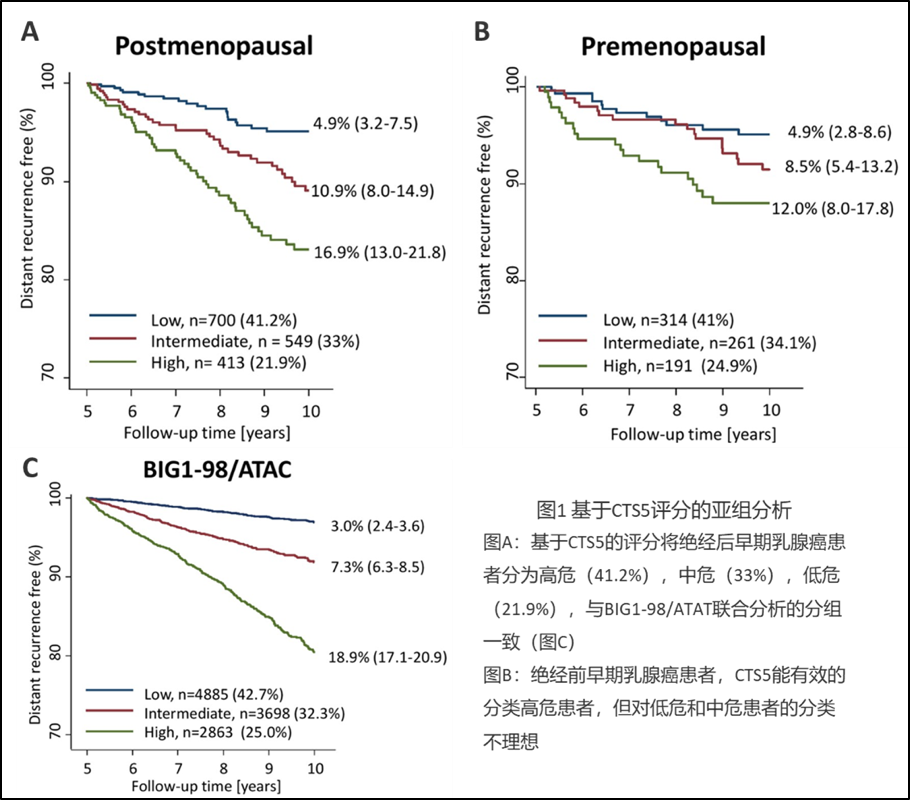
图1 CTS5对绝经后和绝经前的远期远处转移的复发风险分层
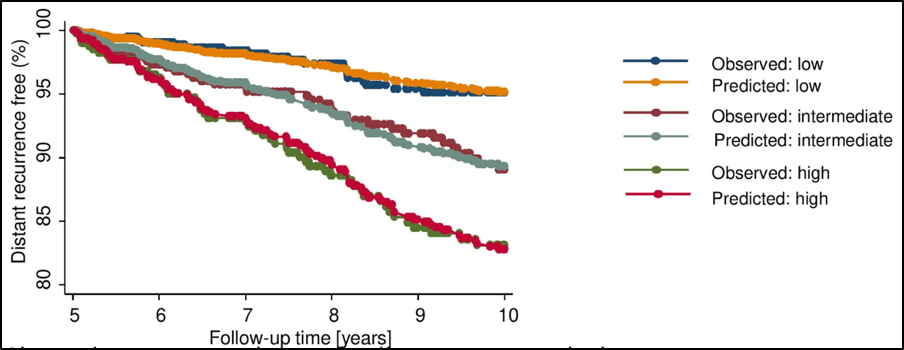
图2 CTS5对绝经后远期远处转移的复发风险与观察结果高度一致
研究结论
CTS5在大样本的未经筛选的,包括绝经前妇女的非试验患者中证明了其预测远期远处转移的临床有效性。CTS5筛选的低风险人群远期远处转移的风险较低,不能确定内分泌治疗延长至10年。
因此,使用CTS5准确的筛选出48%的中高危患者,给予其延长内分泌治疗,使其获得更大的治疗获益。临床上,CTS5可用于精准化治疗,使乳腺癌患者得到更大的内分泌治疗获益,同时由于CTS5的评估基于临床医生可便于获取的临床病理信息,易于在临床实践中开展,复旦大学附属肿瘤医院与上海市防癌抗癌事业发展基金会正在联合开发便于医生使用的CTS5程序,预计在2019年7月即可上线使用,希望能帮助到更多的医生,使更多患者获益。
目前对于远期复发风险的预测工具较多,一类是基于是临床病理信息的预测模型,例如STEEP和CTS5,另一类是Oncotype DX(21基因检测)、PAM 50等基因检测工具,两类工具各有优缺点,未来对于HR阳性乳腺癌的复发风险预测可能是基于临床病理信息和基因检测综合评估来完成(图3)。
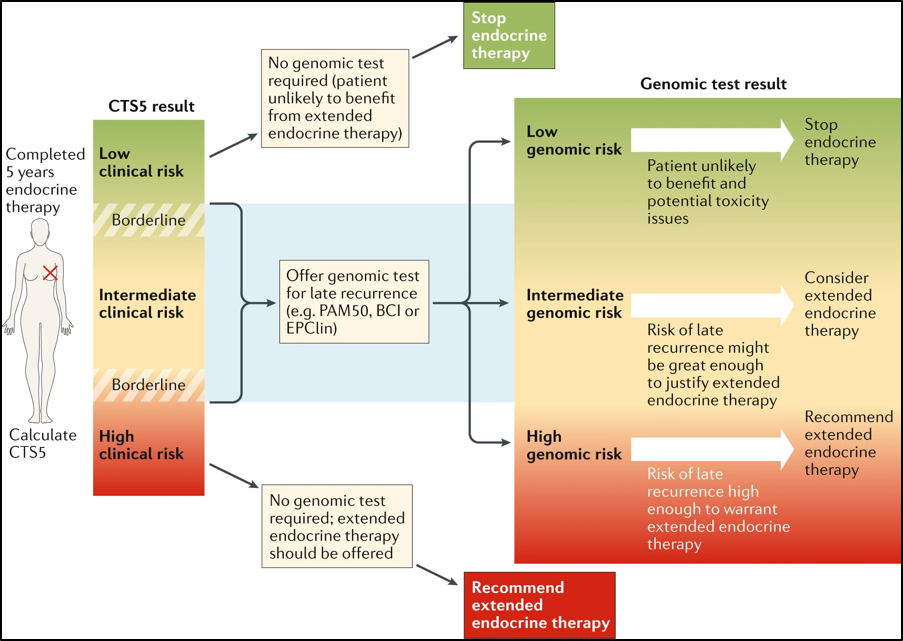
图3 延长辅助内分泌治疗决策模型
(Richman and Dowsett, Nature Reviews Clinical Oncology,2018)
[1] Dowsett M, Sestak I, Regan MM,et al. Integration of clinical variables for the prediction of late distant recurrence in patients with estrogen receptor–positive breast cancer treated with 5 years of endocrine therapy: CTS5[J]. Journal of Clinical Oncology, 2018,36.
[2] Goss PE, Ingle JN, Pritchard KI, et al.Extending aromatase-inhibitor adjuvant therapy to 10 yearsc[J]. N Engl J Med,2016, 375:209-219.
[3] Mamounas E, Bandos H, Lembersky BC, et al.A randomized, double-blinded, placebo-controlled clinical trial of extended adjuvant endocrine therapy (tx) with letrozole (L) in postmenopausal women withhormone-receptor (+) breast cancer (BC) who havecompleted previous adjuvant tx with an aromatase inhibitor (AI): results from NRG Oncology/NSABPB-42[J]. Cancer Res,2017, 77 (suppl 4; abstr S1-05).
[4]Blok EJ, Kroep JR, Kranenbarg EM-K, et al.Optimal duration of extended adjuvant endocrinetherapy for early breast cancer; results of the IDEAL trial (BOOG 2006-05) [J]. J Natl Cancer Inst,2018,110.
[5]Cuzick J, Sestak I, Baum M, et al.Effect of anastrozole and tamoxifen as adjuvant treatment for early-stage breast cancer: 10-year analysis of the ATAC trial[J]. Lancet Oncol ,2010,11:1135-1141.
[6]Regan MM, Neven P, Giobbie-Hurder A,et al. Assessment of letrozole and tamoxifen alone and in sequence for postmenopausal women with steroid hormone receptor-positive breast cancer:The BIG 1-98 randomised clinical trial at 8.1 years median follow-up[J]. Lancet Oncol,2011, 12:1101-1108.
[7] Pan H, Gray R, Braybrooke J,et al. 20-Year risks of breast-cancer recurrence after stopping endocrine therapy at 5 years[J]. N Engl J Med, 2017,377:1836-1846.
[8]Richman, Juliet, Mitch Dowsett. Beyond 5 years: enduring risk of recurrence in oestrogen receptor-positive breast cancer[J].Nature Reviews Clinical Oncology ,2018: 1.











 苏公网安备32059002004080号
苏公网安备32059002004080号


