临床中已经证明微卫星高度不稳定(dMMR/MSI-H)型转移性结直肠癌(mCRC)患者是免疫检查点抑制剂治疗的获益群体,但占95%的微卫星稳定型(MSS/pMMR)mCRC对免疫检查点抑制剂单药治疗无应答,此类亚型表现出肿瘤免疫原性低、免疫微环境抑制性强。晚期MSS/pMMR患者在多线化疗、靶向治疗进展后,后续治疗手段计穷智竭,生存预后极差,亟需填补治疗空白。
本期【好西例】分享一例57岁男性CRC患者,病理提示MSS型、KRAS突变,历经手术及四线多药物治疗(包括化疗、抗血管、TKI及介入治疗)均告失败。在五线治疗的极度困境下,基于CAPability-01研究成果,患者接受西达本胺领衔的CAP方案(西达本胺+替雷利珠单抗+贝伐珠单抗) 治疗后获得 部分缓解(PR),目前无进展生存期(PFS)已超过6个月且持续获益!该方案为多线耐药的MSS型肠癌患者带来了新的生存希望。
病例资料
患者基本信息
患者:男,57岁。
主诉:确诊结肠癌3年半余,综合治疗后。
既往史:体健,无家族性遗传疾病史。
个人史:无吸烟、饮酒史。
初始诊断与一线治疗(2020.09 - 2022.06)
2020-09:因腹痛行肠镜提示升结肠中分化腺癌。行右半结肠癌根治切除术。
术后病理:pT3N1aM0,中分化腺癌,侵及浆膜下,可见神经侵犯及脉管瘤栓。
分子分型:MSS型,KRAS G12V突变,BRAF野生型。
2021-10:术后1年复查CT提示肝转移。行肝部分切除术,术后予 XELOX方案辅助化疗 8周期。
疗效评价:SD。
三线治疗(2022.07 - 2023.04)
方案:伊立替康+雷替曲塞+贝伐珠单抗(3周期),后行腹腔肿物及肝部分切除。
维持治疗:口服呋喹替尼。
疗效评价:SD。PFS约为9个月。局部介入与四线治疗(2023.05 - 2023.10)
2023-05:核磁提示残肝转移瘤增大、增多。行肝动脉灌注化疗(OXA+雷替曲塞)及 钇-90(⁹⁰Y)治疗。
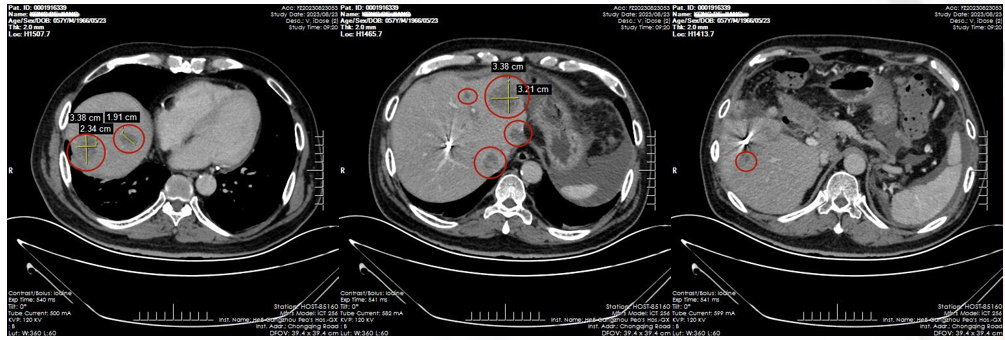
2023-08:复查显示肝内转移、腹膜及大网膜多发转移(图1)。
接受 TAS-102 + 贝伐珠单抗 治疗3周期。
疗效评价:PD。
五线治疗:CAP方案的应用
2023-10:患者病情持续进展,经多学科会诊建议尝试“西达本胺+贝伐珠单抗+免疫治疗”。
方案内容:西达本胺 + 替雷利珠单抗 + 贝伐珠单抗。
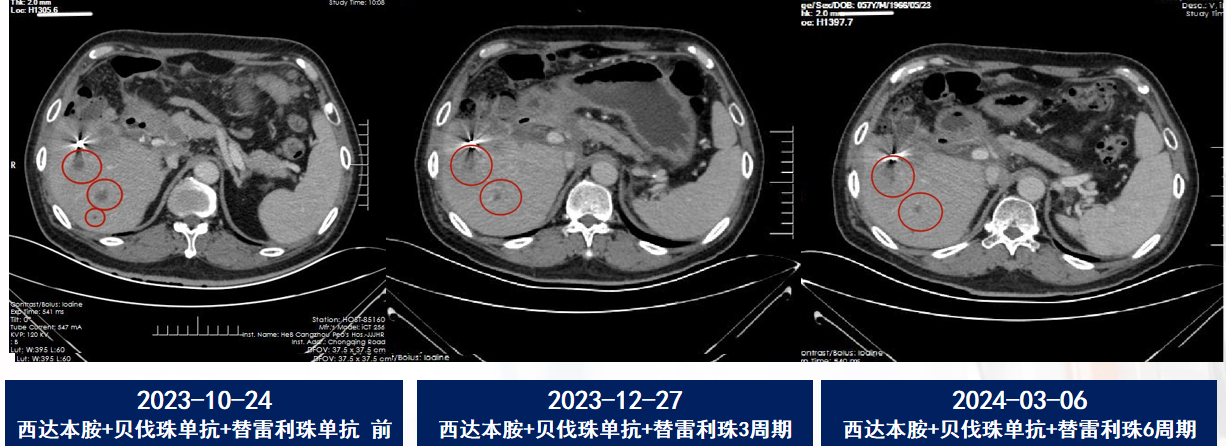
2023-12:3周期后复查评估,肝转移瘤减少及缩小,腹膜增厚好转。
2024-03:6周期后复查评估,病灶持续缩小(图2),疗效评价确认为PR(部分缓解)。
治疗小结
本例患者为典型的MSS/pMMR、KRAS突变型转移性结肠癌,其前线历经了化疗、抗血管、TKI及局部介入等几乎所有标准手段,均未能遏制疾病。采用CAP方案后,肝脏及腹膜转移灶显著缩小,成功实现了由PD向PR的逆转,且耐受性良好,PFS已超6个月,目前仍在持续获益中。
病例点评
结直肠癌根治性手术后,仍有相当比例的患者会出现复发转移。特别是对于占绝大多数的MSS型患者,其肿瘤微环境通常处于“冷”状态(缺乏T细胞浸润),常规免疫单药治疗完全无效。
深度机制解析:西达本胺如何激活“冷肿瘤”的免疫开关?
西达本胺在CAP方案中的核心作用被形容为 “免疫增敏的破冰船”。其分子层面的作用机制主要体现在以下三个维度:
1. 诱导肿瘤免疫识别
MSS型肠癌细胞通过去乙酰化作用,往往关闭了抗原提呈相关基因的表达。西达本胺作为组蛋白去乙酰化酶(HDAC)抑制剂,能够有效:
上调MHC-I类分子表达:增加肿瘤细胞表面抗原的“暴露度”,使其能被T细胞识别。
诱导癌症睾丸抗原(CTA)表达:赋予肿瘤细胞更强的免疫原性。
2. 促进免疫细胞浸润
研究发现,西达本胺能显著上调肿瘤微环境中趋化因子(如CXCL9、CXCL10)的表达。这些因子如同导向雷达,能吸引循环中的有效CD8+ T细胞精准进入肿瘤核心区域,改变“免疫荒漠”的状态。
3. 增强T细胞杀伤力
西达本胺不仅能增加T细胞的数量,还能提升质量。它能显著上调T细胞中 颗粒酶B(GZMB)、干扰素-γ(IFN-γ) 等杀伤因子的释放。在本病例中,这种杀伤力的增强直接反映为影像学上病灶的坏死与缩小。
4. 三药联合的协同逻辑(1+1+1>3)
替雷利珠单抗:解除免疫刹车。
贝伐珠单抗:通过抗血管生成,使肿瘤血管正常化,降低间质压力,改善缺氧,为免疫细胞和药物的进入铺平“高速公路”。
西达本胺:重塑微环境,提供“弹药”。三者形成闭环,全方位打击肿瘤。
CAP方案在机制和临床获益上都展示了西达本胺在结直肠癌难治亚型中的巨大潜力,为极后线、多线耐药的MSS型mCRC患者照亮了生命的曙光。
具体而言,替雷利珠单抗作为PD-1抑制剂,能够特异性地结合T细胞表面的PD-1受体,阻断其与肿瘤细胞表面PD-L1/PD-L2的结合,从而解除肿瘤细胞对T细胞的免疫抑制,释放被“禁锢”的抗肿瘤免疫反应,如同松开了T细胞的“刹车”,使其能够重新识别并攻击肿瘤细胞。而贝伐珠单抗作为抗血管内皮生长因子(VEGF)单克隆抗体,一方面通过抑制肿瘤新生血管的形成,切断肿瘤的营养供应;另一方面,其独特的“血管正常化”作用能够改善肿瘤内部紊乱的血管结构,降低肿瘤间质压力,减少组织间隙液对药物和免疫细胞的物理屏障,使得替雷利珠单抗等免疫治疗药物以及活化的T细胞能够更有效地穿透肿瘤组织,到达病灶核心。在此基础上,西达本胺通过其组蛋白去乙酰化酶抑制作用,不仅如前所述诱导肿瘤免疫识别、促进免疫细胞浸润和增强T细胞杀伤力,为整个免疫治疗过程提供了充足的“弹药”和“靶点”,其对肿瘤微环境的重塑,包括减少免疫抑制性细胞(如调节性T细胞、髓源性抑制细胞)的浸润和功能,进一步优化了替雷利珠单抗发挥作用的“土壤”。因此,西达本胺负责“松土施肥”,改善肿瘤微环境,提升肿瘤的免疫原性;贝伐珠单抗负责“修路搭桥”,确保免疫细胞和药物能够顺畅抵达肿瘤;替雷利珠单抗则负责“解除武装”,激活T细胞的杀伤功能。三者各司其职,又相互促进,形成一个“识别-进入-杀伤”的完整闭环,其协同效应远大于单一药物或两药联合的简单叠加,真正实现了“1+1+1>3”的治疗效果,为MSS型这种传统上“冷肿瘤”的免疫治疗打开了突破口。
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


