晚期结直肠癌(CRC)中约95%的患者属于微卫星稳定(MSS)或错配修复正常(pMMR)型。这类肿瘤由于缺乏有效的肿瘤浸润淋巴细胞,被形象地称为免疫“冷肿瘤”,导致其对常规PD-1/PD-L1单抗治疗几乎“免疫绝缘”。对于这部分患者,一旦经历标准的一、二线化疗及靶向治疗失败,后续治疗便进入了“瓶颈期”,常规三线药物的客观缓解率极低,生存获益有限。因此,如何通过创新机制重塑肿瘤微环境,将“冷肿瘤”转化为“热肿瘤”,从而通过联合治疗打破耐药困局,成为临床探索的热点。
本期【好西例】分享一例60岁女性患者,诊断为乙状结肠中分化腺癌伴肝、肺多发转移,基因检测提示KRAS G12D突变、MSS型。该患者历经四线治疗(包括化疗联合贝伐珠单抗、TAS-102、双免疫/靶向联合等)后病情进展。在五线治疗阶段,基于CAPability-01研究理念,创新性地采用西达本胺 + 信迪利单抗 + 呋喹替尼的三药联合方案,成功逆转耐药,治疗3周期后即获得部分缓解(PR),患者症状显著改善。该病例生动诠释了西达本胺在改善MSS型CRC免疫微环境中的关键作用。
病例资料
患者基本信息
患者:女,60岁
主诉:发现结肠肿物1个月。
一般状态(PS):0分。
初诊和辅助治疗
2021.08.08:行“腹腔镜下乙状结肠癌根治术 + 肝右叶肿物射频消融术”。
术后病理:乙状结肠中分化腺癌(2.5*2*1cm),侵及肠壁全层;脉管癌栓(+),神经侵犯(+)。肠周淋巴结转移(6/12);腹主动脉旁淋巴结癌转移。
分期:pT3N2aM1,Ⅳ期。
免疫组化:pMMR(MLH1/MSH2/MSH6/PMS2均阳性),Her-2(1+),Ki-67(60%+)。
基因检测:KRAS G12D突变,APC突变,TP53突变,BRCA2杂合突变。MSS,TMB-L。PD-L1 (22C3) CPS=6。
2021.09.07:术后PET/CT提示,1.乙状结肠MT术后、肝转移性MT消融术后:肝右叶前上段团块状混杂密度影,边缘伴糖代谢增高,最大SUV值为8.38,大小约为43.2*31.4mm考虑为治疗后改变可能,请结合临床;肝内多发伴糖代谢增高的结节状低密度影,最大SUV值为19.69,大小约为 17.9*15.6mm,考虑为转移;双肺多发不伴糖代谢增高的实性结节影,转移不除外。吻合口局部肠壁伴糖代谢稍升高,考虑为炎症改变可能性大;2.双侧甲状腺良性结节;3. 肝右前叶上段不伴糖代谢增高的结节样低密度影,考虑为良性改变可能性大,建议随诊,肝内多发囊肿;胆囊炎;左肾囊肿;左肾结石;子宫肌瘤;腹膜后腹主动脉及下腔静脉间、双侧腹股沟反应增生型淋巴结;5.骶管囊肿(图1)。
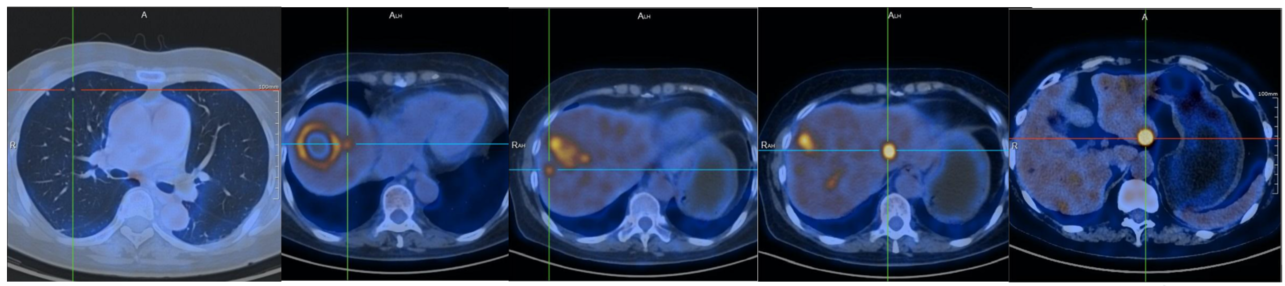
一线治疗
2021.09 - 2022.02:行贝伐珠单抗 + mFOLFOX6方案治疗10周期。
2022.02.25:行肝右叶残留病灶射频消融术。
二线治疗
2022.05 - 2022.08:疾病进展后,调整方案为贝伐珠单抗 + 伊立替康 + 卡培他滨治疗5周期。
3个月后出现缓慢进展(PD)。
三线治疗
2022.09 - 2023.08:调整方案为贝伐珠单抗 + TAS-102。
疗效评估:患者获益明显,病情维持疾病稳定(SD)长达12个月余。
四线治疗
2023.08 - 2023.12:疾病进展,尝试去化疗方案,行信迪利单抗 + 呋喹替尼治疗5周期。
疗效评估:最佳疗效为SD。2023.12:复查CT提示肺部及肝部病灶缓慢进展(Slow PD),PFS约4个月。
五线治疗
治疗策略:鉴于患者四线使用“PD-1单抗+抗血管TKI”后出现缓慢耐药,在此基础上联合西达本胺,以期通过表观遗传调节逆转免疫耐药。
2023.12.20 - 至今:行西达本胺 + 信迪利单抗 + 呋喹替尼三药联合方案。
疗效评估:
三药联合治疗3周期后(2024.02),复查CT显示肺部及肝部多发转移灶明显缩小。
疗效评价为PR。患者转归:症状明显缓解,一般状态改善,体重增加。
治疗小结
本例患者为KRAS突变、MSS型晚期结直肠癌,具有典型的难治性特征。回顾其漫长的抗癌之路,患者在四线治疗出现耐药、病情进展的关键时刻,通过引入西达本胺组成“西达本胺+PD-1+呋喹替尼”的三药联合模式。这一策略不仅没有增加不可耐受的毒副作用,反而成功克服了前线“免疫+靶向”的耐药,使肿瘤达到了PR的深度缓解。该病例有力证实了西达本胺作为“去化疗”方案中的关键增效剂,在晚期后线肠癌治疗中具有极高的临床应用价值。
病例点评
MSS/pMMR型CRC通常被认为是免疫“冷肿瘤”,对免疫检查点抑制剂单药甚至联合方案(如免疫+靶向)反应率有限。本例患者在四线接受“信迪利单抗+呋喹替尼”治疗后病情出现缓慢进展,提示单纯的抗血管生成联合免疫治疗尚不足以完全打破肿瘤的免疫抑制微环境。
CAPability-01研究及其理念为我们提供了破局的思路:HDAC抑制剂西达本胺可以通过表观遗传调控机制,上调肿瘤抗原提呈,增加CD8+ T细胞浸润,将“冷肿瘤”致敏。本病例的独特之处在于,我们在CAP方案的基础上进行了改良,保留了免疫药物(信迪利单抗)和表观遗传药物(西达本胺),但将大分子抗血管药物(贝伐珠单抗)替换为小分子抗血管TKI(呋喹替尼)。
结果令人惊喜:西达本胺的加入成功逆转了耐药,使患者从SD/PD转为PR。这提示我们:
1. 西达本胺是免疫治疗的优秀搭档:它能有效改善MSS肠癌的免疫微环境,提升免疫治疗的敏感性。
2. “去化疗”三药模式的可行性:对于后线身体状况较弱、无法耐受化疗的患者,“西达本胺+PD-1+抗血管TKI”的全口服/注射联合方案(除PD-1外均为口服)具有良好的依从性和安全性,且疗效确切。
本病例为晚期MSS型CRC的三线及后线治疗提供了宝贵的真实世界证据,西达本胺联合免疫及抗血管药物的策略值得在临床中进一步推广和探索。
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


