2025年欧洲肿瘤内科学会(ESMO)年会已圆满落幕,作为全球肿瘤学界的“风向标”,本届大会在肝癌与宫颈癌治疗领域发布了多项重磅研究成果,为临床诊疗实践注入了全新动能。其中,中国原研的艾托组合抗体(艾帕洛利托沃瑞利单抗,QL1706)在此次大会上分别更新了肝癌DUBHE-H-308研究Ⅱ期数据与宫颈癌DUBHE-C-204研究三年随访结果,备受业界关注。为了深入解读这些前沿进展,【肿瘤资讯】特邀青岛大学附属烟台毓璜顶医院陈剑教授与山东大学附属威海市立医院杨福俊教授,分别就肝癌和宫颈癌领域的治疗热点及艾托组合抗体的最新数据进行深度解析,并展望未来的治疗图景。
主任医师 硕士生导师 博士生导师
肿瘤内一科主任
齐鲁卫生与健康领军人才
美国西北大学 博士后
英国卡迪夫大学 访问学者
山东省医学会精准医学分会副主任委员;
山东省医师协会肿瘤精准治疗医师分会 副主任委员
烟台市医学会精准医学专委会 主任委员
山东省医药教育协会肺癌专委会 副主任委员
山东省研究型医院协会肿瘤分子靶向治疗学会 副主任委员
山东省医师协会临床细胞治疗专业委员会 副主任委员
山东省干细胞学会 干细胞技术与临床应用研究专委会 副主任委员
主持国家自然基金2项,国家863项目子课题1项,山东省重点研发等课题4项,教育部归国留学基金1项,以第一作者和通讯作者发表的SCI论文40余篇
医学博士 硕导
山东大学附属威海市立医院 肿瘤医学中心 主任
中国医师协会放射肿瘤治疗医师分会委员
中国抗癌协会放射医学专委会委员
中国医药教育协会疑难肿瘤专委会委员
山东省医师协会放疗医师分会副主委
山东省抗癌协会肿瘤微创分会副主委
山东省中西医结合学会肿瘤专委会副主委
山东省医师协会肿瘤医师分会常委
山东省医学会肿瘤学分会委员
威海市肿瘤质控中心常务副主任
肝癌治疗领域热点
Q1. 陈剑教授,您好。首先请您为我们分享一下,2025年ESMO大会在肝癌治疗领域呈现了哪些最值得关注的趋势和突破?
陈剑教授:2025年ESMO大会在肝癌治疗领域呈现了许多重要的趋势和突破性进展,主要体现在以下几个方面:
免疫联合策略的深度优化。TRIPLET HCC研究(摘要号:1471MO)针对当前免疫联合治疗方案展开了深度优化探究,此项Ⅱ/Ⅲ期研究对在阿替利珠单抗+贝伐珠单抗标准方案基础上±低剂量伊匹木单抗的疗效进行了评估。结果显示,三联方案组的客观缓解率(ORR)为30.1%,虽较双联组(27.4%)有所提高,但未达到预设终点。在安全性方面,两组的3/4级治疗相关不良事件(TRAE)发生率分别为44%和39%。这一研究结果为未来的临床联合用药策略提供了重要的安全性边界参考:即在标准双联方案基础上做加法虽然有效率有所提升,但需警惕治疗相关毒性的增加。
系统治疗挑战中期肝癌传统治疗格局。ABC-HCC研究(摘要号:LBA51)是一项国际IIIb期研究,直接比较了“阿替利珠单抗+贝伐珠单抗”系统治疗与传统的经动脉化疗栓塞(TACE)治疗中期肝癌的疗效。结果显示,系统治疗组中位至治疗策略失败时间(TTFS)达14.6个月,显著优于TACE组的9.5个月(HR 0.55)。这一结果挑战了TACE在中期肝癌中的传统主导地位,提示对于特定中期患者,早期使用系统治疗可能提供更持久的疾病控制。
围手术期治疗的新突破。CARES-009研究(摘要号:1470O)是全球首个在可切除肝细胞癌围术期治疗方案获得阳性结果的Ⅲ期研究,即围手术期卡瑞利珠单抗联合阿帕替尼相较于单纯手术显著改善了伴中高危复发风险可切除肝细胞癌患者的无事件生存期(EFS)。与单纯手术相比,联合治疗组的中位EFS达到42.1个月(对照组19.4个月,HR=0.59),且主要病理缓解率(MPR)更高(35.1% vs 7.5%,P<0.001)。这为降低术后复发提供了强有力的新策略。
双特异性抗体/组合抗体的崛起。以艾托组合抗体为代表的创新药物正重塑治疗格局。它通过工程化手段将PD-1和CTLA-4以固定比例组合,对CTLA-4抗体进行改构优化,解决了传统CTLA-4单抗毒性大的痛点,同时保留了“双免”强效的抗肿瘤活性。这种技术平台的成功为克服肝癌免疫耐药提供了极具潜力的中国方案。
Q2. 艾托组合抗体在本次ESMO大会公布的DUBHE-H-308研究Ⅱ期数据备受关注。您能否为我们详细解读下这项研究结果?展望未来,您认为艾托组合抗体联合方案在肝癌领域中的应用前景如何?
陈剑教授:DUBHE-H-308研究是我国秦叔逵教授和樊嘉院士共同牵头开展的、全球首个双免疫检查点抑制剂+系统化疗+抗血管靶向药物的随机对照、开放标签、全国多中心的Ⅱ/Ⅲ期临床试验,旨在评估艾托组合抗体联合贝伐珠单抗和/或化疗在晚期肝癌一线治疗中的疗效和安全性。本次大会公布了Ⅱ期部分的更新数据(摘要号:1495P)。患者按1:1:1:1的比例随机分配接受艾托组合抗体+贝伐珠单抗+奥沙利铂+卡培他滨(第1组);艾托组合抗体+贝伐珠单抗(第2组);艾托组合抗体+化疗方案(第3组);信迪利单抗+贝伐珠单抗(第4组)。
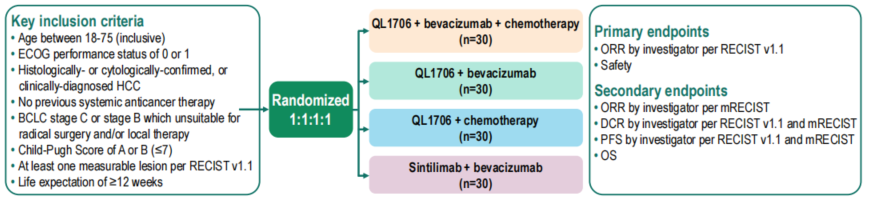
结果显示,中位随访时间为15.2个月。相较于信迪利单抗+贝伐珠单抗对照组(第4组),艾托组合抗体+贝伐珠单抗+化疗组(第1组)表现出显著的疗效优势:ORR高达40.0%(对照组20.7%),中位PFS达到13.1个月(对照组5.9个月),大幅降低了疾病进展风险。虽然中位OS尚未成熟,但第1组的12个月OS率已达73.3%。在安全性方面,艾托组合抗体联合方案组与对照组的≥3级TRAE发生率分别为66.7% vs 44.8%,整体TRAE可控,我们在临床实践中也观察到患者对此方案耐受性良好。
表1 研究疗效
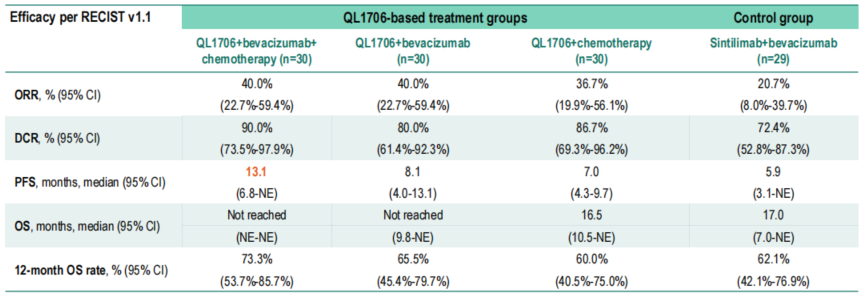
展望未来,艾托组合抗体在肝癌领域的应用前景非常广阔:
一线治疗地位确立:基于DUBHE-H-308研究的优异结果,《CSCO免疫检查点抑制剂临床应用指南2025》已将“艾托组合抗体+贝伐珠单抗+化疗”纳入晚期肝癌一线治疗的Ⅲ级推荐。随着数据的进一步成熟,其推荐级别有望继续提升,为临床医生提供更强有力的治疗选择。
转化治疗潜力巨大:DUBHE-H-308研究显示出较高的ORR,表明艾托组合抗体联合方案在转化治疗中潜力巨大。对于潜在可切除的肝癌患者,该方案能帮助更多患者实现肿瘤降期,从而获得根治性手术(R0切除)的机会。
解决耐药难题:针对既往PD-1/L1单药或靶免联合治疗耐药的患者,引入CTLA-4机制的“双免”策略是公认的破局方向。艾托组合抗体作为一种更安全、经过精细设计的“双免”药物,实现了“增效减毒”,未来在二线及后线治疗的探索同样值得期待。
全球应用前景:作为中国自主研发的全球首创双功能组合抗体,艾托组合抗体具有独特的机制,能够“增效减毒”,不仅有望重塑本土肝癌治疗路径,更将代表中国创新药走向世界。相信在未来的全球化应用中,它能实现从“跟跑”到“并跑”乃至“领跑”的跨越,为全球抗肝癌事业贡献坚实的“中国力量”。相信艾托组合不仅在肝癌治疗中,在其他瘤种的治疗中亦可能取得更为理想的疗效。
宫颈癌治疗领域热点
Q1. 本次 ESMO 年会聚焦肿瘤领域前沿突破,能否请您谈谈,宫颈癌领域有哪些值得关注的新进展或核心亮点?
杨福俊教授:今年ESMO年会在宫颈癌领域可谓成果丰硕,整体呈现出系统治疗证据更扎实、治疗手段更多样、联合模式更精准的特点,共同推动宫颈癌治疗从“广谱联合”向“精准增效”迈进。
在晚期系统治疗领域,多项研究的长期随访数据进一步夯实了循证医学证据。其中,备受关注的DUBHE-C-204研究(摘要号:1174P)三年随访数据,有力验证了双靶点组合抗体免疫治疗在复发转移性宫颈癌一线治疗中的持久获益,为该治疗模式的临床应用提供了坚实支撑。与此同时,抗体偶联药物(ADC)的应用也展现出多样化前景。如innovaTV 205研究(摘要号:1166P)五年随访数据显示,Tisotumab vedotin联合化疗或免疫药物能为患者带来超过两年的中位总生存期(OS),为不同治疗线数的患者提供了高效的个体化选择;芦康沙妥珠单抗单药治疗晚期宫颈癌的I/II期研究(NCT04152499,摘要号:1168P)也展现出良好的抗肿瘤活性与可控的安全性,为治疗方案选择有限的患者带来了新的希望。
在放疗领域,“免疫+放疗”的深度融合正成为提升局部晚期治愈率的关键方向。此前KEYNOTE-A18研究已确立“免疫+同步放化疗”的新标准地位,而本次大会公布的事后亚组分析(摘要号:1170P)进一步提供了精细的临床指导:对于预后较差的FIGO 2014分期III-IVA期患者,无论淋巴结状态如何,加入帕博利珠单抗均能带来稳健的无进展生存期(PFS)和OS改善,死亡风险降低约36%,为临床治疗中极具挑战性的这部分患者群体提供了强有力的新策略。在此基础上,强效免疫联合放疗模式的探索同样值得关注:一项双特异性抗体联合同步放化疗的回顾性分析(摘要号:1213P)显示,放疗后3个月客观缓解率(ORR)达100%,完全缓解(CR)率高达78.3%,即便IVB期患者也有70%实现完全缓解,提示更强效的免疫激活可能带来更深度、更快速的肿瘤退缩;另一项皮下注射PD-L1抑制剂恩沃利单抗联合放化疗的II期研究(摘要号:1189P)也展现出良好前景,其1年无进展生存率达94.4%,且不良事件多为1-2级、可控可逆,为局部晚期患者提供了便捷且安全的联合治疗新选项。
这些研究从系统治疗的长期生存验证,到放疗与免疫的协同,再到不同药物类型的多线探索,不仅为临床提供了更丰富的治疗选择,更奠定了改善患者生存质量、提升长期生存率的坚实基础。
Q2. 本次大会更新了DUBHE-C-204研究三年随访数据,结果显示艾托组合抗体联合方案一线治疗的OS高达35.7个月。您能否为我们深入解读这一数据的临床价值?同时,结合整个领域的治疗进展,您如何展望艾托组合抗体在宫颈癌治疗格局中的未来?
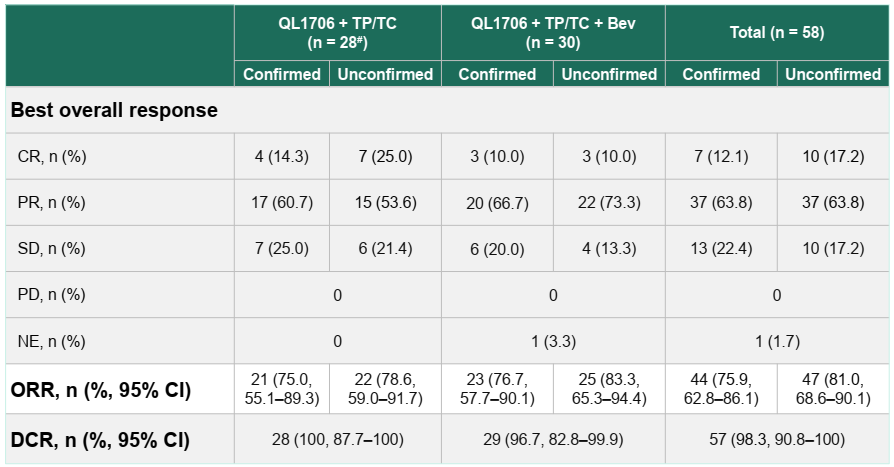
杨福俊教授:DUBHE-C-204 研究这次公布的三年随访数据是本次大会宫颈癌领域的重磅成果之一。该研究显示,艾托组合抗体联合化疗±贝伐珠单抗一线治疗复发转移性宫颈癌,中位总生存期(OS)高达 35.7个月,中位无进展生存期(PFS)15.1个月,确认客观缓解率(ORR)75.9%,疾病控制率(DCR)98.3%。
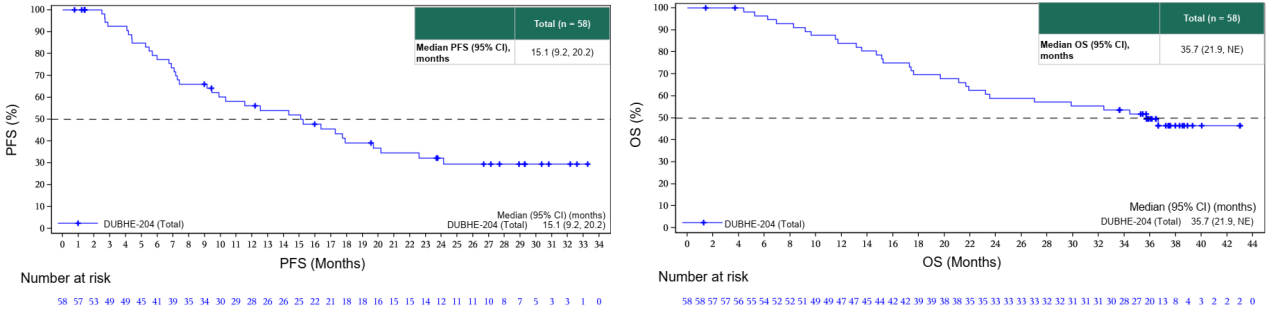
表2 DUBHE-C-204研究的治疗缓解结果
回顾宫颈癌既往一线治疗的历史,从单纯化疗时代的患者中位 OS 不足14个月,到GOG 240研究中加入贝伐珠单抗的17个月,再到KEYNOTE-826研究中加入帕博利珠单抗的24.4个月,我们见证了生存曲线的稳步攀升,而 DUBHE-C-204 研究将生存期推向接近三年的水平,实现了生存获益的大幅度跨越式提升,让复发转移性宫颈癌从“难治性疾病”向“可长期控制”的慢性病迈出了关键一步。
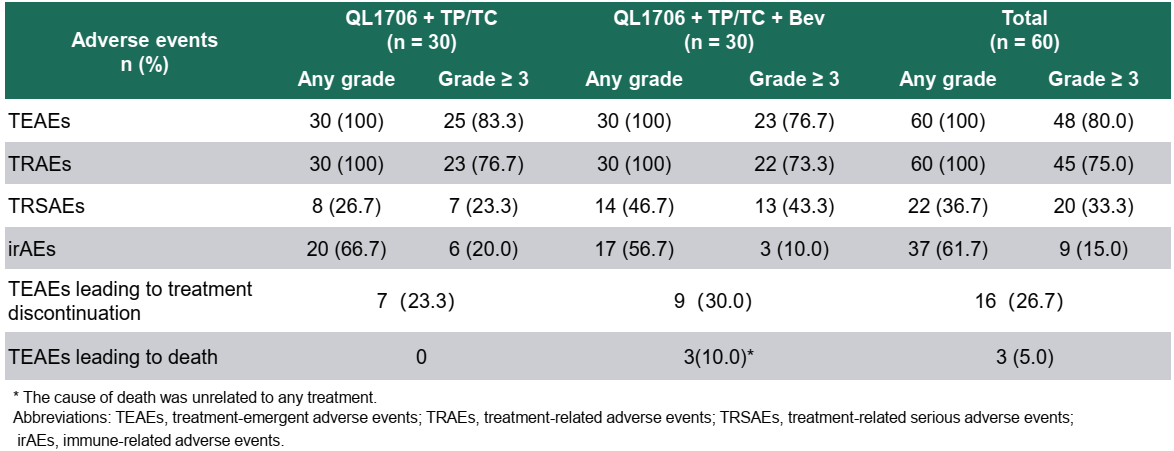
值得关注的是,该方案的安全性特征在长期随访中持续稳定,≥3 级治疗相关不良事件(TRAE)发生率 75%,≥3 级免疫相关不良事件(irAE)为 15%,无新增安全信号,且停药率控制在 26.7%,在同类联合方案中处于较低水平,验证其长期应用的安全性与可管理性。并且该方案的疗效不受限于PD-L1的表达状态,这使其成为一个普适性更强、能够惠及更广泛患者群体的治疗选择,极大地简化了临床实践。
表3 DUBHE-C-204研究的安全性结果
展望未来,结合宫颈癌治疗领域的整体进展,艾托组合抗体在未来治疗格局中有望占据核心地位,其应用场景与临床价值将进一步拓展深化。
从治疗线数来看,该药物已实现“二线及后线 - 一线”的多线覆盖:二线及后线治疗中,艾托组合抗体单药已被国内 4 大权威指南推荐,且已顺利通过国家医保局局务会审议及医保谈判环节,将于明年1月进入医保公示与落地执行阶段,获批适应症为“既往接受含铂化疗失败的复发或转移性宫颈癌”,这将显著提升后线患者的药物可及性;一线治疗中,基于 DUBHE-C-204 研究的早期数据,该联合方案已被《复发转移性宫颈癌诊疗指南(2025 版)》《妇科肿瘤免疫检查点抑制剂临床应用指南(2025 版)》《CSCO 免疫检查点抑制剂临床应用指南 2025》纳入推荐,此次三年随访的长期生存数据,将进一步巩固其推荐地位。目前,一项旨在验证该方案一线疗效与安全性的 Ⅲ 期临床试验(NCT05446883)正在推进中,若能获得阳性结果,不仅有望提升其指南推荐级别,更有望推动一线适应症快速纳入医保,让我国更多的病患在初始阶段受益。
从治疗模式来看,艾托组合抗体与放疗的协同应用有望成为新的探索方向。本次 ESMO 年会多项研究已证实,免疫治疗与高剂量放疗联合能通过诱导免疫原性细胞死亡、与低剂量放疗可重塑肿瘤免疫微环境实现协同增效,而艾托组合抗体的双靶点(PD-1+CTLA-4)设计本身具有更强的免疫激活效应,未来有望进一步开展相关临床研究,探索其在局部晚期宫颈癌同步放化疗中的应用。
总体而言,艾托组合抗体这一类新型免疫药物凭借其突破性的疗效、可控的安全性、广泛的人群适应性以及全治疗线的应用潜力,未来有望成为宫颈癌多模式治疗体系中的核心药物。
排版编辑:肿瘤资讯-jyy











 苏公网安备32059002004080号
苏公网安备32059002004080号


