在激素受体阳性(HR+)/人表皮生长因子受体2阴性(HER2–)晚期乳腺癌(mBC)领域,传统的内分泌治疗联合CDK4/6抑制剂并非是基于生物标记物的选择,对于PIK3CA突变介导内分泌耐药的患者生存仍是严峻挑战。基于生物标记物指导的精准决策,伊那利塞作为新一代高选择性PI3Kα抑制剂及突变体降解剂,其三联方案被国内外各指南推荐为晚期一线精准治疗新标准,这源于伊那利塞(Inavolisib)在Ⅲ期INAVO120研究中证实了其临床的显著获益。本期【PIK TALK】聚焦一例来自中山大学肿瘤防治中心王树森医生团队,由中山大学肿瘤防治中心夏雯医生整理的真实世界案例,该患者在“伊那利塞+哌柏西利+氟维司群”三联方案下,实现了超过40个月的持续部分缓解(PR)。我们特邀中山大学肿瘤防治中心王树森专家和北京大学肿瘤医院李惠平专家深度解析,探讨该案例如何为PIK3CA突变人群的长期治疗策略提供关键启示。
案例报告
案例诊疗经过
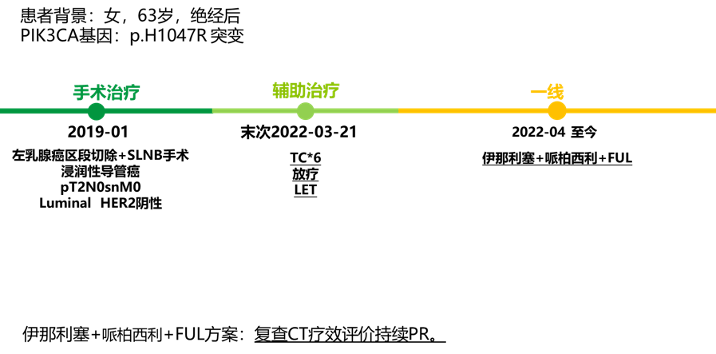
患者为63岁绝经后女性,无乳腺癌家族史及药物过敏史。2019年1月于外院接受左乳腺癌区段切除联合前哨淋巴结活检术。术后病理显示为左乳浸润性导管癌,肿物大小 2.5×2×0.5 cm,SLNB结果为0/7。免疫组化(IHC)结果为:ER (80%+)、PR (3%+)、HER2 (0)、Ki-67 (20%+)。术后诊断为:左乳癌保乳术后 pT2N0snM0 Luminal HER2阴性。辅助治疗方案为TC×6程辅助化疗及放疗,并于2019年6月开始来曲唑辅助内分泌治疗。
复发与分子检测 (2022年2-4月):
2022年2月患者于外院复查MRI提示肝脏多发转移病灶,最大病灶约5×3×3.8 cm 。患者转至中山大学肿瘤防治中心进一步诊治 ,并于3月行肝穿刺活检 。病理结果证实为乳腺癌肝转移 ;转移灶IHC结果为ER (90%+)、PR (5%+)、HER2 (1+)、Ki-67 (20%) 。NGS检测提示,明确存在PIK3CA基因: p.H1047R 突变 。
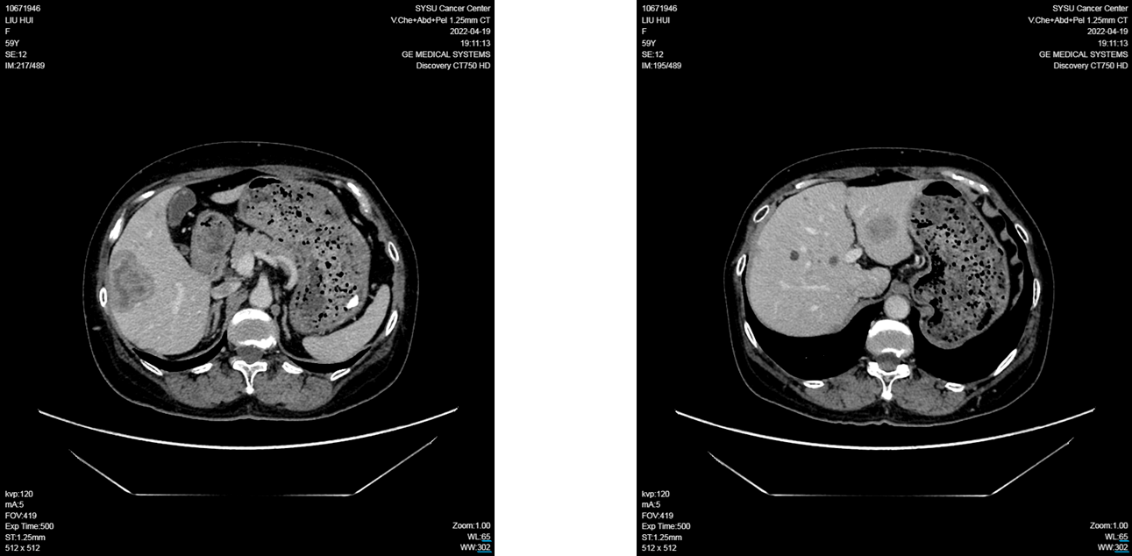
晚期一线治疗与疗效评估 (2022年4月至今):
2022年4月27日,患者入组WO41554临床试验,接受“伊那利塞(GDC0077)/安慰剂+哌柏西利+氟维司群”的三靶点联合治疗。仅2个周期后(2022年6月),影像学即显示肝转移灶明显缩小;后续多次评估均维持部分缓解(PR)。
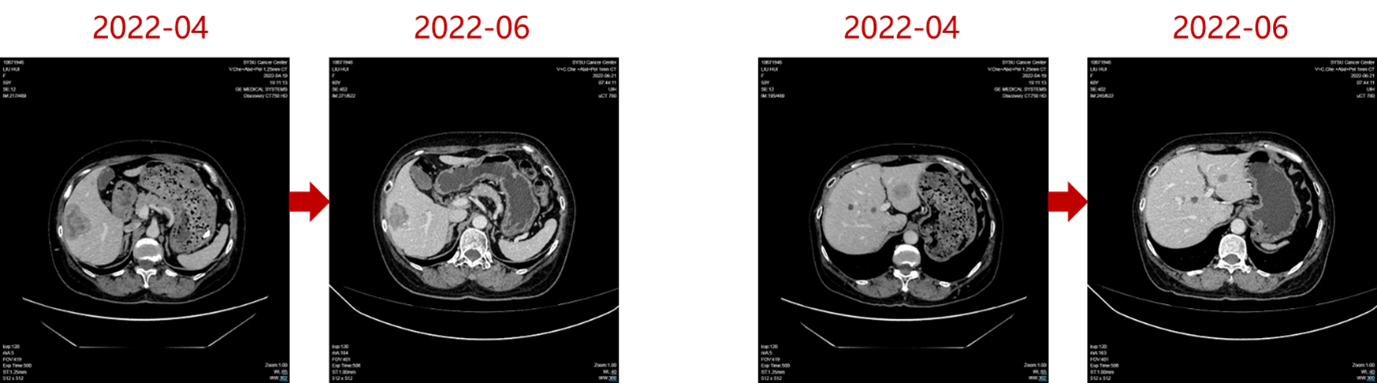
截至2025年9月,患者无进展生存期(PFS)已超过40个月,远超INAVO120研究报道的中位PFS 17.2个月。
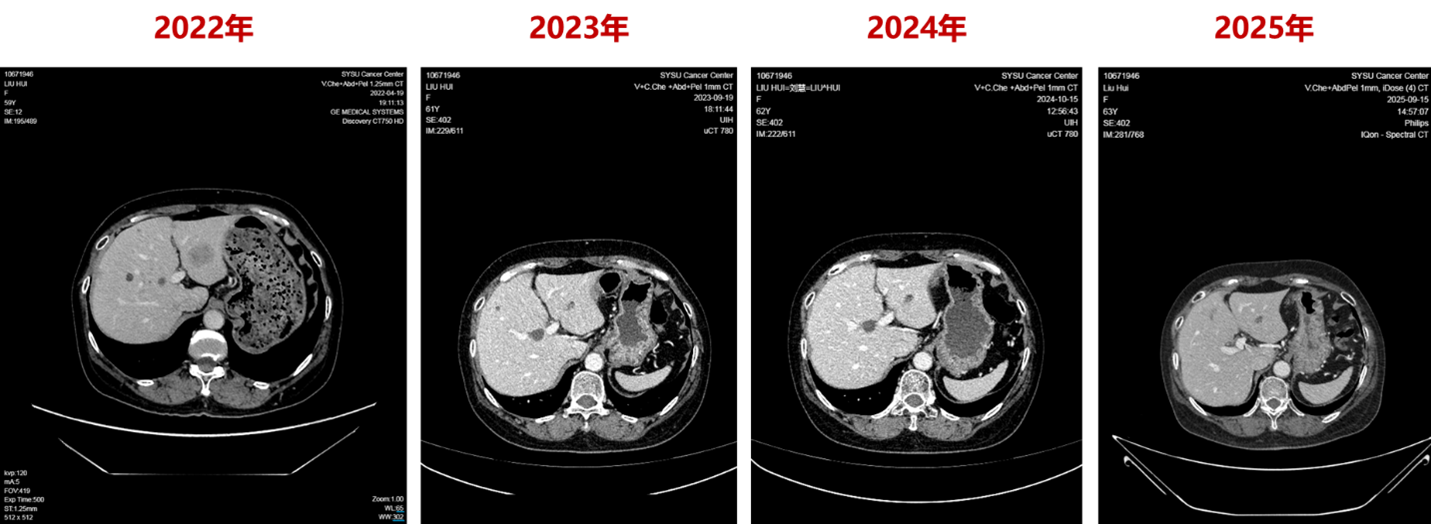
治疗期间的不良反应整体呈可控趋势,并未影响患者的依从性和生活质量。治疗期间出现的不良反应包括1度口腔炎 、1度低钾血症和2度血糖升高。
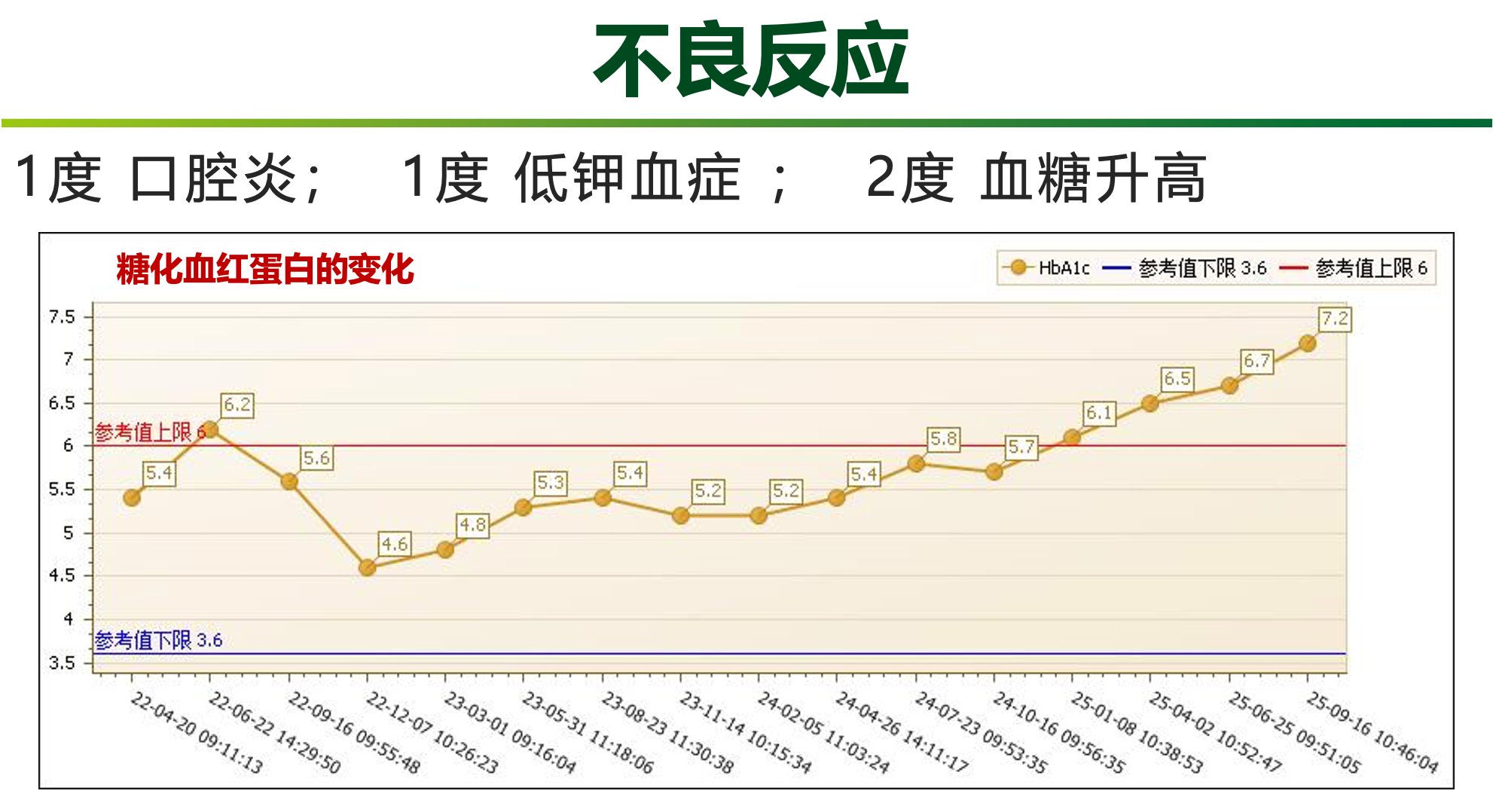
C1周期出现口腔黏膜炎,经规范化口腔护理后逐渐缓解;C6周期因轻度低钾血症及血糖上升暂停伊那利塞,经调整饮食及对症处理后于2022年10月恢复治疗。自2022年8月起患者出现胃部烧灼感及食欲下降,经抑酸与营养支持治疗后明显改善。实验室监测显示肝功能始终保持正常范围,而HbA1c水平随治疗时间延长呈缓慢上升趋势,提示需持续血糖监测及生活方式管理。这一过程显示相较于前代PI3K抑制剂,伊那利塞具有更佳耐受性和更低的3-4级高血糖发生率(停药率仅约6.8%),为持续治疗提供基础保障。
病例总结
专家点评与临床启示
点评专家
中山大学肿瘤防治中心乳腺癌单病种首席专家
香港大学临床肿瘤学系荣誉教授
中国临床肿瘤学会(CSCO)乳腺癌专家委员会副主任委员
中国研究型医院协会乳腺癌专业委员会副主任委员
中国抗癌协会乳腺癌专业委员会常务委员
广东省临床医学学会乳腺癌专委会主任委员
广东省癌症中心乳腺癌诊疗质量控制专家委员会主任委员
广东省胸部肿瘤防治研究会乳腺癌专业委员会主任委员
现在主要从事乳腺癌内科的精准治疗、化疗、内分泌治疗及靶向治疗。
主持国自然重点项目1项、面上项目1项,省科技厅项目3项,获国家科技重大专项资助1项。
主编教材《临床肿瘤学(clinical oncology)》,参编教材或专著多部。
作为主要执笔人或参与者制定了多项国家级的乳腺癌诊疗相关指南。
在国内外期刊以第一作者或通讯作者发表论文多篇, 其中近年以来以第一作者或通讯作者于JAMA、JCO、STTT、CANCER COMMUNICATIONS 等杂志发表SCI论文多篇。
作为主要研究者牵头发起多中心临床研究30多项,其中包括I期临床试验6项目,Ⅱ、Ⅲ期大型多中心临床试验多项。
点评专家
北京大学肿瘤医院乳腺肿瘤内科 主任
美国德克萨斯大学M.D.Anderson 学习2年
中国女医师协会乳腺专业委员会主任委员,
中华医学会肿瘤学分会乳腺肿瘤学组副组长,中国抗癌协会乳腺癌专业委员会常委,中国女医师协会临床肿瘤学专委会副主任委员,
中国进展期乳腺癌共识指南共同组长和执笔人,
Associate Editor of “Breast Cancer Research and Treatment”
王树森教授:
该例患者取得了超过40个月的PFS ,这一卓越的真实世界数据,为我们的临床实践提供了三点重要启示:
首先,该案例的诊疗路径,凸显了在疾病复发转移时,再次进行活检并施行分子病理检测的规范化操作的临床价值。这一步骤是后续治疗得以转向基因层面的精准靶向治疗的前提。当前的精准诊疗共识也强调这点,例如2025版《中国乳腺癌PIK3CA基因突变检测专家共识》已明确指出[1]:对于HR+/HER2-的局部晚期或转移性乳腺癌患者,建议在一线治疗前常规开展PIK3CA基因检测。
其次,一线分子病理检测的价值在于其全面性。它不仅能识别PIK3CA突变,还能同时评估ESR1、BRCA等其他关键驱动基因的状态 。这使得临床医生能够基于明确的生物标记物(Biomarker)制定个体化治疗方案,为患者提供了超越传统经验性治疗的精准选择。
最后,本例的PFS数据(40+月) 明显优于INAVO120研究报道的中位PFS(17.2个月)[2]。这提示在真实世界中,该方案有潜力为部分患者带来更长期的疾病控制,从而有效延缓了进入化疗的时间。鉴于INAVO120研究已证实该方案可降低33%的死亡风险并带来7个月的中位OS获益 ,我们有理由期待这位获得超长PFS的患者,将收获更积极的总生存结局。
从分子机制上看,ER信号轴、细胞周期(CDK4/6)轴与PI3K信号轴共同构成了HR+/HER2-乳腺癌的“治疗黄金三角”。PIK3CA突变肿瘤的进展,常依赖于这三条通路间的协同作用与信号串扰[3-4]。INAVO120研究证实,在内分泌耐药背景下,仅阻断其中一或两条通路,肿瘤细胞仍可能通过旁路激活而逃逸 。伊那利塞(Inavolisib)三联方案的核心价值,在于通过氟维司群、哌柏西利和伊那利塞,同时对这三条核心通路进行阻断,从而实现协同抑制效应,阻止了代偿机制的形成。这是实现该例患者长期疾病控制的生物学基础。值得一提的是,目前的精准治疗策略正向后线延伸。正在进行的INAVO121 III期研究,即是探索CDK4/6抑制剂进展后的关键后线治疗策略。该研究入组既往接受过CDK4/6i+ET治疗的HR+、HER2-、PIK3CA的局部晚期或转移性乳腺癌患者,以1:1随机分配,旨在头对头比较伊那利塞联合氟维司群与Alpelisib联合氟维司群的疗效[5]。其主要终点为BICR评估的PFS,次要终点包括总生存期(OS)、客观缓解率等,其结果将为该类患者的二线治疗提供重要依据。
另外,由我们中山大学肿瘤防治中心牵头的全国多中心研究INAVO123目前也在患者招募的过程中,该研究设计入组了PIK3CA突变的HR+/HER2-晚期一线内分泌敏感人群,我们也期待该研究能获得积极的结果,为乳腺患者提供新的治疗选择。
李惠平教授:
该病例的成功诊治,首先归功于复发后再次进行分子检测的规范化操作。若沿用初诊时的病理信息,将错失此次精准靶向治疗的机会。从经验治疗转向精准机制驱动,是个体化治疗的核心前提。同时,也为PIK3CA突变患者的长期管理提供了重要范例:
第一,对于PIK3CA突变且内分泌耐药的患者,一线采用三联方案是实现长期疾病控制的必要策略。该患者是在辅助AI治疗后约2年半复发,属于继发性内分泌耐药 ,这与INAVO120研究入组的内分泌耐药人群特征一致 。研究数据显示,对于这类患者,双药联合治疗的疗效有限(安慰剂组mPFS仅7.3个月),而伊那利塞三联方案则将mPFS显著延长至17.2个月 。该获益在最具治疗挑战的亚组中同样显著:INAVO120研究中近80%为内脏转移患者 ,该亚组的mPFS同样被延长(13.8个月 vs 7.2个月,HR=0.51)。更重要的是,该方案将中位至首次后续化疗的时间从12.6个月大幅延长至35.6个月 ,化疗风险降低57% 。这说明在PIK3CA突变及内分泌耐药的双重压力下,三药联合是实现有效疾病控制的必需策略。
第二,伊那利塞良好的安全性和耐受性,是患者得以实现长期用药并获得超长PFS的基础。既往PI3K抑制剂的临床应用常因毒副反应受限,而伊那利塞的安全性得到了显著优化。这首先归功于其机制的“精准”升级:伊那利塞是一款高选择性PI3Kα抑制剂,其对p110α亚基的选择性是其他PI3K亚型的300倍以上。这种对α亚型的高度靶向,使其能避免对其他亚型(如β、δ、γ)的不必要抑制,从而显著改善了既往泛PI3K抑制剂常见的严重肝毒性、皮疹等问题。其次,它具备“抑制+降解”的双重作用机制:它不仅抑制激酶活性,更可促进突变p110α蛋白的依赖性降解,实现对PAM通路的持续抑制。INAVO120研究中,因不良事件(AE)导致的治疗终止率仅为6.8%。该例患者的不良反应亦可控,主要为1度口腔炎、1度低钾血症和2度血糖升高。这种“可管可控”的安全性,保证了患者的长期治疗依从性,对维持高质量的患者报告结局(PRO)至关重要。
第三,一线精准检测为患者规划了更长远清晰的后续治疗路径。HR+/HER2-乳腺癌的治疗正进入多靶点精准布局的时代,当这位患者未来进展时,临床上仍有多种基于精准机制的治疗选择。例如,2025年ESMO大会报道的MORPHEUS研究(508P)提示,在CDK4/6抑制剂经治人群中,伊那利塞联合新型口服SERD(Giredestrant)在PIK3CAm患者中显示了积极的疗效(ORR 40%,mPFS 9.5个月)[6]。这些不断丰富的循证依据与新药选择,为后线治疗提供了更多可能。该例患者的成功,正为PIK3CA突变患者的全程管理树立了良好示范。
案例提供专家
中山大学肿瘤防治中心内科
第六届“羊城青年好医生”
中国研究型医院学会乳腺癌专业委员会常委
中国抗癌协会乳腺癌专委会青年委员
中国抗癌协会乳腺癌整合防筛专业委员会委员
广东省胸部疾病学会乳腺病防治专业委员会常委
广东省抗癌协会乳腺癌专业委员会青委会委员
广东省抗癌协会遗传肿瘤专业委员会委员
广东省胸部肿瘤防治研究会乳腺癌专业委员会委员
JCO中文版青年编委
1.中华医学会病理学分会,中国临床肿瘤学会病理专家委员会,国家病理质控中心. 中国乳腺癌PIK3CA基因突变检测专家共识(2025版)[J]. 中华病理学杂志,2025,54(02):120-125.DOI:10.3760/cma.j.cn112151-20241120-00770
2. haveri KL, Im SA, Saura C, et al. N Engl J Med. 2025;393(2):151-161.
3. Tufail M, et al. J Transl Med. 2024 Jan 3;22(1):15.
4. NCCN Clinical Practice Guidelines in Oncology: Breast Cancer (Version 6. 2024).
5.Juric D, et al. 2023 SABCS Abs PO2-19-08
6. Rugo HS, et al. 2025 ESMO Annual Meeting. Abstract 508P.
本文仅为个人观点分享,具体诊断方案需结合实际情况判断。
排版编辑:肿瘤资讯-XZY












 苏公网安备32059002004080号
苏公网安备32059002004080号


