炎性乳腺癌(inflammatory breast cancer, IBC)是乳腺癌中罕见且极具侵袭性的亚型,占乳腺癌相关死亡原因的5%-7%,而双侧受累病例更为罕见,临床诊疗难度极高。本文通过一例合并夏科-马里-图思病(Charcot-Marie-Tooth disease)的 50 岁绝经前女性异时性双侧 IBC 病例,梳理其从诊断、多线治疗到病情进展的全过程,结合文献探讨双侧 IBC 的临床特点、分子演变规律及诊疗策略,旨在为临床医生应对这类罕见复杂病例提供参考。
病例介绍
患者,女,50 岁,绝经前,既往确诊夏科-马里-图思病(一种遗传性周围神经病变),因“右侧乳房急性红斑、皮肤增厚伴橘皮样改变”于 2021 年 2 月就诊。
家族史:母亲 45 岁确诊乳腺癌,患者经遗传咨询未发现致病性生殖系突变。
初始诊断(2021 年 2 月)
临床表现:右乳弥漫性红斑、皮肤增厚、橘皮样改变,无明显肿块;右腋窝可触及肿大淋巴结。
影像学检查:
右乳钼靶:皮肤增厚,右腋窝淋巴结肿大;
乳腺 MRI:右乳内象限可见 41×40×56 mm 病灶,伴弥漫性皮肤增厚及腋窝淋巴结异常强化(图 1A);
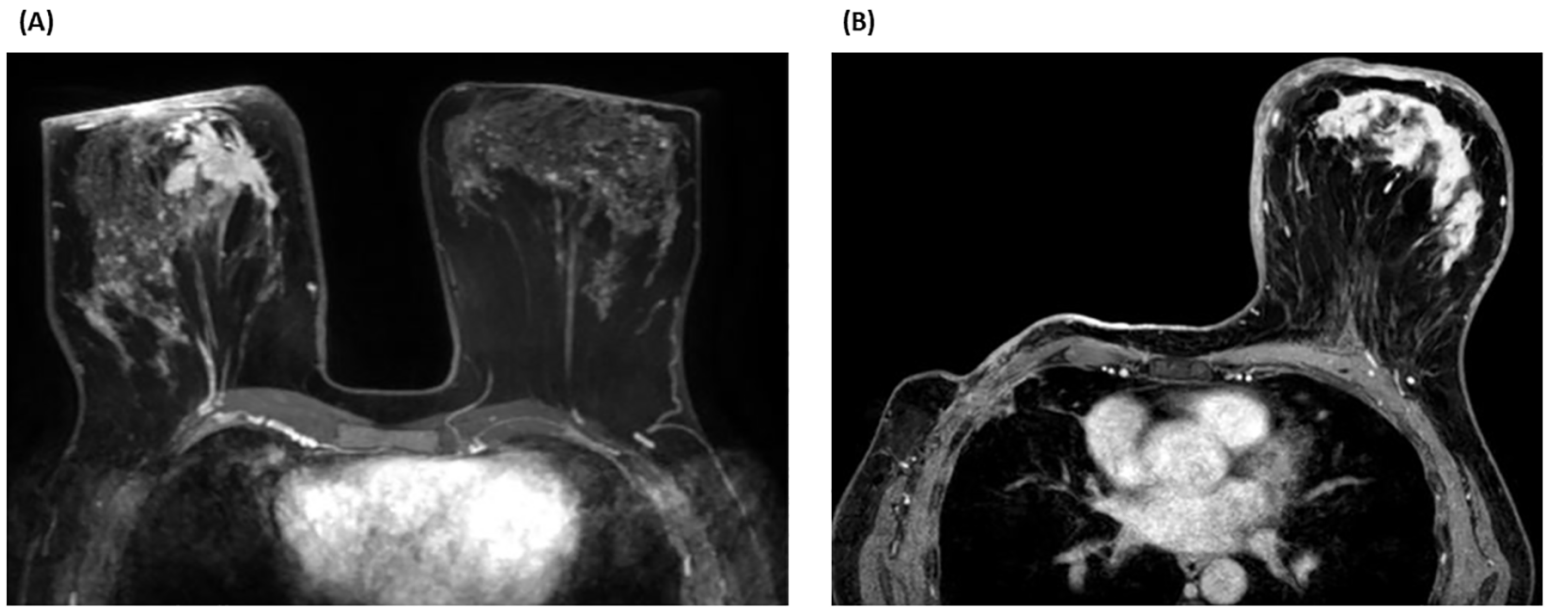
(B)(2022 年)MRI轴位像 ——3D 脂肪抑制 T1 加权序列(DIXON 技术)增强扫描。可见左侧乳房皮肤增厚,伴多发斑片状强化区(提示可能为淋巴道转移灶),且乳房中央区域亦存在强化灶。
全身 CT:无远处转移征象。
病理与免疫组化:右乳病灶及腋窝淋巴结芯针活检示浸润性导管癌 Ⅱ 级;免疫组化:雌激素受体(ER)阳性、孕激素受体(PR)阳性,人表皮生长因子受体 2(HER2)阴性(评分 0),Ki67 增殖指数 50%。
分期:依据美国癌症联合委员会(AJCC)第 8 版分期标准,确诊为右乳 IBC(cT4dN1M0,ⅢB 期)。
诊疗经过:多线治疗与病情演变
初始治疗(2021 年 3 月 - 2021 年 12 月)
新辅助化疗:2021 年 3 月启动蒽环类方案(4 周期)序贯多西他赛(80mg/m²,每 3 周 1 次,共 4 周期)。因患者合并夏科-马里-图思病,需警惕化疗相关神经毒性,联合神经科密切监测,未出现明显神经不良反应。
手术治疗:2021 年 9 月行右乳单纯乳房切除术+腋窝淋巴结清扫术,未行乳房重建。术后病理:残余浸润性癌灶大小 9mm,16 枚淋巴结中 1 枚见微转移(ypT1bN1mi)。
辅助治疗:术后行右胸壁、腋窝及内乳淋巴结链放疗(总剂量 50Gy,分 25 次);同步启动他莫昔芬(20mg/日)联合促黄体生成素释放激素(LHRH)类似物内分泌治疗。
首次复发(2022年8月-2022年11月)
临床表现:无病生存期 11个月后,左乳出现红斑,伴左腋窝固定肿大淋巴结;右乳手术瘢痕处新发红斑(图 2)。
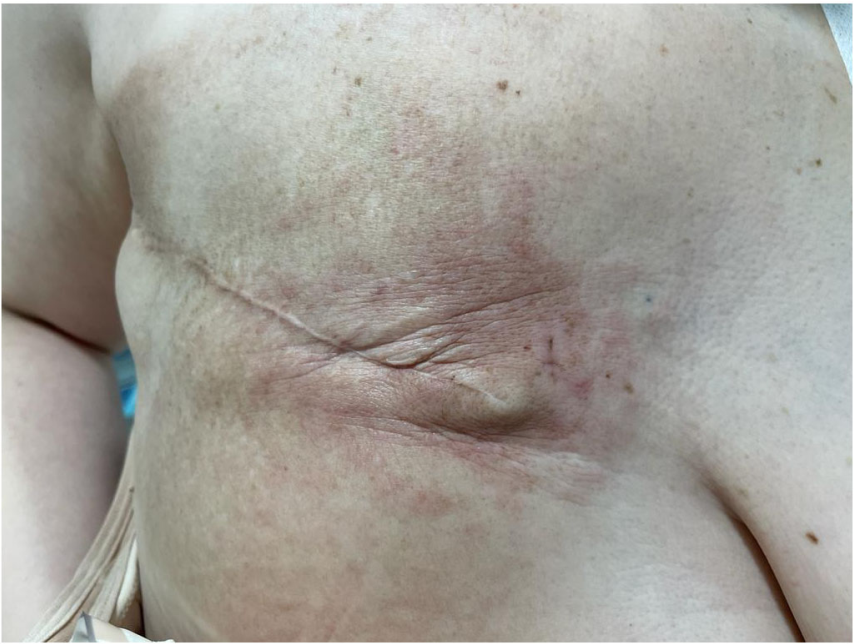
病理与分期:左乳皮肤及腋窝淋巴结活检示浸润性导管癌,ER 阳性、PR 阴性、HER2 阴性(评分 0),Ki67 指数 40%;右乳瘢痕处活检示同型肿瘤浸润(图 3)。分期为左乳 IBC(cT4dN2M0)。
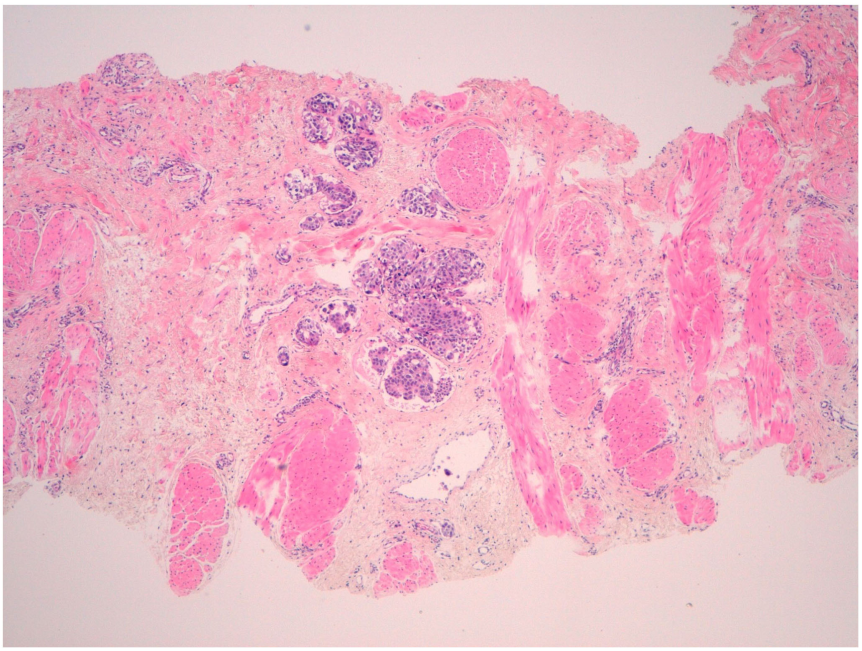
治疗方案:予脂质体阿霉素(60mg/m²)联合环磷酰胺(600mg/m²)化疗 4 周期,病情进展。
转移性治疗阶段(2022 年 12 月 - 2025 年 4 月)
一线治疗:2022 年 12 月启动阿贝西利(150mg,每 12 小时 1 次)联合来曲唑(2.5mg / 日),6 个月后皮肤病变进展。
分子检测与二线治疗:肿瘤下一代测序(NGS)示 PIK3CA 突变,肿瘤突变负荷(TMB)6.17个突变/兆碱基,错配修复蛋白表达正常。
2023 年 7 月启动卡培他滨(1250mg/m²,每日 2 次)二线治疗,皮肤症状显著改善,耐受良好,持续 8个月。
三线治疗:2024 年 3 月因局部进展入组临床试验,予氟维司群(500mg/月)联合阿培利司(300mg/ 日)。2 周期后出现 3 级皮疹,停用阿培利司,单药氟维司群治疗 3个月后病情进展。
四线治疗:2024 年 6 月启动艾立布林(1.23mg/m²,第 1、8 天给药,21 天为 1 周期),治疗期间出现胸腔积液,病情持续进展。
肿瘤生物学演变与五线治疗:重复皮肤活检示肿瘤生物学改变:HR 阴性、HER2 1+,Ki67 指数 27%。2024 年 9 月启动戈沙妥珠单抗(10mg/kg,第 1、8 天给药,21 天为 1 周期),3 周期后因呼吸衰竭停用。
结局:患者于 2025 年 4 月死亡,自初始诊断后总生存期 4 年。
讨论:双侧 IBC 的临床特点与诊疗关键
临床特点与罕见性
IBC以真皮淋巴管内肿瘤栓塞为特征,临床表现易与乳腺炎混淆,导致诊断延迟。双侧 IBC 占所有乳腺癌的1%以下,分为同步性(两侧发病间隔≤6 个月)与异时性(间隔>6 个月),本例为异时性(间隔 18 个月),符合“转移而非独立原发肿瘤”的时间特征。其侵袭性强,中位总生存期显著短于非炎性乳腺癌(Ⅲ 期 IBC 为 4.75 年 vs 非 IBC 13.40 年),且易早期出现局部复发与远处转移。
诊断要点
影像学评估:MRI 是诊断 IBC 的首选手段,可清晰显示皮肤增厚、病灶范围及淋巴结受累(图 2A、2B);动态增强 MRI(尤其 T2 加权成像)对鉴别良恶性炎症性病变敏感性最高;全身 CT/PET-CT 可排除远处转移,指导分期。
病理确诊:皮肤及淋巴结活检是关键,需重点关注真皮淋巴管内肿瘤栓塞(图 3),免疫组化明确 HR、HER2状态,为治疗方案制定提供依据。
治疗策略与分子指导
多模态初始治疗:双侧 IBC 治疗以“新辅助化疗→手术→辅助放疗”的三联模式为基础,本例初始治疗遵循该原则,实现局部控制。但双侧受累增加手术切口设计与放疗靶区规划难度,需多学科协作。
分子靶向治疗价值:NGS 检测发现 PIK3CA 突变后,启用氟维司群联合阿培利司(PI3Kα 抑制剂),符合 SOLAR-1 试验结论 —— 该联合方案可显著延长 HR+/HER2-、PIK3CA 突变晚期乳腺癌患者的无进展生存期,体现精准治疗的重要性。
肿瘤生物学演变应对:本例治疗过程中出现 HR 表达丢失(从 HR 阳性转为阴性),提示需定期重新活检评估肿瘤表型,及时调整治疗方案(如从内分泌治疗转为化疗或抗体药物偶联物治疗)。
特殊人群管理
患者合并夏科 - 马里 - 图思病,需平衡化疗疗效与神经毒性风险。本例选择多西他赛等神经毒性相对可控的药物,联合神经科监测,未出现严重不良反应,为合并基础神经疾病的 IBC 患者治疗提供参考。
小结
双侧异时性 IBC 作为罕见且侵袭性极强的乳腺癌亚型,需临床医生保持高度警惕:对于单侧 IBC 患者,需长期密切随访(尤其 2 年内),监测对侧乳房及手术区域变化;诊断时需结合 MRI、病理活检明确分期与分子分型;治疗中需动态评估肿瘤生物学特征,依托多学科协作制定个体化方案,必要时通过 NGS 指导靶向治疗。本例虽最终预后不佳,但完整的诊疗过程为双侧 IBC 的临床管理提供了宝贵经验,强调了“早期识别、精准分型、动态调整”在这类罕见疾病中的核心价值。
Sabaté-Ortega J, Ribera-Montserrat A, Del Barco S, et al. Double trouble, managing bilateral inflammatory breast cancer: a case report. Front Oncol. 2025;15:1595513. Published 2025 Aug 20. doi:10.3389/fonc.2025.1595513
排版编辑:肿瘤资讯-Jina











 苏公网安备32059002004080号
苏公网安备32059002004080号


