神经内分泌肿瘤(neuroendocrine neoplasms, NENs)是一类起源于肽能神经元和神经内分泌细胞,具有神经内分泌分化特性并表达神经内分泌标志物的少见肿瘤,可发生于全身各处,以肺和胃肠胰最为常见[1]。由于该类肿瘤异质性显著,且目前缺乏针对的精准治疗策略,整体预后仍不理想。间变性淋巴瘤激酶(anaplastic lymphoma kinase, ALK)基因融合是非小细胞肺癌(non-small cell lung cancer, NSCLC)的一种重要分子亚型,占NSCLC的5-7%[2]。随着靶向药物的研发进展,ALK酪氨酸激酶抑制剂(ALK-TKIs)凭借其显著的疗效和可控的安全性,已被国内外权威指南一致推荐为ALK融合阳性晚期NSCLC的标准治疗方案[3-4]。然而,现有文献中关于伴ALK重排神经内分泌肿瘤靶向治疗的报道极为有限;为此,【肿瘤资讯】特邀泉州市第一医院呼吸与危重症医学科主任林艺坚教授结合洛拉替尼(lorlatinib)在临床研究中优异的疗效数据以及在临床实践中对伴ALK融合晚期神经内分泌肿瘤经洛拉替尼治疗后实现长期生存获益的典型案例进行分享,旨在为这一特殊亚群患者的个体化治疗提供关键循证依据,并为后续临床研究探索ALK-TKI在神经内分泌肿瘤中的应用价值提供新的思路与启示。
泉州市第一医院刺桐院区呼吸与危重症医学科 科主任
呼吸与危重症医学科党支部书记
海医会台海医学发展工作委员会呼吸介入和胸部肿瘤学组组员
福建省医学会呼吸病学分会第二届青委
福建省癌症康复协会肺部肿瘤康复专委会委员
福建省海峡医药卫生交流协会临床肿瘤学诊疗分会理事、小细胞学组和罕见靶点学组委员、健康科普工作委员会委员
泉州市医学会呼吸病学分会委员兼秘书
泉州市结核病综合防治质量控制专家指导委员会委员
泉州市康复医学会肺康复专业委员会委员
泉州市青年联合会第十二届委员会委员
泉州市第一医院老年病分院 呼吸与危重症医学科刺桐院区主治医师
福建省海峡肿瘤防治科技交流协会肿瘤整合专业青年委员会委员
中国抗癌协会个案管理专业委员会
一、临床试验到真实世界研究,洛拉替尼打破靶向治疗瓶颈,助力患者走向长生存
1. CROWN 研究:洛拉替尼破局 ALK 领域,重塑长期生存新标杆
洛拉替尼作为唯一的三代ALK-TKI,采用独特大环结构,从而获得更强的抗肿瘤活性、更高的血脑屏障穿透性和更广的抗ALK突变谱,显示出前所未有的全身疗效和颅内疗效。CROWN研究中,经过5年的随访,洛拉替尼组的mPFS仍未达到,远高于对照组克唑替尼的mPFS (9.1个月),且HR仅为0.19,显著降低疾病进展或死亡风险。同时,洛拉替尼一线治疗ALK阳性NSCLC的5年PFS率高达60%,是迄今为止报道的小分子靶向药物单药治疗晚期NSCLC乃至转移性实体瘤最长的mPFS[5]。
在颅内疗效方面,对于基线有可测量颅内病灶患者,颅内病灶ORR为92%,颅内病灶CR率高达58%,显示出洛拉替尼可以有效控制脑转移病灶;在基线无脑转移患者中5年无颅内进展率高达96%,114例基线无脑转移患者中仅4例发生脑转移,5年脑转移累积发生率5%,尤其在亚裔人群中5年脑转移累积发生率0%,显示出洛拉替尼不仅可以有效控制脑转移病灶而且可以预防新发脑转移,且无论基线是否有脑转移,洛拉替尼组均显示出更优的PFS获益[5]。
CROWN研究亚洲亚组数据已公布,亚洲人群及中国人群展现出与全球患者一致的生存获益;在亚洲人群中,洛拉替尼的5年PFS率为63%,克唑替尼为7%,HR为0.22(95% CI: 0.13-0.37)。在中国亚组中,经5年随访,洛拉替尼组mPFS仍未达到,5年PFS率为70%[6-7]。
总之,洛拉替尼可为ALK阳性NSCLC带来持久的生存获益,助力肿瘤患者实现“长生存”和“慢病化”的治疗目标,是ALK阳性晚期NSCLC一线治疗首选之一。
2.真实世界证据加码:洛拉替尼疗效持续领跑ALK阳性治疗赛道
在今年在AACR大会上公布了一项在中国人群中开展的真实世界研究[8],纳入了2020年2月至2025年2月在中国医学科学院肿瘤医院接受洛拉替尼治疗的63例ALK阳性晚期NSCLC患者,其中一线治疗26例。中位随访时间为10.9个月,一线治疗患者的ORR达到了90.9%,DCR 100%,12个月的PFS率为94.1%,中位PFS仍未达到。结合CROWN研究的中国人群数据,表明洛拉替尼在真实世界和临床研究中观察到的获益程度一致。
另一项回顾性研究分析了2017年9月至2024年8月在北京大学肿瘤医院接受洛拉替尼治疗的65例晚期ALK阳性非小细胞肺癌(NSCLC)患者(一线8例,后线57例)[9]。所有患者的真实世界客观缓解率(rwORR)为49.2%,真实世界疾病控制率(rwDCR)为92.3%。整个队列mPFS为37.83个月,mOS未达到。其中在一线治疗组(n=8)中,洛拉替尼的客观缓解率为100%,在中位随访9个月期间,无患者出现疾病进展(PD)。并且在此研究中洛拉替尼展现出强大的颅内疗效,在基线脑转移患者中的颅内ORR为45.2%。
还有一项回顾性研究[10]收集了陆军军医大学第一附属医院和四川大学华西医院呼吸与危重症医学科医学数据库中至2024年4月1日期间,接受洛拉替尼治疗至少1个月的ALK阳性的44例NSCLC患者,所有患者的客观缓解率为59%,疾病控制率为93%;其中15例患者接受洛拉替尼一线治疗,ORR达93%,DCR达100%;对23例于基线伴随脑转移的患者,总体颅内客观反应率(IC-ORR)为74%,颅内疾病控制率(IC-DCR)为96%,其中有7例基线伴脑转移患者洛拉替尼一线治疗,IC-ORR和IC-DCR均为100%。
总之,跨越临床与现实的边界,真实世界研究再次确证洛拉替尼以全方位疗效获益,为中国ALK阳性晚期肺癌患者构筑起坚实的生存防线。
二、临床实践:一例晚期神经内分泌肿瘤伴脑转移患者使用洛拉替尼治疗的逆袭之战
1、基本情况:
1.1、基本信息:女,40岁
1.2、初诊主诉:发现肺结节2月余
1.3、现病史:缘于入院前2月余外院体检发现肺部结节(2022.12.30“外院”肺部CT:右肺下叶占位)
1.4、既往史:“小三阳”,乙肝DNA拷贝数高,未诊治。“外院”予行“肝血管瘤、胆囊”切除手术,术后恢复可
1.5、相关检查:
影像学检查:消化+泌尿+腹腔腹膜后+肾上腺+颈部及锁骨上窝彩超显示右侧锁骨上多发肿大淋巴结肝内多发结节(最大4.1cm*3.1cm);肺部增强CT显示右肺下叶结节(29mm*21mm*22mm),MT可能;右侧肺门及纵隔多发淋巴结肿大,转移可能;头颅MR增强:颅脑MRI平扫+增强未见明显异常;胸水定位彩超:右侧胸腔积液,液深3.1cm。
肺癌相关肿瘤标志物:癌胚抗原2.04ng/mL、细胞角蛋白19片段测定4.23ug/L、神经元特异性烯醇化酶19.04ug/L、鳞癌抗原SCC0.79ng/ml、胃泌素释放肽前体353.8pg/ml。
病理检查:(右肺)纤维间质及肺泡腔中见上皮细胞巢团,细胞核大小较一致,胞浆淡染,核分裂象约3个/2mm2,结合免疫组化结果,符合神经内分泌肿瘤(G2);
基因检测:ALK融合突变,PD-L1:TPS=0
临床诊断:右下肺非小细胞癌(不典型类癌)ALK融合突变cT1cN2M1cⅣB期(肝多发)、慢性乙型病毒性肝炎、肝右叶多发转移瘤伴出血、肝多发海绵状血管瘤(介入术后)、胆囊术后、双侧胸腔积液。
2、治疗经过
一线治疗:于2023.3.3开始服用“阿来替尼600mg bid”靶向治疗和“富马酸丙酚替诺福韦片”抗乙肝病毒,考虑患者年轻女性,基线肝多发转移,为进一步提高疗效,于2023.6.8-2023.8.29期间使用“贝伐珠单抗300mg d1 ivgtt”联合“阿来替尼600mg bid”治疗;治疗6个月后,发现邻近胸膜下多发结节,较前增大增多,考虑转移灶;头颅MRI平扫+增强显示颅脑多发转移瘤。阿来替尼一线治疗的无进展生存期(PFS)为6个月左右。
后线治疗:由于患者拒绝放化疗及二次活检,因此于2023.9.27予“贝伐珠单抗300mg d1 ivgtt”联合“洛拉替尼100mg qd”治疗;治疗一个月后邻近胸膜下多发结节较前缩小,原颅脑多发转移瘤大部分消失;
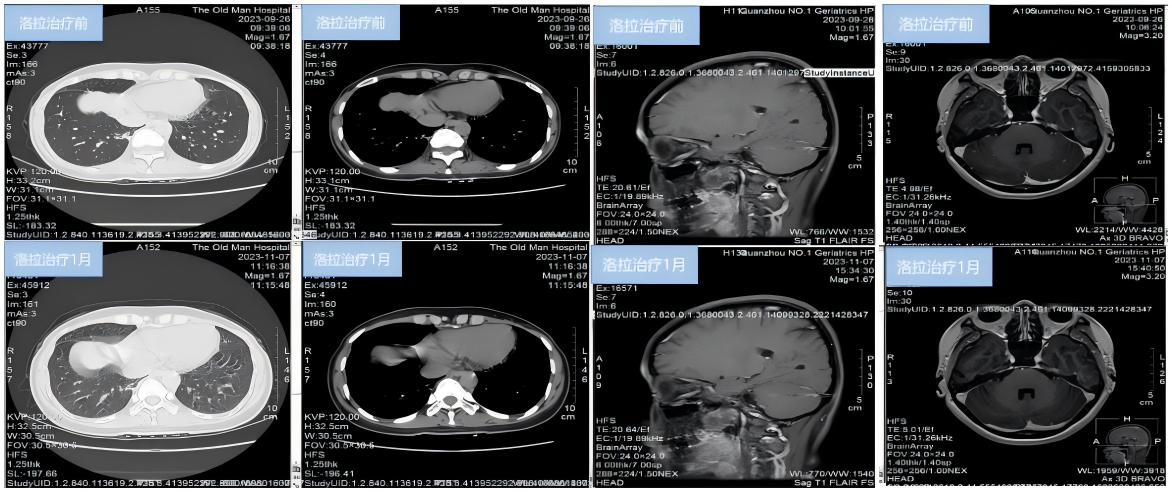
之后患者继续于2023.11.8-2024.6.25继续予“贝伐珠单抗300mg d1 ivgtt”联合“洛拉替尼100mg qd”治疗,之后洛拉替尼单药维持治疗,期间因情绪变化、睡眠障碍于2024.4.22减量为“洛拉替尼75mg qd”,因高脂血症,加用“瑞舒伐他汀”调脂后改善。由于2025年1月(洛拉治疗14个月)影像学显示右下肺病灶较前有所增大的表现,但头颅MRI平扫+增强检查显示“颅内转移瘤治疗后”,颅内未见明显异常强化灶;随即于2025年1月-4月再次给予“贝伐珠单抗300mg d1 ivgtt”联合“洛拉替尼100mg qd”治疗;
患者于2025年4月再次行右颈部淋巴结穿刺活检,病理检查显示仍符合转移性神经内分泌肿瘤(G2);免疫组化结果:Syn(+)、CgA(+)、CD56(+)、SSTR-2(-)、INSM1(+)、TTF-1(+)、Ki67热点区阳性率约为30%+;PD-L1肿瘤细胞TPS=0;血液和淋巴结基因检测显示ALK基因,EML4(IVS13)-ALK(IVS19),融合突变,丰度39.44%,同时伴随KRAS G12D错义突变,丰度69.81%以及BRCA2 p.L2165Vfs错义突变,丰度35.89%。因此继续口服“洛拉替尼100mg qd同时联合姑息放疗,之后于2025.7.21开始予“洛拉替尼+索凡替尼”治疗至今。截至目前患者使用洛拉替尼已持续近2年,一般情况良好,PS评分0分,食欲良好生活可自理。
总结
洛拉替尼作为唯一第三代ALK-TKI,凭借其独特的大环结构设计,在CROWN研究中展现出突破性的生存获益——5年PFS率高达60%,颅内缓解率达92%,不仅重塑了ALK阳性NSCLC的长期生存标杆,更以长预防+治疗”的双重脑保护机制为患者筑牢生命防线。真实世界研究进一步验证其疗效的普适性,中国人群数据与全球结果高度一致,一线治疗ORR达90%以上,后线治疗仍可带来超30个月的PFS,彰显“全程管理”价值。并且通过本文报道的神经内分泌肿瘤伴ALK融合病例,通过洛拉替尼联合治疗实现近2年疾病稳定,颅内病灶显著消退,为这类少见难治的肺癌患者提供了“靶向破局”的新思路。
从循证证据到临床实践,洛拉替尼正推动肺癌治疗向“临床治愈”迈进。未来,随着更多数据的积累,洛拉替尼有望为更多患者点燃希望之火,书写生命的新可能。
[1]中国抗癌协会神经内分泌肿瘤专业委员会,陈洁,聂勇战,吴文铭.中国抗癌协会神经内分泌肿瘤诊治指南
(2025 年版)[J].中国癌症杂志,2025,35(1):85-142.
[2] Tao H, Shi L, Zhou A et al. Distribution of EML4-ALK fusion variants and clinical outcomes in patients with resected non-small cell lung cancer. Lung Cancer. 2020 Nov;149:154-161.
[3] Riely GJ, Wood DE, Ettinger DS, et al. Non-small cell lung cancer, version10.2024, NCCN Clinical Practice Guidelines in Oncology. J Natl Compr Canc Netw, 2024.
[4]中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南 2025.
[5] Solomon BJ, Liu G, Felip E et al. Lorlatinib Versus Crizotinib in Patients With Advanced ALK Positive Non-Small Cell Lung Cancer: 5-Year Outcomes From the Phase III CROWN Study. J Clin
Oncol. 2024 Oct 10;42(29):3400-3409.
[6] Yi-Long Wu, et al. First-line lorlatinib vs crizotinib in Asian patients with ALK+ non-small cell
lung cancer (NSCLC): 5-year outcomes from the CROWN study. 2024 ESMO. Poster 1279P.
[7] Wu YL, Kim HR, Soo RA et al. First-line lorlatinib versus crizotinib in Asian patients with advanced ALK-positive NSCLC: 5-year outcomes from the CROWN study. J Thorac Oncol. 2025 Feb 28:S1556-0864(25)00097-8.
[8] 2025 AACR #5947 Poster.
[9] Tian G, Nie J, Dai L, et al. Real-world analysis of the efficacy and safety of lorlatinib in ALK positive non-small cell lung cancer patients in China. Front Oncol. 2025;15:1577607. Published 2025 May 1. doi:10.3389/fonc.2025.1577607
[10] Chen Z, Tang C, Ma X, Tian P, Gong L. Efficacy and safety analysis of lorlatinib for ALK-positive advanced NSCLC: a multicentre real-world study in China. BMC Cancer. 2025;25(1):1216. Published 2025 Jul 25. doi:10.1186/s12885-025-14631-w
排版编辑:肿瘤资讯-IR











 苏公网安备32059002004080号
苏公网安备32059002004080号


