在吉林大学第一医院I期药物临床试验病房工作,作为Sub-I负责10余项抗肿瘤药物(肝癌、乳腺癌、肺癌等实体瘤)的I期新药临床试验,负责把控整体试验流程及肿瘤患者的安全性。
发表SCI论文3篇、核心期刊2篇。
ASCO 解读文献
LB4008
Nivolumab (NIVO) plus ipilimumab (IPI) vs lenvatinib (LEN) or sorafenib (SOR) as first-line treatment for unresectable hepatocellular carcinoma (uHCC): First results from CheckMate 9DW.
研究背景
基于程序性死亡配体1(PD-L1)抑制剂的疗法已成为不可切除肝细胞癌(uHCC)的一线标准治疗,其疗效优于索拉非尼,然而患者预后仍较差,目前仍需长期生存获益的替代疗法。在CheckMate 040研究中,纳武利尤单抗(NIVO)联合伊匹木单抗(IPI)作为二线方案,在索拉非尼经治的肝细胞癌(HCC)患者中表现出具有临床意义的疗效和可控的安全性,并因此在美国获得加速批准。本研究旨在评估NIVO + IPI对比仑伐替尼(LEN)或索拉非尼(SOR)作为uHCC一线治疗在III期CheckMate 9DW临床试验中的疗效与安全性。
研究方法
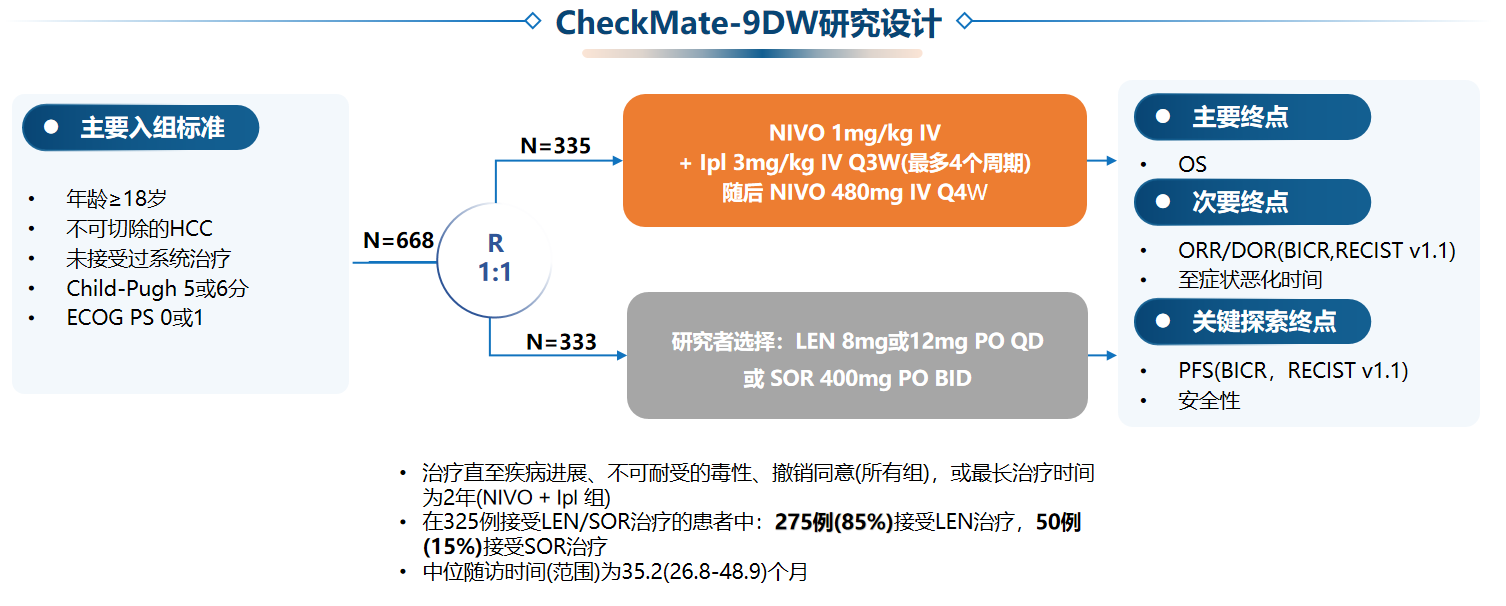
研究纳入标准:年龄≥18岁、既往未接受过治疗且不适合根治性手术或局部治疗的uHCC成人患者,Child-Pugh评分为5–6分,ECOG PS评分为0–1分。患者按1:1随机分配至两组:试验组(NIVO+IPI):接受纳武利尤单抗(1 mg/kg)联合伊匹木单抗(3 mg/kg)静脉输注,每3周一次(最多4个周期),后序贯纳武利尤单抗单药480 mg每4周一次维持治疗;对照组(LEN/SOR):由研究者选择口服仑伐替尼(根据体重8 mg或12 mg 每日一次)或索拉非尼(400 mg每日两次)。治疗持续至疾病进展或出现不可耐受的毒性。纳武利尤单抗总用药时间不超过2年。
研究结果
总计668例患者被随机分配至NIVO+IPI组(n=335)或LEN/SOR组(n=333),在LEN/SOR组接受治疗的 325 名患者中,275 名(85%)接受了仑伐替尼治疗。中位随访时间35.2个月(26.8–48.9个月),结果显示:NIVO+IPI组和LEN/SOR组中位总生存期(OS )分别为23.7 个月和20.6 个月 (HR= 0·79),24个月OS率分别为49%和39%。NIVO+IPI组的客观缓解率(ORR)显著高于LEN/SOR组(36% vs13%),完全缓解率(CR)较LEN/SOR组更高(7% vs 2%)。NIVO+IPI组和LEN/SOR组的中位缓解持续时间(DOR)分别为30.4个月和12.9个月。NIVO+IPI组3-4级与药物相关的不良反应(TRAEs)发生率与对照组治疗相当(41% vs 42%),导致停药的TRAEs发生率也处于较低水平。药物相关不良反应汇总情况见下表。

研究总结
在既往未经治疗的uHCC患者中,纳武利尤单抗联合伊匹木单抗对比仑伐替尼或索拉非尼,展现出显著的总生存期获益以及更高的客观缓解率,且持久应答并安全可控。以上结果支持该双免疫联合方案成为uHCC一线治疗的潜在新标准治疗方案。
临床研究信息: NCT04039607
解读
2008年,索拉非尼开启HCC靶向治疗的新阶段,历经十年仑伐替尼横空出世,对比索拉非尼,总体生存期非劣于索拉非尼,PFS和ORR显著获益[1],已逐步替代索拉非尼成为不可切除肝癌的一线标准治疗方案。酪氨酸激酶抑制剂(TKI)虽作为不可切除HCC的一线标准治疗方案,但其中位OS仅约12-14个月,且安全性结果不尽人意。近年来,为了探索长期生存获益的替代疗法,以免疫治疗为基础的联合治疗研究风起云涌。肝癌治疗已进入以免疫为基础的治疗时代,免疫联合靶向治疗和双免疫治疗,已经成为晚期uHCC系统治疗的新趋势。
免疫联合靶向治疗对比单靶一线治疗uHCC具有显著的生存获益。IMbrave150 研究[2]表明,阿替利珠单抗联合贝伐珠单抗在一线治疗uHCC患者中,对比索拉非尼组,中位OS和PFS均明显延长,中位OS可长达19.2个月。在ORIENT 32研究[3]显示,信迪利单抗联合贝伐珠单抗类似物在中国uHCC患者的一线治疗中,对比索拉非尼显示出了显著的OS和PFS获益,且具有良好的安全性。
CARES-310研究[4]同样显示,阿帕替尼联合卡瑞利珠单抗与索拉非尼组相比,OS和PFS显著获益,开创了HCC一线治疗III期研究中最长OS记录,中位OS长达22.1个月。
双免疫联合治疗在uHCC一线治疗领域也取得了成功。HIMALAYA 研究[5]中,对比索拉非尼,度伐利尤单抗联合替西木单抗在初治uHCC患者的一线治疗中具有较好的临床疗效和可控的安全性,降低死亡风险 22%。
虽然基于PD-L1抑制剂的治疗方案一线治疗uHCC的 OS和PFS显著优于索拉非尼,中位OS可延长至16-19个月,但uHCC的长期预后仍有待改善,仍需可实现长期生存获益且安全的替代疗法。目前关于治疗uHCC的临床研究中多以索拉非尼为对照组,鲜有研究敢于直面仑伐替尼的挑战,LEAP-002研究[6]中,仑伐替尼联合帕博利珠单抗对比仑伐替尼联合安慰剂组,在OS和PFS方面未达到预计统计学终点。目前未有靶免联合方案在研究中被确证优于仑伐替尼。
本研究Checkmate 9DW [7]是全球首个以仑伐替尼作为主要对照在一线uHCC中取得阳性结果的III期研究,评估了NIVO+IPI对比LEN或SOR作为uHCC一线治疗的疗效和安全性。CheckMate 040[8]研究中,纳武利尤单抗联合伊匹木单抗作为在索拉非尼经治的HCC二线方案,具有临床意义的疗效,中位OS可达22.2个月 ,同时安全可控,从而奠定了本研究Checkmate 9DW的基础。本研究首次证实双免疫联合疗法一线治疗uHCC显著优于传统靶向药,接受NIVO+IPI治疗相比接受LEN和SOR均显示出了总生存获益,HR分别为0.42[95%CI 0.24–0.73]和0.77 [95% CI 0.62–0.95],中位生存长达 23.7个月,应答患者有望突破4年。NIVO+IPI组ORR和CR显著优于对照组:ORR 36% vs 13%;CR 7% vs 2%。与对照组相比,NIVO+IPI组DoR 30.4个月,实现短期疗效转化为长期生存。NIVO+IPI组可快速缩瘤,中位起效时间快于对照组:TTR 2.2个月 vs. 3.7个月,同时缩瘤效果显著,有37%患者靶病灶缩小一半以上,为转化切除创造可能。NIVO + IPl安全可控,与既往以PD-1抑制剂为基础的联合治疗相比未观察到新的安全性信号。基于CheckMate 9DW 的突破性数据,NIVO+IPI成为中国唯一获批HCC双免治疗方案,成为uHCC一线治疗的新标准。
NIVO+IPI(PD-1+CTLA-4抑制剂)双免协同激活免疫,可以克服肿瘤免疫微环境抑制,从多重抑制到强效激活,实现免疫记忆效应。一线使用NIVO+IPI,通过改变肿瘤微环境,提高后续治疗的敏感性,后续序贯靶向治疗,可能产生更好的协同效应,或许可以克服双免方案出现的耐药问题,有望为患者带来更优的全程获益。
目前本研究中位随访35.2个月,免疫治疗的“长拖尾效应”可能尚未完全体现,需更长时间随访确认最终OS获益。另外双免治疗发生irAE的时间早于单免,肝癌患者发生肝炎的风险增加,双免联合治疗需注意基线风险评估和治疗期间的肝功能监测。同时仍需进一步识别NIVO+IPI方案的优势人群,从而获得更显著的治疗获益。
王楠娅 吉林大学第一医院
从2007年索拉非尼横空出世至今,晚期HCC的系统治疗发生了翻天覆地的变化。一方面是新的抗血管生成靶向药物层出不穷;另一方面,以PD-1/PD-L1为代表的免疫检查点抑制剂彻底改变了晚期HCC的治疗格局与预后。晚期HCC也从单药靶向到靶免联合再到双免治疗不断的变迁,未来也会面临更多的联合治疗策略与模式,为患者带来更多的选择。
【温馨提示】:如果您觉得周景医生解读的好,请在下方为她点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
[1] Kudo M, Finn RS, Qin S, et al. Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomised phase 3 non-inferiority trial. Lancet. 2018 Mar 24;391(10126):1163-1173.
[2] Cheng AL, Qin S, Ikeda M, et al. Updated efficacy and safety data from IMbrave150: Atezolizumab plus bevacizumab vs. sorafenib for unresectable hepatocellular carcinoma. J Hepatol. 2022 Apr;76(4):862-873.
[3] Ren Z, Xu J, Bai Y, et al. Sintilimab plus a bevacizumab biosimilar (IBI305) versus sorafenib in unresectable hepatocellular carcinoma (ORIENT-32): a randomised, open-label, phase 2–3 study. Lancet Oncol. 2021 Jul;22(7):977-990.
[4] Qin S, Chan SL, Gu S, et al. Camrelizumab plus rivoceranib versus sorafenib as first-line therapy for unresectable hepatocellular carcinoma (CARES-310): a randomised, open-label, international phase 3 study. Lancet. 2023 Sep 30;402(10408):1133-1146.
[5] Sangro B, Chan SL, Kelley RK, et al. Four-year overall survival update from the phase III HIMALAYA study of tremelimumab plus durvalumab in unresectable hepatocellular carcinoma.Ann Oncol. 2024 May;35(5):448-457.
[6] Llovet JM, Kudo M, Merle P, et al. Lenvatinib plus pembrolizumab versus lenvatinib plus placebo for advanced hepatocellular carcinoma (LEAP-002): a randomised, double-blind, phase 3 trial. Lancet Oncol. 2023 Dec;24(12):1399-1410.
[7] Yau T, Galle PR, Decaens T, et al. Nivolumab plus ipilimumab versus lenvatinib or sorafenib as first-line treatment for unresectable hepatocellular carcinoma (CheckMate 9DW): an open-label, randomised, phase 3 trial. Lancet. 2025 May 24;405(10492):1851-1864.
[8] Melero I, Yau T, Kang YK, et al. Nivolumab plus ipilimumab combination therapy in patients with advanced hepatocellular carcinoma previously treated with sorafenib: 5-year results from CheckMate 040. Ann Oncol. 2024 Jun;35(6):537-548.











 苏公网安备32059002004080号
苏公网安备32059002004080号


