病例介绍
初诊发现与初步评估
患者,女性,64岁。于2022年8月体检时发现肝脏多发病灶。腹部增强CT提示肝内多发异常强化结节(最大约3 cm),门静脉旁及腹膜后多发稍大淋巴结。FDG-PET/CT提示肝脏多发恶性肿瘤可能,同时见胃壁稍增厚和肛管处良性病变可能。外院胃镜检查未见明显异常。后续肝脏病灶穿刺活检病理提示NET G3级,Ki-67阳性率在热点区约为 30%。

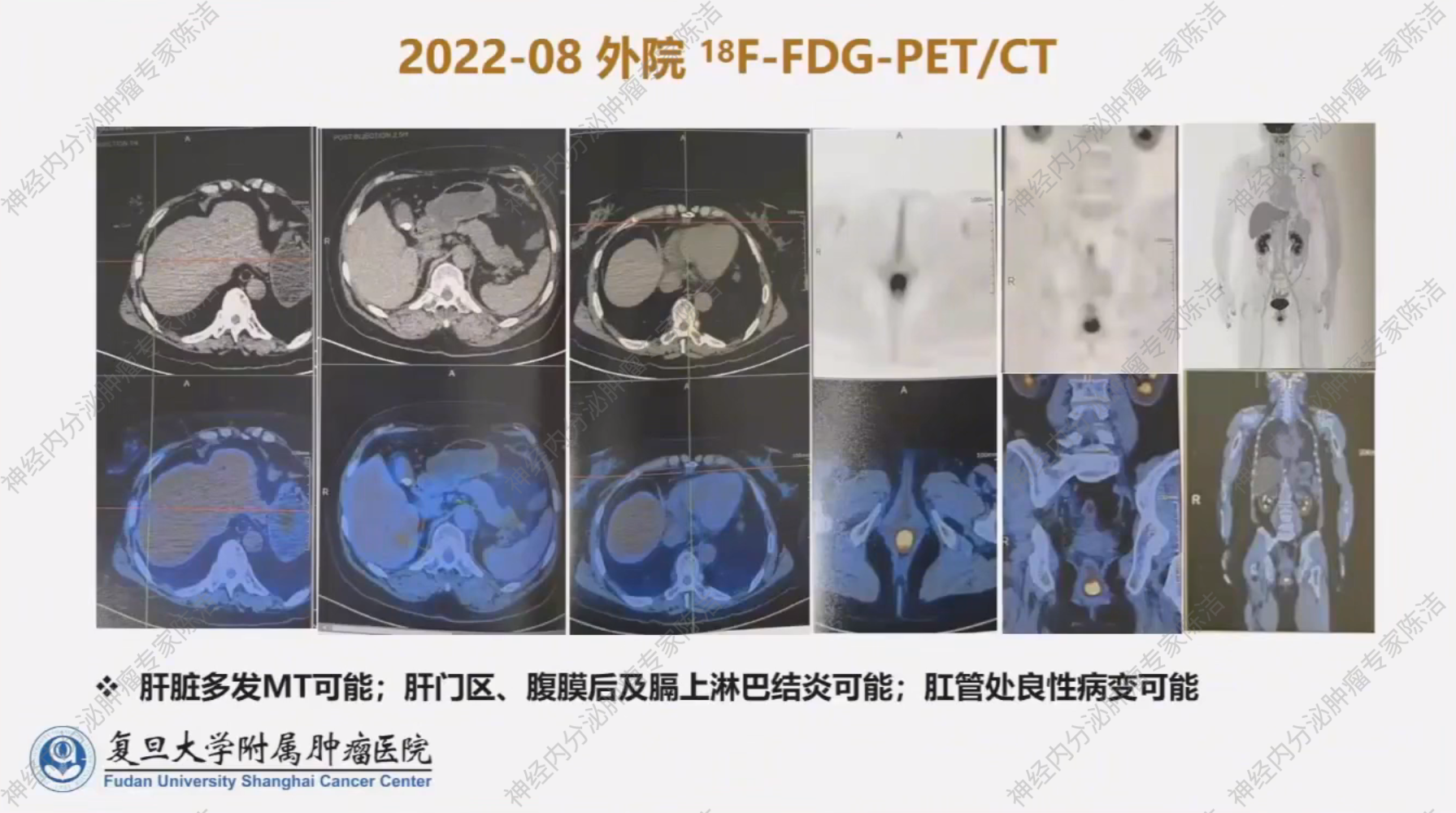
全面评估与原发灶定位
患者于2022年9月就诊于复旦大学附属肿瘤医院,完善 68Ga-SSA PET/CT,提示肝内多发SSTR高表达转移灶、胰腺体尾部多发SSTR高表达病灶以及直肠下段局灶性 SSTR高表达病灶(距肛缘6cm,大小约1.5 cm隆起),提示原发灶位于直肠。肠镜也证实了直肠存在一隆起病灶,考虑为NET原发病灶。
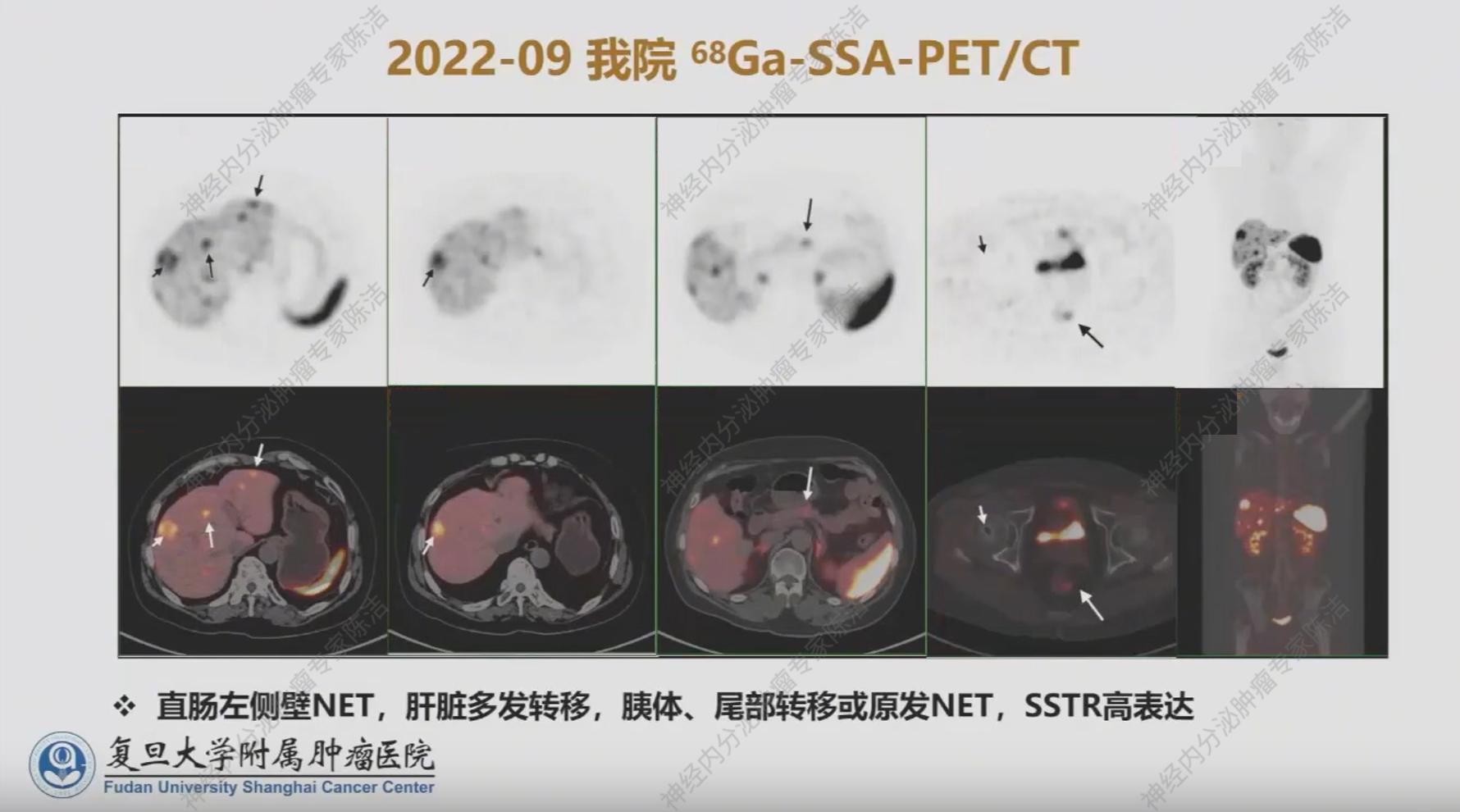
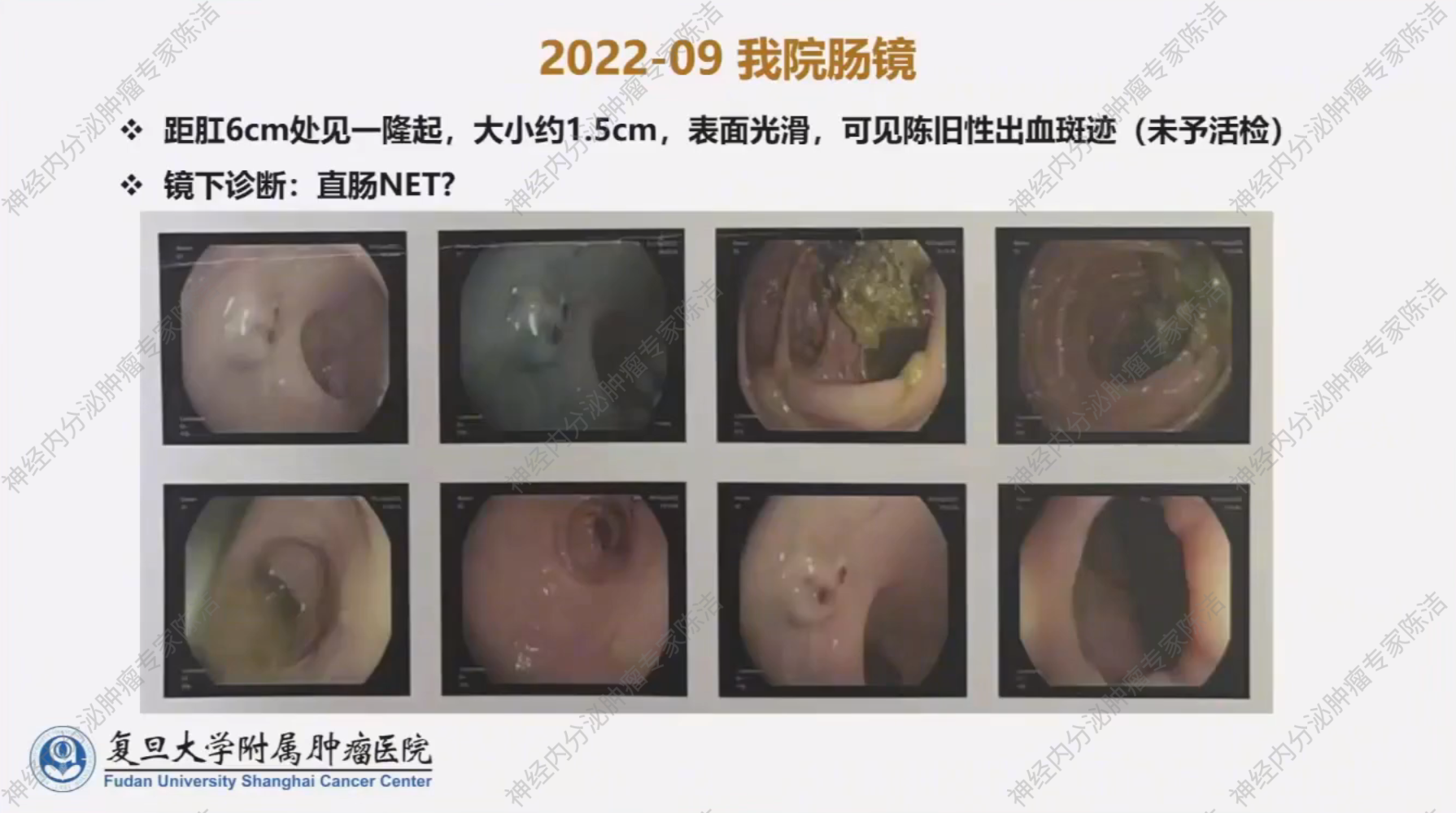
增强CT进一步证实了肝脏及胰腺多发转移。基线肝脏普美显磁共振提示肝脏病灶数量较常规CT多,这些小病灶在常规CT上难以发现,也证实了普美显磁共振在肝脏肿瘤负荷评估中的重要性。
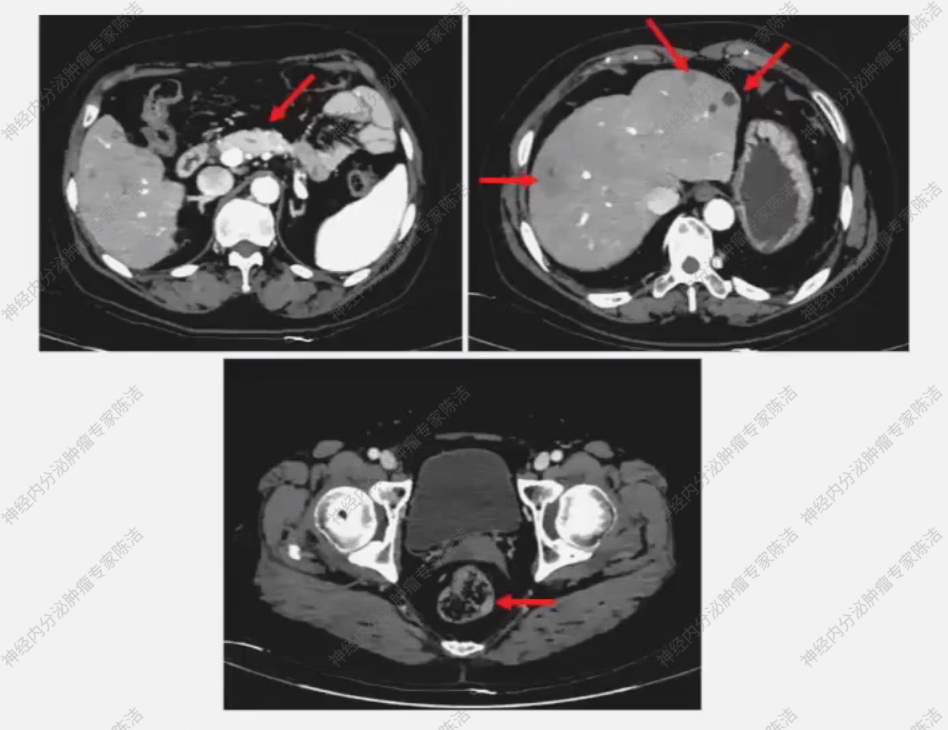
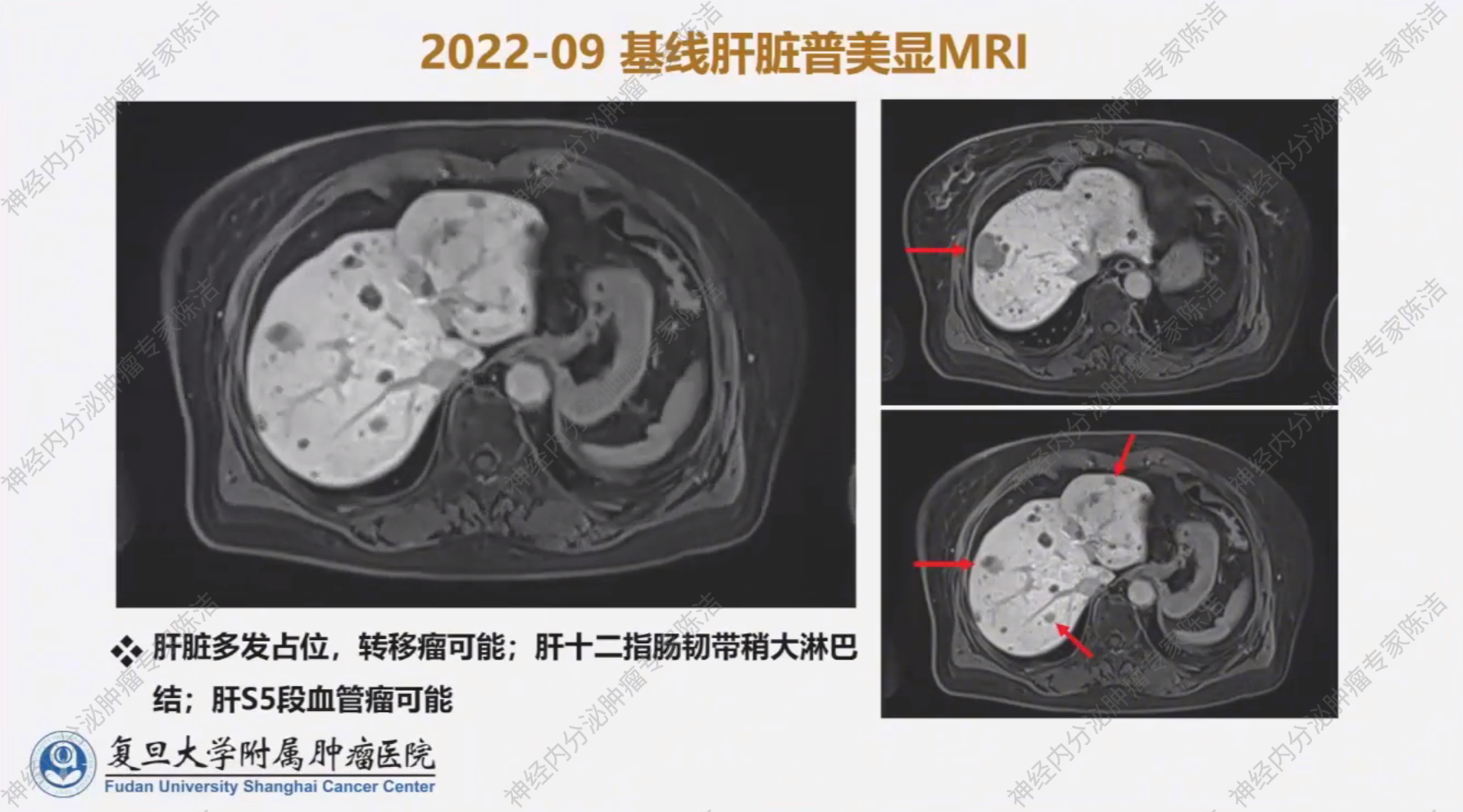
治疗历程
一线治疗及首次疾病进展
根据患者病史及辅助检查结果,诊断为直肠NET,伴肝、胰腺转移,IV期,G3级。鉴于患者肝脏转移灶多发且可见血供,介入科建议行肝内转移瘤栓塞治疗。患者肿瘤Ki-67指数低于55%,且PET/CT显示病灶均为生长抑素受体高表达和FDG低糖代谢,尽管外院病理提示为G3级,考虑肿瘤属于生物学行为良好的G3级,患者可能从SSA类药物治疗中获益。综合考虑,患者初期治疗方案为:长效奥曲肽30mg,每4周一次,联合肝脏局部介入栓塞治疗。
从2022年9月至11月,患者共接受了3次肝脏局部介入栓塞治疗。2022年12月复查结果提示肝脏病灶明显缩小,直肠原发灶及胰腺转移灶基本稳定,疗效评估为部分缓解 (PR)。
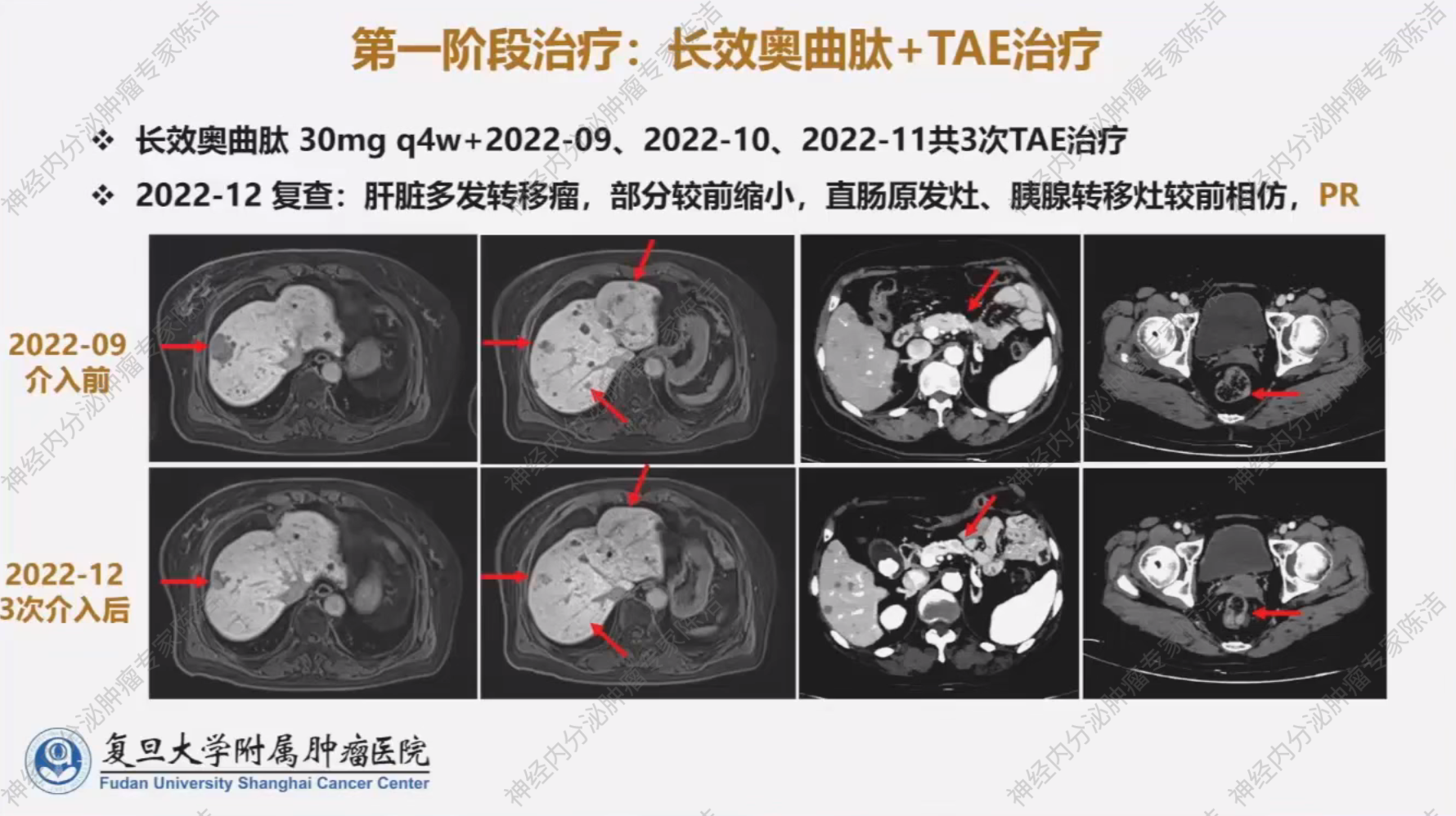
患者随后维持长效奥曲肽治疗6个月。然而,在2023年6月的复查中,肝脏病灶出现了新的小结节,提示疾病进展,疗效评估为疾病进展 (PD)。
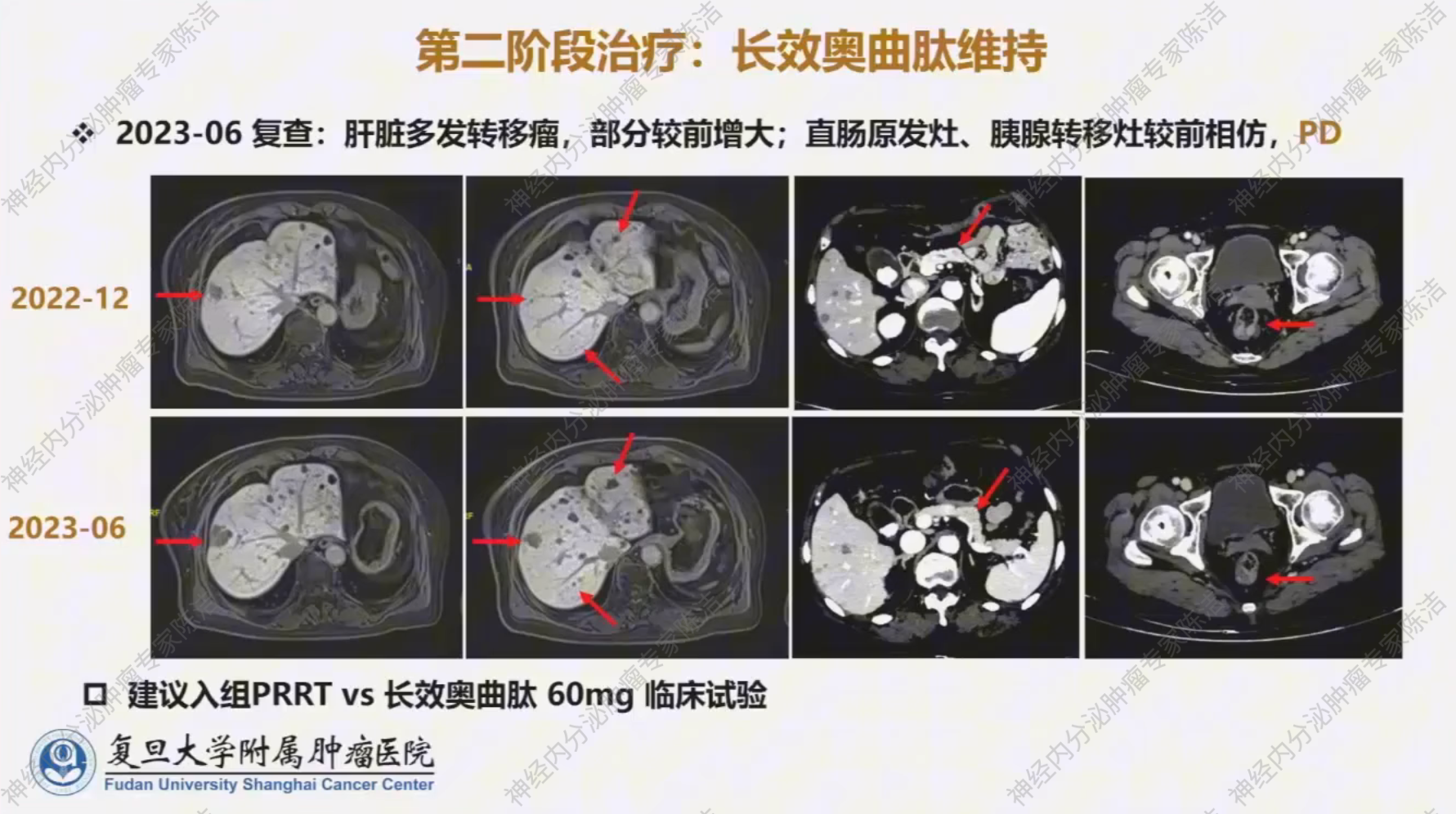
PRRT 治疗、骨髓抑制与再次疾病进展
在疾病进展后,患者入组 PRRT 临床试验。在入组前,对患者的肝脏穿刺活检病理进行了复核。复旦肿瘤医院病理科会诊结果显示,Ki-67阳性率仅为10%(G2 级),这低于外院的评估结果。同时,免疫组化可见SSTR2 强阳性。

再次进行的 68Ga-SSA PET/CT检查显示,肝内、胰腺及直肠病灶的SSTR表达仍然很高,左侧锁骨新见一个小灶性成骨性改变,提示可能存在骨转移。
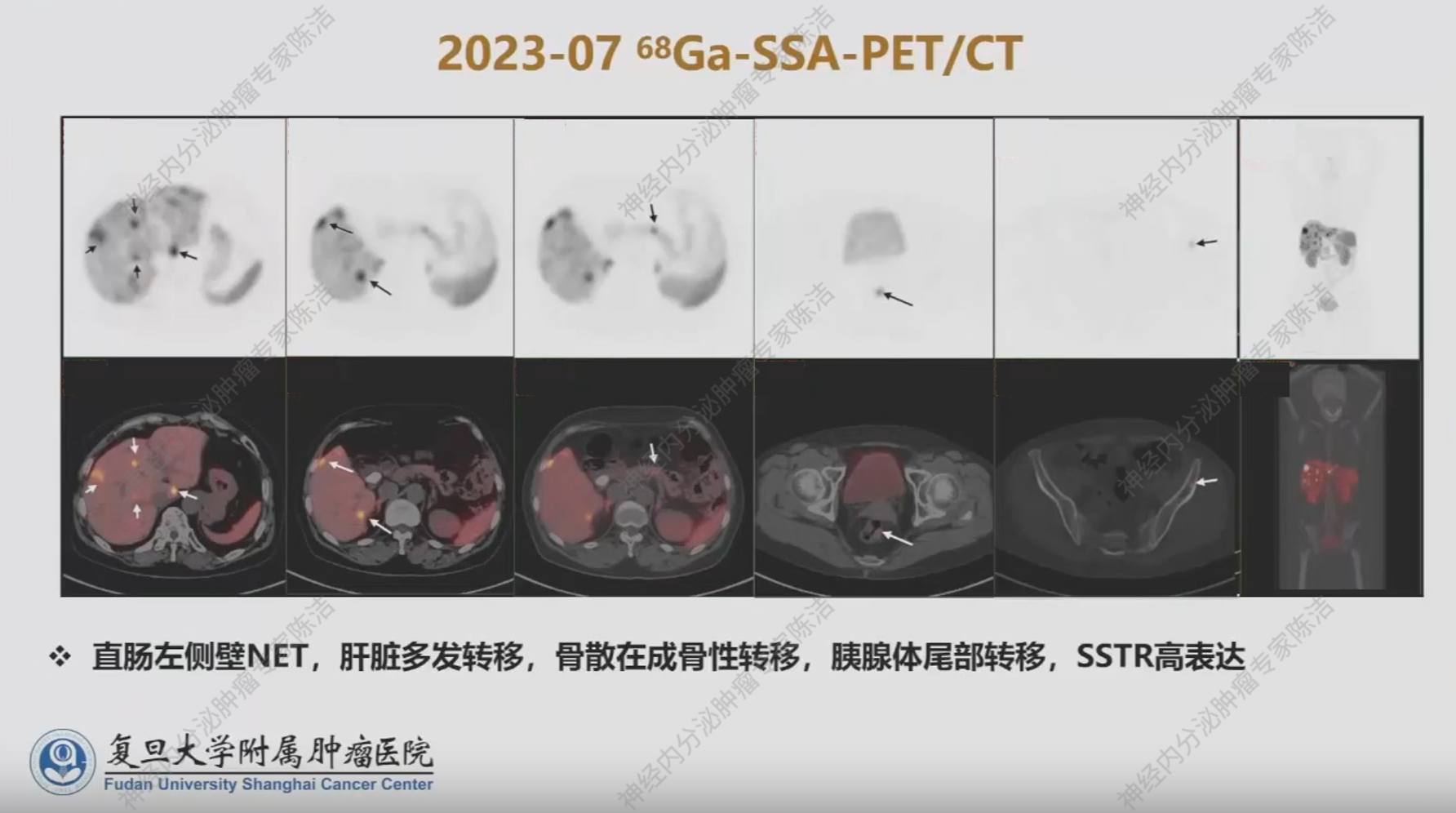
患者于2023年8月至2024年4月期间共接受了4次PRRT治疗。治疗后的SPECT 图像显示肿瘤对 Lu-177 的摄取效果良好。
2024 年 4 月复查时,肝脏病灶明显退缩,疗效评估为部分缓解 (PR),无进展生存期 (PFS) 达到了19.5个月。
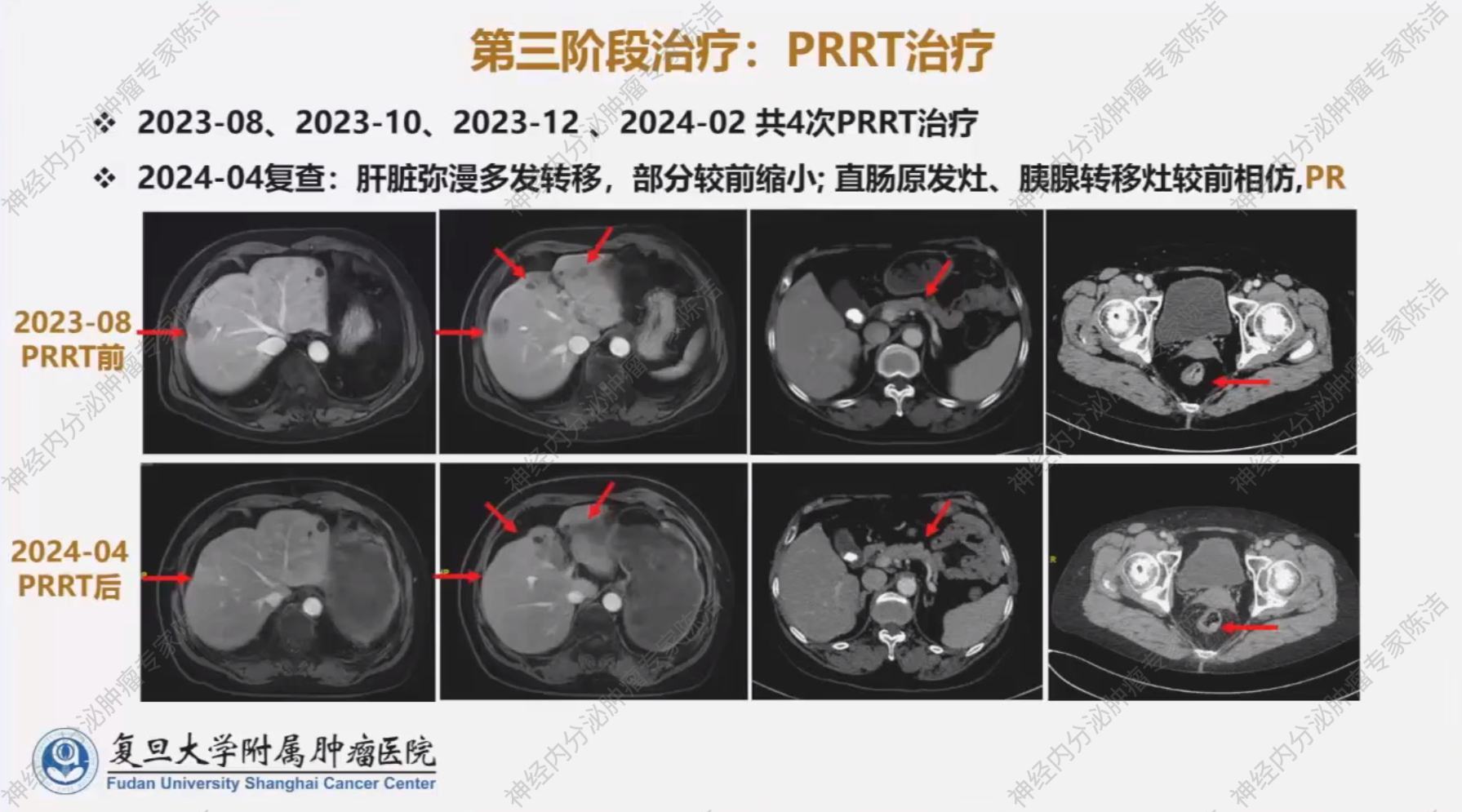
然而,PRRT 治疗也带来了显著的副作用:患者出现了长达20个月的长期骨髓抑制,最严重时达到III度,主要表现为白细胞、中性粒细胞和血小板的减少,需要长期对症治疗。
2025年3月复查提示,肝内新见较多弥漫分布的微小结节。
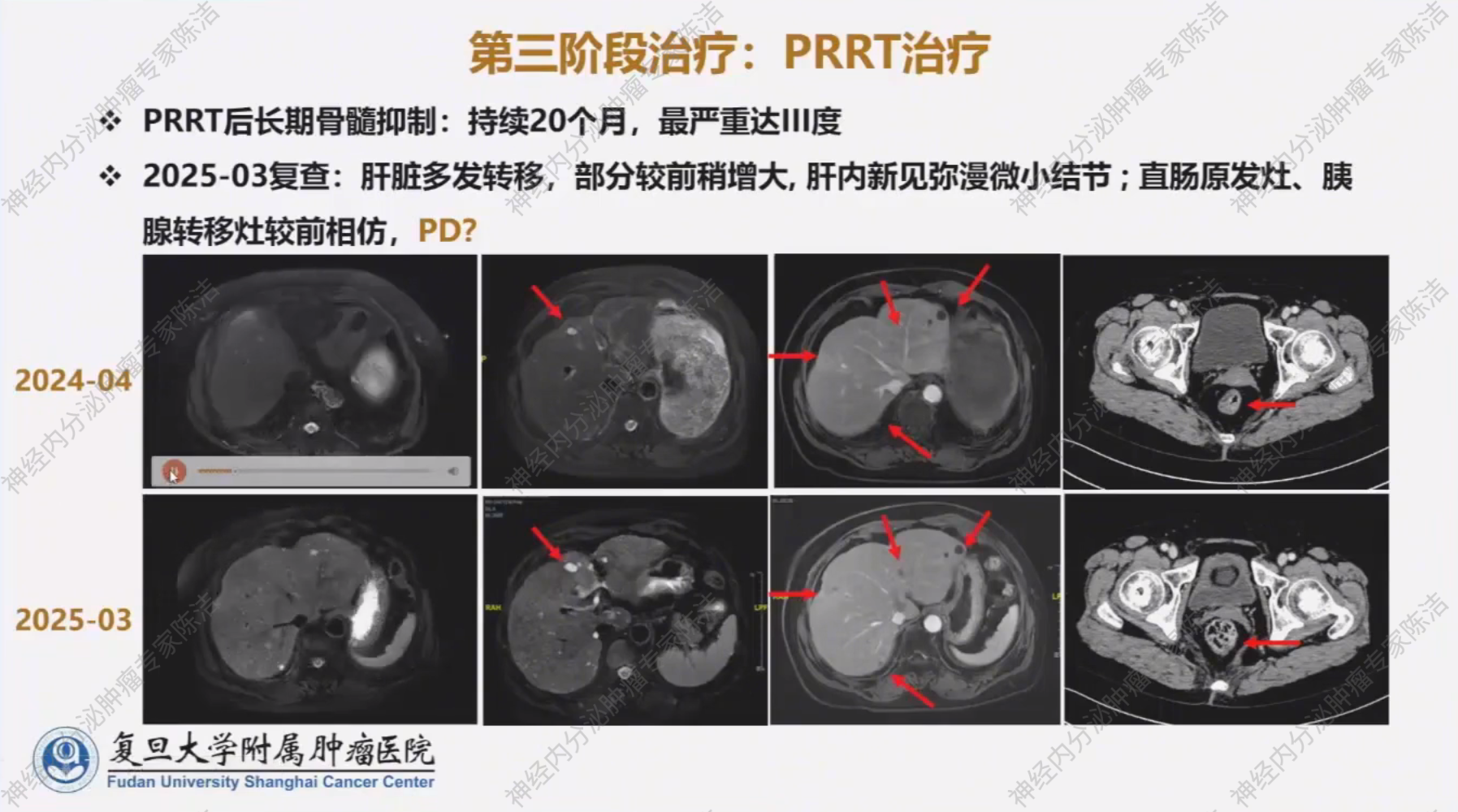
考虑患者短期内新发较多且弥漫分布的结节,依据影像学检查难以明确是否为新发转移病灶,为此,对新发肝脏病变进行了再次活检。病理结果仍然提示 NET G2级,Ki-67 指数仍为 10%,未观察到肿瘤级别升高或瘤癌转化的倾向。基因检测显示 PD-L1 低表达,肿瘤突变负荷 (TMB) 和 CD8+ T 细胞浸润也较低,提示免疫治疗获益的可能性不大。

FDG-PET/CT 显示肝脏病灶仍为本底摄取,骨转移灶和胰腺转移灶也为低代谢,与Ki-67指数相符,未见明显升级。综合评估疗效为疾病进展 (PD),但肿瘤级别并未提高。
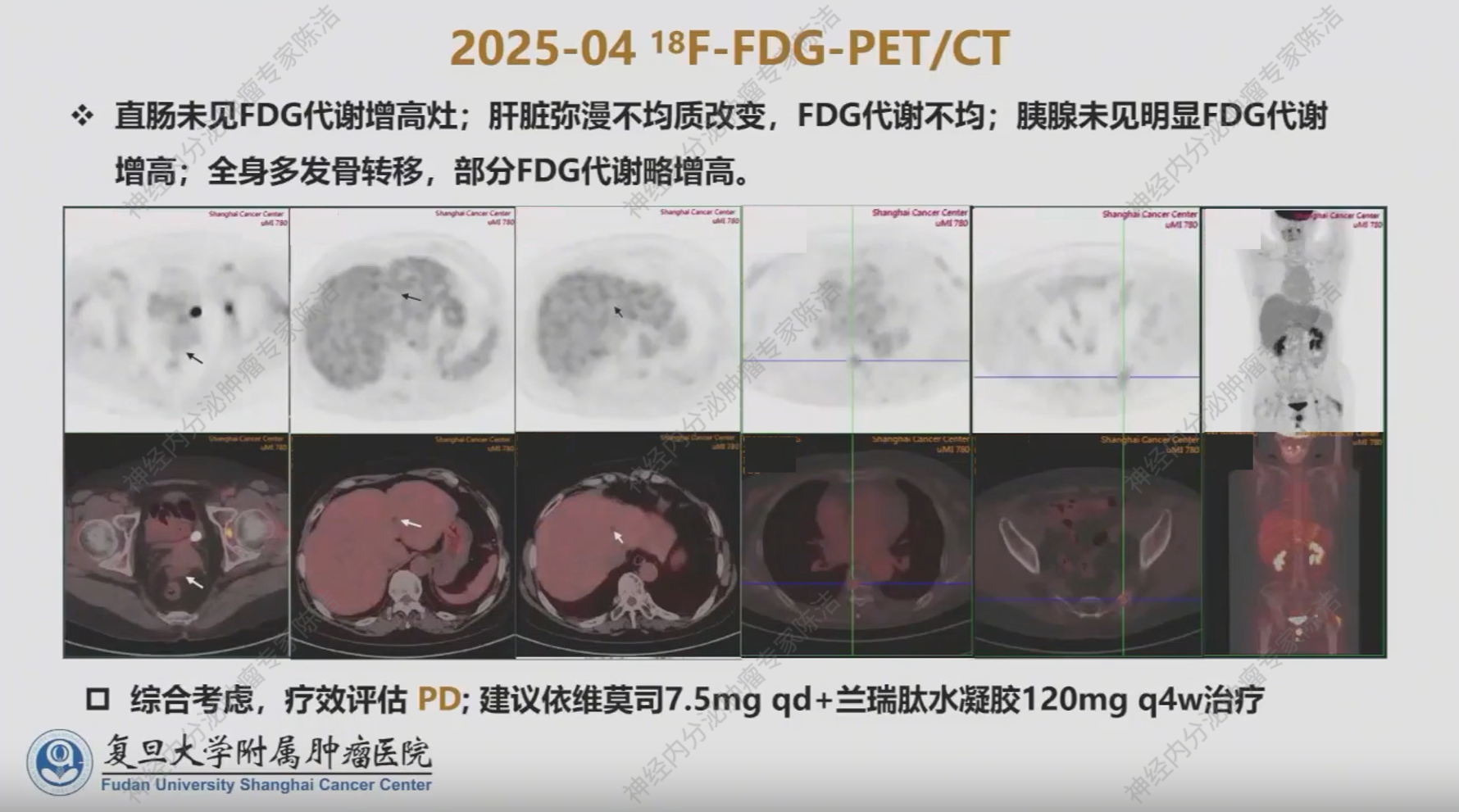
后续治疗方案
考虑到原发灶为直肠,且PRRT治疗后长期存在骨髓抑制,于2025年4月予调整第四阶段治疗方案为:依维莫司7.5mg qd联合兰瑞肽水凝胶120mg每4周一次。目前尚未进行首次疗效评估。
MDT讨论
李珊珊教授:该患者的病理学评估结果揭示了该神经内分泌瘤(NET)在不同时间点的稳定生物学特性。2022年外院肝脏穿刺活检的病理诊断为 NET G3级,Ki-67增殖指数为30%。然而,经复旦肿瘤医院病理科会诊后,Ki-67阳性率复核为10%(G2 级)。尽管在不同评估中 Ki-67 存在差异,但该患者的病理形态和增殖活性在较长时间内变化不显著。同时,肿瘤的生长抑素受体表达始终维持强阳性。这种持续且稳定的生长抑素受体高表达,以及异质性表达不明显的特点,为后续靶向生长抑素受体的治疗策略提供了坚实的病理学基础。这表明肿瘤细胞在较长时间内保持了相对一致的生物学行为,为选择合适的治疗方案提供了重要依据。
徐俊彦教授:该患者外院基线的FDG-PET/CT显示肝内病灶糖代谢水平不高,与最初的G3 级病理不完全符合,因此建议进行病理会诊。同时,肛管局部摄取增高可能由痔疮或炎症引起,与肿瘤关系不大。在我院进行的68Ga-SSA PET/CT结果确认,该患者肝内多发转移灶、胰腺病灶以及直肠原发灶均为SSTR 高表达,并且直肠 NET 中胰腺转移相对多见。在患者进展后再次复查的68Ga-SSA PET/CT中,SSTR表达依然高,同时发现左侧锁骨小灶性成骨性改变,可疑骨转移。该患者在PRRT治疗后的SPECT结果证实,肿瘤对药物摄取良好,尤其是在肝内肿瘤区域。对于疾病进展后再次进行的 FDG-PET/CT,即使该患者肝脏出现弥漫性转移,其糖代谢仍处于本底水平,没有明显高代谢病灶,这与Ki-67指数相符,未见肿瘤级别升级。
汤伟教授:直肠NET的特点是原发灶较小但常伴肝脏转移,且CT容易漏诊小病灶。影像科医生需特别注意,直肠、肺、纵隔和肾脏的NET容易向胰腺转移,应避免漏报。在评估该患者肝脏病灶时,普美显磁共振在发现CT难以识别的小灶性肝脏转移瘤以及准确评估肝脏肿瘤负荷方面至关重要,这直接影响外科减瘤和内科治疗方案的制定。在疗效评估方面,该患者介入治疗后肝脏病灶缩小被明确判断为PR。当疾病进展时,影像表现为肝脏转移瘤明确增大且出现新发转移,疗效评估为PD。对于该患者第四阶段复查时肝内新见的弥漫性微小结节,影像学上诊断为新发转移的证据尚不充分,建议结合临床并考虑穿刺鉴别,这也促成了后续的再次活检。
专家讨论
本次多学科会诊的专家点评环节,由郑州大学第一附属医院岳松伟教授和李向柯教授聚焦于该直肠神经内分泌肿瘤病例,分享了各自领域的深刻见解。
岳松伟教授作为影像诊断专家指出,神经内分泌肿瘤虽为“小瘤种”,却充分体现了临床诊疗的“大综合”与“大作为”,涵盖了诊断、治疗、内外科及介入等多个维度。从影像学角度,该病例展示了 CT、超声内镜、磁共振以及 PET/CT 等多种形态学与功能性影像手段的综合应用。岳教授强调,影像学在肿瘤的 早期诊断、定位、定性、分期诊断中发挥着关键作用,并在肿瘤治疗过程中的疗效评估中占据重要地位。他提及 CACA 指南详细阐述了各种影像学技术的优势,建议深入研读以掌握不同检查方法的特点,从而为疾病诊疗提供参考。
李向柯教授认为神经内分泌肿瘤在诊断和治疗中面临着显著的异质性挑战,包括肿瘤本身的多样性以及不同医疗机构间病理诊断的一致性问题。若能结合双核素显像和多点穿刺,能对肿瘤生物学行为进行更全面评估。患者在PRRT后肿瘤再次进展,再次穿刺后Ki-67指数仍为10%(G2 级),基于近期公布的依维莫司联合兰瑞肽的研究数据,该患者有望从目前选择的依维莫司联合兰瑞肽方案中获益。
陈洁教授总结
本例患者为直肠原发神经内分泌肿瘤伴肝、胰腺及骨多发转移。其治疗过程中有两个方面值得关注:一方面,该患者在PRRT后的复查中,发现肝内快速出现的弥漫分布的小结节,单纯从常规影像学上难以确认新发结节为肿瘤病灶,最终通过穿刺活检明确了弥漫分布的新发结节确实为肝转移病灶。不过,再次活检的病例并没有发现肿瘤出现明显的级别上升或瘤癌转换现象,这为后续治疗方案调整提供了重要依据;另一方面,虽然患者在PRRT治疗后获得较长的PFS获益,但患者也出现PRRT主要的副作用之一,即骨髓抑制。且该患者骨髓抑制程度及持续时间较长,后续进展后药物方案选择受到一定限制。基于患者再次穿刺活检病理结果(肿瘤仍为G2级),以及近期公布结果的3期临床试验(JCOG1901研究,兰瑞肽联合依维莫司对照依维莫司单药),为患者选择了骨髓抑制风险较低的兰瑞肽联合依维莫司方案,希望患者能从中获益。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看CACA神经内分泌肿瘤指南巡讲-南阳站回放:
https://doctor.liangyihui.net/#/live/147592

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。











 苏公网安备32059002004080号
苏公网安备32059002004080号


