晚期胃癌,特别是HER2阳性晚期胃癌,经过多线治疗疾病进展后的预后不容乐观。寻找有效的后线治疗方案对于延长患者的生存期至关重要。新型抗体偶联药物(ADC)维迪西妥单抗(RC48)的出现和应用为HER2阳性晚期胃癌患者带来了新希望。上海市东方医院海亚楠医生分享1例HER2阳性晚期胃癌后线使用维迪西妥单抗联合治疗获长生存病例:患者女性,70岁,胃癌术后复发,伴有腹腔积液,在经历了包括手术、化疗、靶向治疗在内的多线治疗失败后,采用维迪西妥单抗联合信迪利单抗和阿帕替尼治疗,实现了长期疾病控制,明显延长了生存,无进展生存期(PFS)接近2年半,长达29个月。【肿瘤资讯】将病例诊疗过程整理如下,并邀请上海市东方医院周英教授对病例进行点评,以飨读者。
病例介绍
专家介绍
同济大学附属东方医院肿瘤科
上海交通大学医学院肿瘤学博士
上海市浦东新区肿瘤专业委员会秘书
上海市中西医结合学会第二届胰腺疾病专委会青委
上海健康生活促进会肿瘤科普与综合诊疗专委会委员
上海市社会医疗机构协会肿瘤学分会患教专委会委员
聚焦消化道肿瘤,尤其结直肠癌、胃癌、食管癌等的化疗 靶向 免疫等综合治疗。作为Sub-I参加科室多项临床研究,负责肿瘤营养GPS病房建设。
主持CSCO-肠癌基金一项,参与多项国自然研究项目,发表SCI论文数篇
既往诊疗情况
基本情况
患者,女性,70岁。ECOG PS 1分。
2020年11月11日体检胃镜确诊胃癌。
2020年12月07日行全胃切除术。术中:胃体小弯侧见一溃疡型肿物,大小10*9*1cm,切面灰白色,实性,质硬,肿物中心距胃食管交界处5cm。术后病理:低分化腺癌,部分为黏液腺癌,肿瘤最大径10cm,浸润深度:浆膜层,癌结节2枚,神经侵犯(+),脉管癌栓(+),贲门周淋巴结(1/1),胃小弯淋巴结(5/9),胃大弯淋巴结(1/6),幽门下淋巴结(3/5),另送淋巴结:第一组(1/1),第8组(1/4)可见癌组织,第7组为癌结节1枚,第2组(0/4),第3组(0/1),第5组(0/1),第6组(0/2),第4组、第9组(为纤维脂肪组织均未见癌转移)。IHC:pMMR、Topo II(70%)、Ki-67(90%)、 CerbB2(3+)。
术后分期:pT4aN3aM0 HER2 IHC(3+)
2020年12月25日复查盆腔MRI+CT:盆腔积液;周围腹膜改变,腹膜后肿大淋巴结,转移考虑。
一线治疗
2020年12月29日至2021年2月20日予XELOX+曲妥珠单抗治疗3周期。评效:腹水控制不佳。
二线治疗
2021年3月19日予白蛋白结合型紫杉醇+替吉奥+曲妥珠单抗治疗1周期。评效:1个月后复查腹水较前增多。
三线治疗
2021年4月22日至2021年5月31日予FOLFIRI+阿帕替尼治疗3周期。评效:腹水控制不佳。2021年6月19日至2021年8月7日予FOLFIRI +阿帕替尼+曲妥珠单抗治疗3周期。评效:腹水控制不佳。
本次诊疗情况
2021年8月19日来我院就诊,当天上腹部(CT平扫):胃术后改变,腹腔积液,大网膜、肠系膜增厚伴结节影,结合病史考虑转移(图1)。胆囊显示欠清,肝内、外胆管轻度扩张。
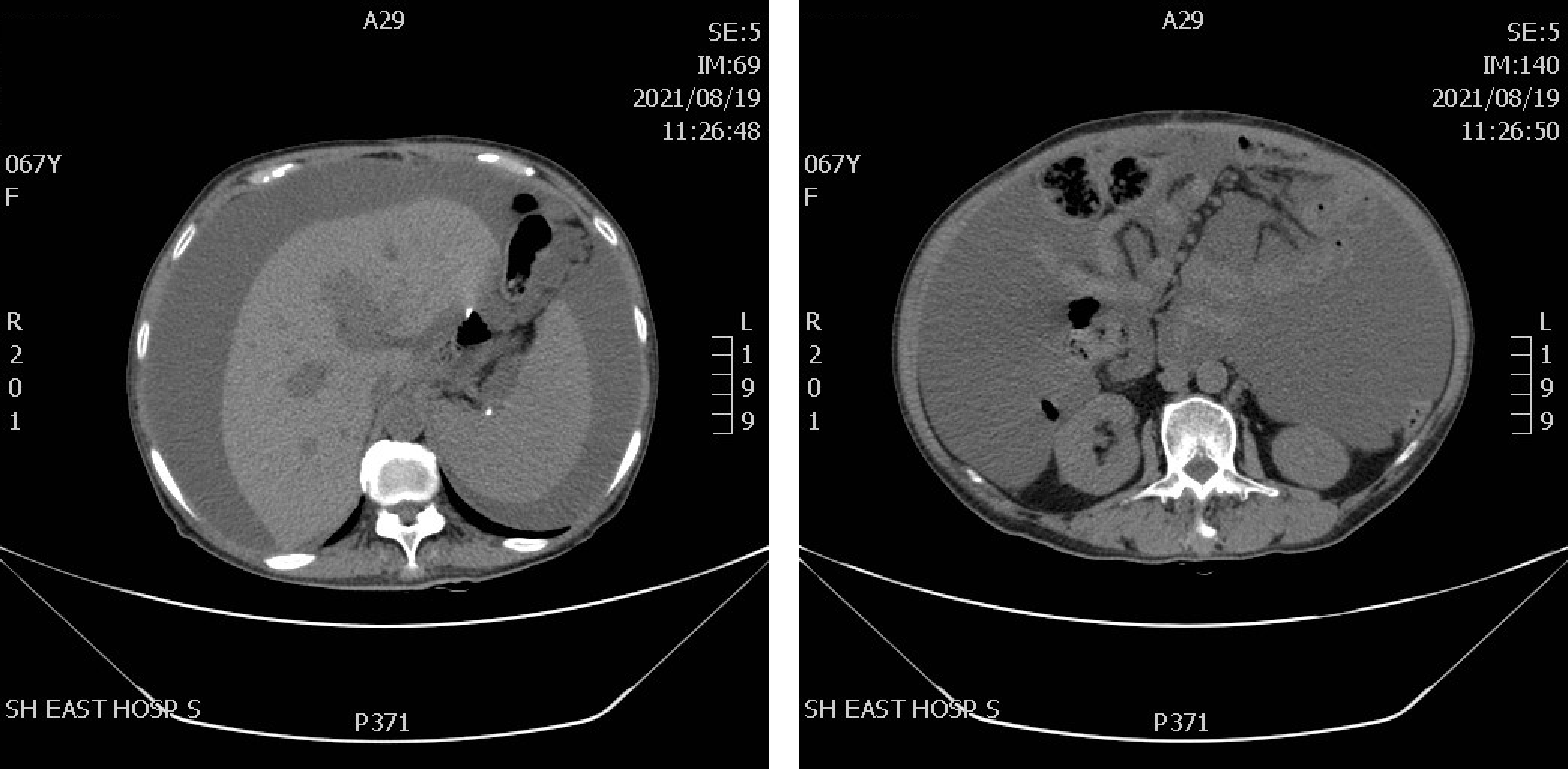
图1 2021年8月上腹部CT平扫
2021年8月23日予白蛋白结合型紫杉醇腹腔热灌注化疗3次。
2021年9月9日,腹腔热灌注化疗半个月后、系统治疗前影像学检查提示:胃术后改变,腹腔积液较前(2021年8月19日)吸收,腹膜后多发肿大淋巴结(图2)。评效:腹水控制良好。
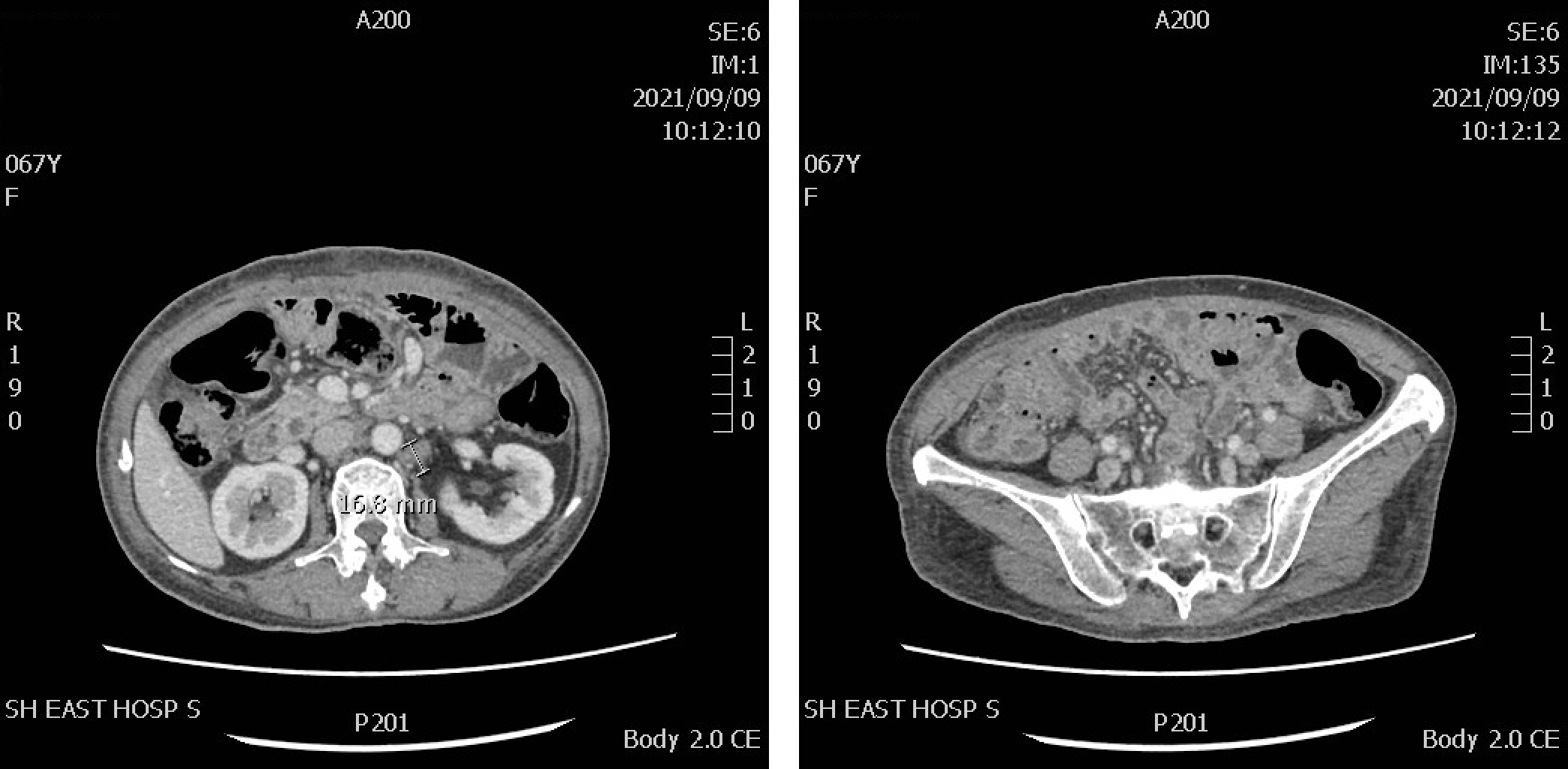
图2 2021年9月腹部CT平扫
2021年9月14日至2024年1月4日予维迪西妥单抗+信迪利单抗+阿帕替尼q2w治疗。
2021年10月27日,系统治疗后7周影像学检查提示:胃术后改变,腹腔少量积液,腹膜后多发肿大淋巴结(图3)。评效:疾病稳定(SD)。
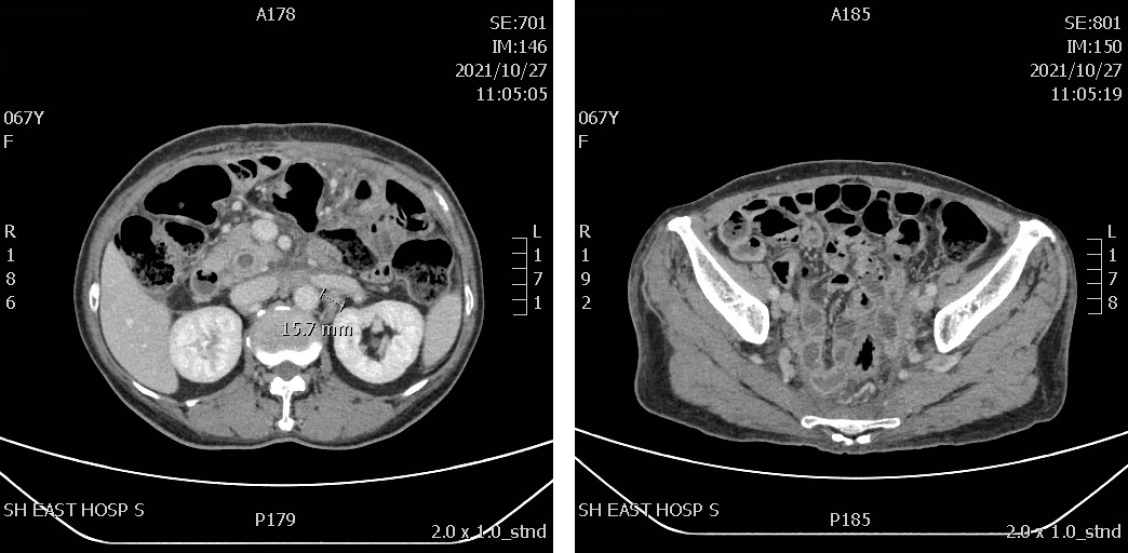
2022年1月20日,系统治疗后4+个月影像学检查提示:胃术后改变,腹腔渗出,腹膜后多发肿大淋巴结(图4)。评效:SD。
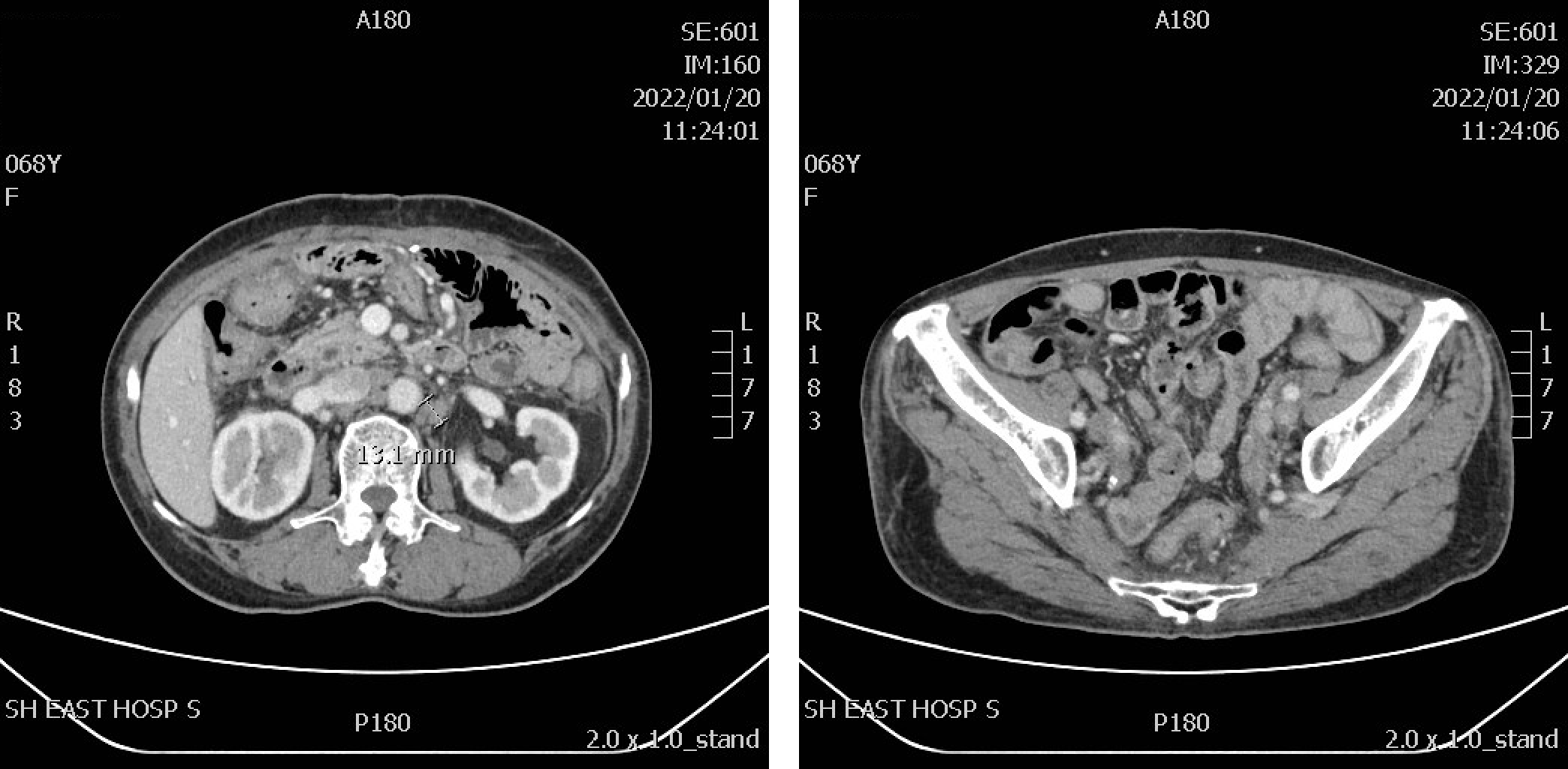
2023年11月24日,系统治疗后27个月影像学检查提示:胃术后改变,腹膜后稍大淋巴结(图5)。评效:SD+。
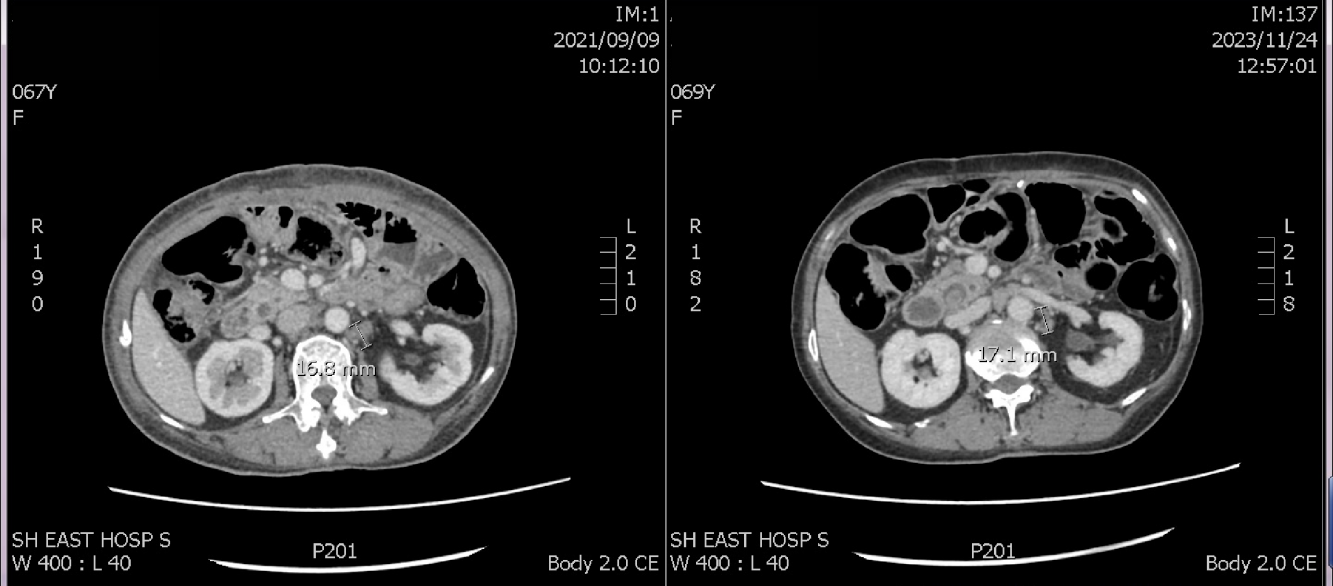
2024年1月20日,系统治疗后29个月影像学检查提示:双侧髂血管旁、腹股沟区多发肿大淋巴结,部分较前(2023年11月24日)增大。盆腔少量积液(图6)。评效:疾病进展(PD)。
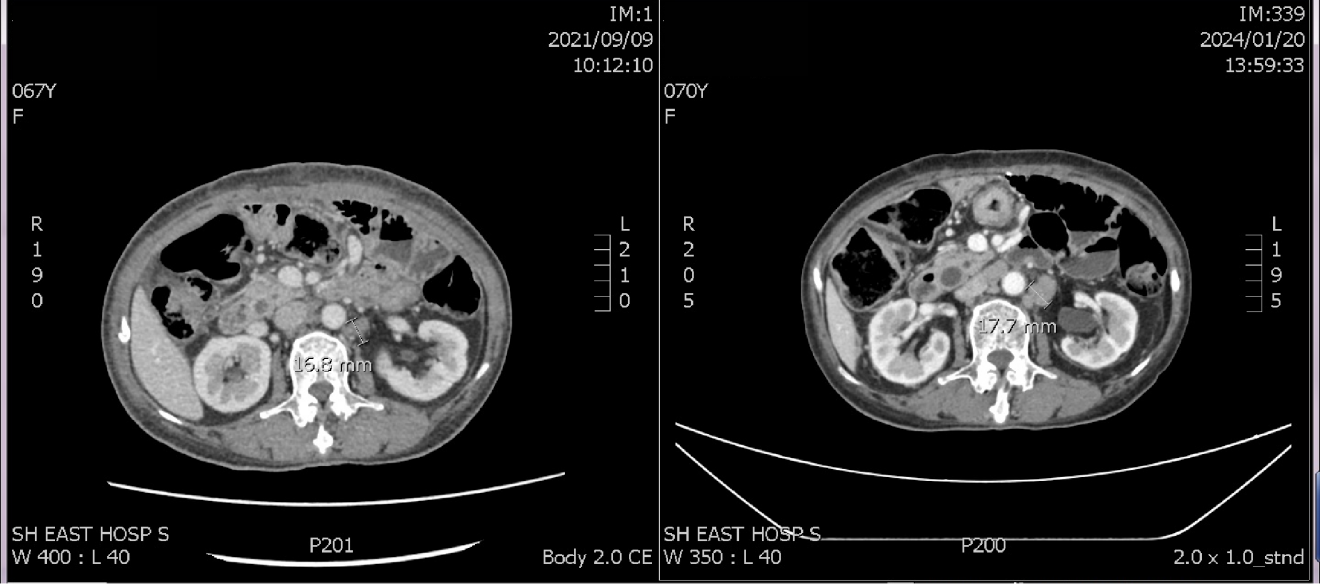
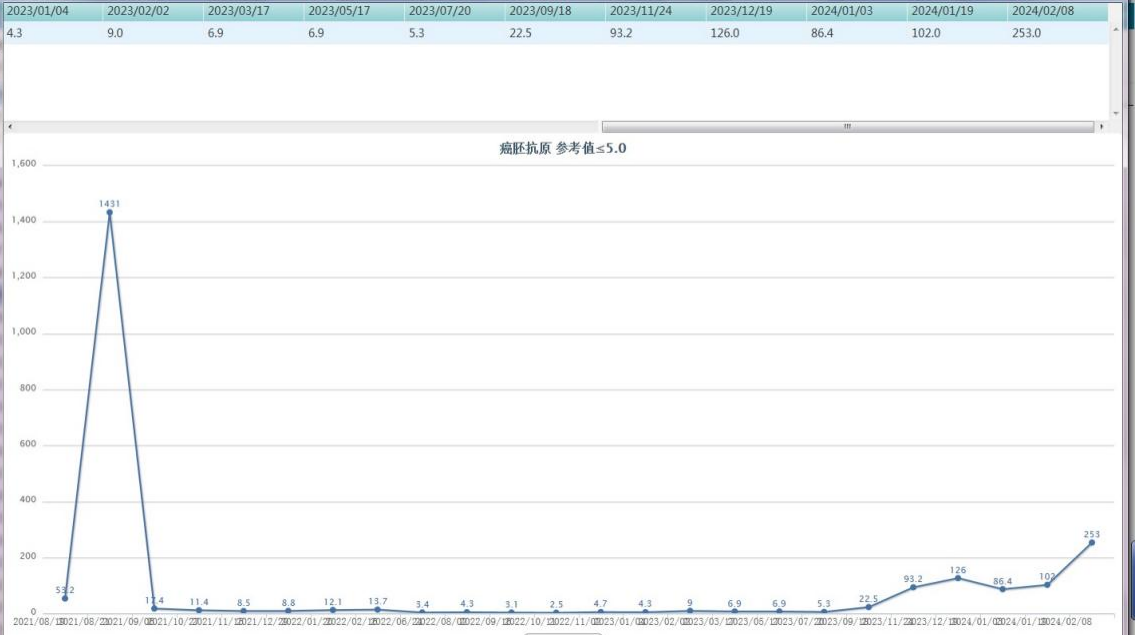
2021年8月至2024年2月患者的癌胚抗原(CEA)变化情况见图7。入院予维迪西妥单抗+信迪利单抗+阿帕替尼治疗后,CEA从1431ng/mL快速降至17.4ng/mL,并长期维持在较低水平,直至2023年12月开始上升。
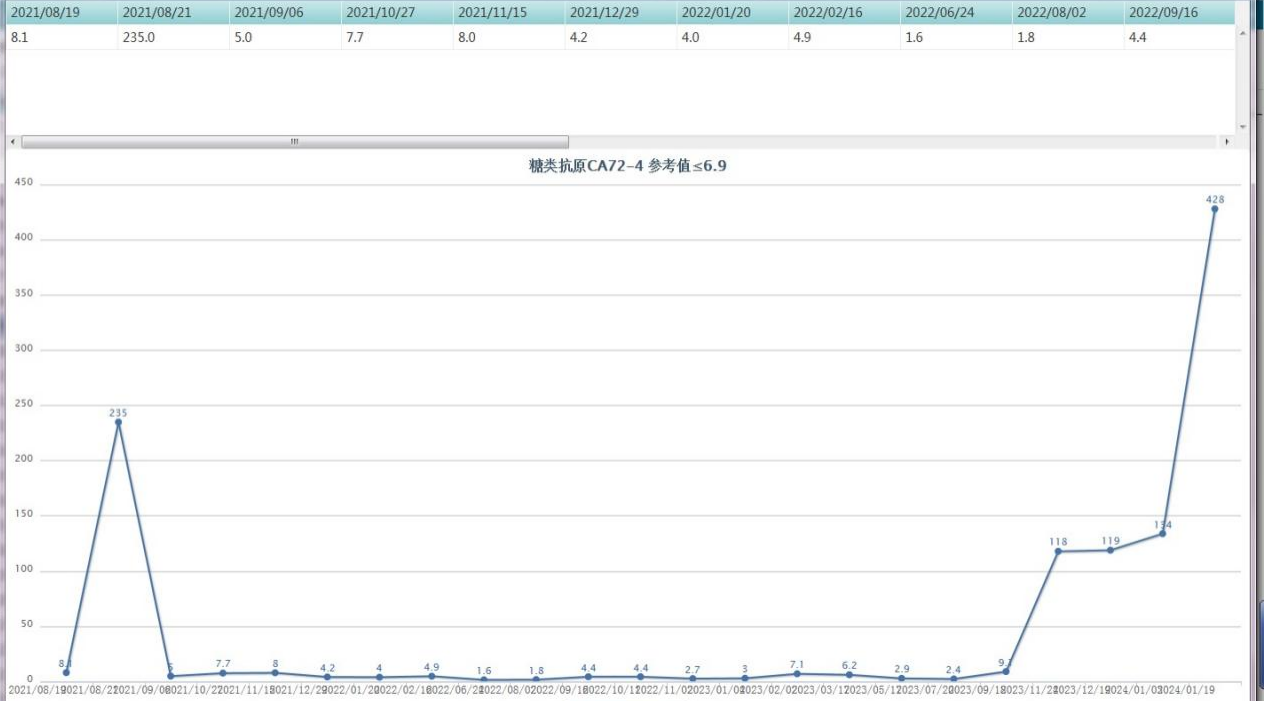
2021年8月至2024年1月患者的CA72-4变化情况见图8。入院予维迪西妥单抗+信迪利单抗+阿帕替尼治疗后,CA72-4从235U/mL快速降至5U/mL,并长期维持在正常范围,直至2023年12月开始上升。
2024年1月20日后患者的肿瘤进展,逐渐出现不全性肠梗阻、恶液质等,于2024年2月18日宣告临床死亡。
病例总结
该患者为70岁女性,因体检发现胃癌,行全胃切除术后病理确诊为HER2阳性(IHC 3+)低分化腺癌(pT4aN3aM0),术后出现腹膜转移和腹腔积液。患者先后接受了XELOX联合曲妥珠单抗、白蛋白结合型紫杉醇联合替吉奥和曲妥珠单抗、FOLFIRI联合阿帕替尼和曲妥珠单抗等多线治疗,但疗效欠佳,腹水控制不佳。后至我院就诊,予白蛋白结合型紫杉醇腹腔热灌注化疗联合维迪西妥单抗、信迪利单抗和阿帕替尼治疗。治疗后患者腹水控制良好,实现了长期疾病稳定(SD),无进展生存期(PFS)达到29个月,总生存期(OS)超过34个月。
病例点评
专家介绍
上海市东方医院肿瘤科 副主任医师
上海市女医师协会肺癌专业委员会委员
上海市抗癌协会肉瘤专业委员会委员
上海市社会医疗机构协会肿瘤学分会委员
主攻方向:胃及结直肠肿瘤的诊治及全程化管理,晚期肿瘤局部治疗、化疗、免疫治疗、靶向治疗、临床研究的优化治疗。擅长胃癌、结直肠癌、肺癌的综合治疗,肿瘤并发症及药物不良反应的处理。
参与多项国家自然基金科研项目,发表论著及SCI文章数篇
该患者70岁,HER2阳性晚期胃癌术后复发,伴有腹腔积液,经历了包括手术、化疗、靶向治疗在内的多线治疗后疾病进展,提示预后不良。患者2021年8月来我院就诊时,如何选择合适的后续治疗方案成为一个关键问题。既往治疗方案的频繁更换及疗效不佳提示需要重新评估疾病状态,同时也凸显了寻找新的有效治疗方案的迫切性。
腹水控制不佳提示需要考虑局部治疗手段,例如腹腔热灌注化疗。对于HER2阳性晚期胃癌患者,抗HER2治疗是重要的治疗策略。考虑到本例患者既往接受过曲妥珠单抗治疗,但疗效欠佳,且未接受过免疫治疗,因此最终选择了包含抗HER2 ADC药物、免疫治疗和抗血管生成靶向治疗的联合方案,即维迪西妥单抗+信迪利单抗+阿帕替尼。从治疗结果来看,腹腔热灌注化疗有效控制了腹水,后续的系统治疗使患者的肿瘤获得长期疾病控制,PFS、OS均明显延长。
15%~20%的晚期胃/胃食管结合部(G/GEJ)癌患者存在HER2过表达/扩增。在过去二十年里,曲妥珠单抗及ADC等抗HER2药物的应用已经彻底改变了HER2阳性G/GEJ癌的治疗策略。维迪西妥单抗是首个国产靶向HER2的ADC药物,因其在多中心C008研究中的优异疗效,已在国内获批用于既往接受至少二线化疗后进展的HER2阳性(IHC 3+/2+,无需FISH检测)胃癌患者并获《CSCO胃癌诊疗指南》高级别推荐[1-2]。此外,一项多中心、开放标签C013研究探索了维迪西妥单抗联合PD-1抑制剂在HER2表达晚期实体瘤二线及以上治疗中的有效性和安全性,其中胃癌队列的结果令人振奋:整体确认的ORR 43%,DCR 75%,DOR 5.1个月,mPFS 6.2个月,mOS 16.8个月[3]。这些数据为维迪西妥单抗联合治疗方案的应用提供了有力依据。本病例中,维迪西妥单抗联合PD-1抑制剂和阿帕替尼方案使患者获得了长期生存获益(PFS接近2年半,OS超过34个月),进一步证实了维迪西妥单抗联合治疗的临床价值。此外,本病例也提示,对于晚期胃癌患者,特别是HER2阳性的患者,即便既往多线治疗失败,仍有机会从新的治疗方案中获益。积极探索新的治疗策略,例如ADC药物、免疫治疗和靶向治疗的联合应用,有望为更多晚期胃癌患者带来长生存。未来,需要开展更多临床研究来探索最佳的联合治疗方案,以最大程度地提高疗效。
[1] 国家药品监督管理局药品审评中心.
[2] 2023《CSCO胃癌诊疗指南》.
[3] Yakun Wang, Jifang Gong, Airong Wang, et al. Disitamab vedotin (RC48) plus toripalimab for HER2-expressing advanced gastric or gastroesophageal junction and other solid tumours: a multicentre, open label, dose escalation and expansion phase 1 trial. EClinicalMedicine. 2024;68:102415.
排版编辑:肿瘤资讯-C Y X











 苏公网安备32059002004080号
苏公网安备32059002004080号


