在多发性骨髓瘤(MM)的治疗领域,尤其是针对复发/难治性(R/R)患者,G蛋白偶联受体C类5组成员D(GPRC5D)已成为一个备受关注的免疫治疗靶点。《【中国好声音】徐开林教授、赵恺教授团队发表综述——靶向GPRC5D用于多发性骨髓瘤治疗(上篇)》介绍了GPRC5D的生物学特性,并概述了 GPRC5D 靶向治疗的研究进程。目前,已有多种GPRC5D靶向药物正在临床前研究中,本篇我们将详细介绍这些治疗方法的最新研究进展,包括它们的临床效果和安全性评估。
GPRC5D靶向免疫疗法
GPRC5D已成为 R/R MM 患者有前途的免疫治疗靶点。目前,已经报道了两种BsAb和七种CAR-T细胞产品的安全性和有效性,而许多 GPRC5D 靶向药物正在临床前试验中研究(图1、表1)。
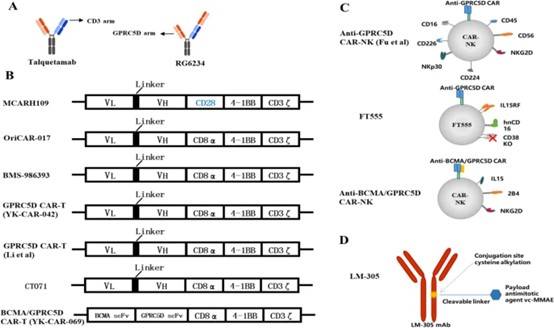
表1. GPRC5D的靶向药物的特征
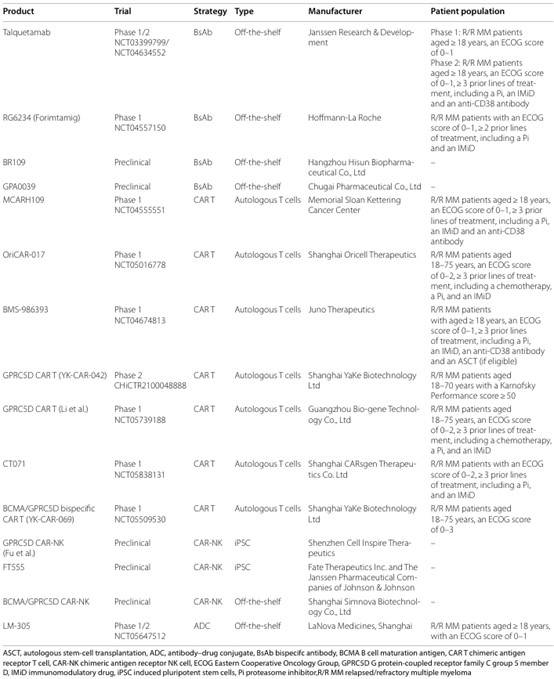
靶向GPRC5D BsAb的疗效
Talquetamab(JNJ-64407564)是一种现成的、经人源化的免疫球蛋白G4 BsAb。在MonumenTAL-1Ⅰ期试验中,显示出治疗R/R MM的显著疗效。在232例患者中,405μg皮下注射组的客观缓解率(ORR)为70%,800μg组ORR为64%,两组的完全缓解率/严格意义上的完全缓解率(CR/sCR)均为23%。该药物在三重耐药患者中疗效显著,优于塞利尼索联合地塞米松等其他推荐治疗方案。
RG6234(Forimtamig)是一种BsAb,靶向GPRC5D和CD3。Ⅰ期临床试验(NCT04557150)在108例至少接受过两种前线治疗的R/R MM患者中进行。静脉注射组的ORR为71.4%,CR为34.7%;皮下注射组的ORR为63.6%,CR为25.5%。RG6234通过皮下注射途径方便使用,克服了CAR-T细胞疗法的复杂性。
BR109和GPA0039是靶向GPRC5D的BsAb,能够通过激活T细胞介导的细胞毒性抑制GPRC5D阳性骨髓瘤细胞的生长。尽管它们在动物模型中表现出良好的抗肿瘤效应,但尚无临床安全性和有效性数据。
表2.靶向GPRC5D BsAb的临床数据
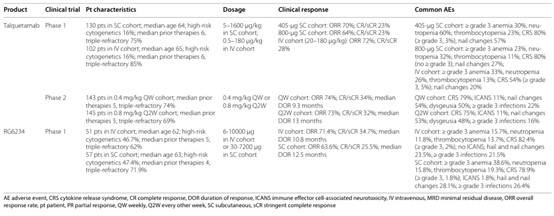
靶向GPRC5D CAR-T细胞疗法的疗效
MCARH109是一种新型CAR-T细胞疗法,针对GPRC5D抗原,用于R/R MM患者。I期临床试验中,17例患者接受了不同剂量的CAR-T细胞治疗,ORR为71%,其中35%的患者达到了CR或更好反应,中位缓解持续时间(DOR)为7.8个月。此外,47%患者实现了MRD阴性,即使在较低剂量(25 × 106)下,MCARH109依然表现出显著的疗效,尤其在抗原表达减少和髓外疾病等条件下仍具有较强的治疗活性。
OriCAR-017是一项I期临床试验,招募了10例经过大量预处理的R/R MM患者。截止至2024年1月16日,患者的ORR为100%,其中80%达到sCR,20%达到非常好的部分缓解(PR)。中位DOR为10.4个月,PFS为11.4个月,OS尚未达到。OriCAR-017的积极疗效可能归因于使用纳米抗体作为靶向分子,纳米抗体通过识别GPRC5D的两个表位,提升了CAR-T细胞的持久性、亲和力及抗肿瘤能力,且相比scFv更加稳定。
BMS-986393 I期试验共招募了70例接受过≥3种治疗的MM患者,其中34%为五重耐药性。剂量递增和扩展阶段测试了不同剂量的CAR-T细胞,疗效数据显示,患者的ORR为86%,38%达到CR/sCR,31%达到VGPR。该疗法在高危细胞遗传学和五重耐药性患者中显示出持久反应和显著疗效。
YK-CAR-042在33例R/R MM患者的II期临床试验中ORR为91%,CR/sCR为63%,79%的患者达到骨髓MRD阴性。相比其他第二代CAR-T产品,YK-CAR-042展现了更高的完全缓解率,可能与其高效转导和适当的输注剂量有关。中国临床试验中的患者既往治疗强度较低,需进一步研究不同产品的长期疗效。
GPRC5D CAR-T细胞疗法(Li等)的I期临床试验显示,在10例R/R MM患者中,GPRC5D CAR-T细胞疗法的ORR为90%。
CT071的I期临床试验在10例R/R MM患者中评估了1.0×105/kg和3.0×105/kg的CAR-T细胞剂量,ORR为90%,且所有可评估的患者达到了MRD阴性。
BCMA/GPRC5D双特异性CAR-T细胞疗法(YK-CAR-069)的I期临床试验在21例R/R MM患者中ORR为86%,且在不同剂量下表现出较高的疗效,尤其在抗原阴性患者中表现出增强的疗效。
表3. 靶向GPRC5D CAR-T细胞疗法的临床疗效
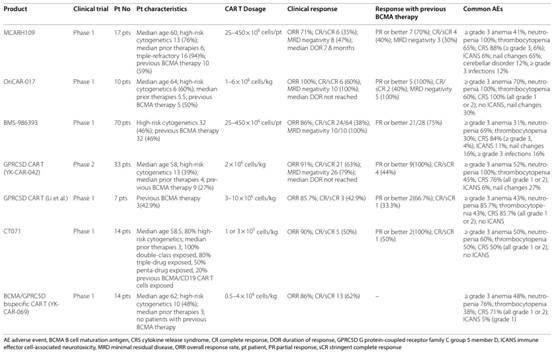
靶向GPRC5D CAR-NK细胞疗法的疗效
抗GPRC5D CAR-iNK细胞疗法,Li等开发了源自诱导性多能干细胞(iPSC)的抗GPRC5D CAR-NK细胞,显示出对高表达GPRC5D的MM细胞的强效杀伤能力,优于抗BCMA CAR-iNK细胞。
FT555是另一种iPSC衍生的抗GPRC5D CAR-NK细胞FT555,在体外和体内模型中展现出持久的抗肿瘤活性,并且与达雷木单抗联合使用可以增强抗肿瘤效果。
BCMA/GPRC5D双靶向CAR-NK细胞疗法对BCMA和GPRC5D阳性骨髓瘤细胞具有强效杀伤作用,并可有效防止BCMA抗原逃逸,增强肿瘤控制的持久性。
抗GPRC5D ADC药物的疗效
LM-305是一种新型抗GPRC5D的ADC药物,具有剂量依赖性高效抑制MM细胞生长的能力。在体外和体内模型中,LM-305展现了强效的抗肿瘤活性,尤其在GPRC5D高表达的MM细胞系中达到了CR。目前,LM-305的I/II期临床试验正在进行。
既往接受过 BCMA 靶向免疫疗法的患者的应答情况
GPRC5D × CD3 BsAb的II期临床试验中,43例患者曾接受BCMA CAR-T细胞疗法治疗,18例患者接受BCMA BsAb治疗,总体ORR为65.7%,其中接受BCMA CAR-T细胞疗法患者ORR为72.9%,接受BCMA BsAb患者ORR为52.2%。接受BCMA CAR-T细胞疗法患者中位DOR为12.3个月,显著长于BCMA BsAb治疗组的6.5个月。这表明BCMA CAR -T细胞疗法治疗后患者在抗GPRC5D BsAb治疗中有更好的缓解率和更长的DOR,可能与T细胞的不同作用机制有关。
在MCARH109治疗中,47%的患者曾接受过BCMA CAR-T细胞疗法治疗,75%患者获得PR或更好反应。OriCAR-017治疗中,所有曾接受抗BCMA CAR-T细胞疗法治疗的患者均有应答。在BMS-986393试验中,46%的患者曾接受BCMA靶向治疗,且75%有效性可评估的患者获得了PR或更好的反应,而耐药患者的ORR达85%。YK-CAR-042治疗的9例患者中,均取得了PR或更好的反应。尽管样本量较小,但当前研究表明GPRC5D治疗可能为BCMA靶向治疗后患者提供有效的替代选择,未来需要进一步研究其疗效差异。
EMD对R/R MM患者的疗效
髓外病变(EMD)是MM的一种高危表现,预后较差。尽管MM治疗有所进展,但EMD患者的疗效仍不理想。在Talquetamab的II期临床试验中,EMD患者的ORR在405 μg组为45.5%,800 μg组ORR为40%。与Teclistamab联合治疗后,ORR提高至73%,CR/sCR率为31%。此外,OriCAR-017和YK-CAR-069的I期试验中,EMD患者的ORR也分别达到了100%和75%。这些结果表明,联合针对不同骨髓瘤抗原的免疫疗法可能是改善 EMD 治疗效果的有效策略。
血液学毒性
GPRC5D靶向免疫治疗中,血液学毒性是最常见的不良事件,且可能持续数月或数年,严重时难以治疗。相比CAR-T细胞治疗,GPRC5D BsAb引起的血液学毒性较轻,恢复较快,因其不需接受淋巴细胞消耗性化疗。MonumenTAL-1试验显示,GPRC5D BsAb的3级或4级血液学毒性包括中性粒细胞减少、贫血和血小板减少,发生率较低且恢复较快。相比之下,CAR-T细胞疗法治疗前需要淋巴细胞耗竭化疗,血液学毒性更为严重。多项GPRC5D CAR-T细胞试验显示,中性粒细胞减少、贫血和血小板减少为主要毒性反应。双靶点CAR-T细胞未表现出比单靶点CAR-T更高的血液学毒性,提示双靶策略可能更安全有效。
CRS、ICANS
在Talquetamab治疗中,细胞因子释放综合征(CRS)是常见的非血液学不良事件,皮下注射较静脉注射更温和,神经毒性事件多为轻度且可控。GPRC5D CAR-T细胞疗法的CRS发生率较高,但多数为轻度,免疫效应细胞相关神经毒性综合征(ICANS)的发生率低且严重程度有限。GPRC5D BsAb治疗相比CAR-T细胞治疗,CRS相似,但ICANS发生率和严重程度较高,需要更多多中心研究验证。
靶向、非肿瘤毒性
GPRC5D×CD3 BsAb的靶向毒性:在talquetamab的临床试验中,常见的靶向肿瘤外毒性包括指甲、皮肤和味觉变化,主要为1/2级,大多可控。味觉障碍的原因尚有争议,但可能与GPRC5D及其相关的受体家族有关。
GPRC5D CAR-T细胞疗法的靶向毒性:MCARH109和其他GPRC5D CAR-T细胞疗法治疗引发了指甲、皮肤变化及少数小脑毒性,频率和严重程度相对较低。与BsAb相比,CAR-T疗法的毒性类型和程度存在差异。
靶向毒性的种族差异与小脑毒性:GPRC5D相关靶向毒性在欧美患者中更常见,种族差异尚待研究。此外,小脑毒性目前只在CAR-T细胞疗法中发现,BsAb治疗未见报道,需进一步调查其发生机制。
感染和低丙种球蛋白血症
T细胞重定向免疫疗法后,感染是常见并发症,而严重的B细胞消失和低免疫球蛋白血症会加重感染风险。在talquetamab治疗中,GPRC5D×CD3 BsAb未显著降低CD19 B细胞水平,约20%的患者出现了3/4级感染,且低免疫球蛋白血症在治疗前已普遍存在。与靶向BCMA BsAb相比,GPRC5D×CD3 BsAb的感染发生率较低,这可能是由于其在免疫系统中的表达相对有限。GPRC5D CAR-T细胞疗法的感染率与BsAb相近,但目前的数据不足,尚无法有效比较其与其他CAR-T细胞疗法的感染情况。
剂量限制性毒性和致命性AE
在MonumenTAL-1试验中,talquetamab治疗观察到4例剂量限制性毒性(DLT)和3例致命不良事件(AE),研究人员认为这些死亡与治疗无关。MCARH109治疗中有60%的患者出现DLT,未报告致命性AE。其他药物如OriCAR-017和BMS-986393的试验中也未发现致命性AE。YK-CAR-042患者中观察到2例剂量限制性毒性,1例患者因颅内出血死亡,但与治疗无关。总体来看,靶向GPRC5D BsAb和CAR-T细胞疗法均可出现DLT,但大多数为可逆且非致命的,且低于最大耐受剂量的患者未见致命性AE。
展望
BCMA是R/R MM的理想靶点,相关免疫疗法已显示出显著疗效,但复发和BCMA表达降低仍是治疗失败的常见原因。GPRC5D作为另一有效靶点,其靶向疗法同样在R/R MM患者中展现出良好反应。虽然GPRC5D CAR-T细胞疗法的疗效与毒性与BCMA CAR-T细胞疗法相当,但缺乏直接比较试验,未来需要通过随机对照试验探索两者的优先使用顺序。
展望未来,GPRC5D靶向免疫疗法在早期治疗中可能尤为有效,但部分患者因合并症或治疗毒性而失去治疗机会。因此,研究GPRC5D在抗BCMA治疗后的长期疗效至关重要。同时,组合不同靶点的免疫疗法可能有助于克服耐药机制,提高抗肿瘤效果。开发靶向双重或多重抗原的T细胞重定向疗法,将为MM的治疗带来新的希望和突破。
Zhou D, Wang Y, Chen C, Li Z, Xu K, Zhao K. Targeting GPRC5D for multiple myeloma therapy. J Hematol Oncol. 2024;17(1):88. Published 2024 Sep 28.
排版编辑:肿瘤资讯-Kaylee











 苏公网安备32059002004080号
苏公网安备32059002004080号


