虽然部分胆道癌患者可手术切除,但多数会复发。针对晚期 BTC 患者,现有标准方案的中位 OS 为 1 年,亟需研究其他多种治疗方案,这需要对肿瘤基因组学有深入的了解。现有的下一代测序技术虽然增进了我们对多癌种基因变异的认识,但仍存在一些局限性。有研究表明,游离 DNA 检测可获得肿瘤基因变异信息。一项发表在 Annals of Oncology 上面的研究分析了 cfDNA 检测用于分析晚期 BTC 基因变异情况的效果[1]。【肿瘤资讯】整理如下,以飨读者。
研究背景
胆道癌(BTC)包括肝内胆管癌、肝外胆管癌和胆囊癌。虽然手术可切除局部病变,但大多数患者会复发。针对不可切除或转移性 BTC 患者,吉西他滨+顺铂+PD-1/PD-L1 成为标准一线治疗,但其中位 OS 为 1年。迫切需要研究其他多种治疗方案[2-3]。
大规模基因组分析工作已经为 BTC 患者带来了治疗机会,它可识别出多种变异包括 FGFR2、IDH1、 BRAF、NTRK、RET 和 ERBB2(HER2)。随着这些靶标的出现,精准治疗也有所发展。FDA 首次批准用于胆管癌的是选择性 FGFR2 抑制剂 pemigatinib 和 infigratinib,用于晚期难治性 FGFR2 融合或重排阳性胆管癌。IDH1 抑制剂 ivosidenib 随后被批准用于治疗 IDH1 突变型胆管癌。NCCN 还建议针对 BRAF V600E 突变、NTRK 融合、RET 融合或 HER2 阳性的患者进行靶向治疗。免疫检查点抑制剂获得 FDA 批准用于 MSI-H、错配修复缺陷或高肿瘤突变负担的患者[4-6]。
下一代测序(NGS)增进了我们对许多癌种基因变异的认识。然而这种方法有局限性。例如转移性组织的活检通常没有足够的肿瘤细胞用于测序,导致检测失败率高。
游离 DNA (cfDNA)分析是一种有吸引力的方法,其用于癌症基因组分析可以克服许多问题。(i)当无法获得组织或组织不足时,cfDNA 可以提供基因组信息;(ii)肿瘤 DNA 从多个病变部位脱落进入血液,因此可能更好捕获患者内部肿瘤异质性。(iii)一系列 cfDNA 分析可以促进对肿瘤进化和耐药的研究。(iv)cfDNA还可以提供预测和预后信息。
在本报告中,我们分析了 1671 例晚期 BTC 患者的 2068 份cfDNA 样本。我们评估了使用cfDNA 检测变异的可行性,还提供了对 BTC 肿瘤生物学的见解。
研究方法
在 2015 年 10 月 1 日至 2019 年 1 月 28 日期间,收集 1671 例晚期 BTC 患者的 cfDNA 样本,使用
Guardant360 cfDNA NGS 进行分析。
研究结果
cfDNA 检测结果和临床变异的发生率
队列的中位年龄为 65 岁,52%的患者为女性,91%的患者患有胆管癌,而 9%的患者患有胆囊癌(图 1A 和 B)。我们首先确定了 20 个最常变异的基因——非同义单核苷酸变异(SNV)、插入缺失、扩增和融合的发生率。如果在单个基因中检测到多个变异,这种情况将报告为单个变异,其中 SNV 优先于其他基因变异(图 1C)。与之前通过 NGS 对组织样本进行的分析一致,TP53 和 KRAS 是最常变异的基因。
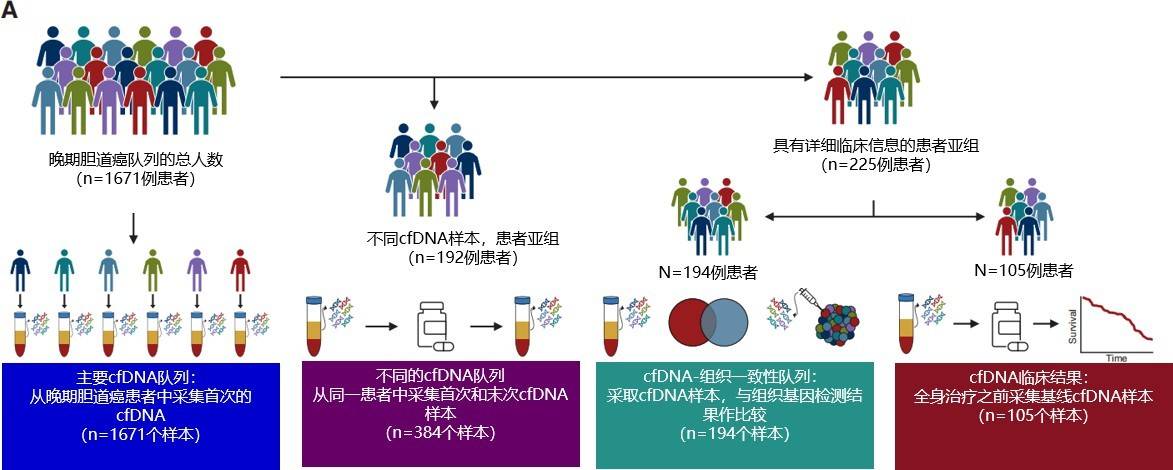
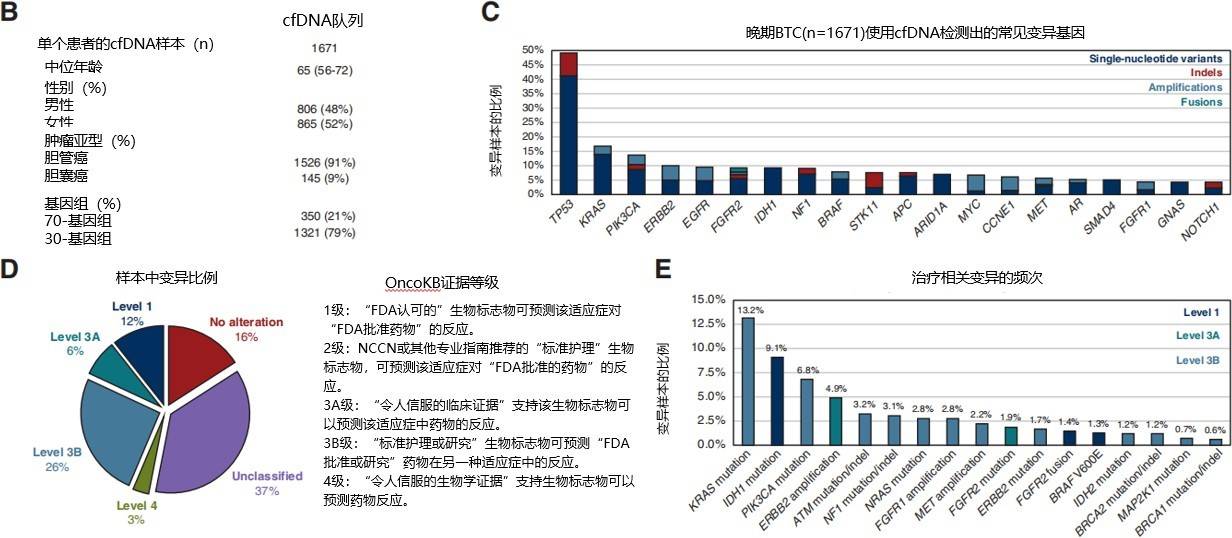
图 1 1671 例晚期 BTC 患者使用 cfDNA 检测分析临床基因变异的概况
84%患者的 cfDNA 中检测到基因变异,其中 44%的患者检测到靶向变异。IDH1 突变、FGFR2 融合、 BRAF V600E 突变、NTRK 融合、RET 融合的发生率分别为 9.1%、1.4%、1.3%、0.1%、0.1%。ERBB2 扩增、PIK3CA 突变、KRAS G12D、KRAS G12C 的发生率分别为 4.9%、6.8%、5.1%、1.0%。
cfDNA 和组织基因组分析之间的一致性
cfDNA 的检测结果与AACR 项目GENIE 数据库的样本结果显示很强的正相关性(R2=0.96;P< 0.001)。 cfDNA 和组织检测出变异率之间存在明显的相似点和差异点(图 2B)。IDH1 突变(cfDNA 和组织中分别为 9.3%、9.5%;P= 0.92)、ERBB2 扩增(4.9% vs. 5.6%;P=0.66)和 BRAF V600E 突变(1.3% vs. 2.3% P=0.14)
的发生率相似。然而,在 cfDNA 样本中检测到 FGFR2 融合的频率较低(1.4% vs. 4.3% P=0.0018)。在 cfDNA 样本中检测到 FGFR2 突变的频率较高(5.3% vs. 2.0% P=0.0077)。最常见的两种突变基因 TP53和 KRAS 在 cfDNA 和组织样本检测中的发生率相似(图 2C)。
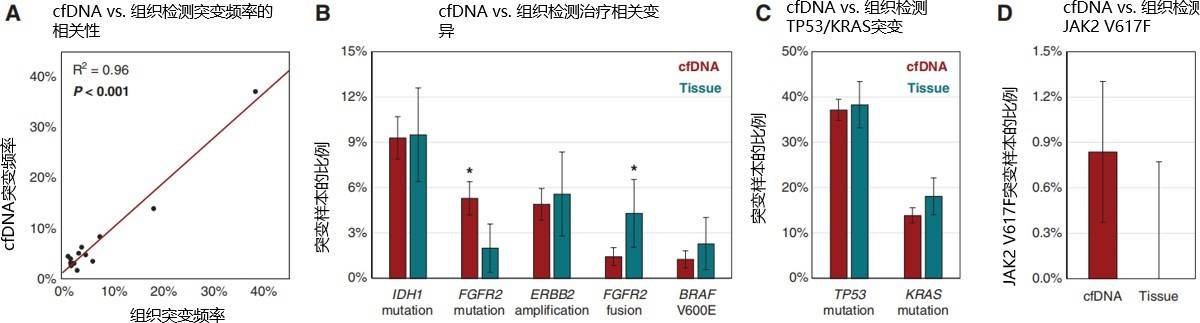
图 2 cfDNA 检测和组织检测之间的相关性
在组织中检测到 IDH1 突变的患者中,87% (41/47) 的患者也在 cfDNA 中检测到这些突变。cfDNA队列中的大多数 IDH1 突变是 R132C。
讨论
我们分析了 1671 例晚期 BTC 患者的 2068 个血浆样本的基因组结果。多项研究结果对于晚期 BTC 患者的治疗具有临床意义。cfDNA 分析与组织分析相比,对临床变异检测的发生率相似;(ii) 检测到大多数 IDH1 突变、BRAF V600E 突变和 FGFR2 胞外域突变,但 FGFR2 融合的检测效果不佳;(iii) 揭示了 BTC常见变异 IDH1 突变、BRAF V600E 突变和 FGFR2 融合具有高度克隆性,提示这些是 BTC 患者早期的驱动事件;(iv)揭示肿瘤活检未检测到的靶向治疗耐药的新机制;(v)提供预后和预测数据以整合到临床决策中。
非同义 SNVs 的 cfDNA 和组织基因组分析之间的相关性非常好(R2=0.96),与结直肠癌中的发现结果一致(R2=0.95)。针对 IDH1 突变和 BRAF V600E 突变这两种 SNV,BTC 患者已有标准治疗方案,令人欣慰的是在本研究中看到 cfDNA 结果与组织分析具有高度一致性。然而,当对治疗期间或疾病稳定期间收集的样本进行分析时,cfDNA 分析的敏感性显著下降。总体而言,这些数据强烈支持晚期BTC 患者使用cfDNA检测 IDH1 突变和 BRAF V600E 突变。
结论
总之,我们的研究结果强烈支持 cfDNA 基因组分析的实用性,为晚期 BTC 患者的临床治疗提供医学支持。随着靶向治疗进入一线和新辅助临床试验,cfDNA 分析将成为促进患者及时入组的重要工具。与此同时,临床医生应认识到 cfDNA 在检测FGFR2 融合方面的局限性,并考虑将肿瘤活检作为一种补充方法。总的来说,这项研究的结果支持了 cfDNA 分析在当前临床实践中的作用,并强调了将 cfDNA 纳入临床试验的重要性,以进一步确定其作为 BTC 患者预测和预后生物标志物的效用。
[1] Berchuck JE, Facchinetti F, DiToro DF, et al. The lcinical landscape of cell-free DNA alterations in 1671 patients with advanced biliary tract cancer. Annals of Oncology. 2022;33(12):1269-1283.
[2] Okusaka T, Nakachi K, Fukutomi A, et al. Gemcitabine alone or in combination with cisplatin in patients with biliary tract cancer: a comparative multicentre study in Japan. Br J Cancer. 2010;103:469-474.
[3] Oh D-Y, Ruth HA, Qin S, et al. Durvalumab plus gemcitabine and cisplatin in advanced biliary tract cancer. NEJM Evid. 2022;1.
[4] Abou-Alfa GK, Sahai V, Hollebecque A, et al. Pemigatinib for previously treated, locally advanced or metastatic cholangiocarcinoma: a multicentre, open-label, phase 2 study. Lancet Oncol. 2020;21:671-684.
[5] Abou-Alfa GK, Macarulla T, Javle MM, et al. Ivosidenib in IDH1-mutant, chemotherapy-refractory cholangiocarcinoma (ClarIDHy): a multicentre, randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol. 2020;21:796-807.
[6] Zhu AX, Macarulla T, Javle MM, et al. Final overall survival efficacy results of ivosidenib for patients with advanced cholangiocarcinoma with IDH1 mutation: the phase 3 randomized clinical ClarIDHy trial. JAMA Oncol. 2021;7:1669-1677.
声明:材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批编码:CN-139116
有效期至:2025/7/14
排版编辑:肿瘤资讯-REX











 苏公网安备32059002004080号
苏公网安备32059002004080号


