经动脉化疗栓塞(TACE)治疗是中晚期肝癌标准的治疗手段。在肿瘤多治疗手段并存的时代背景下,TACE与免疫治疗、抗血管生成治疗又能擦出哪些火花,未来还有哪些方向可予进一步探索?【肿瘤资讯】特邀浙江大学附属第一医院方维佳教授分享在今年美国临床肿瘤学会(ASCO)消化道肿瘤(GI)大会上所公布的EMERALD-1研究的最新进展。
专家简介
国家卫健委能力建设及继教肿瘤专委会委员
中国临床肿瘤学会理事
中国临床肿瘤学会胆道肿瘤专委会常委
中国临床肿瘤学会放射介入专委会常委
中国医师协会肿瘤医师分会 委员
中国医师协会多学科综合治疗专委会委员
中国转化/精准医学学会细胞治疗分会委员
浙江省可持续发展研究会医疗专委会委员
浙江省抗癌协会整合肿瘤专委会 副主委
香港大学 访问学者
美国印第安纳大学 访问学者
精彩视频
充满异质性:EMERALD-1研究设计
当前,临床上TACE联合抗血管生成治疗以及程序性死亡受体-1/-L1(PD-1/PD-L1)单抗的治疗方案已经开展应用,但是,既往并无Ⅲ期临床研究证实该治疗方案的有效性。在今年的ASCO GI大会上,Ⅲ期、随机、安慰剂对照的EMERALD-1研究1给予了非常好的答案。
EMERALD-1研究探索的是TACE联合度伐利尤单抗联合或不联合贝伐珠单抗治疗不可切除肝细胞癌患者的有效性和安全性。值得关注的是,在不同的国家和地区,肝细胞癌分期具有异质性,治疗手段同样具有异质性。与此同时,由于TACE不单用于晚期肿瘤,故需要明确哪些为不可切除性肿瘤。当然,不论是2019年西安国际医学中心医院韩国宏教授基于主导的Six-and-twelve评分模型的研究2,还是2021年中国台湾Yi-Hsiang Huang教授主导的基于Seven-Eleven标准的研究3,都是从不同角度将肿瘤的最大直径与数目进行了叠加。EMERALD-1研究对于Yi-Hsiang Huang教授的研究进行了采纳,并特别强调了中期的患者中还包括了10%的BCLC C期的患者。前面所述的研究,均是针对中期肝癌患者的研究。通常而言,中期肿瘤病灶数较多,但未侵犯血管、未发生肝外转移。按照分期,BCLC C既可以是发生了肝外转移,亦可以是出现了更多血管侵犯的肝癌患者。在EMERALD-1研究中,BCLC C分期的患者定义为没有肝外转移的患者,排除了Vp3和Vp4(图1)。从该角度而言,相比既往研究的中期肝癌患者,本研究中的中期肝癌患者的成分更加复杂。方教授指出,面对如此复杂的情况,Ⅲ期临床研究一定进行了非常好的质控,因此其研究结果值得期待与关注。 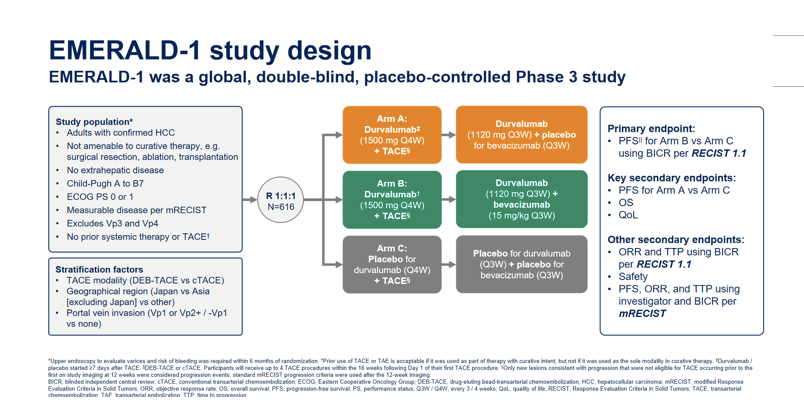
图1: EMERALD-1研究设计
此外,从研究设计可知,研究者亦非常纠结,不知道该进行多少次TACE之后,再予用药,因此,采取的是1~4次。与此同时,大家需要注意的是,该研究在进行TACE治疗时,就已经加入了度伐利尤单抗,而在后续治疗时,又划分为了度伐利尤单抗+安慰剂、度伐利尤单抗+贝伐珠单抗以及安慰剂联合治疗的情况。因此,在该研究中充满了异质性。
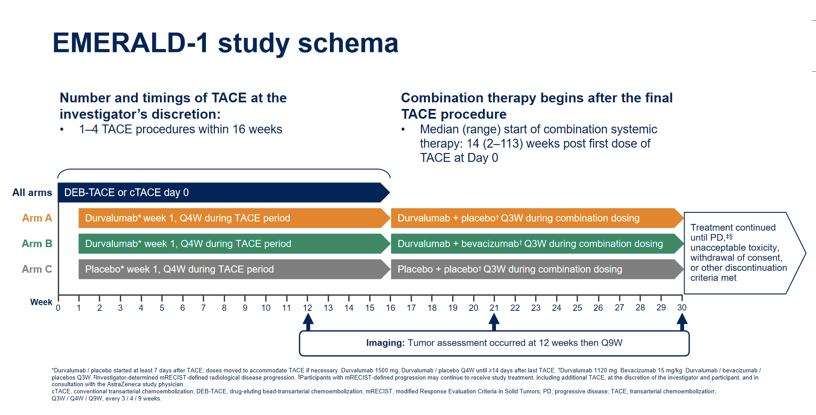
图2: EMERALD-1研究流程
大家可能会非常疑惑,为何要在TACE的基础上联合免疫和抗血管生成治疗?这主要是因为基于研究者的假设,TACE联合免疫及抗血管生成治疗能够促进肿瘤释放新抗原。当然,在近年来的研究中发现,这样操作所释放的新抗原中,有效性抗原并不多。部分抗原不能被”生信“(生物信息学)所验证,更妄论被动物实验和体内外实验所验证。
当然,抗血管生成治疗的作用也存争议。在研究设计中可知,抗血管生成治疗的应用预设了最佳治疗时机,然而,迄今为止大家并不知道最佳治疗时机是何时。未来可能会有生物标志物的研究帮助研究者探索最佳治疗时间。
入组患者并非易治患者:EMERALD-1研究基线情况
截至目前,EMERALD-1研究结果非常惊艳,符合大家既往的观点。该研究严谨的临床研究设计,也使其成为了具备里程碑意义的临床研究。绝大多数患者都进行了不足两次的TACE治疗,而且,进行两次和三次TACE治疗的患者比例相近。因此,可见TACE的治疗次数具备一定的灵活度。最终究竟需要进行多少次TACE治疗,需要与介入科医生进行讨论。当然,本研究中还存在着诸多的未知领域。在患者的依从性方面,三种治疗方式中断治疗的患者比例亦相近(图3)。
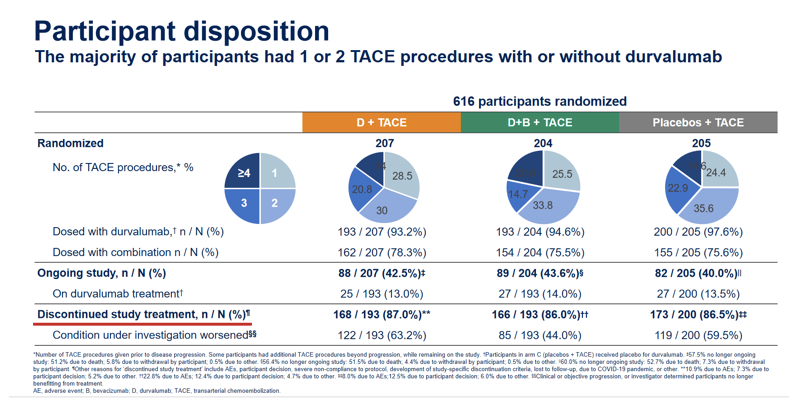
图3: EMERALD-1研究患者的随机分组和依从性情况
方维佳教授指出,EMERALD-1研究中非肿瘤进展导致的死亡较多;可能是由于副反应的关系,但仅为猜想,尚需进一步的验证。在基线图中还可以看到TACE的治疗模式,以cTACE为主。HBV的感染率将近40%左右,表明该数据可以代表中国人群。此外,BCLC C期的人群占比为15%左右。由于EMERALD-1研究在进行患者入组时,对于患者肝功能的评价非常谨慎,纳入了Child-Pugh评分、白蛋白-胆红素(ALBI)、肝癌动脉栓塞预后(HAP)评分,使得EMERALD-1研究中的患者能够非常好的耐受TACE及相应药物的治疗。当然,肿瘤负荷亦是值得关注的指标,中位数值是7及以下,表明EMERALD-1研究中的患者并非易于治疗的患者(图4)。因此,能够取得令人惊艳的研究结果非常不容易。
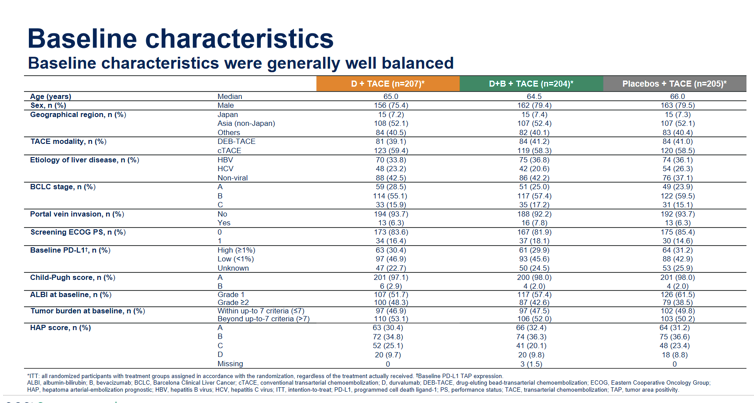 图4: EMERALD-1研究患者的基线情况
图4: EMERALD-1研究患者的基线情况
令人惊艳:EMERALD-1研究结果
首先来看无进展生存期(PFS):D+B+TACE相当于将所有能用的治疗都已用上,只是这里并未使用tremelimumab。结合以中山肿瘤防治中心为代表的临床研究理念,对于此类无肝外转移的肝癌治疗,不论是晚期患者,还是接受了转化治疗,采取多治疗手段联合,可能会产生多种治疗结果,但并非每个治疗方案都能通过Ⅲ期研究加以验证。D+B+ TACE最终取得了15.0个月的中位PFS时间。虽然既往有一项PD-1单抗+化疗+抗血管生成治疗Ⅱ期研究取得了17个月的中位PFS时间,但是,对于不可切除肝癌而言,15个月的中位PFS已实属不易。虽然,目前OS尚未成熟,但是,PFS的延长势必会延长相应的OS时间。在生存曲线图中可以看到这样的趋势(图5)。
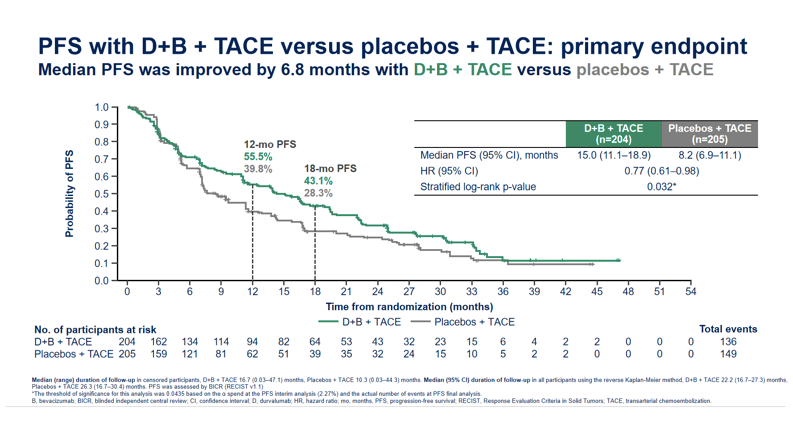
图5: EMERALD-1研究D+B+TACE与安慰剂+TACE的中位PFS结果
亚组结果分析显示,各亚组获益趋势一致,并无显著的差异。然而,稍加分析,例如将肿瘤负荷进行>7和<7的划分,可以发现这将对患者的生存造成很大的影响。说明D+B+TACE的治疗方式,可以改善此类患者的预后,不论去掉任何一个均不行(图6)。
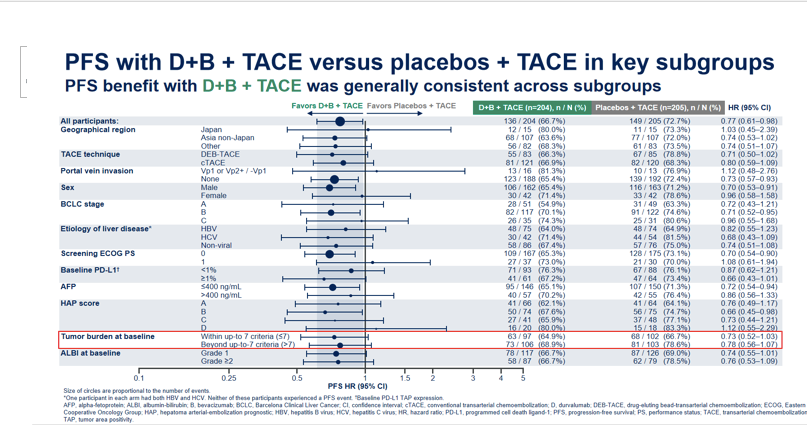
图6: EMERALD-1研究亚组分析结果
虽然D+TACE与安慰剂+TACE相比,在中位PFS的比较上并无显著的统计学差异,但是可以看到数据的显著延长(图7),说明D+TACE相比安慰剂+TACE能够更好的控制肿瘤,进而尽可能避免和减少肿瘤进展。
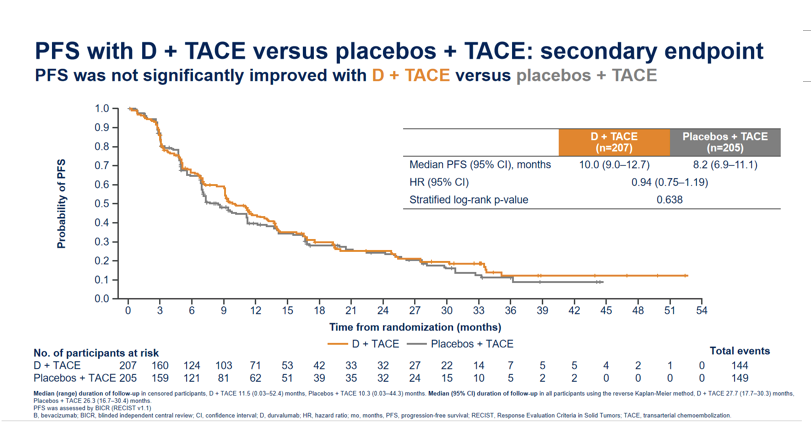
图5: EMERALD-1研究D+TACE与安慰剂+TACE的中位PFS结果
目前尚不可知PFS和疾病进展(TTP)时间的差异。虽然,PFS是判断疗效的一个金标准,但是,如果TTP结果令人惊艳(图6),是否值得进一步挖掘?这一点有待深入思考。
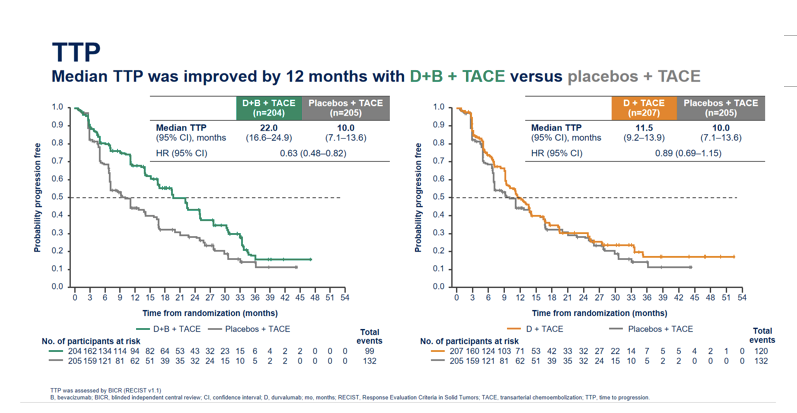
图6: EMERALD-1研究D+B+TACE与安慰剂+TACE的中位TTP结果
众所周知,此类肝癌患者的治疗,如同结直肠癌患者一样,如果不予放疗,则客观缓解率(ORR)提升较为有限(图7)。然而,诸如PD-1单抗、贝伐珠单抗、酪氨酸激酶抑制剂(TKI)一类内科治疗,可以给患者带来长期生存或者减少远处转移的获益。与此同时,接受这些内科治疗的患者依从性高,自然获益时间相对亦长。
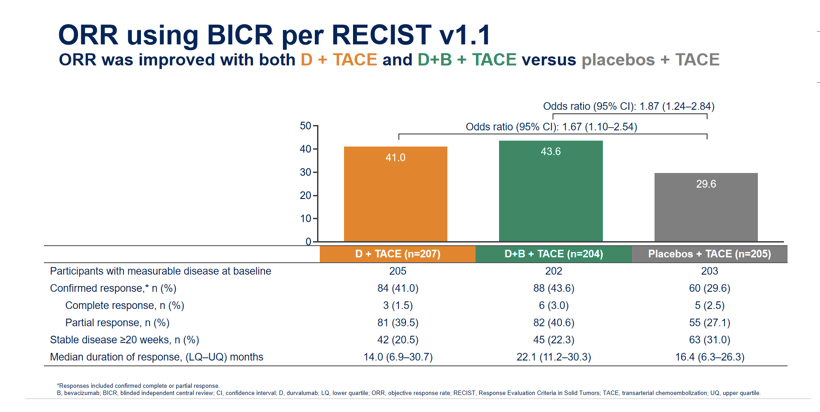
图7: EMERALD-1研究D+B+TACE与安慰剂+TACE的ORR结果
D+B+TACE:安全性可耐受
在安全性方面,截至目前未观察到新的不良事件的出现。当前,中国医生的TACE操作水平已非常高。虽然,在操作过程中可能亦会存在已定的异质性,但是,在临床研究的背景下,暂不进行过多考虑。EMERALD-1研究中,所出现的不良反应皆在可控范围之内,不过,的确D+B+TACE的不良反应所致治疗中断的患者比例更高。这是否会给非肿瘤进展所致死亡带来影响尚不清楚,关于这一点,期待后续的深度分析和报道。对于大家都关心的3~4级不良反应中,D+B+TACE组出现高血压的比例较高,其他组的高血压比例并不高(图8)。这表明药物需要充分暴露,只有充分暴露才能产生良好的治疗效果。
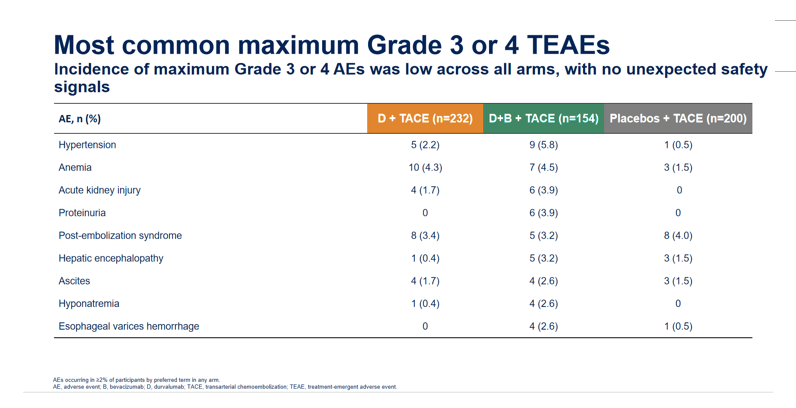
图8: EMERALD-1研究中最常见的3~4级不良反应
未来可期:TACE联合全身治疗前景
TACE作为一种成熟的治疗手段,现在已发展至联合治疗阶段。在晚期肝癌的治疗中,已将TACE与PD-1/PD-L1单抗+贝伐珠单抗以及TKI进行联合。当然,对于BCLC C分期的肝癌患者,既往不乏非常具有标志性的临床研究。这些研究将在BCLC C分期肝癌的治疗中发挥着承前启后的作用。不论如何,EMERALD-1研究是一个非常令人惊艳的研究,在毒副反应可控的情况下,不论PFS、TTP都有非常令人惊艳的结果。
在该背景之下,方教授认为,未来或许可以进行生物标志物的分析以及免疫特质的分析,或可帮助研究能够从这种治疗方案中获益的肿瘤患者。此外,或许还可以在辅助治疗,乃至新辅助治疗中进行探索,以期能够让更多肝癌患者从这种治疗中获益。
1. Lencioni, R. et al. EMERALD-1: A phase 3, randomized, placebo-controlled study of transarterial chemoembolization combined with durvalumab with or without bevacizumab in participants with unresectable hepatocellular carcinoma eligible for embolization. JCO 42, LBA432–LBA432 (2024).
2. Wang, Q. et al. Development of a prognostic score for recommended TACE candidates with hepatocellular carcinoma: A multicentre observational study. J Hepatol 70, 893–903 (2019).
3. Hung, Y.-W. et al. Redefining Tumor Burden in Patients with Intermediate-Stage Hepatocellular Carcinoma: The Seven-Eleven Criteria. Liver Cancer 10, 629–640 (2021).
排版编辑:肿瘤资讯-胡一帆











 苏公网安备32059002004080号
苏公网安备32059002004080号


