审校:范磊
单位:江苏省人民医院
2020年新型冠状病毒肺炎的疫情全球肆虐,但疫情并未阻挡学术的进步与分享。6月11-14日,第25届欧洲血液学协会(EHA)年会在众多期待中将与今年ASCO一样采取线上虚拟网络会的模式举行。当地时间5月14日15:00,大会摘要公布。【肿瘤资讯】特邀江苏省人民医院范磊教授针对BCL-2抑制剂相关方案在慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)中的应用进展进行了筛选与点评,详情如下。

江苏省人民医院血液科 科室副主任
医学博士、主任医师、副教授
中国抗癌协会第一届青年常务理事
中国抗癌协会血液肿瘤专业委员会委员
中华医学会血液分会第十一届青年委员
江苏省医学会血液分会青委副主委
美国纽约哥伦比亚和康奈尔大学附属纽约长老会医院博士后
研究方向为淋巴肿瘤的精确诊疗

苏北人民医院
内科学(血液病学) 住院医师
毕业于南京医科大学第一临床医学院
导师:范磊 教授
【Abstract S158】一线IBRUTINIB(Ibr)+ VENETOCLAX(Ven)治疗慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者:来自CAPTIVATE MRD队列研究的有效性和安全性结果
背景
Ibrutinib(Ibr)是唯一每日给药一次的布鲁顿酪氨酸激酶(BTK)抑制剂,并在一线CLL的两项随机3期研究中(RESONATE-2、ECOG1912)显示出显著的总体生存(OS)获益。当联用Ibr + Venetoclax(Ven,口服BCL-2抑制剂)时可能具有协同的抗肿瘤活性,通过从外周血(PB)和骨髓(BM)以外的保护性部位中动员出CLL细胞并将其清除。全口服、每日一次、固定疗程的 Ibr +Ven两药联合方案表现出更好的患者便利性同时方便管理,不仅降低了肿瘤溶解综合征(TLS)的发生风险,还减少Ven给药初期的住院需求。CAPTIVATE (PCYC-1142)是一项评估Ibr + Ven在CLL/SLL一线治疗中能否达到深度反应的多中心二期研究(NCT02910583),评估指标包括无法检测的微小残留疾病(uMRD)。
目的
报告3个周期Ib单药和12个周期Ibr + Ven联合用药的CAPTIVATE MRD队列结果。
方法
年龄小于70岁、先前未接受过治疗且有治疗指征的CLL/SLL患者先接受3个周期Ibr诱导治疗,随后是12个周期Ibr + Ven(Ibr 420 mg/天;Ven逐渐递增至400 mg/天)。 关键终点是研究中定期评估(每3个周期)的uMRD率(通过8色流式细胞术检测MRD<10-4)、临床反应、TLS风险和不良事件(AEs)、Ibr + Ven联合用药12个周期后的BM MRD。
结果
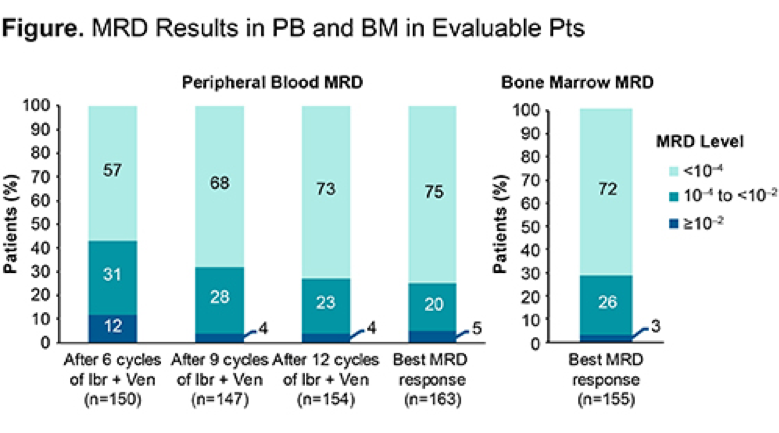
该研究共纳入了164例患者:中位年龄58岁,16%伴有del(17p),20%伴有del(17p) 或 TP53突变,16%伴有del(11q),19%伴有复杂核型(CK),59%有IGHV无突变状态,32%伴有≥5cm的肿大淋巴结。共有148(90%)例患者完成了研究设计方案(3个周期Ib单药和12个周期Ibr + Ven联合用药)。在75%(123/163)患者的PB及72%(111/155)患者的BM中uMRD达到最佳MRD响应,且高度一致(90%)。PB中uMRD率随时间不断增加(图)。在所有接受治疗的人群(N=164)中,75%患者外周血和68%患者骨髓达到uMRD。BM(可评估的患者)中uMRD的高发生率独立于基线亚组,包括伴有del(17p)(75%)、del(17p)或TP53突变(70%)、del(11q)(83%)、CK(83%)和IGHV无突变(81%)的高危患者。在所有治疗的患者中,中位随访时间为14.8个月(范围14.5~21.7),总体ORR为97%,完全缓解(CR)率为51%。在15个月时,98%的患者无进展、无死亡。在基线TLS风险高的患者中,经过3个周期的Ibr诱导治疗后,90%患者降至中等/低风险,75%患者避免因启动Ven治疗而住院。共3例患者发生实验室TLS被报道为AE,其中只有1例符合Howard标准。没有患者出现临床TLS。Ibr中位治疗持续时间为14.7 个月(范围0.5~20.1),Ven中位治疗持续时间为12.0 个月(范围0.8~12.7)。Ibr + Ven最常见AEs主要为1/2级,没有新发安全事件。最常见3/4级AEs是中性粒细胞减少症(35%)、高血压(7%)、血小板减少症(5%)和腹泻(5%),没有出现致命AEs,导致所有研究治疗中断的AEs罕见(5%)。
结论
Ibr + Ven是一种全口服、每日一次、无化疗的靶向方案,可在CLL一线治疗中使患者PB和BM中获得较高uMRD率,PB和BM之间uMRD结果高度一致。CAPTIVATE结果证实了这种联合用药的临床前协同作用。Ibr引入大大降低了与Ven相关的TLS风险及密切监测/住院治疗需要。Ibr + Ven安全性良好,由于AE导致停药率低,90%患者完成了3个Ibr周期和12个Ibr + Ven联合治疗周期的所有治疗计划。
【AbstractS155】采用固定治疗周期VENETOCLAX-OBINUTUZUMAB联合方案治疗先前未经治疗的慢性淋巴细胞白血病:多中心、开放标签、随机3期CLL14试验的疗效和安全性的随访结果
背景
在CLL14试验中,与苯丁酸氮芥-Obinutuzumab(ClbG)相比,在先前未经治疗、具有合并症的CLL患者中采用固定治疗周期的Venetoclax-Obinutuzumab (VenG)治疗表现出无进展生存期(PFS)明显改善。
目的
本报道目的是提供CLL14试验随访有效性和安全性数据,目前所有患者均已停药至少2年。
方法
将先前未经治疗、具有合并症的CLL患者按1:1比例随机分配为接收12个周期的Venetoclax和6个周期的Obinutuzumab或12个周期的苯丁酸氮芥和6个周期的Obinutuzumab两个治疗队列。主要终点为研究者评估的PFS。关键的次要终点是治疗反应率、微小残留病灶率(每6个月检测一次,直到最后一个患者登记入组后的5年)及总体生存率。随访正在进行中,但所有患者都停止了研究治疗。该试验在ClinicalTrials.gov上注册,编号为NCT02242942。
结果
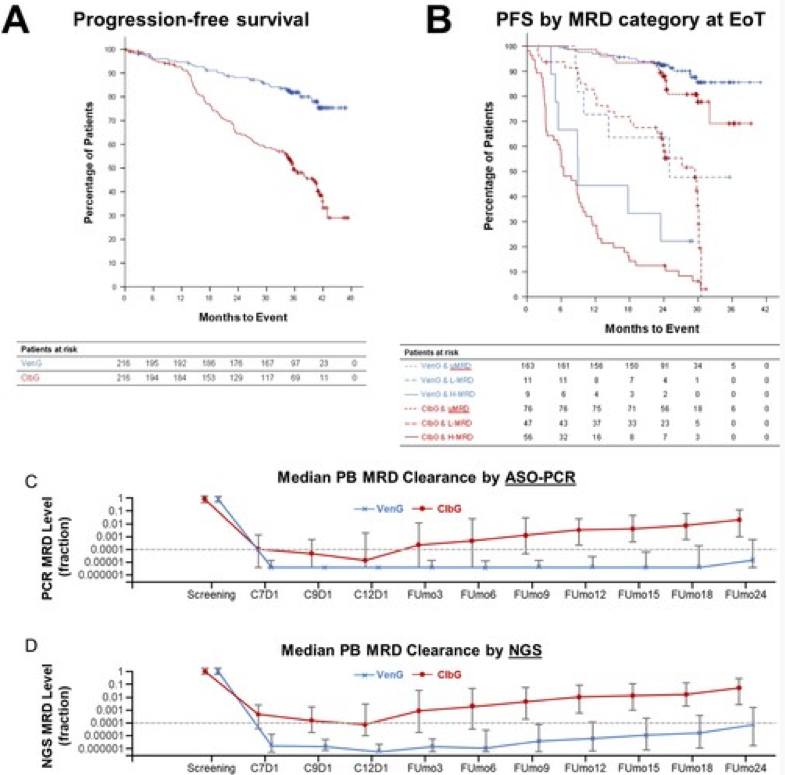
在432例入组患者中,216例被随机分配至接受VenG、216例接受ClbG。中位随访时间为39.6个月(四分位数间36.8 - 43.0),与ClbG相比,VenG的无进展生存期持续优于ClbG(中位数未达到vs 35.6个月;危险比[HR] 0.31 [0.22~0.44], p<0.001) (图A)。3年时,VenG组PFS发生率为81.9%,ClbG组为49.5%。在所有临床和生物风险组中,包括TP53突变/缺失和IGHV未突变状态的患者,这种益处是一致的。值得注意的是,与ClbG相比,接受VenG治疗的伴有IGHV突变的患者PFS也明显更长(HR 0.33 [0.16~0.70];p = 0.004)。总的来说,在VenG治疗后已经观察到21例疾病进展。在治疗结束后18个月评估外周血微小残留病灶,可见VenG队列中47.2%的患者仍然无法检测到(u)uMRD (< 10-4),13%为低(L)-MRD (≥ 10-4 和 < 10-2),7.9%为高(H)-MRD (≥ 10-2),而在ClbG队列中三组分别为7.4%、17.1%、26.9%。VenG组未达到MRD转换(即升高至≥10-4)的中位时间,ClbG组为6个月。在标志性分析中,VenG组中20例L-MRD或H-MRD的患者在末次治疗暴露后的中位PFS为17.7个月,而uMRD的患者中位PFS仍未达到(图B)。进一步分析显示,uMRD患者无论是PR或CR状态, PFS均相似;与可检测到MRD的CR患者相比,uMRD/PR患者PFS更长。通过下一代测序(NGS)进行的MRD评估表明,在90(41.7%)例接受VenG治疗的患者中的水平低于10-6,而在ClbG组中则为14(6.5%)例(图D)。对于VenG, NGS (<10-6) 评估为uMRD患者的中位MRD转换时间(即≥10-6)为12.0个月,且仅有一例病情进展。两组总体生存率没有观察到任何差异;36个月时,VenG组有88.9%患者存活,ClbG组有88.0%存活(HR 1.03, p=0.921)。第二原发恶性肿瘤在VenG组有36例(17%),在ClbG组有22例(10.3%)。没有观察到新发安全事件。
结论
结果证实,与ClbG相比,固定周期VenG具有更长的PFS和深度缓解的优势。这表明,在完成12个周期VenG治疗后,长期受益可维持2年以上。
【AbstractS164】外周血反应动力学预测在BLOODWISE TAP CLARITY试验中IBRUTINIB + VENETOCLAX治疗复发/难治CLL的长期反应
背景
靶向B细胞受体途径抑制剂如Ibrutinib(Ibr)和重新激活细胞凋亡的分子如Venetoclax(Ven),彻底改变了慢性淋巴细胞性白血病(CLL)的治疗。为了在可测量残留疾病(MRD)达到<0.01%的时停止治疗,Bloodwise TAP CLARITY试验联用Ibr与Ven以清除可检测的CLL。所有患者26个月这一时间点的疾病状态目前均可获得。
目的
通过外周血分析确定预测长期结果的关键时间点。
方法
CLARITY是一项采用Ibr与Ven联合方案治疗50例复发或难治性CLL患者的二期临床试验。在2个月 Ibr单药治疗后, Ven逐渐增加到400mg/天。使用>6CLR ERIC标准流式细胞仪对CLL MRD进行定量(检测下限低至10-5/0.001%)。在第8、14、26个月(分别在Ibr+Ven治疗之后的6、12和24个月)评估配对的外周血(PB)和骨髓(BM)样本。在多个时间点采集额外的PB样本。
结果
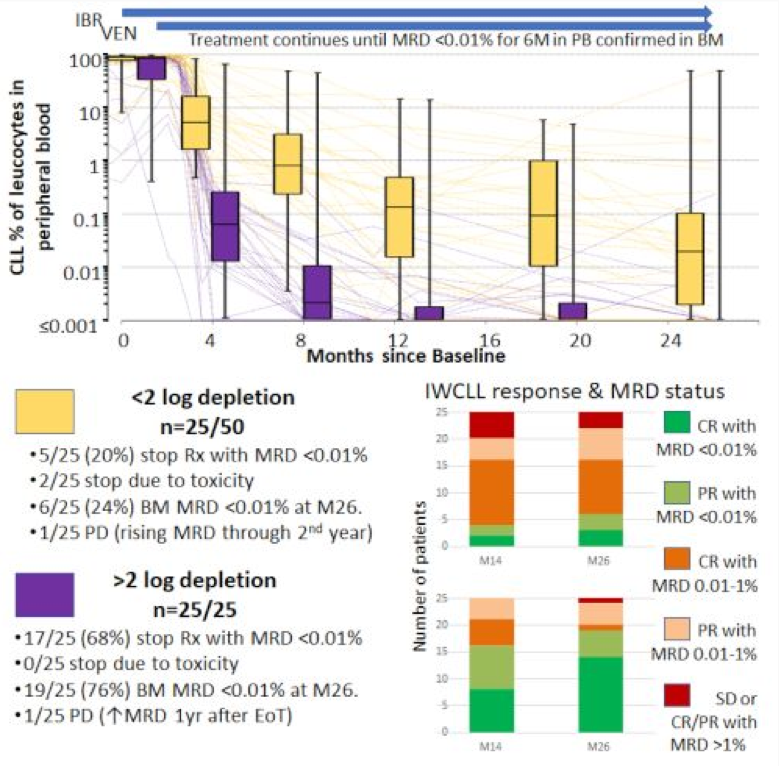
总体MRD反应在联合治疗的第1年后持续改善,在26个月时24/50(48%)的患者在骨髓中达到MRD <0.01%,而在14个月时为20/50(40%)(其中2例在第26个月时MRD水平回升到阈值0.01%以上,而6例在第14个月时MRD>0.01%的患者在26个月时达到了MRD<0.01%)。PB MRD动力学在起先两个月(仅Ibr)水平稳定,随后在所有患者中于接受随后的两个月联合治疗后迅速下降,然后在接下来的22个月里出现了一个变化模式。
在第4个月(Ibr+Ven联合治疗2个月后),对于第26个月MRD <0.01%的患者其log CLL消除中位数为2.9(范围为0.2~4.8),而该数值在第26个月时MRD≥0.01%的患者为1.4(范围为0.1~4.6)。所有组在第4个月至第8个月期间的疾病消除均较慢, 当患者在第26个月MRD <0.01%和≥0.01%时,中位log CLL消除值分别为1.1(范围0.1~2.9)和0.7(范围0.4~2.3)。在第8个月(Ibr + Ven联合治疗的6个月)后,MRD持续≥0.01%的患者的疾病水平通常保持稳定(<0.5log消除)。在第26个月达到BM MRD<0.01%的阳性预测值和阴性预测值为:在Ibr+Ven联合暴露的最初2个月期间为80%和76%;第8个月达到PB MRD<0.01%分别为72%和76%;14个月达到PB MRD<0.01%分别为86%和72%。
仅有1例患者在治疗过程中病情加重。23例患者由于PB和BM MRD均持续<0.01%而停止治疗,于治疗结束后1年检测MRD,其中15/23的患者MRD持续<0.01%,6/23的患者MRD在0.01%~1%之间,2/23的患者MRD> 1%(在停药时两者MRD均为0.001%~0.01%)。
结论
疾病消除的初始速率(在Ibr+Ven联合暴露的前两个月)对于复发/难治性CLL中Ibr+Ven联合治疗的长期疗效具有高度预测性。Ibr+ Ven联合治疗12个月后未显示出快速的疾病清除并持续存在MRD的患者通常具有稳定或缓慢降低的疾病水平,通常见于Ibr单药治疗过程中。在停止治疗1年余后,大多数患者的MRD水平仍然无法检测或较低。
【Abstract S156】复发/难治性慢性淋巴白血病患者中VENETOCLAX的疗效:国际3B期试验的主要终点分析(VENICE I)
背景
复发/难治性(R/R)慢性淋巴细胞白血病(CLL)患者仍有未满足的医疗需求,17p/TP53异常带来了进一步的挑战。Venetoclax(Ven)是一种高度选择性的BCL-2抑制剂。在此介绍迄今为止最大病例数、评估VEN单药治疗对R/R CLL患者疗效的多中心研究VENICE-I(NCT02756611)的结果,其中包括大量经B细胞受体途径抑制剂(BCRi)治疗的患者。
目的
评估Ven单药治疗在R/RCLL患者中的疗效。
方法
在这项开放标签、单臂、3b期研究中,包括17p/TP53异常患者在内的R/R CLL患者接受了Ven治疗,从20mgQD开始,连续加量5周后达最终剂量400mgQD,共2年。患者提供知情同意。在第24、36和48周评估临床反应 (iwCLL 2008)。收集基线(BL)、24和48周时的外周血(PB)进行MRD评估。主要终点是第48周时未经BCRi治疗的(BCRi-N)患者的CR或不完全骨髓恢复(CRi)的CR率。次要终点包括:ORR、PFS、OS、通过癌症治疗功能评估-白血病问卷评估的生活质量(QOL)和安全性。基于二代测序的MRD是一个探索性终点。
结果
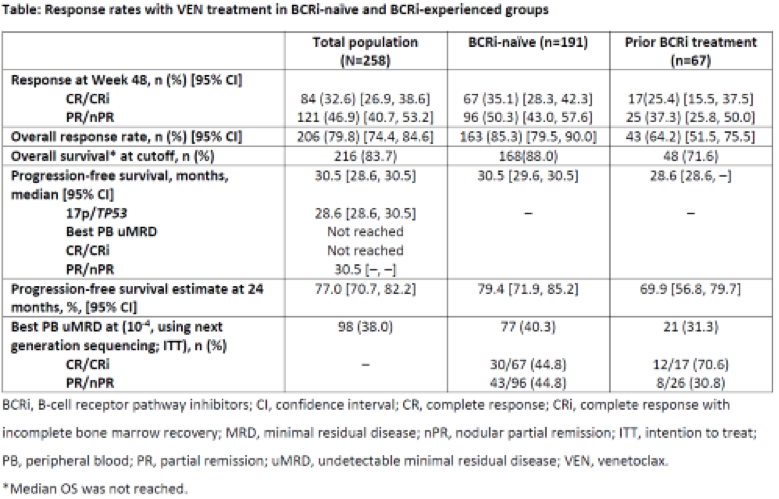
截至2019年6月30日,该试验纳入258例患者(男性占69.8%;年龄≥65岁占63.6%),其中BCRi-N为191例,67例先前接受过BCRi治疗(BCRi-EXP)。BCRi-N组患者先前接受过中位治疗数为1而BCRi-EXP组中位接受过3线治疗(开始Ven前BCRi治疗的中位时间为9月)。 BCRi-N及BCRi-EXP患者合并17p / TP53异常比例分别为16.8%和43.3%。在BCRi-EXP组中,有20例因复发或难治或疾病进展(PD)导致BTKi治疗失败,而36例因毒性而使BTKi失败。 BCRi-N和BCRi-EXP组中位Ven持续时间分别为20.4月和23.2月。在258例患者中,有192例(74.4%)经历了3级以上不良事件(AEs)(中性粒细胞减少症[37.2%];感染[19.0%]),其中32名(12.4%)由于AEs减少了剂量 ,并且有109例(42.2%)停用Ven(12.8%由于AE;10.9%由于PD)。 没有观察到新发安全事件。BCRi-N组与BCRi-EXP组相比,第48周ORR和CR / CRi率分别为85.3% vs 64.2%和35.1% vs 25.4%(表)。总体PFS(24个月PFS估计%)为30.5个月 (77.0%),伴17p/TP53异常的患者PFS为28.6个月(67.1%), BCRi-N和 BCRi-EXP组的PFS分别为30.5个月(79.4%)和 28.6个月(69.9%)。达到uMRD或CR/CRi状态患者中位PFS均未达到。部分缓解/结节性部分缓解(PR/nPR)的PFS为30.5个月。 总体OS率为83.7%,BCRi-N与-EXP组的OS分别为88.0%和71.6%。计划进行更多MRD和BCRi治疗失败(PD与毒性)分析。在第48周时出现有临床意义的QOL改善(FACT-Leu白血病量表评估对比BL状态的变化均值:BRCi-N为6.5; BCRi-EXP为7.8)。
结论
这项3b期研究证实Ven单药治疗在R / R CLL患者中达到深度治疗反应(CR和/或uMRD),且耐受性可、安全性可控。获得uMRD患者PFS持续时间更长,iwCLL疗效评估更好。
范磊教授点评
慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)是主要发生在老年人群的成熟B细胞克隆增殖性肿瘤。近几年,CLL治疗方面取得了很大进展,各种新药不断涌现,使得CLL治疗进入无化疗的靶向治疗时代,同时也为CLL一线治疗的优化选择及R/R CLL的治疗策略提供了新思路。
Venetoclax(Ven)是一类口服BCL-2抑制剂,基于Ven为基础的CLL14研究中的数据,现已被FDA批准用于成人CLL/SLL的治疗,也在R/R或伴del(17p)/TP53突变的CLL患者的治疗中表现出了高度有效性。
本届EHA会议上Abstract S158结合CAPTIVATE MRD队列研究的数据,证实一线使用Ibrutinb(Ibr)+Ven治疗CLL/SLL患者可以获得深度的疾病缓解(uMRD发生率高),同时也表现出良好的安全性。Abstract EP688报道采用Obinutuzumab和Ven方案在一线不耐受FCR的慢性淋巴细胞性白血病患者中也得到了相似的结论。Abstract S155更新了CLL14研究停药两年的随访数据,结果证实与ClbG相比,固定周期的VenG具有更长的PFS和深度缓解的优势,而在完成12个周期VenG治疗后,长期受益可维持两年以上。
目前R/R CLL(尤其是BTKi-EXP)及伴有del(17p)/TP53突变的高危CLL患者的预后仍差。本届EHA会议上分别利用Ven单药或与BTKi或CD20单抗联用的治疗策略探索治疗此类患者并对疗效预测及中断/停药风险等方面进行了研究。Abstract S156报道了Ven单药治疗R/R CLL患者的疗效,总体PFS为30.5个月,伴17p/TP53异常的患者PFS为28.6个月。达到uMRD或CR/CRi状态患者的中位PFS均未达到。部分缓解/结节性部分缓解(PR / nPR)的PFS为30.5个月。 总体OS率为83.7%。BCRi-N与-EXP组相比,CR率、PFS及OS均较高。这项3b期研究证实Ven单药治疗在R / R CLL患者中达到深度治疗反应(CR和/或uMRD),其耐受性可、安全性可控。获得uMRD患者PFS持续时间更长,iwCLL反应更好。
以Ibrutinib为代表的靶向治疗改变了CLL治疗的模式,并且显示出可以控制的临床安全性。Venetoclax作为BCL2抑制剂,针对CLL凋亡受抑的根本发病机制在包括TP53异常的CLL患者中取得良好疗效,并且多项基于Venetoclax的治疗方案显示可以达到深度缓解,为CLL的临床治愈提供可能,但是我们也观察到个别患者在达到MRD阴性后出现复燃,因此基于Venetoclax方案是CLL患者治疗的新选择,但是中长期疗效仍然需要进一步观察。
排版编辑:Amiee













 苏公网安备32059002004080号
苏公网安备32059002004080号


