PARP抑制剂研发的源头,要追溯到1963年Paul Mandel等对PARP酶活性的描述报道,以及1964年Pierre Chambon等人正式发现PARP酶[1]。在此之后的20年里,科学家们不断深入研究PARP酶的生物学功能,发现其参与DNA修复功能,如果抑制其酶活性,则会阻断DNA修复[1,2]。另一方面,有研究者发现一种非常有趣的现象,PARP与受损DNA紧密结合会产生细胞毒性[1,3]。这些前期的生物学研究,表明PARP在DNA损伤修复中的重要角色,为PARP抑制剂的研发奠定了基础。PARP酶催化PARP修饰介导的DNA单链损伤修复,以及PARP酶与DNA紧密结合不解离导致的细胞毒性,这两种生物学性质被用于指导PARP抑制剂的开发,成为PARP抑制剂的直接作用机制[4,5]。
由于PARP的生物学功能是DNA损伤修复,而化疗和放疗都会产生大量的DNA损伤,因此在PARP抑制剂用于肿瘤治疗的早期开发阶段,被认为可与这些治疗方案联用,增加化疗药物或放疗的疗效[5]。2008年,Plummer等人首次报道了Rucaparib和替莫唑胺联用的Ⅰ期临床研究,验证了这样的设想[5,6]。但在后期的临床研究发现,PARP抑制剂会产生骨髓抑制的毒副作用,而化疗和放疗都有比较强的骨髓抑制作用,两者毒副反应的交叉重叠,使两者联合需要降低剂量和缩短给药疗程,从而导致疗效下降[5,7]。

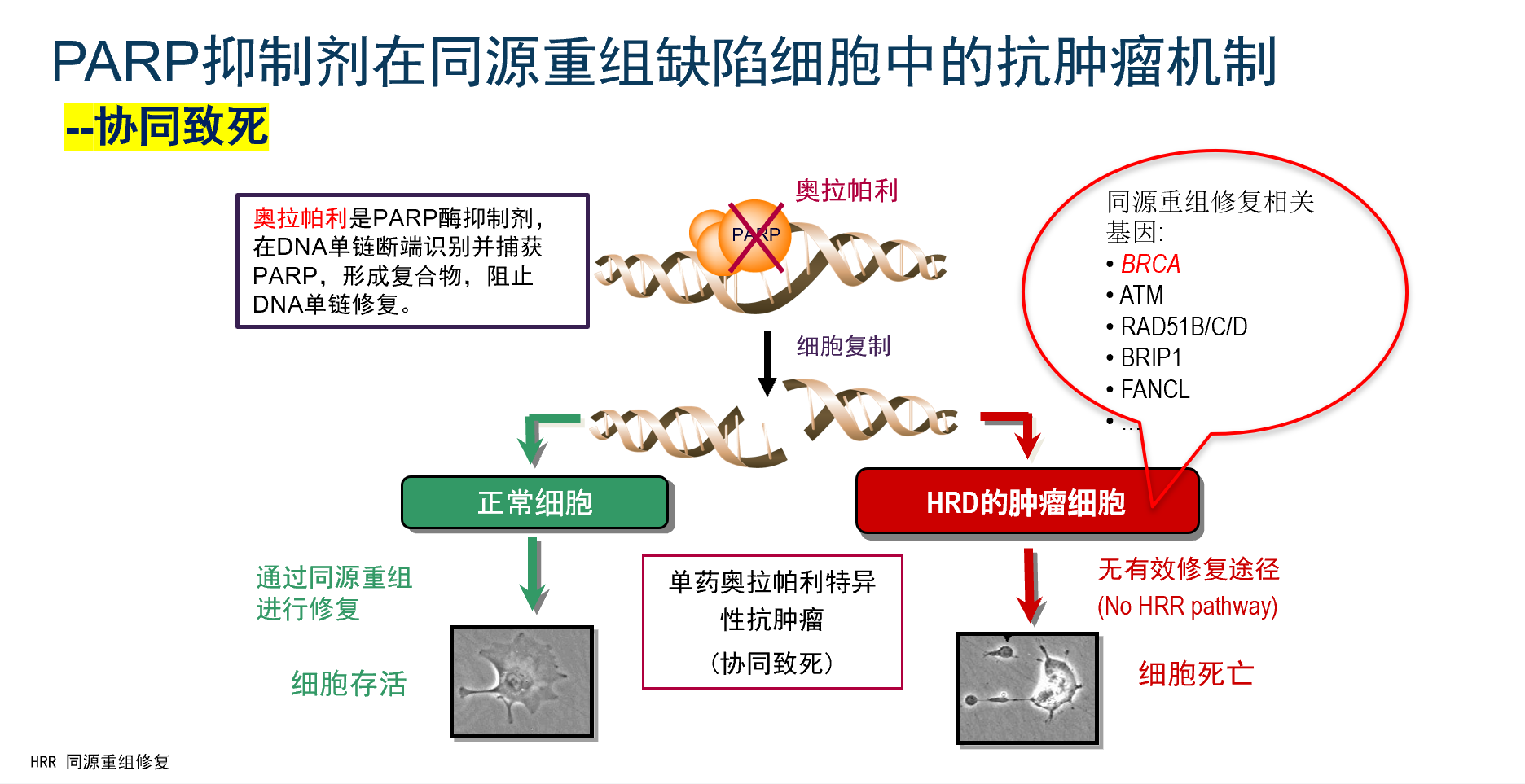
探索PARP抑制剂单药治疗的起点,来自于2005年Nature杂志同期发表的两篇文章,两个研究团队分别报道BRCA突变的肿瘤对PARP抑制剂的敏感性,第一次证实PARP抑制剂与BRCA基因突变的“合成致死”效应[5,8,9]。4年后,奥拉帕利的一项Ⅰ期临床研究证实其在携带BRCA突变的卵巢癌等肿瘤患者中具有显著疗效,并且具有合适的安全性和PK/PD 性质,这是第一项PARP抑制剂在BRCA突变人群中的临床试验报道[5,10]。2010年,奥拉帕利在BRCA突变人群中的疗效在另一项概念验证性Ⅱ期临床研究中得到证实[11]。随后的另一项Ⅰ期研究发现,奥拉帕利的疗效与患者的铂敏感状态和化疗线数有关,铂敏感患者的疗效明显更好,化疗线数越多,可能造成患者对PARP抑制剂耐药性越大[5,12]。在这项研究中,携带BRCA突变的复发性卵巢癌铂敏感患者对奥拉帕利的客观缓解率(ORR)高达69%,铂耐药患者为45%,而铂抵抗患者仅23%。这为后续开发铂敏感复发性卵巢癌的治疗提供了证据。
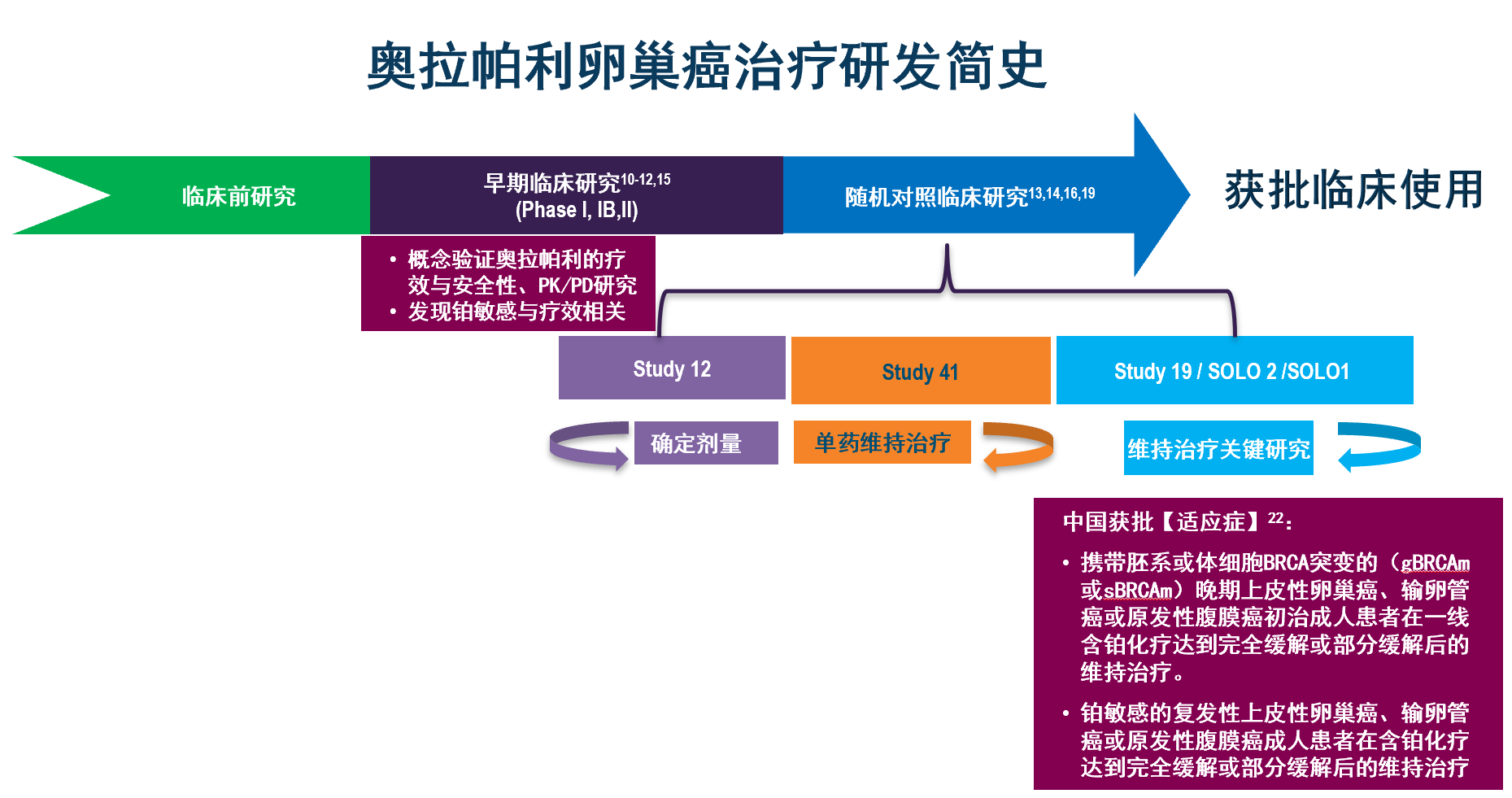
研究人员也曾探索奥拉帕利与化疗药物的联合使用。在Ⅱ临床研究Study 12中,对于携带BRCA1/2突变的复发性卵巢癌,奥拉帕利分为200mg和400mg组与脂质体多柔比星联用,尽管两个剂量奥拉帕利联用组的无进展生存(PFS)和ORR都高于脂质体多柔比星,但均未达到统计学显著性[13]。Study12作为随机对照试验,也确定了奥拉帕利400mg BID作为推荐剂量(胶囊剂型未在国内上市,请见文末标注说明)。奥拉帕利作为单药维持治疗的方案,则由Study 41研究确定[14]。Study 41研究是一项评估奥拉帕利联合化疗用于铂敏感复发性卵巢癌治疗和随后奥拉帕利单药维持治疗对比单用化疗的疗效与安全性的Ⅱ期临床研究。该研究的结果发现,尽管联合用药组的PFS显著长于单用化疗组,但生存曲线显示PFS的延长主要来自于奥拉帕利单药维持治疗阶段,因此推荐单药维持治疗方案。
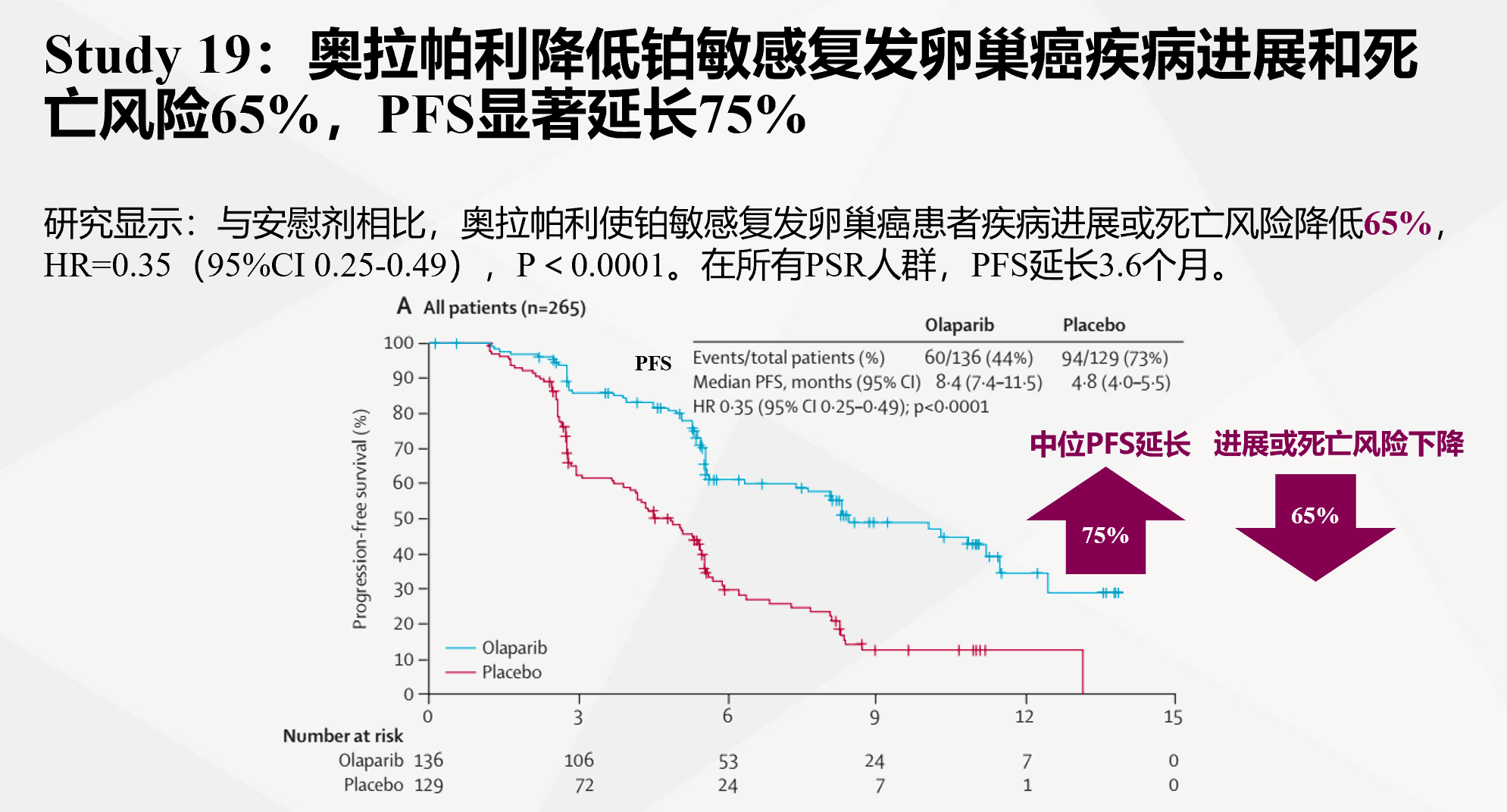
2012年,奥拉帕利再次在两项Ⅱ期研究中显示出显著疗效,尤其是对BRCA突变患者[15,16]。其中一项研究显示奥拉帕利对于高级别浆液性或未分化卵巢癌,即使是未携带BRCA突变的患者ORR也达到24%。另一项Ⅱ期研究即Study 19,第一项随机对照的大型临床研究证实了PARP抑制剂用于铂敏感复发患者维持治疗的疗效,在该研究所有铂敏感人群中奥拉帕利降低疾病进展或死亡风险达到65%,延长PFS 75%(中位PFS:奥拉帕利组为8.4个月,安慰剂组为4.8个月),并且13%的患者在5年时仍未进展;而亚组分析显示,对于BRCA突变患者,奥拉帕利维持治疗的疗效则更加显著[17]。2014年奥拉帕利获得欧洲EMA批准,成为全球第一个上市的PARP抑制剂[18]。
 随后SOLO2研究、NOVA研究以及ARIEL3研究等大型III期临床试验表明,PARP抑制剂用于铂敏感复发性卵巢癌含铂化疗达到缓解后维持治疗,无论患者是否携带BRCA基因突变,均可显著延长患者PFS、降低疾病进展或死亡风险[19-21]。因此,奥拉帕利在美国和中国等多个国家获批用于铂敏感复发性卵巢癌的维持治疗,并获得NCCN卵巢癌指南推荐[22-24]。
随后SOLO2研究、NOVA研究以及ARIEL3研究等大型III期临床试验表明,PARP抑制剂用于铂敏感复发性卵巢癌含铂化疗达到缓解后维持治疗,无论患者是否携带BRCA基因突变,均可显著延长患者PFS、降低疾病进展或死亡风险[19-21]。因此,奥拉帕利在美国和中国等多个国家获批用于铂敏感复发性卵巢癌的维持治疗,并获得NCCN卵巢癌指南推荐[22-24]。
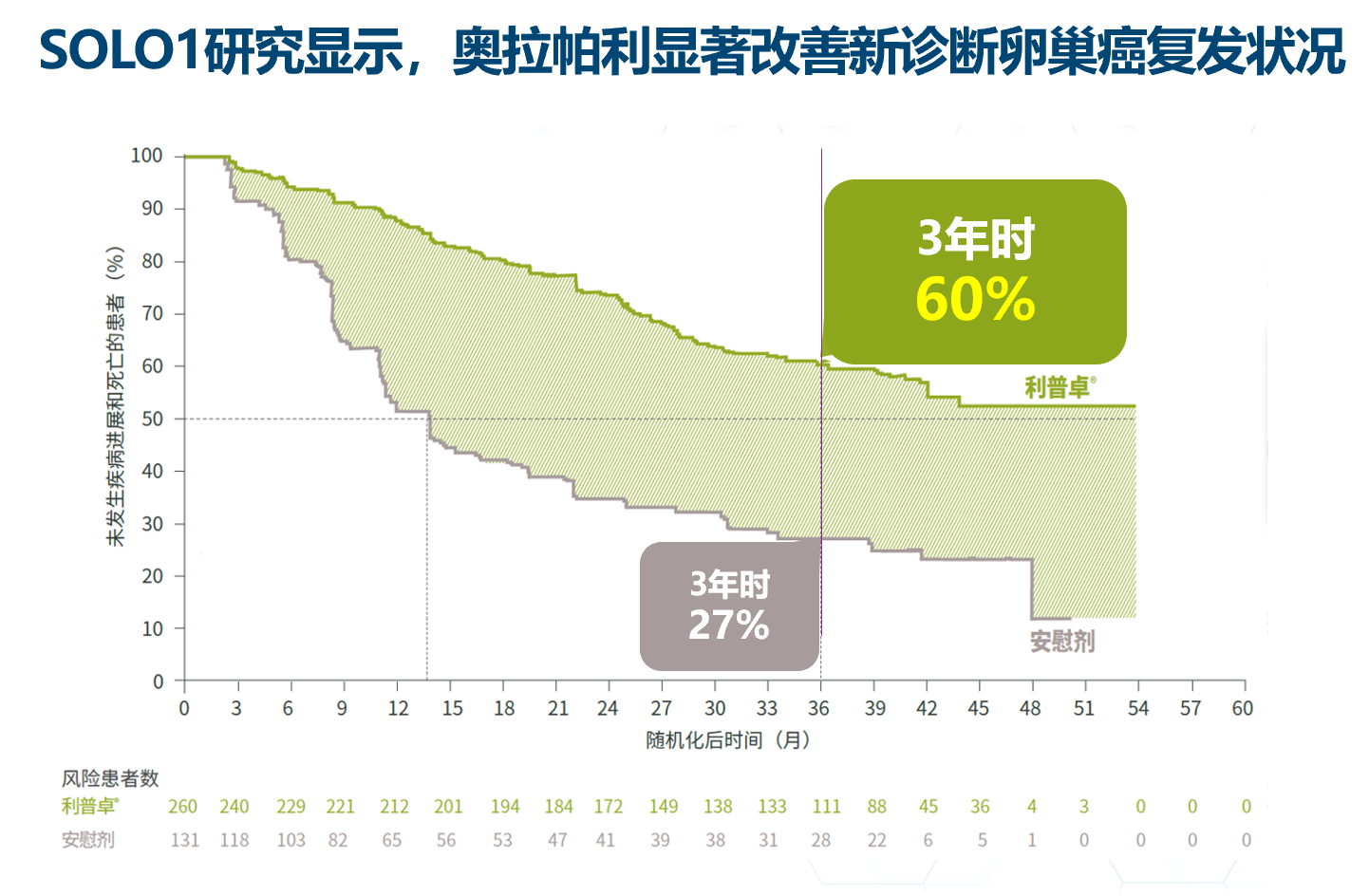
2018年,在ESMO大会上,SOLO1研究公布疗效数据,奥拉帕利再次成为卵巢癌治疗领域令人瞩目的焦点。SOLO1研究显示,奥拉帕利可显著延长携带BRCA突变的新诊断晚期卵巢癌的PFS,降低疾病进展或死亡风险达70%,并且使用奥拉帕利维持治疗的患者高达60%在3年时仍未发生疾病进展(安慰剂组仅27%)[25]。SOLO1的疗效被现场专家称为卵巢癌治疗史上前所未有,因此在2018年12月24日即迅速获得FDA批准用于BRCA突变患者的一线维持治疗,同时中国国家药品监督管理局(NMPA)也在2019年11月30日批准奥拉帕利用于BRCA突变患者的一线维持治疗[22,23]。奥拉帕利用于BRCA突变患者一线维持治疗,同样也得到NCCN指南的高级别推荐,已成为新诊断卵巢癌患者的标准治疗药物之一[24]。
注:胶囊剂型未在中国申报上市,阿斯利康不推荐任何未被批准的药品使用。请参照中国批准的说明书使用。奥拉帕利在中国批准的剂型是片剂,推荐剂量为300mg,每日2次。
1. Pilié PG, Tang C, Mills GB, et al. State-of-the-art strategies for targeting the DNA damage response in cancer[J]. Nat Rev Clin Oncol, 2019,16(2):81-104.
2. Durkacz BW, Omidiji O, Gray DA, et al. (ADP-ribose) n participates in DNA excision repair. Nature, 1980,283(5747):593.
3. Satoh MS & Lindahl, T. Role of poly (ADP-ribose) formation in DNA repair[J]. Nature, 1992,356(6367):356-358.
4. Taylor KN & EskandeR RN. PARP inhibitors in epithelial ovarian cancer[J]. Recent Pat Anticancer Drug Discov, 2018,13(2):145-158.
5. Pommier Y, O’Connor, MJ, & de Bono J. Laying a trap to kill cancer cells: PARP inhibitors and their mechanisms of action. Sci Transl Med, 2016,8(362), 362ps17-362ps17.
6. Plummer R, Jones C, Middleton M, et al. Phase I study of the poly (ADP-ribose) polymerase inhibitor, AG014699, in combination with temozolomide in patients with advanced solid tumors[J]. Clin Cancer Res, 2008,14(23):7917-7923.
7. Plummer R, Lorigan P, Steven N, et al. A phase II study of the potent PARP inhibitor, Rucaparib (PF-01367338, AG014699), with temozolomide in patients with metastatic melanoma demonstrating evidence of chemopotentiation[J]. Cancer Chemother Pharmaco, 2013,71(5):1191-1199.
8. Bryant HE, Schultz N, Thomas HD, et al. Specific killing of BRCA2-deficient tumours with inhibitors of poly (ADP-ribose) polymerase. Nature, 2005,434(7035):913.
9. Farmer H, McCabe N, Lord CJ, et al. Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy. Nature, 2005,34(7035):917.
10. Fong PC, Boss DS, Yap TA, et al. Inhibition of poly (ADP-ribose) polymerase in tumors from BRCA mutation carriers[J]. New Engl J Med, 2009,361(2):123-134.
11. Tutt A, Robson M, Garber JE, et al. Oral poly (ADP-ribose) polymerase inhibitor olaparib in patients with BRCA1 or BRCA2 mutations and advanced breast cancer: a proof-of-concept trial[J]. Lancet, 2010,376(9737):235-244.
12. Fong PC, Yap TA, Boss DS, et al. Poly (ADP)-ribose polymerase inhibition: frequent durable responses in BRCA carrier ovarian cancer correlating with platinum-free interval[J]. J Clin Oncol, 2010,28(15): 2512-2519.
13. Kaye SB, Lubinski J, Matulonis U, et al. Phase II, open-label, randomized, multicenter study comparing the efficacy and safety of olaparib, a poly (ADP-ribose) polymerase inhibitor, and pegylated liposomal doxorubicin in patients with BRCA1 or BRCA2 mutations and recurrent ovarian cancer[J]. J Clin Oncol, 2011,30(4):372-379.
14. Oza AM, Cibula D, Benzaquen AO, et al. Olaparib combined with chemotherapy for recurrent platinum-sensitive ovarian cancer: a randomised phase 2 trial[J]. Lancet Oncol, 2015,16(1):87-97.
15. Gelmon KA, Tischkowitz M, Mackay H, et al. Olaparib in patients with recurrent high-grade serous or poorly differentiated ovarian carcinoma or triple-negative breast cancer: a phase 2, multicentre, open-label, non-randomised study[J]. Lancet Oncol, 2011,12(9):852-861.
16. Ledermann J, Harter P, Gourley C, et al. Olaparib maintenance therapy in platinum-sensitive relapsed ovarian cancer[J]. New Engl J Med, 2012,366(15):1382-1392.
17. Ledermann JA, Harter P, Gourley C, et al. Overall survival in patients with platinum-sensitive recurrent serous ovarian cancer receiving olaparib maintenance monotherapy: an updated analysis from a randomised, placebo-controlled, double-blind, phase 2 trial[J]. Lancet Oncol, 2016,17(11):1579-1589.
18. Lynparza™approved in the European Union as first-in-class treatment for advanced BRCA-mutated ovarian cancer. https://www.astrazeneca.com/media-centre/press-releases/2014/lynparza-approved-european-union-brca-mutated-ovarian-cancer-treatment-18122014.html#!
19. Pujade-Lauraine E, Ledermann JA, Selle F, et al. Olaparib tablets as maintenance therapy in patients with platinum-sensitive, relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a double-blind, randomised, placebo-controlled, phase 3 trial[J]. Lancet Oncol, 2017,18(9), 1274-1284.
20. Coleman RL, Oza AM, Lorusso D, et al. Rucaparib maintenance treatment for recurrent ovarian carcinoma after response to platinum therapy (ARIEL3): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2017,390(10106):1949-1961.
21. Mirza MR, Monk BJ, Herrstedt J, et al. Niraparib maintenance therapy in platinum-sensitive, recurrent ovarian cancer[J]. New Engl J Med, 2016,375(22):2154-2164.
22. 奥拉帕利-中国-利普卓 药品说明书
23. 奥拉帕利-美国-Lynparza药品说明书
24. NCCN Clinical Practice Guidelines in Oncology-Ovarian Cancer, 2019 v3.
25. Moore K, Colombo N, Scambia G, et al. Maintenance Olaparib in Patients with Newly Diagnosed Advanced Ovarian Cancer. N Engl J Med, 2018,379(26):2495-2505.
*仅供医疗卫生专业人士参考
审批编号:CN-44436 有效期至:2021-2-2
排版编辑:Myrna















 苏公网安备32059002004080号
苏公网安备32059002004080号


