作为免疫治疗的明星产品,嵌合抗原受体T细胞免疫疗法(CAR-T)已在血液系统恶性疾病中展现出巨大的实力,并且已有相关CAR-T产品在国外获批。但目前产品由于安全性等方面有待完善,因此临床应用受到限制。JWCAR029是国内细胞治疗领军企业——药明巨诺在美国JUNO Therapeutics公司的CAR-T工艺技术平台的基础上,自主研发的一款自体CAR-T细胞治疗产品,在I期临床研究中用于治疗复发/难治(R/R)B细胞非霍奇金淋巴瘤(B-NHL)显示出良好的疗效和安全性。第61届美国血液学会(ASH)年会于2019年12月7-10日在美国奥兰多隆重举行,JWCAR029有两项治疗R/R B-NHL的重要研究结果在大会公布。【肿瘤资讯】特作梳理,以飨读者。

研究一:CD19 CAR-T产品JWCAR029治疗R/R B-NHL的临床疗效(摘要号2876)
研究介绍
对化疗耐药或自体造血干细胞移植(auto-HCT)后12个月内复发的侵袭性B-NHL预后很差,现有疗法的总缓解率(ORR)<40%,完全缓解(CR)率<20%。对于难治的弥漫性大B细胞淋巴瘤(DLBCL)患者,现有疗法的ORR为26%,CR率为7%。JWCAR029由源自鼠源单克隆抗体(FMC63)的抗CD19单链抗体(scFv)、CD3ζ激活区域和4-1BB共刺激域所组成,以CD4+和CD8+ CAR-T细胞按非固定比例生产和输注。JWCAR029-001研究为单臂、开放标签的Ⅰ期临床剂量爬坡研究(NCT03344367和NCT03355859),用于评估JWCAR029治疗R/R B-NHL的安全性和有效性。JWCAR029-001/002研究是中国国家药品监督管理局(NMPA)首个IND批准的以CD19为靶点的CAR-T产品的临床研究。
研究设计与入组标准
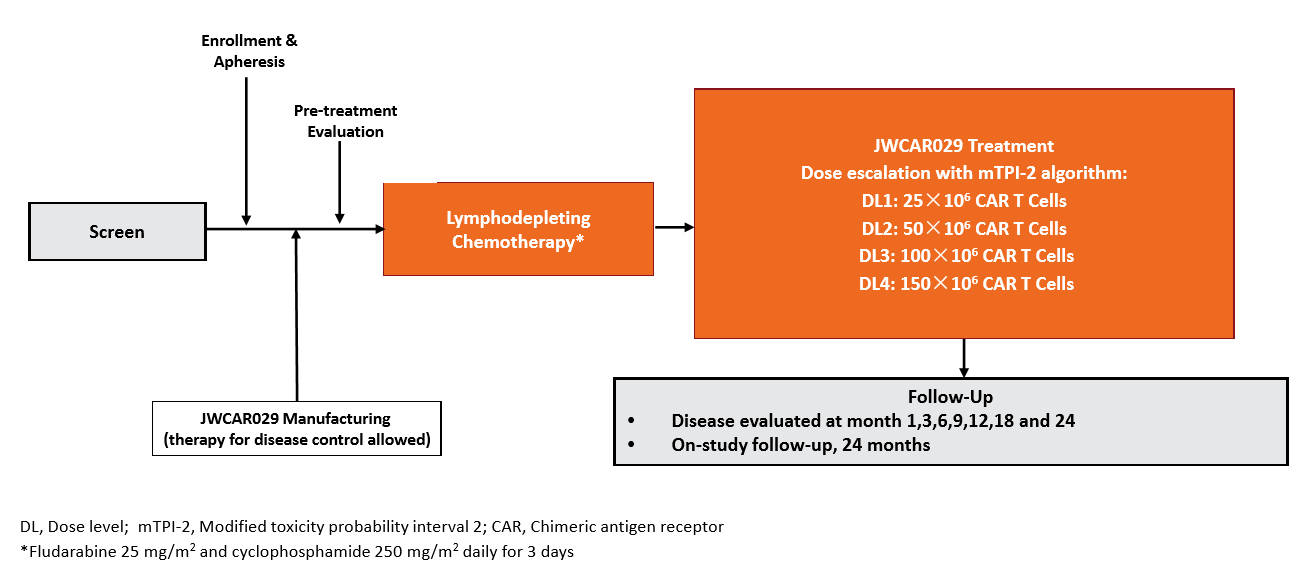
图1. JWCAR029-001研究设计
JWCAR029-001/002研究的入组标准包括:年龄≥18岁;经活检确认为R/R B-NHL;依据Lugano标准确定的PET阳性病灶;美国东部肿瘤协作组(ECOG)体能状态为0或1。符合条件的患者既往均接受过至少二线治疗。所有患者在接受JWCAR029之前接受了清淋化疗,随后以递增的剂量水平(DL)单次输注JWCAR029,剂量从25×106CAR-T细胞(DL1),50×106CAR-T细胞(DL2),100×106CAR-T细胞(DL3)至150×106CAR-T细胞(DL4),以评估JWCAR029的安全性和有效性。安全性评估包括不良事件(AE)、剂量限制毒性(DLT)、细胞因子释放综合征(CRS)和神经毒性(NT)。疗效评估包括ORR、CR、缓解持续时间(DOR)、无进展生存(PFS)、总生存时间(OS)以及药代动力学(PK)/药效学(PD)。
研究结果
截至2019年7月5日,共32例患者在2个国内临床研究中心接受了JWCAR029治疗,最终有29例可评估疗效并随访至少6个月,其中20例DLBCL,5例滤泡淋巴瘤(FL),2例套细胞淋巴瘤(MCL),1例边缘区淋巴瘤(MZL),1例黏膜相关淋巴组织(MALT)型结外MZL。患者中位年龄为56岁。各DL组情况详见下图2。
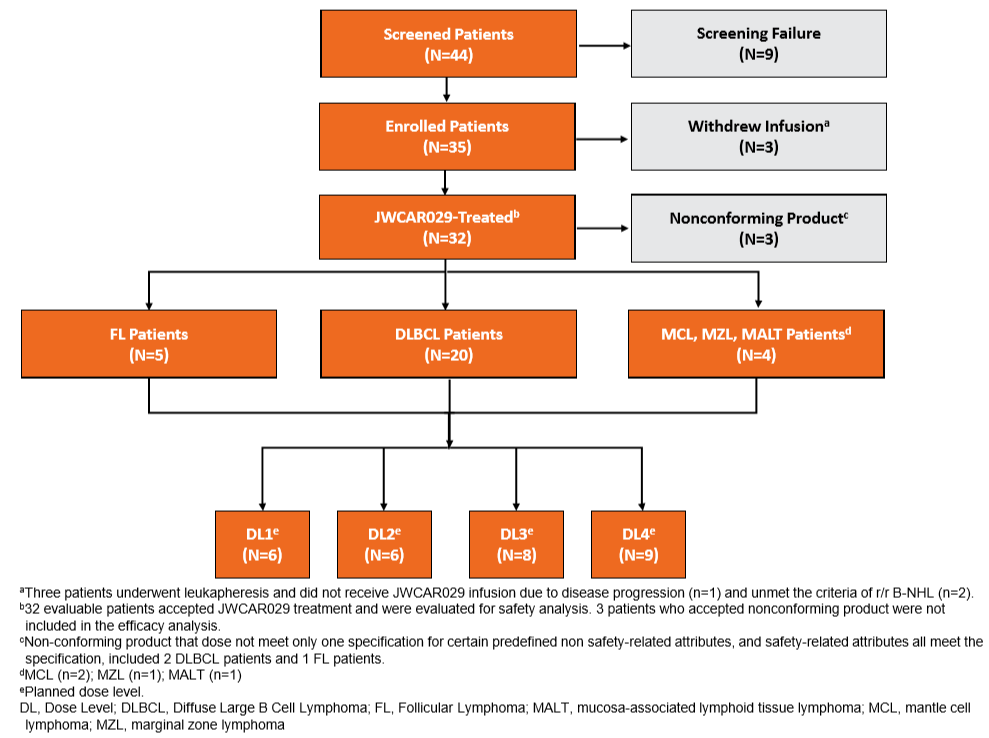
图2. JWCAR029-001研究入组情况
安全性
无DLT和治疗相关的死亡发生。最常见的AE(发生率>20%)包括白细胞减少(1-2级:43.8%,3-4级:21.9%),淋巴细胞减少(1-2级:21.9%,3-4级:21.9%),中性粒细胞减少(1-2级:37.5%,3-4级:28.2%),血小板减少(1-2级:21.9%,3-4级:3.1%),发热(1-2级:21.9%)和免疫球蛋白降低(1级:28.1%)。

图3. JWCAR029治疗相关的AE和血液学异常情况
17例(53.1%)报告发生了CRS,其中16例(50%)为1或2级,1例(3.1%)为3级;未观察到4或5级CRS;主要症状为发热、疲劳和肌肉酸痛;各DL组的CRS发生率相似。在5例(15.6%)患者中观察到1和2级NT;1例 (3.1%)发生≥3级NT。CRS和NT的中位发生时间分别为6天和10天,只有9.4%的患者在接受JWCAR029治疗72小时内出现CRS。CRS和NT的中位完全解决时间分别为8天和4天。探索性分析表明,基线时的肿瘤负荷如乳酸脱氢酶(LDH)、铁蛋白、C-反应蛋白(CRP)的升高可能与CRS或NT的发生有关。需要继续评估潜在的血液学生物标志物以识别高危患者的CRS或NT的发生。
表1. CRS和NT的发生情况
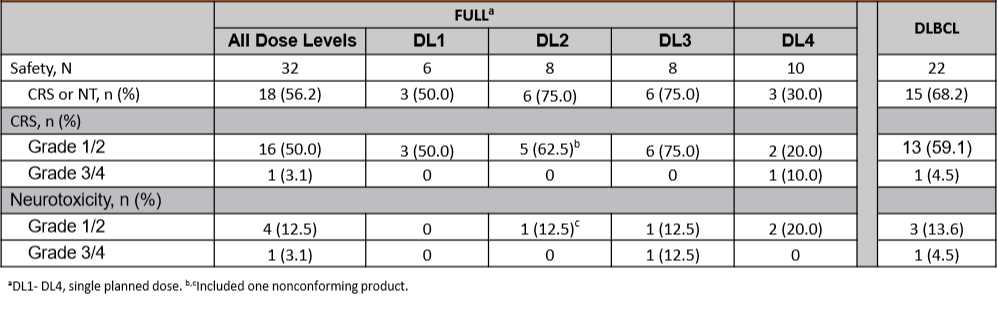
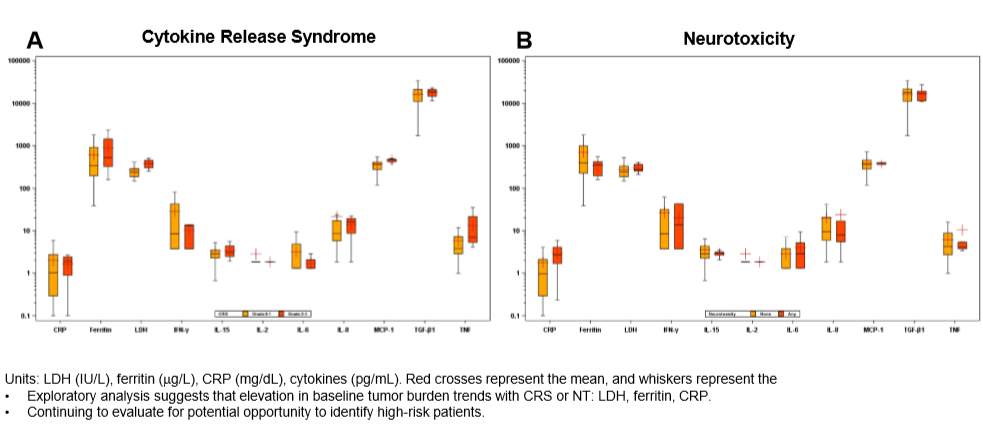
图4. 治疗前血液学分析指标与CRS(图A)和NT(图B)的发生趋势
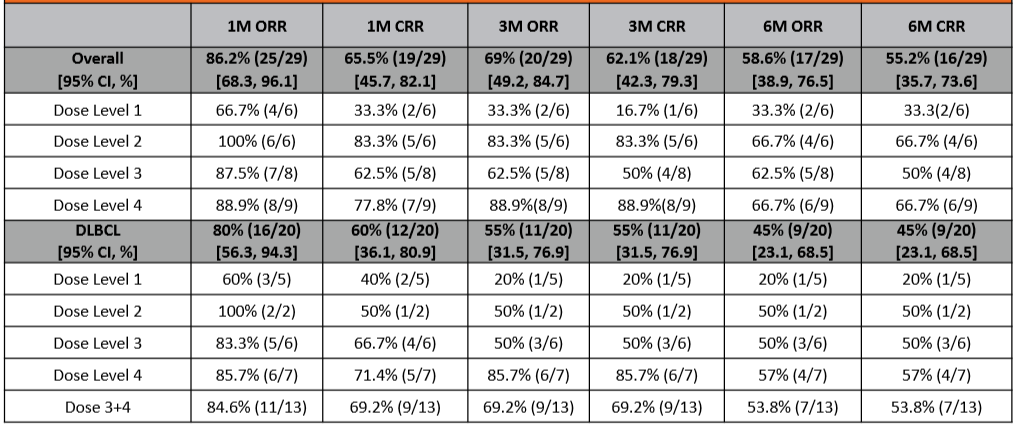
截至2019年10月28日,在所有29例可评估疗效的患者中(DL1组6例,DL2组6例,DL3组8例,DL4组9例),最佳ORR为89.7%,其中DLBCL患者的最佳ORR为85%。在第1、3和6个月时,所有可评估患者的ORR/CR率分别为86.2%/65.5%,69%/62.1%和58.6%/55.2%;对于20例DLBCL患者,ORR/CR率分别为80%/60%,55%/55%和45%/45%。
表2. 第1、3和6个月的ORR与CR率
研究结论
对于预后较差的R/R侵袭性B-NHL患者,输注JWCAR029可获得良好且持久的缓解,6个月时所有患者的ORR为58.6%,CR率为55.2%;DLBCL患者的ORR为45%,CR率为45%。安全性方面,JWCAR029相关不良事件可控,未发生CRS或NT相关性死亡,3/4级CRS或NT发生率低,约为6%。目前正在开展Ⅱ期注册临床试验(NCT04089215),用以进一步评估JWCAR029在DLBCL和FL患者中的安全性和有效性,并已开放入组。

研究二:JWCAR029治疗R/R B-NHL患者的细胞动力学和抗治疗抗体(摘要号4083)
研究介绍
JWCAR029-001研究已初步证实JWCAR029具有较高的CR率和良好的安全性。在DLBCL队列中(有效性子集n=20;安全性子集n=22),ORR为80%,其中CR率为60%;严重CRS发生率为4.5%,严重NT发生率为4.5%。本研究报道了在JWCAR029-001研究中,JWCAR029的药代动力学(PK),药效学(PD)和抗治疗抗体(ATA)情况。
研究方法
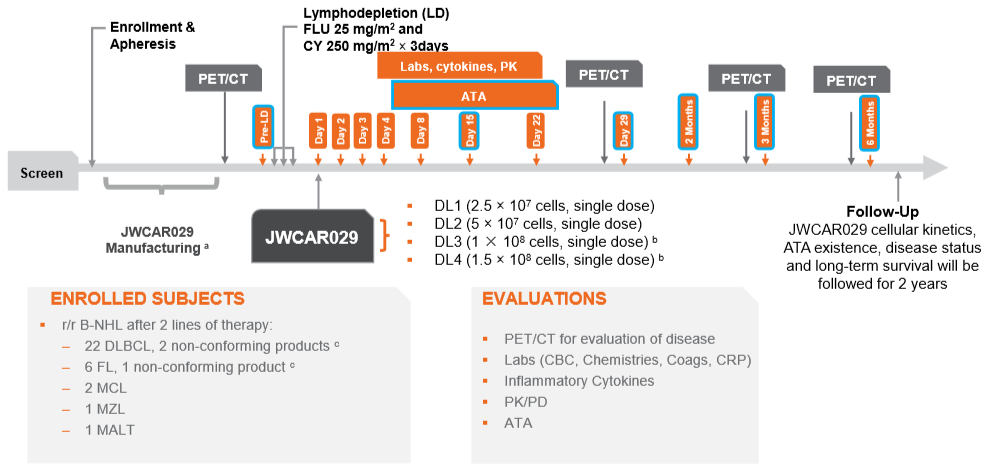
图5. 患者治疗和评估流程
使用经验证的流式细胞术和定量PCR(qPCR)为基础的分析方法测定外周血中CAR-T细胞的存在和持续时间。PK分析主要采用qPCR方法进行;通过流式细胞仪分析检测转染的T细胞膜表面上与CD19特异性CAR共表达的EGFRt蛋白,并分别分析CD3+/CD8+和CD3+/CD4+ CAR-T细胞亚群的PK。通过定性电化学发光法(ECL)测定CD19特异性鼠源单克隆抗体(FMC63)在血浆中的ATA。
研究结果
PK/PD
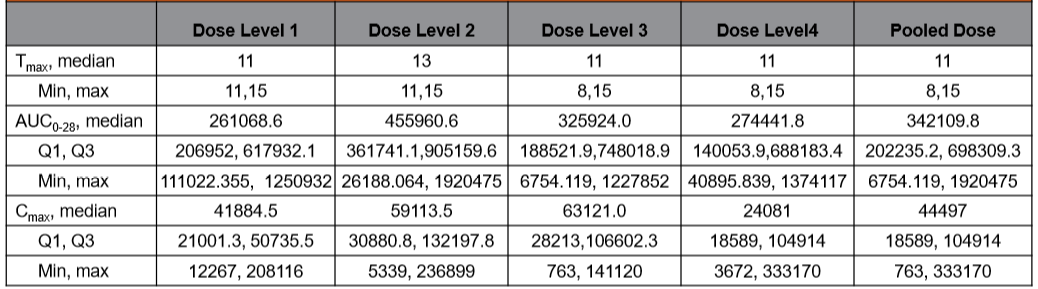
截至2019年7月5日,研究人员分析了JWCAR029-001研究中可评估的29例患者的血液样本。所有DL组中的患者均可检测到JWCAR029细胞。JWCAR029转基因拷贝数的中位药峰浓度(Cmax)、药峰时间(Tmax)和0至28天的血药浓度-时间曲线下面积(AUC0-28)在各DL组之间没有差异。
表3. 各DL组中qPCR测定的JWCAR029的Cmax、Tmax和AUC0-28
 基于qPCR和流式细胞术,发现JWCAR029在6个月时获得更好缓解的患者体内有更高的扩增。在对治疗有反应的患者中,CD8+CAR+ T细胞浓度高于CD4+CAR+ T细胞,中位Cmax(单位:copies/µg)为30.6 vs 5.64。
基于qPCR和流式细胞术,发现JWCAR029在6个月时获得更好缓解的患者体内有更高的扩增。在对治疗有反应的患者中,CD8+CAR+ T细胞浓度高于CD4+CAR+ T细胞,中位Cmax(单位:copies/µg)为30.6 vs 5.64。
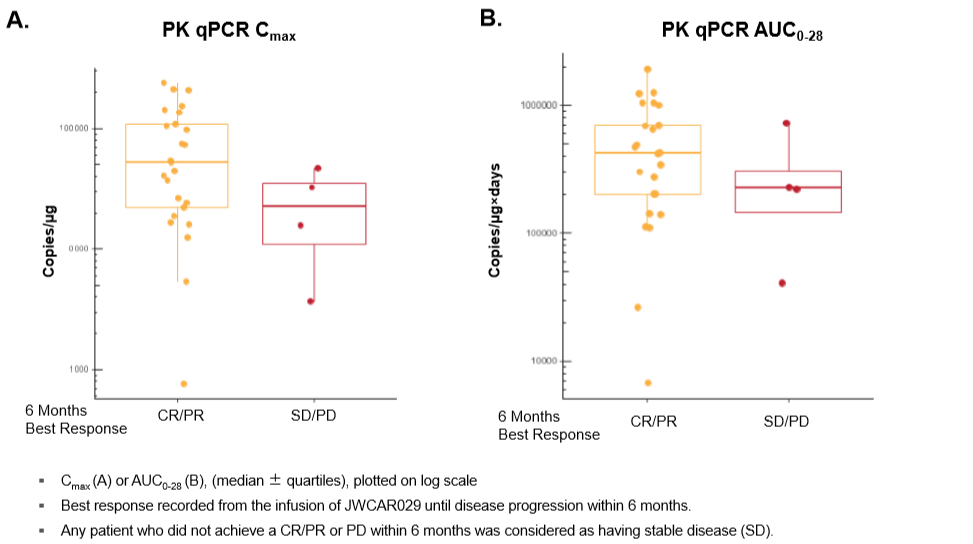
图6. 6个月时达到完全缓解(CR)/部分缓解(PR)和疾病稳定(SD)/疾病进展(PD)患者的Cmax(图A)和AUC0-28(图B)
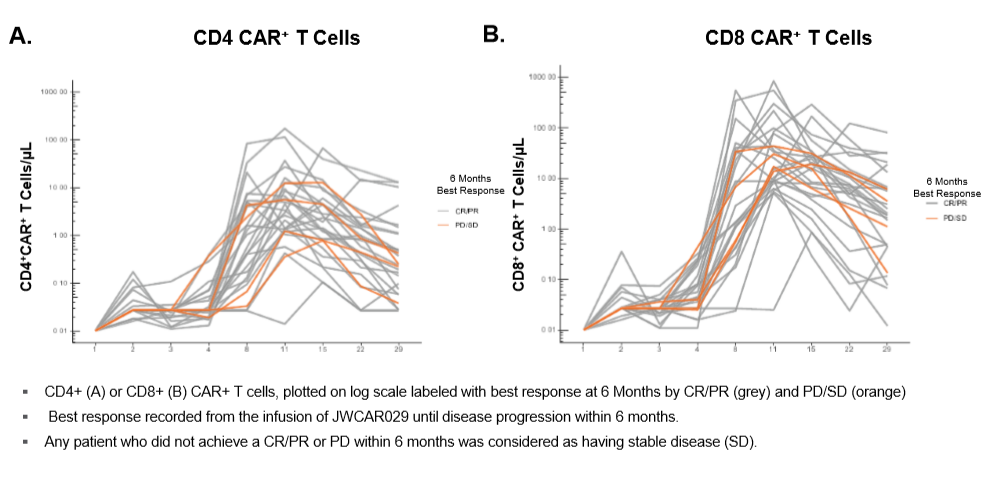
图7.CD8+CAR+ T(图B)细胞药峰浓度在完全缓解(CR)/部分缓解(PR)患者中高于CD4+CAR+ T(图A)细胞药峰浓度
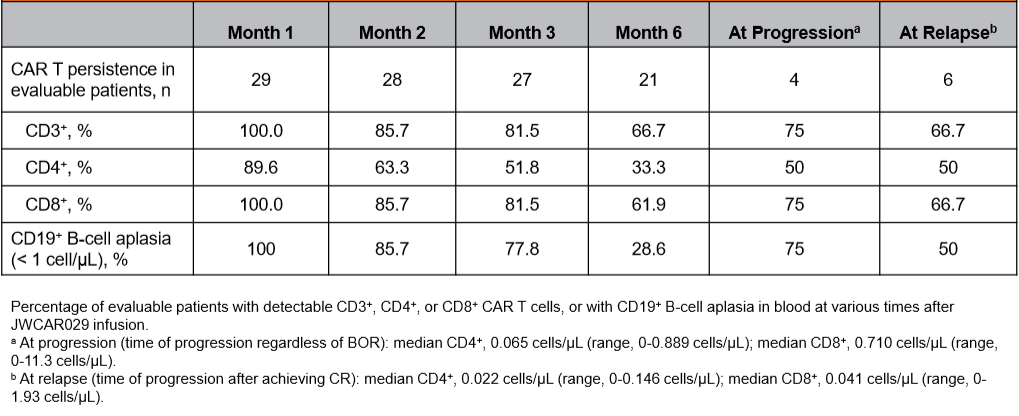
3个月时,分别有81.5%和51.8%的患者可检测到CD8+和CD4+ CAR+ T细胞,这些患者在6个月时分别有61.9%和33.3%的患者可检测到CD8+和CD4+ CAR+ T细胞。
表4. JWCAR029的长期有效性
 JWCAR029 CAR-T细胞在体内扩增可能与CRS和NT相关。在发生≥1级CRS的患者中观察到了显著性更高的Cmax和AUC0-28(中位Cmax为72916 vs 21855,P=0.007; AUC0-28为547357 vs 202452,P=0.022)。在发生≥1级NT的患者中同样观察到更高的Cmax和AUC0-28(中位Cmax为107660 vs 40391,P=0.026; AUC0-28为688181 vs 301033,P=0.077)。
JWCAR029 CAR-T细胞在体内扩增可能与CRS和NT相关。在发生≥1级CRS的患者中观察到了显著性更高的Cmax和AUC0-28(中位Cmax为72916 vs 21855,P=0.007; AUC0-28为547357 vs 202452,P=0.022)。在发生≥1级NT的患者中同样观察到更高的Cmax和AUC0-28(中位Cmax为107660 vs 40391,P=0.026; AUC0-28为688181 vs 301033,P=0.077)。
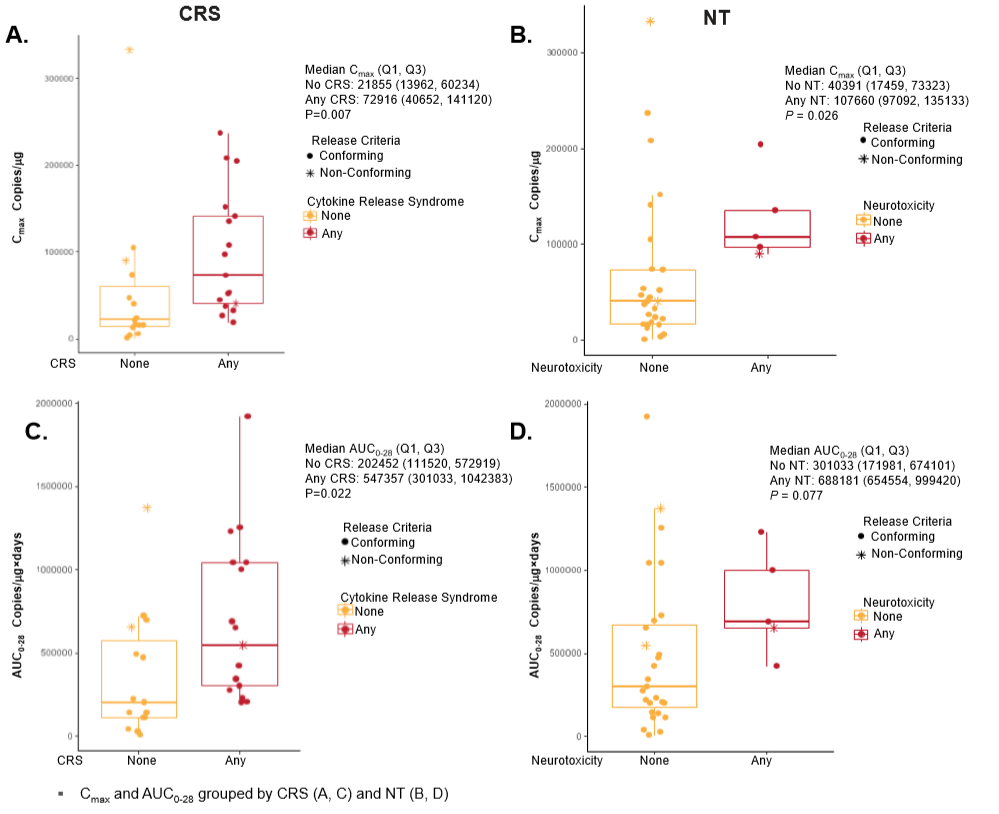
图8. 按CRS(图A、C)和NT(图B、D)分组测定的Cmax和AUC0-28
ATA
所有患者中有27.5%(8/29)的患者血浆中可检测到ATA。在检测到ATA的8例患者中,2例患者在输注CAR-T细胞之前已检测到ATA,其余6例被认为是治疗后诱导产生。治疗诱导的ATA中位出现时间为6个月。对于输注前已存在ATA的患者,其抗治疗抗体血浆中含量在6个月的中位时间有所提高。在ATA阴性组和治疗诱导产生的ATA阳性组之间,JWCAR029转基因拷贝数水平的PK无显著性差异。对于输注前已存在ATA的患者,其CAR-T细胞的扩增趋势较未出现ATA的患者更低。输注JWCAR029后,随着CD19+ B细胞的恢复,治疗诱导的ATA开始出现,这提示了ATA出现后第二次回输JWCAR029 CAR-T细胞在体内扩增(PK)可能会不如第一次回输。
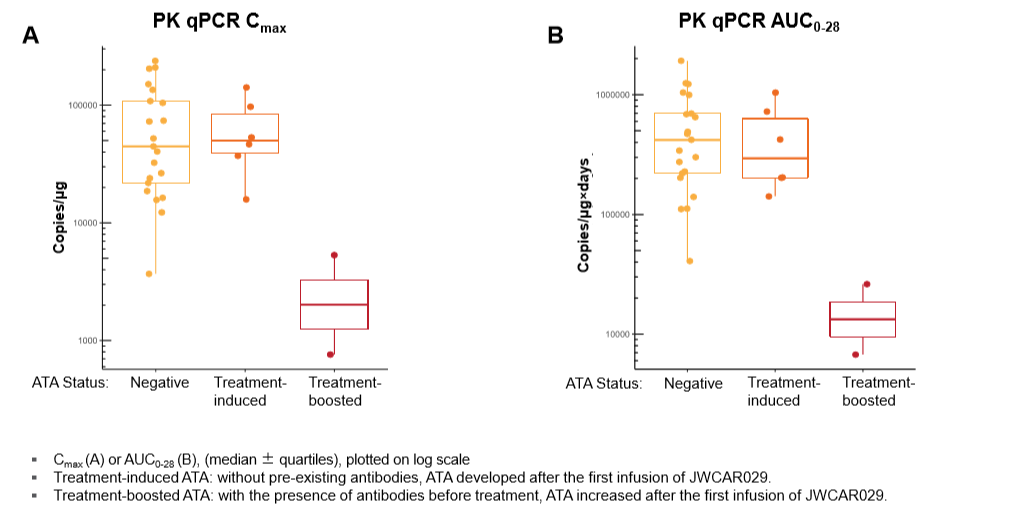
图9. 输注前已存在的ATA可能降低CAR-T细胞的Cmax(A)和AUC0-28(B)
研究结论
JWCAR029 CAR-T细胞在所有患者的外周血中均有扩增,扩增水平在不同患者和DL组中存在较大差异。CAR-T细胞在体内的扩增不随输注剂量而变化。CAR-T细胞的高扩增与CRS和NT发生率增加可能有关。CAR-T细胞的扩增趋势越大,临床疗效可能越好,但不同患者中存在广泛差异,提示患者特征和肿瘤微环境等其他因素可能会影响CAR-T疗效。JWCAR029表现出长期的持久性,可评估患者中有66.7%(14/21)在6个月时可检测到CAR-T细胞。在疾病进展或复发时,CAR-T细胞和B细胞发育不全仍存在,抗原逃逸或T细胞衰竭可能是潜在的机制,需要进一步研究。输注前已存在的ATA可能降低CAR-T细胞的扩增。
综上,在入组的32例R/R B-NHL患者、4个爬坡剂量的I期研究中,JWCAR029显示了良好的安全性和有效性;JWCAR029 CAR-T细胞在所有患者的外周血中均有扩增,并且表现出长期的持久性;临床的ORR、CR率和不良事件发生率都达到国际先进水平。未来还需要更长的随访时间和更大的样本量来进行验证,期待其Ⅱ期临床研究(NCT04089215)的结果。
1. Ying et al. Clinical Response in Relapsed/Refractory (R/R) B-NHL Treated with the CD19-Directed CAR T Cell Product JWCAR029. ASH 2019 [abstract 2876].
2. Ying et al. Cellular Kinetics and Anti-Therapeutic Antibody in Relapsed/Refractory B-NHL Patients Treated with JWCAR029. ASH 2019 [abstract 4083].
3. Abramson et al. High CR Rates in Relapsed/Refractory (R/R) Aggressive B-NHL Treated With the CD19Directed CAR T Cell Product JCAR017 (TRANSCEND NHL001). ASH 2017 [abstract 7513].
4. Crump et al. Outcomes in refractory diffuse large B-cell lymphoma: results from the international SCHOLAR-1 study. Blood, 19 October 2017.
5. Yan, Z.X., et al. Efficacy and Safety of JWCAR029 in Adult Patients with Relapsed and Refractory B-Cell Non-Hodgkin Lymphoma. ASH 2018 [abstract 4187].
6. Yan, Z.X., et al. Clinical Efficacy and Tumor Microenvironment Influence in a Dose-Escalation Study of Anti-CD19 Chimeric Antigen Receptor T Cells in Refractory B-Cell Non-Hodgkin's Lymphoma. Clinical Cancer Research 2019.











 苏公网安备32059002004080号
苏公网安备32059002004080号


