对于激素受体阳性HER2阴性乳腺癌来说,内分泌治疗是非常重要的治疗手段。虽然内分泌治疗改变了这部分患者的自然病程,但是仍有部分患者会因为内分泌耐药而出现疾病复发、进展。近年来,新药研发层出不穷,包括细胞周期蛋白依赖性激酶4/6抑制剂(CDK4/6i)、mTOR抑制剂、PI3K抑制剂、AKT抑制剂、组蛋白去乙酰化酶抑制剂等多个通路的药物用于阻断耐药通路,提高内分泌治的疗效。近日,《新英格兰医学杂志》(The New England Journal of Medicine)发表了Alpelisib用于PIK3CA突变的激素受体阳性乳腺癌患者的SLOAR-1研究成果,【肿瘤资讯】特邀河北医科大学第四医院乳腺中心马力教授为大家解读该研究。

第三军医大学博士后、博士研究生导师
河北医科大学第四医院乳腺中心副主任
中国抗癌协会乳腺癌专业委员会委员
中国医药教育协会乳腺疾病专业委员会常委
河北省肿瘤防治联合会副秘书长
河北省肿瘤防治联合会乳腺癌专业委员会 候任主任委员
中国医药教育协会乳腺病专委会河北分会 副主任委员
河北省抗癌协会乳腺癌专业委员会常委
河北省抗癌协会乳腺癌专业青年委员会主任委员

《新见》是由中华医学会肿瘤分会乳腺肿瘤青年学组主办的国际会议期刊文献解读与点评专栏。
研究背景
乳腺癌患者中70%为激素受体阳性(HR+),人体表皮生长因子受体2阴性(HER2-),其中约40%会发生PIK3CA基因突变,而PIK3CA突变会诱发PI3K的催化亚基α(p110α)发生超活化,从而增加细胞侵袭和转移能力。对于HR+/HER2-的晚期乳腺癌患者,无论是否联合CDK4/6抑制剂,内分泌治疗均是标准治疗方案。然而,内分泌治疗的获得性耐药仍然是临床中的一项挑战。 Alpelisib (BYL719),是一种口服的小分子α特异性PI3K抑制剂,可选择性地抑制p110α,抑制强度约是其它亚型的50倍。在临床前的肿瘤模型以及晚期实体肿瘤患者的I期临床试验中已经证实,PIK3CA突变的肿瘤对alpelisib敏感。在PIK3CA突变、ER+的异种移植模型中,alpelisib联合氟维司群与分别单独使用相比具有协同抗肿瘤活性。在1b期试验中,alpelisib 联合氟维司群可以使29% PIK3CA突变的晚期乳腺癌患者出现完全或部分应答,未发生PIK3CA突变的患者则无应答或仅有部分应答。Alpelisib最常见的3级或4级不良事件是高血糖和斑丘疹。Ⅲ期临床研究SOLAR-1 (Alpelisib在乳腺癌的临床研究1)主要评估α特异性PI3K抑制剂联合氟维司群在HR+/HER2-,既往接受内分泌治疗的晚期乳腺癌患者中的有效性和安全性。
研究方法
SOLAR-1是一项全球性的Ⅲ期随机、双盲、安慰剂对照试验,入组患者来自全球34个城市198个中心,根据是否携带PIK3CA突变分为两组,按照1:1随机接受alpelisib(300mg)+氟维司群(第一个周期的第1天和第15天,以及随后的28天周期的第1天,肌肉注射500mg)或安慰剂+氟维司群的治疗。每组队列中,根据患者是否有肺转移或肝转移或既往是否接受CDK4/6抑制剂进行分层。患者停药的指征包括出现疾病进展,出现不可耐受的毒副作用,要求退出试验,失访或者死亡。出现不能耐受的毒副作用时alpelisib允许减量(每日剂量300mg减量至250mg再到200mg)。不允许氟维司群减量,停用alpelisib或安慰剂的患者可以继续使用氟维司群。
入组标准:HR+/HER2-绝经后女性或男性晚期乳腺癌患者,在新辅助或辅助或者疾病出现进展后正在使用或曾经使用过芳香酶抑制剂,研究者判定可以继续应用内分泌治疗。根据RECIST 1.1标准,患者至少有1处可测量病灶或至少1处溶骨性病变,ECOG评分0或1分,器官及骨髓功能正常。
排除标准:既往接受过卵巢放射治疗或使用促黄体生成素释放激素激动剂诱导卵巢抑制的绝经后患者;疾病出现进展后接受过化疗;接受过氟维司群治疗;接受过PI3K、AKT或mTOR抑制剂治疗;炎性乳腺癌;不可控制的中枢神经系统转移;随机化之前3年内并发其它癌症(基底细胞癌或鳞状细胞癌、非黑色素瘤性皮肤癌或宫颈癌得到充分治疗的除外);1型糖尿病或不可控制的2型糖尿病或目前存在肺炎的患者。
主要研究终点为携带PIK3CA突变患者的无进展生存期(PFS)。关键的次要研究终点为PIK3CA突变患者的总生存期。其它的次要终点包括不携带PIK3CA突变患者的PFS以及总生存期,根据循环肿瘤细胞水平判定的PFS(但在本研究结果中未报道),总体缓解率,临床获益率以及安全性。
随访:随机前4周进行影像学评估(CT或MRI),开始治疗后的18个月内每8周评估一次,之后每12周评估一次直至疾病进展或因为任何原因退出。筛查时需进行生命体征、血液学以及生化检测,第一个8周内每2周随访一次,之后每4周随访一次。持续记录不良事件,直到最后一次试验治疗后的30天。
研究结果
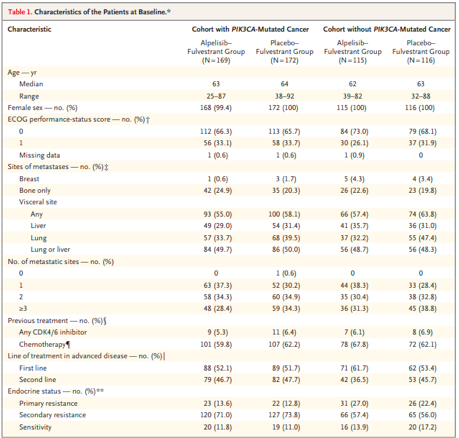
2015年7月26日—2017年7月21日,共有1244名患者接受PIK3CA突变检测,1173例患者可获得准确结果。最终共有572例患者接受随机分组,341例患者携带PIK3CA突变,其中169例患者接受alpelisib联合氟维司群治疗,172例患者接受安慰剂联合氟维司群治疗。在携带PIK3CA突变队列中,两组患者基线特征均衡(表1)。患者的中位年龄63岁,170例(49.9%)患者发生肺或肝转移,77例(22.6%)患者仅有骨转移,20例(5.9%)患者既往接受过CDK4/6抑制剂的治疗。不携带PIK3CA突变队列中的患者中的随机分组特征见表1。
表1 患者的临床基线特征
中位随访20个月,携带PIK3CA突变队列中,alpelisib+氟维司群组中位PFS为11.0个月(95%CI, 7.5~14.5),安慰剂+氟维司群组为5.7个月(95% CI,3.7~7.4) (HR,0.65;95% CI,0.50~0.85,P<0.001,图1A)。12个月时,alpelisib+氟维司群组PFS患者的比例为46.3%,安慰剂+氟维司群组为32.9%。独立评审委员会的评估结果显示,接受alpelisib+氟维司群治疗的85名患者中位PFS为11.1个月(95% CI,7.3~16.8),接受alpelisib+氟维司群治疗的88名患者中位PFS为3.7个月(95% CI, 2.1~5.6)(HR,0.48;95% CI,0.32~0.71)。在预先设定的亚组中,alpelisib+氟维司群治疗均有PFS的获益(图2)。
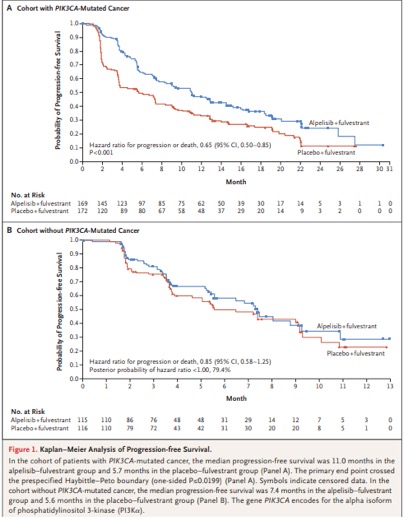
图1根据有无携带PIK3CA突变两组患者的PFS KM曲线分析
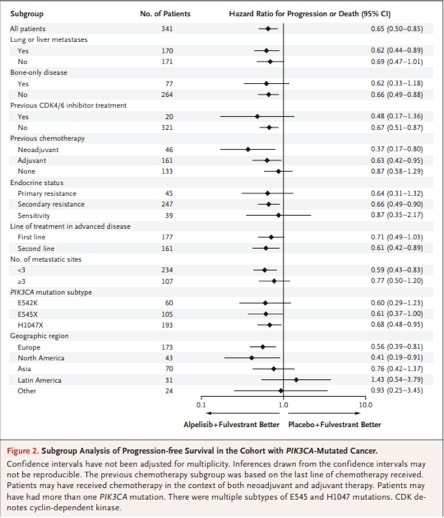
图2携带PIK3CA突变患者PFS亚组分析
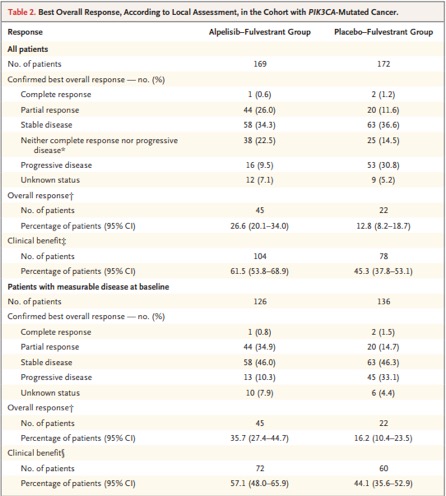
在携带PIK3CA突变队列中,alpelisib+氟维司群组的总体应答率高于安慰剂+氟维司群组(26.6% vs. 12.8%);较高的临床获益率同样在alpelisib+氟维司群组(61.5% vs. 45.3%)(表2)。有可测量病灶的患者中,alpelisib+氟维司群组和安慰剂+氟维司群组的总体缓解率分别为35.7%和16.2%。临床获益患者的比例分别为57.1%和44.1%(表2)。在未携带PIK3CA突变队列中,alpelisib+氟维司群组和安慰剂+氟维司群组患者的中位PFS分别为7.4个月(95% CI,5.4 ~9.3)和5.6个月(95% CI,3.9~9.1)(HR,0.85;95% CI, 0.58~1.25;校正后的HR<1.00, 79.4%)(图1B)。随访12个月时,alpelisib+氟维司群组PFS患者的比例为28.4%,安慰剂+氟维司群组为22.2%。
表2 携带PIK3CA突变患者的总体缓解率
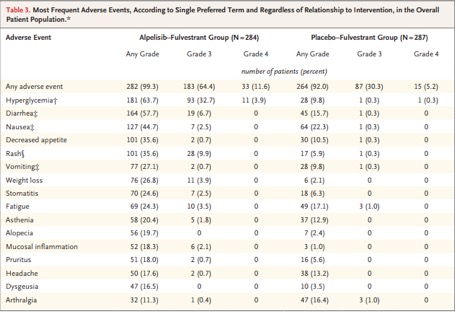
安全性方面,总体不良事件的发生率为35%。在alpelisib+氟维司群组和安慰剂+氟维司群组的不良事件主要有高血糖(63.7%和9.8%),腹泻(57.7%和15.7%),恶心(44.7%和22.3%),食欲下降(35.6%和10.5%)和皮疹(35.6%和5.9%)或斑丘疹(14.1%和1.7%)(表3)。两组至少5%的患者发生3或4级不良事件,alpelisib+氟维司群组和安慰剂+氟维司群组最常见的3或4级不良事件有高血糖(36.6%和0.7%),皮疹(9.9%和0.3%),斑丘疹(8.8%和0.3%)和腹泻(6.7%和0.3%)。因不良事件导致alpelisib和安慰剂停药的患者在两组分别为71例(25.0%)和12例 (4.2%)。导致alpelisib停药的主要不良反应有高血糖(18例,6.3%)和皮疹(9例,3.2%)。安慰剂组无因为高血糖和皮疹而停药的患者。alpelisib和安慰剂组分别观察到99例(34.9%)和48例(16.7%)严重不良事件。试验过程中共发生19例死亡事件(包括在干预后30天的安全期内),alpelisib+氟维司群组7例死亡(2.5%),5例死于乳腺癌,其它死因为心肺骤停和第二原发癌。安慰剂+氟维司群组12例死亡(4.2%),8例患者死于乳腺癌。
表3 总体人群常见的不良反应
结论
这项Ⅲ期临床试验结果显示,在HR阳性、HER2阴性、PIK3CA突变,既往接受过内分泌治疗进展的晚期乳腺癌患者中,相比较安慰剂联合氟维司群,alpelisib联合氟维司群可显著延长患者PFS并且有更高的总反应率。alpelisib主要的不良反应为高血糖,皮疹以及腹泻。
马力教授点评
SOLAR-1研究结果最早在2018年圣安东尼奥乳腺癌大会(San Antonio Breast Cancer Symposium,SABCS)上发布,显示在激素受体阳性,HER2阴性、PIK3CA突变,并且内分泌耐药的患者中应用口服小分子α特异性PI3K抑制剂alpelisib联合氟维司群可延长患者PFS达11.0个月,为HR阳性既往内分泌耐药并且有PIK3CA突变的患者提供了一个新的治疗方案。
内分泌治疗是激素受体阳性乳腺癌的主要治疗手段。在无内脏危象的HR阳性晚期乳腺癌患者中,首选内分泌治疗已成为专家共识,随着内分泌治疗的广泛应用,耐药成为亟待解决的问题。内分泌治疗耐药主要分为原发性和继发性耐药。原发性耐药定义为辅助内分泌治疗2年内或者晚期一线内分泌治疗不超过6个月即出现肿瘤复发转移或进展。继发性耐药定义为辅助内分泌治疗超过2年或者结束后1年内出现复发转移,或者一线内分泌治疗超过6个月出现肿瘤进展。
如何进一步提高内分泌治疗疗效、克服内分泌耐药,已成为国内外研究的热点。纵观国内外关于内分泌耐药的相关研究,主要可以总结为以下几方面:ESR1基因的核心突变;上游激活,如EGFR/HER2/GFR通路的激活;旁路出错,主要为PI3K/AKT/mTOR通路;下游异常:CDK4/6细胞周期通路发生异常。
在针对以上几种主要耐药机制中进行的靶向研究药物有很多取得了可喜的结果,如针对ESR1突变的患者中,含氟维司群的治疗优于传统的单药AI的治疗。2016年ESMO会议上一项全球性三期、随机、双盲的FALCON研究,头对头地比较了氟维司群与阿那曲唑在绝经后激素受体阳性乳腺癌患者中一线内分泌治疗的疗效,结果显示氟维司群组患者中位PFS达到16.6个月。
近几年关于CDK4/6抑制剂方面的报道非常多,成绩也很喜人。PALOMA系列的哌柏西利(Palbociclib),MONALEESA系列研究的Ribociclib以及MONARCH系列研究的Abemaciclib三个主要的CDK4/6抑制剂在无论是在一线还是后线联合内分泌治疗都取得了较好阳性的结果。一线治疗中CDK4/6抑制剂联合内分泌治疗和单药内分泌相比PFS都延长了近2倍的时间;在二线治疗中联合氟维司群,针对既往AI治疗失败的患者PFS时间也能达到11个月,最长的可达18个月。2019刚刚结束的ASCO会议上MOMALEESA-7试验(摘要号:LBA1008)公布了绝经前患者OS的获益,这是目前唯一一项公布OS结果的单纯针对未绝经一线患者的Ⅲ期临床试验,对照组和实验组的OS分别为40.9个月和尚未达到(NR),P<0.01。这是有史以来第一个得到OS统计学获益的CDK4/6抑制剂一线治疗研究,这将对我们的临床实践将产生非常重要的影响。目前的研究结果显示CDK4/6抑制剂联合内分泌治疗中不管是一线还是二线都已取得了非常好的成绩,也成为国内外各个指南共识推荐的对晚期HR+/HER2-乳腺癌的标准一线治疗方案。
但即便在CDK4/6抑制剂取得良好效果的同时,仍然有一部分患者出现耐药,那么在后CDK4/6抑制剂时代研究比较火的就是PI3K/AKT/mTOR通路,而该通路的主要研究靶点为mTOR抑制剂,而明确与内分泌耐药相关的研究主要有两个,BOLERO-2是其中之一,这是一项Ⅲ期临床研究,纳入724例NSAI治疗失败后的绝经后ER+晚期乳腺癌患者,2:1随机接受依维莫司+依西美坦或单纯依西美坦治疗,主要终点为PFS。结果显示,联合治疗组可显着延长中位PFS,分别为6.9个月和2.8个月(HR,0.43;95%CI:0.35~0.54;P<0.001)。
除了mTOR抑制剂,但在此通路上,PI3K抑制剂的研究也进展迅速,多个PI3K抑制剂已经进入临床研究。BELLE-2研究是一项随机、双盲、安慰剂对照的III期研究。入组患者1:1随机分配接受buparlisib(100mg/天,连续用药,28天为1个治疗周期)或安慰剂联合氟维司群治疗AI治疗进展的HR+/HER2-绝经后局部晚期或转移性乳腺癌。至数据截止时,bupalisib组和安慰剂组的OS分别为33.2和30.4个月,但无统计学差异。在PI3K活化状态已知的患者中,Bupalisib组和安慰剂组患者的mOS分别为30.9和28.9个月,差异也无统计学意义(HR 0.91;95%CI 0.75~1.09,P=0.144)。总之,在内分泌耐药,HR+/HER2-的晚期乳腺癌患者中,Buparlisib联合氟维司群显著改善总体人群和PI3K通路活化状态已知患者的PFS。在最终OS分析中,总体人群和PI3K通路活化状态已知人群中均观察到Buparlisib联合氟维司群组OS更优的趋势,分别降低13%和9%的死亡风险,然而,这些差异均无统计学意义。虽然Buparlisib的不良事件可管理,但安全性还是令人担忧,也让这一药物的后续研究充满挑战,可以说,Buparlisib的研究以失败告终。
另一项名为PEGGY的Ⅱ期临床研究,比较一种口服的选择性Ⅰ类PI3K抑制剂Pictilisib联合紫杉醇或单用紫杉醇治疗局部复发或晚期HER2阴性、HR阳性乳腺癌。主要终点是ITT人群和PIK3CA突变人群的无进展生存(PFS)。结果显示在ITT人群,中位PFS在Pictilisib联合紫杉醇组为8.2个月,单药紫杉醇组为7.8个月,两者差异较小,无统计学意义。在PIK3CA突变患者中,Pictilisib联合紫杉醇组的PFS为7.3个月,而单药紫杉醇组为5.8个月,差异无统计学意义(P=0.88)。在ITT人群中,Pictilisib联合紫杉醇组的ORR为22.0%,而单药紫杉醇组为19.6%,两者接近,同样无统计学差异。并且在安全性方面,Pictilisib联合紫杉醇组患者中,≥3级不良事件、严重AE及因AE减量或中断治疗的发生率更高。可以说PI3K抑制剂的开发可谓困难重重,大都是因为其疗效有限和一些不良事件的发生而导致研究失败。
在该研究中,我们可以看到在HR阳性,HER2阴性,内分泌治疗耐药并且携带PIK3CA突变的乳腺癌患者中,接受α特异性PI3K抑制剂alpelisib联合氟维司群治疗比氟维司群单药治疗PFS达到11个月,获益大约5.3个月,几乎延长了近两倍,并且有统计学差异,这样一项有临床意义的PFS 延长对于临床实践是非常重要的结果。可以说这是第一个PI3K抑制剂取得阳性结果的试验。alpelisib的不良事件多数为轻度至中度,主要为高血糖和斑丘疹,可以通过减少剂量或停药来控制,可以说患者的耐受性达到了预期的结果。
但是该试验也有其局限性,我们看到在SOLAR-1研究中纳入的人群全部是内分泌治疗耐药患者,只有不到10%的患者是CDK4/6抑制剂失败,期望在未来的研究中纳入更多CDK4/6抑制剂失败的患者,为内分泌治疗耐药的患者提供更多的治疗选择。
André F, Ciruelos E, Rubovszky G, et al. Alpelisib for -Mutated, Hormone Receptor-Positive Advanced Breast Cancer.[J] .N. Engl. J. Med., 2019, 380: 1929-1940.
精彩回顾












 苏公网安备32059002004080号
苏公网安备32059002004080号


