泌尿系统肿瘤缺乏有效靶向治疗,免疫治疗初显成效,但有效率有待提高。明确肿瘤的基因组学特征,可以探寻潜在的治疗靶点。在刚刚落幕的ASCO大会上,多项研究采用全面基因组测序(CGP检测)检测泌尿系统肿瘤的基因图谱,探寻可能从靶向或免疫治疗中获益的人群。
ABS 4581采用CGP检测上泌尿道(UTUC)和膀胱尿路上皮癌(BUC),探寻潜在治疗靶点
背景
探寻UTUC和BUC的潜在治疗靶点,有望给这类患者带来新的治疗策略。
方法
对49例UTUC和1984例BUC的组织标本进行CGP检测(315个癌症相关基因和28个癌症常见融合基因内含子)。基因变异(GA)形式包括碱基置换、插入缺失、拷贝数变异和重排。评估1.14Mb测序DNA的肿瘤突变负荷(TMB)。同时采用FoundationOne Liquid(70个癌症相关基因)对cfDNA进行检测。根据ESMO临床可靶向分子靶点评估量表(ESCAT)评估潜在可靶向GA。
结果
39%的UC携带≥1个1~2类可能从获批或正在研究的靶向药物中获益的GA;29%的患者携带1个3类GA,强烈支持其参加临床试验。1%的患者(UTUC 0.6% vs BUC 1.1%)检测到非FGFR3激酶融合,其中BRAF/RAF1融合占0.5%。2%(49/2463)的患者检测到BRAF突变/融合,这些变异与FGFR3不共存(P=0.002)。
原发灶和转移灶中TMB-H(≥20 mut/Mb)/MSI-H患者比例无显著差异;但UTUC相比于BUC,MSI-H的比例显著更高(3.4% vs 0.77%,所有患者均为TMB-H型)。排除MSI-H患者,UTUC中位TMB低于BUC(4.35 mut/Mb vs 6.96 mut/Mb)。UTUC vs BUC,FGFR3 GA(26% vs 19%,P<0.05),且特定的短片段变异(SV)(7.3% vs 3.0%)发生率也更高,主要归因于这些变异在肾盂UC中变异率显著高于尿路UC(10.1% vs 1.8%,P<0.05)。BUC中RB1 GA发生率高于UTUC(21% vs 7.8%,P<0.001)。
表1. BUC和UTUC临床和基因变异特征对比
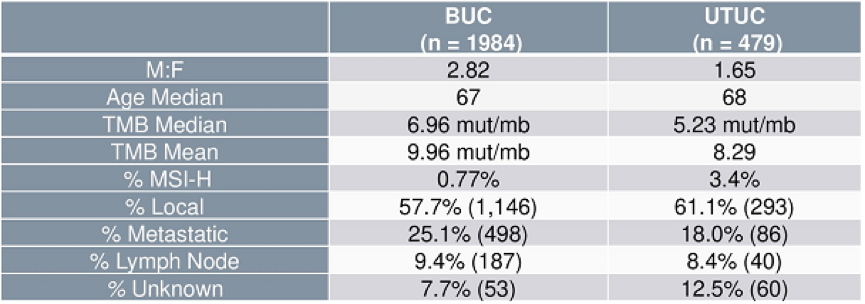

图1. 根据活检部位对比BUC和UTUC的TMB
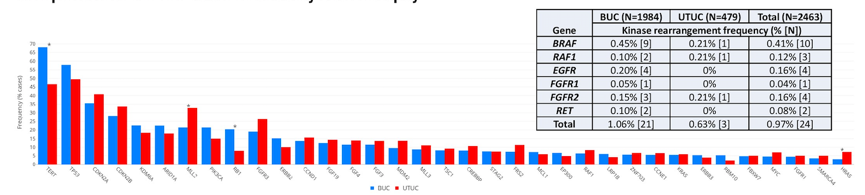
图2. 对比BUC和UTUC的基因变异谱
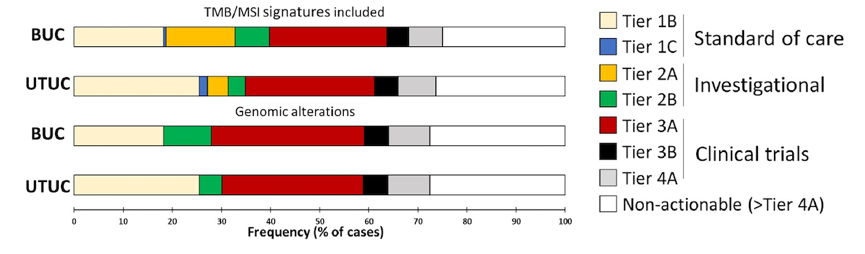
图3. BUC和UTUC中检测到的可靶向基因变异
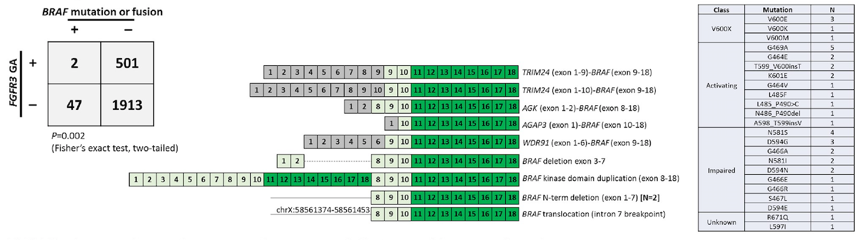
图4. BRAF融合和突变组成了潜在可靶向基因变异亚组
对2463例非配对组织和93例可检测到ctDNA的血浆标本突变谱进行分析,评估FGFR3突变率,组织和血浆标本中FGFR3突变率无显著差异。对比21例有配对组织和血浆标本突变谱,以组织检测作为金标准,评估组织和血浆标本的阳性一致性(PPA):可靶向FGFR3突变频率和分布相似;标本采集间隔时间的差异(<90天,<180天和≥180天)影响两者基因突变频率的一致性。
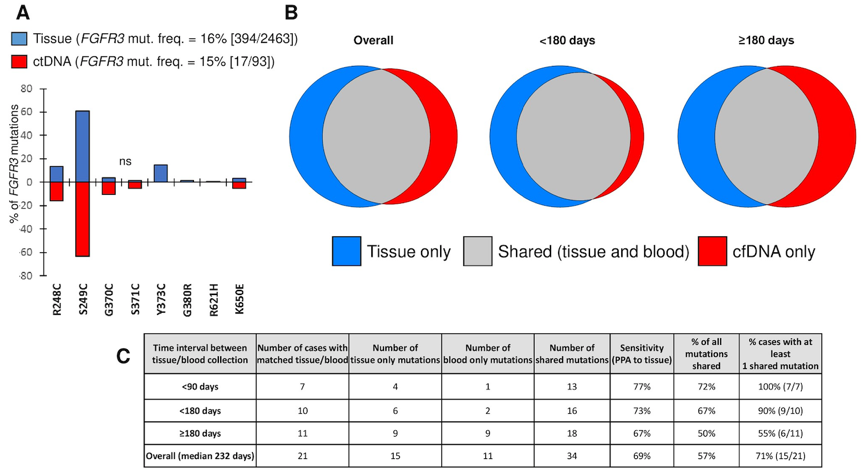
图5. 组织和血浆标本的突变谱对比
小结
50%UC携带可靶向变异,可能从免疫、靶向或两者联合治疗中获益。HRAS突变主要见于肾盂UC,提示后续应该评估不同解剖起源部位的基因变异模式。这一研究结果强烈支持转移性UC应在开始系统性治疗前常规进行CGP检测。
ABS 4545对EGFR突变型UC患者进行分析,揭示出不同对突变谱
背景
研究旨在分析晚期UTUC和BUC的基因突变谱,评估可靶向EGFR突变。
方法
对2402例BUC和407例UTUC的组织标本进行CGP检测,评估常见的4种GA和TMB、MSI。
结果
分别在17例UTUC和93例BUC中检测到EGFR突变。BUC患者的中位TMB显著更高(5.2mut/Mb vs 7.8 mut/Mb;P=0.046),但两个亚组中MSI-H患者比例无显著差异(表1)。
表1. 对比EGFR野生型、突变和exon20插入突变患者的年龄、性别、TMB、MSI和有意义共存变异
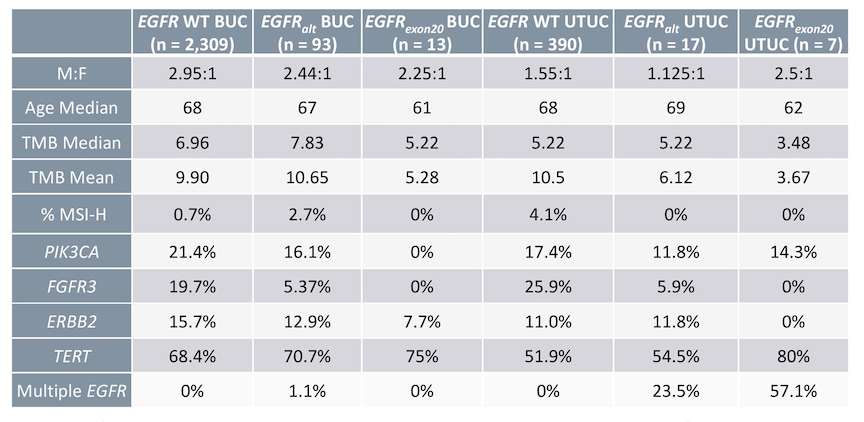
在UTUC和BUC中,EGFR扩增是最常见的变异,分别占76%(13/17)和61%(57/93)。大多数EGFR SV为EGFR exon20ins,发生率在UTUC中高于BUC(7/17,41% vs 13/93,14%;P=0.01)。
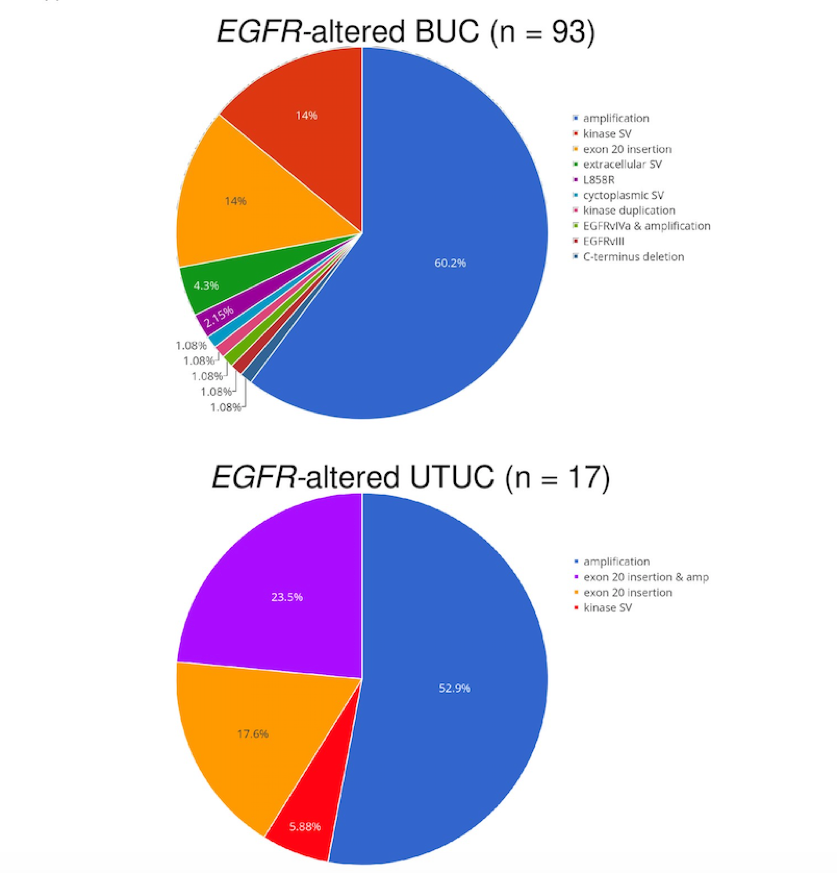
图1. BUC和UTUC患者EGFR不同突变模式
BUC中,仅2.2%(2/93)的EGFR突变为L858R突变,未观察到EGFR exon19del(0/93);UTUC中两类活化变异均未观察到。
表2. 相比于NSCLC,UC具有独特的EGFR活化突变
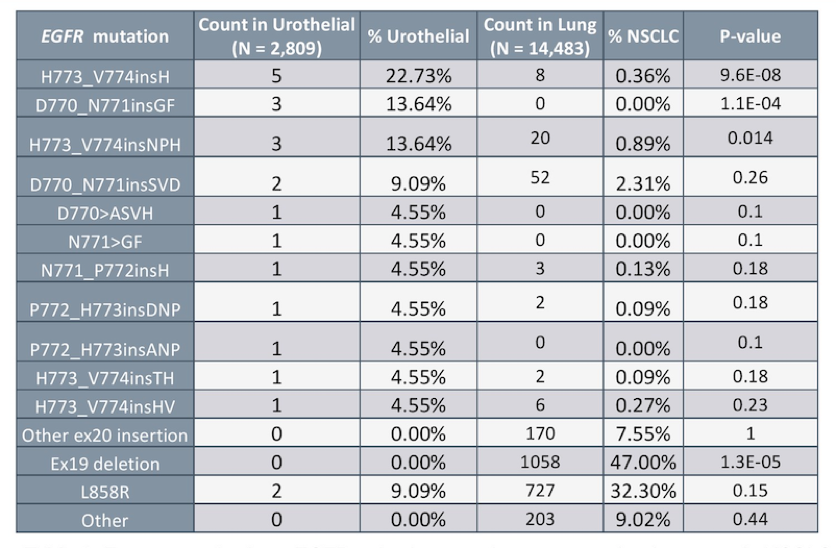
EGFR变异的UTUC和BUC中,TERT(55% vs 71%)和TP53(59% vs 74%)是最常见突变基因。对比其他EGFR变异,EGFR exon20ins与UC中其他常见突变互斥更明显:TP53(UTUC EGFR exon20ins vs EGFR其他变异:0% vs 100%;P<0.001;BUC EGFR exon20ins vs EGFR其他变异:0% vs 86%;P<0.001);PIK3CA(14% vs 10%;0% vs 19%);RAF1(0% vs 10%;0% vs 16%),或FGFR3(0% vs 10%;0% vs 6.3%)。
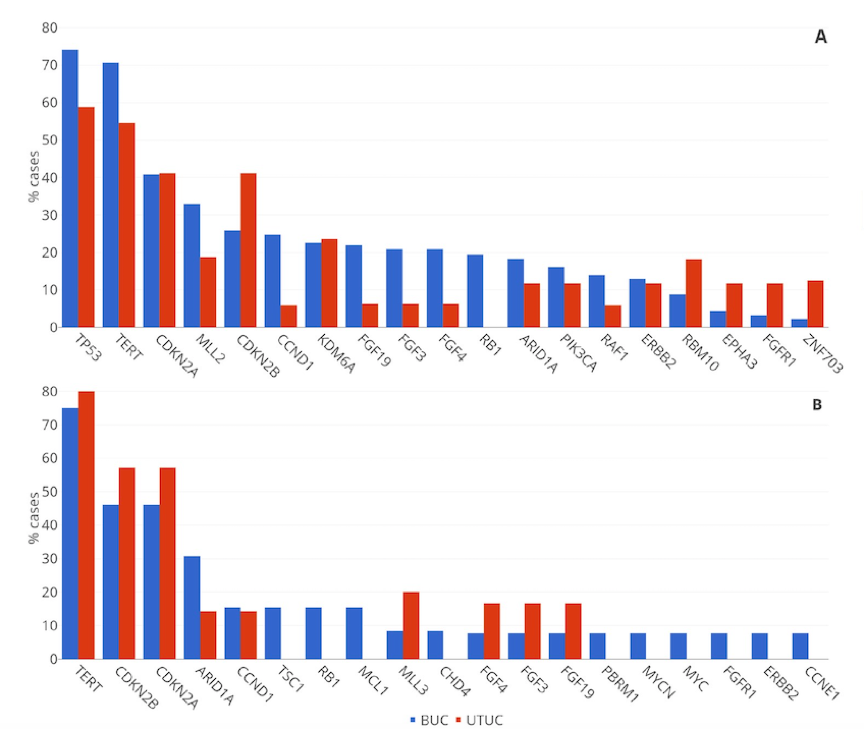
图2. EGFR突变UC(A)和EGFR exon20ins突变UC共存变异基因分析
小结
UC具有独特的EGFR变异模式。相比于NSCLC,EGFR exon20ins的UC变异模式不同,可以考虑接受相应的EGFR TKI治疗,如poziotinib、TAK-788或Hsp90抑制剂luminespib。
ABS 4535肌层浸润的膀胱癌(MIBC)鳞状细胞组织亚型(SCC-VH):从多个数据库中进行全面的临床、基因和治疗评估
研究汇总多个临床和基因数据库,检测SCC基因谱,探索其对新辅助化疗疗效预测作用,并评估SCC-VH患者接受帕博利珠单抗新辅助治疗疗效。
方法
纳入San Raffaele医院泌尿系统疾病研究所(URI,n=2209)和回顾性全球浸润性/晚期尿路上皮癌研究(RISC,n=2598)中接受膀胱切除非转移性MIBC。同时纳入1984例UC作为外部队列,97例为SCC,在临床实践中接受了CGP检测。
结果
1. 不同组织学亚型比例
据URI/RISC数据库中组织亚型将其分类:UC最常见,占78%;其余亚型可分为6类,包括鳞癌、腺癌、微乳头型、其他分化型、神经内分泌型和肉瘤样组织亚型。
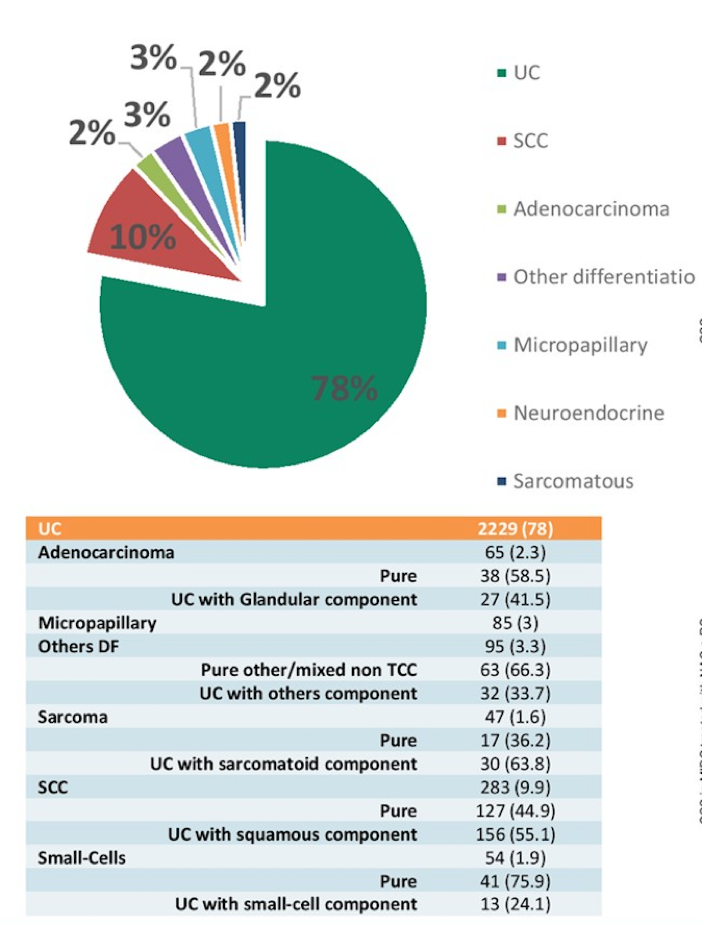
图1. 不同组织学亚型患者比例
2. 新辅助治疗的癌症特异性生存率(CSS)
以UC作对照,分析6种组织学亚型接受新辅助治疗的CSS。单因素分析中,鳞癌对比UC显示出显著更差的CSS率:顺铂为基础的方案(33个月 vs NA个月,P=0.009),其他方案(5个月 vs 49个月,P<0.0001);多因素分析观察到相似的结果(HR=2.1;95%CI:1.1~4.2,P=0.03)。
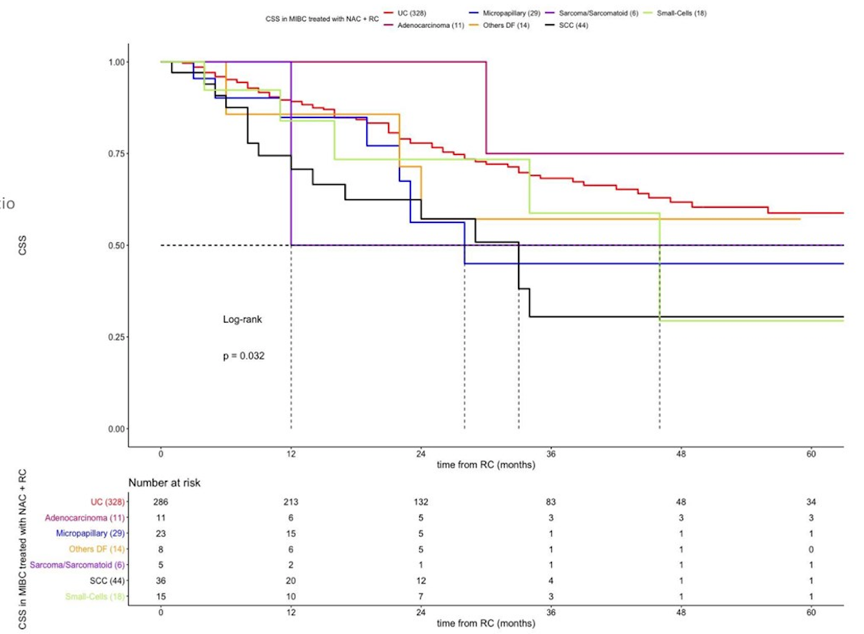
图2. 接受新辅助治疗患者,根据组织学亚型不同分析CSS率
3. 膀胱鳞癌基因特征分析
1984例UC和97例SCC接受FoundationOne检测,临床有意义变异多见于PIK3CA(42.3%)、CCND1(15.5%)、PTEN(9.3%)、FGFR3(9.3%)和ERBB2(6.2%)。分别有27%和14%的患者TMB>10 mut/Mb和>20mut/Mb;UC中相应比例分别为37%(730/1984)和13%(255/1984)。对比SCC和UC,最有意义的基因变异差异见于CDKN2A、PI3KCA和NFE2L2,在SCC中更常见。
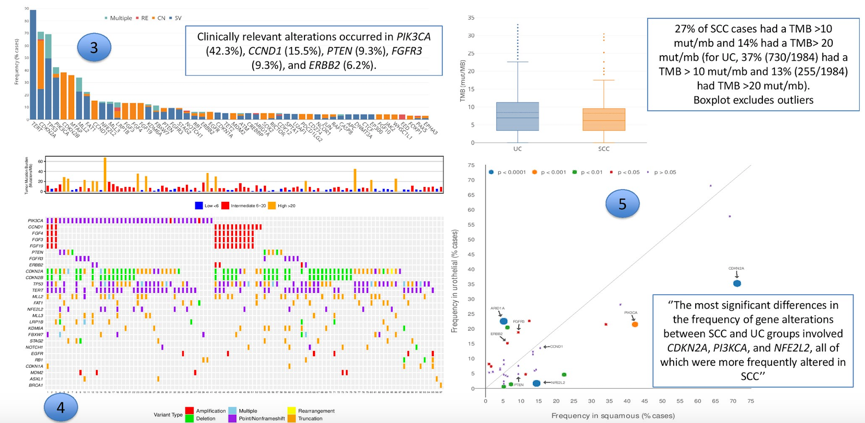
图3. 膀胱鳞癌患者的基因特征
4. SCC接受新辅助免疫治疗的疗效
PURE-01研究在cT2-3bN0M0膀胱癌(以UC为主)中评估帕博利珠单抗新辅助治疗。研究方案近期修改允许纳入不同组织学亚型患者,如SCC(n=12)。在SCC中,4例取得pT0(33.3%),10例取得pT≤1(83.3%)。
小结
对比UC,SCC接受新辅助化疗的CSS最差,基因组学研究提示其可能从靶向免疫治疗中获益。PURE-01研究显示SCC对新辅助免疫治疗非常敏感。
总结
3项研究对大样本量的泌尿系统肿瘤进行CGP检测,发现潜在可靶向基因变异,并评估TMB和MSI状态,为探寻靶向或免疫治疗优势人群提供重要信息。

中国临床肿瘤学会前列腺癌专家委员会秘书长
2019年复旦大学青年五四奖章
上海市卫健委青年五四奖章获得者
入选2018年上海市“医苑新星”杰出青年医学人才
入选第七届复旦大学十大医务青年
入选第三批复旦大学卓学人才计划
入选2015年上海市青年科技启明星计划
入选2018年复旦大学附属肿瘤医院院级杰出青年计划
[1]Comprehensive genomic profiling (CGP) of upper-tract (UTUC) and bladder (BUC) urothelial carcinoma reveals opportunities for therapeutic and biomarker development. 2019 ASCO. Abs 4581.
[2] Analysis of EGFR mutant urothelial carcinoma (UC) reveals distinct mutational
landscape. 2019 ASCO. Abs 4545.
[3] Squamous-cell carcinoma variant histology (SCC-VH) in muscle-invasive bladder cancer (MIBC): A comprehensive clinical, genomic, and therapeutic assessment from multiple datasets. 2019 ASCO. Abs 4535.












 苏公网安备32059002004080号
苏公网安备32059002004080号


