
第55例
早期乳腺癌患者中30%~40%可发展为晚期乳腺癌,5年生存率约20%。ABC患者的总体中位生存期为2~3年,不同分子亚型的情况有所不同。对于HER2阳性晚期乳腺癌患者,抗HER2治疗显著延长了HER2阳性乳腺癌生存时间。本文通过回顾一例乳腺导管内原位癌(DCIS)在辅助治疗阶段无需使用抗HER2治疗而在复发转移后采用不同机制靶向治疗药物联合使用并长期获益的病例,介绍目前有关该类患者的临床治疗思路。

鞍山市肿瘤医院化疗四病区主任
中国医药教育协会乳腺疾病专业委员会委员
辽宁省抗癌协会肿瘤标志委员会常委康复与姑息治疗专业委员会委员
中国老年学和老年医学学会肿瘤康复分会委员
辽宁省细胞生物学学会胸部肿瘤分会会员
中国研究型医院学会精准医学与肿瘤MDT专业委员会乳腺学组委员

鞍山市肿瘤医院
中国抗癌协会肿瘤标志委员会委员
北京肿瘤防治研究会乳腺癌分委会会员
辽宁省细胞生物学学会肿瘤精准医疗与大数据管理专业委员会会员
病史回顾
患者女性,57岁,ECOG 0分,既往史无特殊,否认家族史。2013年5月7日,全麻下行右乳腺癌根治术,术后病理:(右乳)导管内癌(中、高级别,部分粉刺癌),局灶间质浸润,肿物大小2cm×1.5cm×1.5cm,腋窝淋巴结转移(0/10)。免疫组:ER(-),PR(-),HER2(3+),Ki-67:20%。病理会诊:(右乳腺)导管原位癌(高级别)。免疫组化:P63(+),Actin(SM)(+),ER(-),PR(-),HER2(3+)。术后诊断:右侧乳腺癌,右测乳腺癌根治术后,pTispN0M0。因为患者诊断为导管内癌,处于早期,患者出于经济压力,决定放弃曲妥珠单抗辅助治疗,遂予以多西他赛+环磷酰胺(DC)方案辅助治疗4周期。
第一次复发转移
2014年8月15日,患者随访时发现肝脏转移。无病生存期(disease-free survival,DFS)约15个月。彩超下行肝脏病灶穿刺,病理回报:癌,考虑乳腺来源,ER(25%+),PR(15%+),HER2(3+),Ki-67:30%,GCDFP-15(+),Mammaglobin(-)。诊断:右侧乳腺癌术后,多发肝转移,rT0N0M1,Ⅳ期。治疗:曲妥珠单抗+长春瑞滨+卡培他滨(H+NX)方案化疗8周期,综合疗效评价为完全缓解(complete response,CR)。后续予以曲妥珠单抗+卡培他滨(H+X)维持治疗至2016年9月。
第二次复发转移
2016年9月,上腹部MRI检查发现多发肝转移(图1)。彩超:右锁骨上可见2.1cm×1.7cm淋巴结,形态略不规整,边界欠清,内呈不均匀低回声,提示右锁骨上淋巴结肿大。
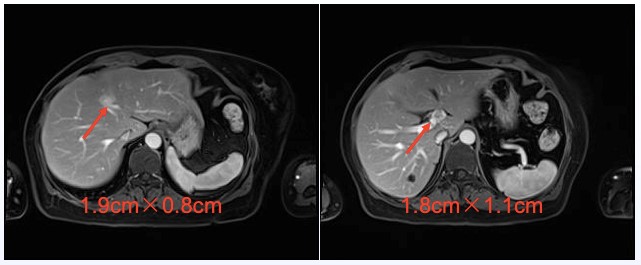
图1 上腹部MRI多发肝转移
肿瘤无进展生存时间(progression-free survival, PFS)1达25个月。临床诊断:右乳癌术后rT0N0M1,IV期,肝转移、右锁骨上淋巴结转移。治疗方案:曲妥珠单抗+吉西他滨(GH)方案治疗2周期。不良反应:II度骨髓抑制、I度胃肠道反应。
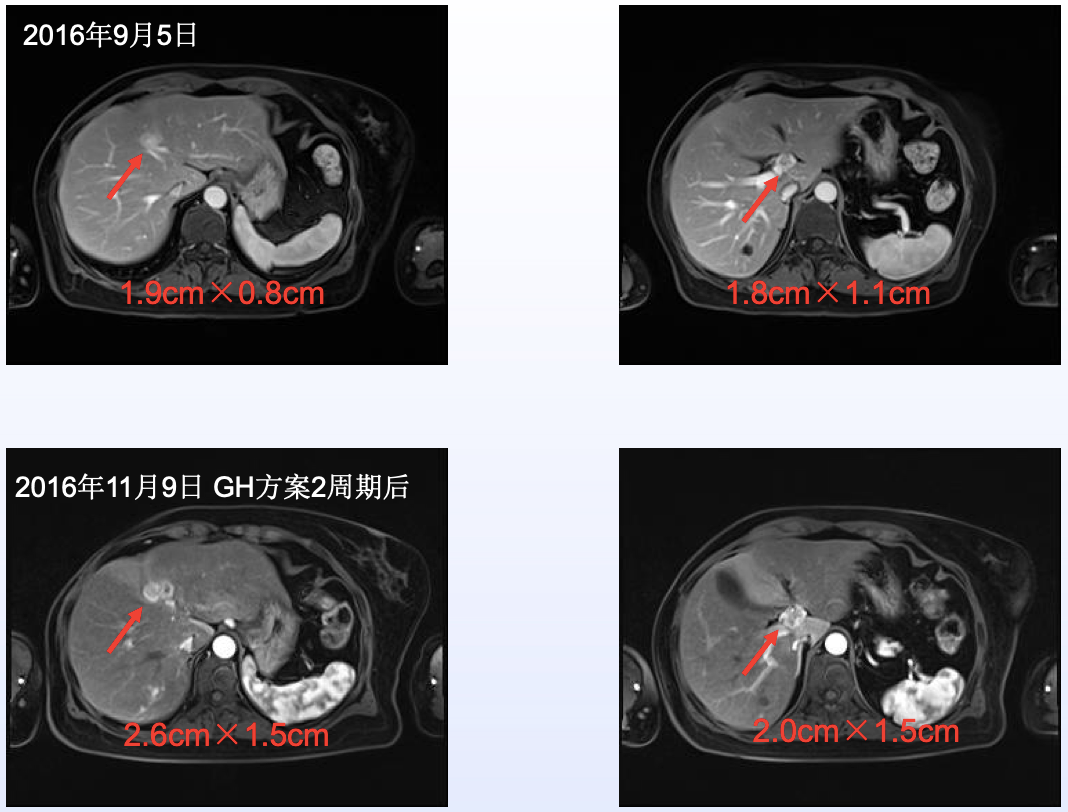
图2上腹部MRI对照
GH方案治疗2周期后,上腹部MRI(图2)和彩超检查(表1),综合疗效评价疾病进展(progressive disease,PD)。
2016年11月,予以更换治疗方案为曲妥珠单抗+多西他赛+卡铂(TCH),共应用8周期,不良反应:II度骨髓抑制,I度胃肠道反应。
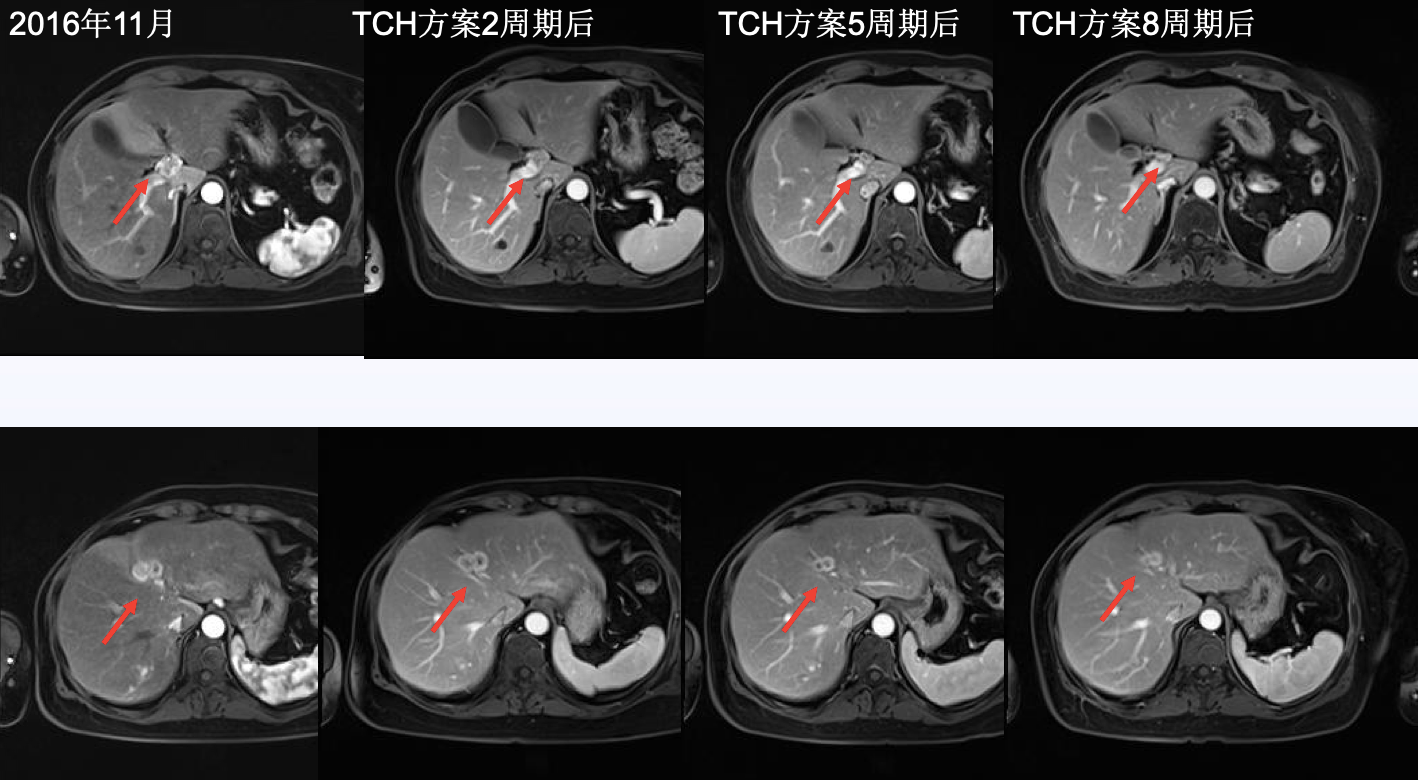
图3 患者更换方案后上腹部MRI增强结果
表1 曲妥珠单抗+多西他赛+卡铂彩超检查对照表
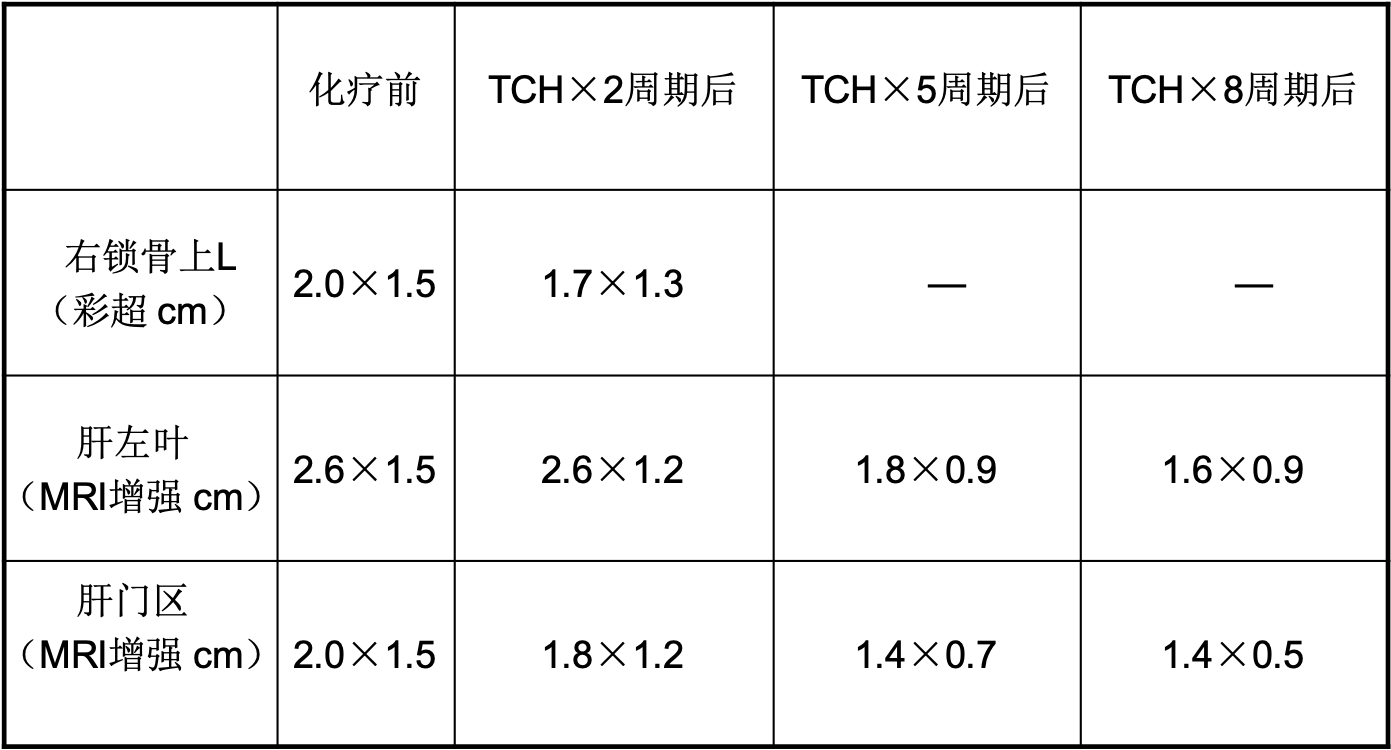
患者综合疗效评价为部分缓解(partial response,PR)。其后予以H+T化疗2周期,综合疗效评价为疾病稳定(stable disease,SD),经MDT讨论,病情处于稳定,建议给予肝脏局部治疗。
2017年6月8日,全麻下行经皮彩超引导下肝左内叶转移癌及第二肝门区病灶微波消融治疗术。术中肝转移灶穿刺病理:癌。免疫组化:ER(+)30%,PR(+)10%,HER2(3+),Ki-67(+)45%。
维持治疗:H+T化疗8周期,耐受性下降,乏力较著,III度骨髓抑制,2017年12月停药。
PFS3为13个月。2017年12月25日,患者复查上腹部MRI,提示肝内病灶进展(图4)。
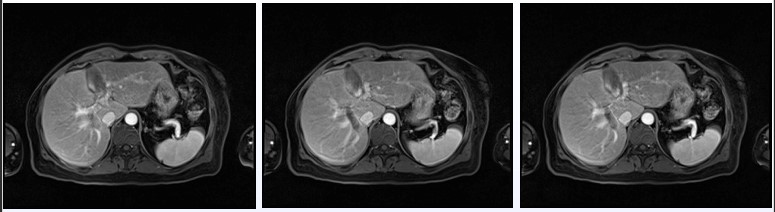
图4 上腹部MRI增强(2017年12月25日)
2017年12月28日,开始予以曲妥珠单抗+阿那曲唑治疗4个月。复查上腹部MRI提示肝内病灶进展(图5)。
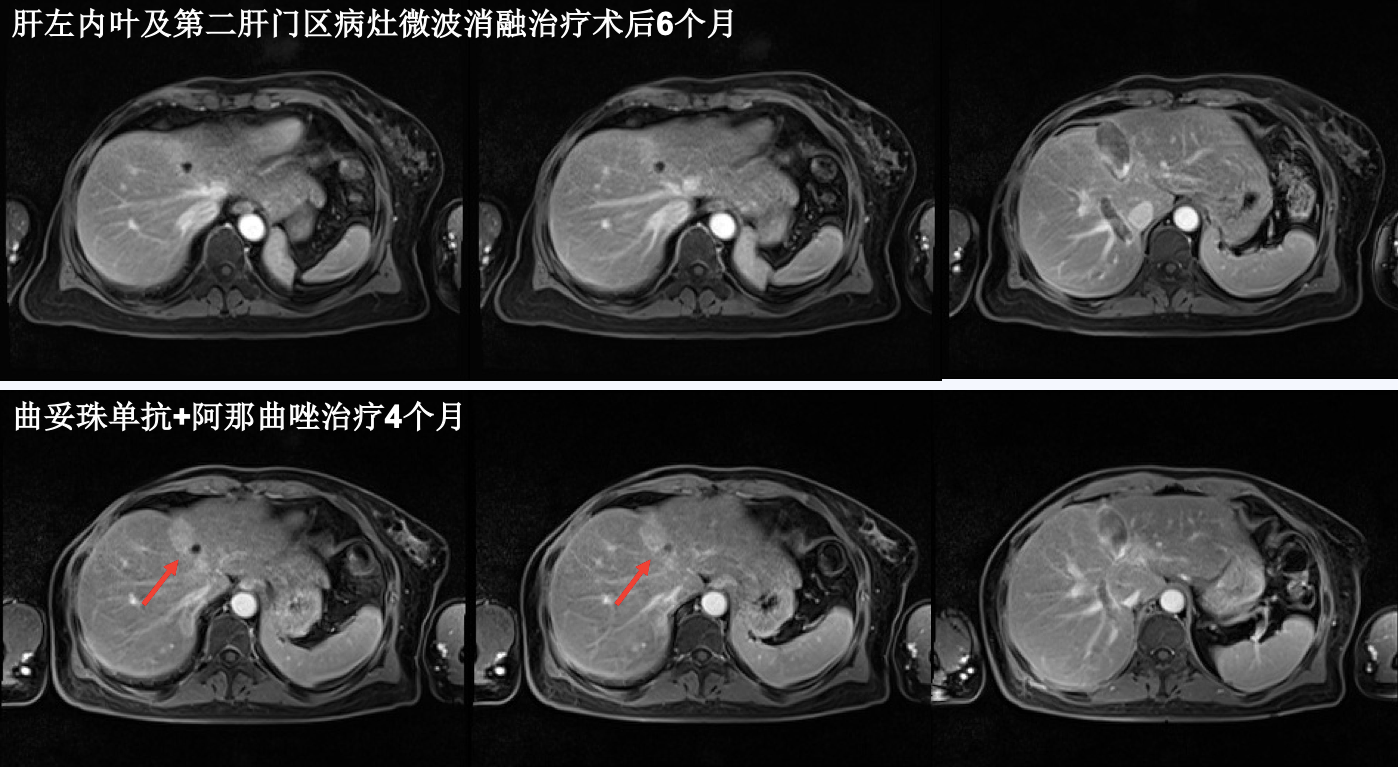
图5 曲妥珠单抗+阿那曲唑治疗4个月后上腹部MRI对照
2018年4月27日,患者应为肝脏病灶再次进展,予以更换治疗方案为曲妥珠单抗+白蛋白结合型紫杉醇共计治疗2周期,不良反应:III度骨髓抑制、II度胃肠道反应、乏力、食欲差。2周期后复查彩超,结果示:右锁骨上可见大小1.8cm×1.3cm淋巴结,形态不规整,边界欠清。右锁骨上淋巴结穿刺病理:癌。免疫组化:ER(+)1%,PR(+)25%,HER2(3+),Ki-67(+)35%。综合疗效评价为PD(图6)。
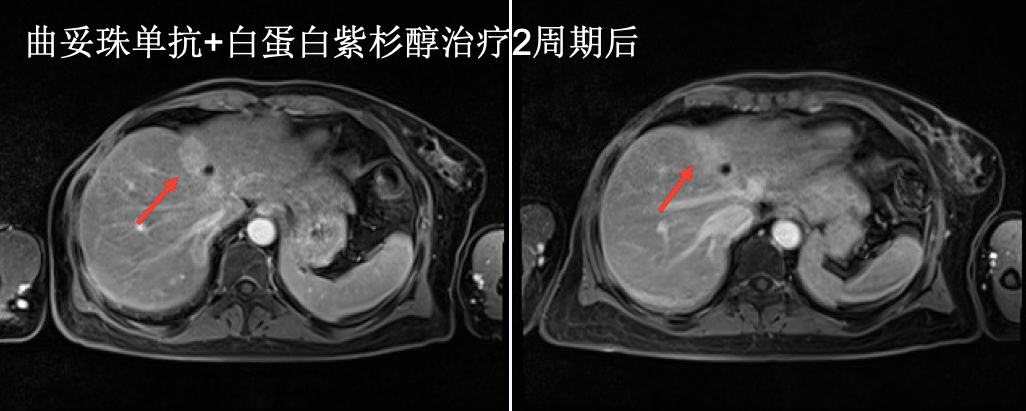
图6 曲妥珠单抗+白蛋白结合型紫杉醇2周期后复查上腹部MRI
2018年7月2日,患者因为肝脏病灶进展,右锁骨上淋巴结转移,予以更换治疗方案为拉帕替尼+白蛋白结合型紫杉醇,共计4周期,不良反应提示为Ⅵ度骨髓抑制、Ⅱ度胃肠道反应、乏力、食欲差。患者耐受性差,治疗持续至2018年12月,锁骨区CT可见小于1cm淋巴结,彩超锁骨区未见肿大淋巴结。综合疗效评价为PR(图7)。
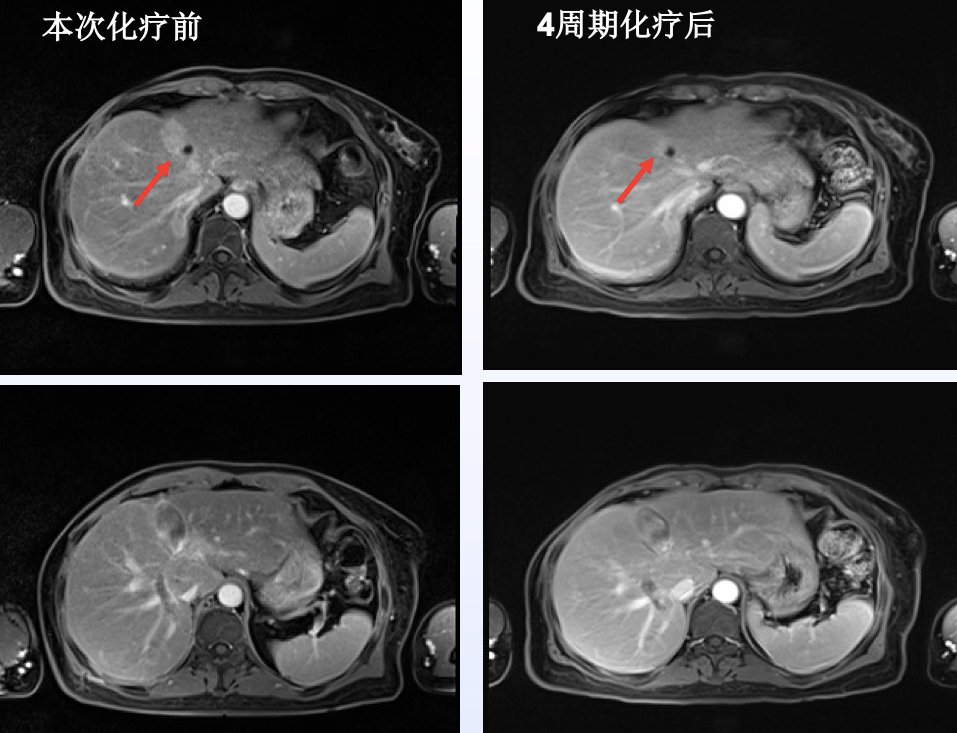
图7 拉帕替尼+白蛋白结合型紫杉醇化疗4周期
2018年12月19日,患者因为药物不能耐受,再次更换化疗方案为拉帕替尼+曲妥珠单抗+依西美坦治疗持续至今,不良反应:I度胃肠道反应、面部1级皮疹、乏力。
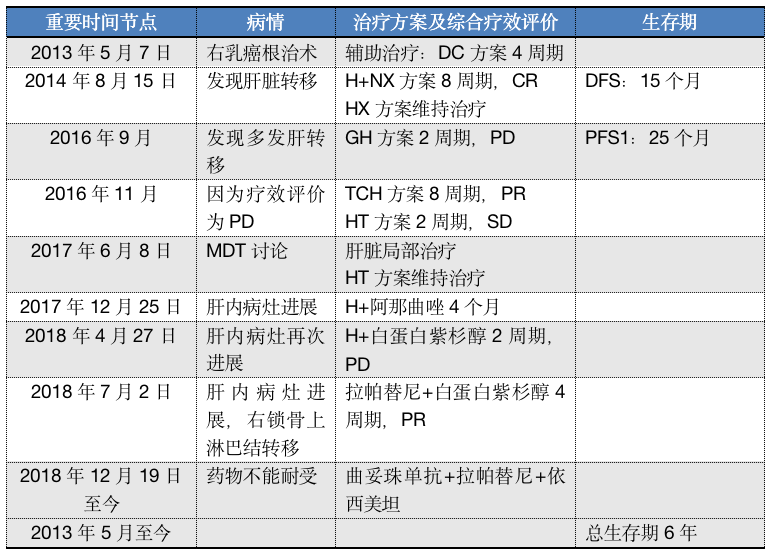
目前该患者总生存期6年(表2)。
表2 患者治疗历程回顾
点评专家

中央保健会诊专家,北京医院肿瘤科副主任
北京肿瘤防治研究会乳腺癌分委会副主任委员
北京中西医慢病防治促进会中西医乳腺癌防治全国专家委员会副主任委员
北京乳腺病防治学会乳腺健康管理专委会副主任,内科/转化医学专委会常委
中国性学会乳腺疾病分会副主任委员
北京医学会乳腺疾病分会常委
北京肿瘤学会理事
中国老年学和老年医学学会老年肿瘤分会理事,基础与转化/肿瘤康复分会委员
中国抗癌协会肿瘤营养与支持治疗专业委员会精准肿瘤营养学组委员
中国心理卫生协会老年心理卫生专业委员会委员
国家卫生计生委人才交流服务中心卫生人才评价领域专家
点评
本病例为首诊乳腺导管内原位癌(ductal carcinoma in situ, DCIS),虽然肿物偏大且HER2阳性,但考虑未见浸润癌成分,无抗HER2治疗指征。此后出现转移,转移病灶穿刺病理回报为癌,但病理并未报告肿瘤类型,影响诊疗过程中选择治疗方案。且患者诊疗过程中应定期进行随访、复查,以明确患者病情,该患者在手术前后至第一次复发转移过程中影像资料缺失,影响诊疗规范进行。后续按照HER2阳性晚期乳腺癌抗HER2治疗后,多线治疗获得不同程度的缓解,而使用曲妥珠单抗+拉帕替尼这样不同作用机制的靶向联合治疗后,目前患者病情稳定,耐受性良好,获益明显。
1.关于HER2阳性DCIS是否需要抗HER2治疗?
2017年《乳腺原位(内)癌治疗指南》指出:DCIS为非浸润性癌,多数发生于终末导管小叶单位(TDLU),也可发生于大导管,是局限于乳腺导管内的原位癌。在实际工作中,多将DCIS分为3级,即低级别、中级别和高级别。高级别DCIS往往由较大的多形性细胞构成,核仁明显、核分裂象常见。DCIS进展为浸润性癌的危险因素与患者年龄、肿瘤体积、切缘状况及组织病理学分级有关。对于HER2阳性的DCIS患者,目前尚无HER2阳性导管原位癌或者伴有微浸润患者能够从靶向辅助治疗中获益的明确相关证据,而且对于抗HER2治疗不能依据肿瘤大小进行主观判断,因此不需要行抗HER2治疗。但需要注意的是当病理诊断为微浸润时,应严格遵循病理诊断标准,避免将T1a诊断为微浸润,造成低估,必要时可以在重复检测病理或者病理会诊。Ⅲ期NSABPB-43临床研究[1]预计入组2000例接受乳房肿块切除术和放疗的HER2阳性DCIS患者,随机进入放疗+曲妥珠单抗治疗组或者单纯放疗组,随访结果尚未公布。由此可知,虽然目前尚未推荐HER2阳性的DCIS进行抗HER2治疗,但针对高危患者的密切随访是必要的。本例患者未进行抗HER2治疗,但术后短期内即出现肝多发转移,可见对于DCIS而言,HER2+可能也是高危因素之一。
此外,对于激素受体阳性的DCIS患者可以接受5年他莫昔芬的治疗,他莫昔芬可以明显降低所有(包括同侧和对侧)乳腺肿瘤事件的发生。
2.HER2阳性晚期乳腺癌,抗HER2是成功的关键
《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南2019》指出:对于既往未接受过曲妥珠单抗辅助治疗的HER-2 阳性复发转移乳腺癌,以曲妥珠单抗为基础联合化疗的方案是这部分患者晚期一线治疗标准方案。本例患者在辅助治疗中已使用了多西他赛,但《HER2阳性乳腺癌临床诊疗专家共识》指出对于以下患者可以考虑紫杉类药物再应用:①紫杉类药物新辅助治疗有效;②紫杉类药物辅助治疗结束一年以后复发;③紫杉类药物解救治疗有效后停药。本病例中,患者一线抗HER2治疗使用曲妥珠单抗,但在化疗方面选用的药物欠佳,应考虑继续以紫杉类为基础的化疗联合靶向治疗,即TXH方案,争取一线治疗取得更加明显的临床获益。回顾患者一线NXH方案后续予以HX方案维持,获得了长达25个月的缓解时间。而对于复发转移乳腺癌曲妥珠单抗治疗进展后,需要根据患者既往治疗判断。如果既往治疗有效,因为毒性或经济原因停药,则优先考虑继续使用曲妥珠单抗,换用其他化疗药;如果在短期治疗中进展,则优先考虑更换抗HER2药物。本病例中,患者一线治疗使用曲妥珠单抗,治疗有效1年后停药,虽然已从治疗中获益,但因为患者是一线治疗,曲妥珠单抗应使用至疾病进展,而不应该停药,这为后期的疾病复发埋下了伏笔。
后续疾病再次复发,原则上可以继续使用曲妥珠单抗至疾病进展。HERMINE研究[2]发现,疾病进展后乳腺癌患者继续接受曲妥珠治疗的中位OS和TTP均比停止使用显著延长。该研究进一步确认了曲妥珠单抗作为一线药物适用于临床治疗转移性乳腺癌。本病例中患者反复因抗HER2治疗获益,可见对于HER2+晚期乳腺癌患者而言,抗HER2治疗才是关键。但患者在XH维持治疗期间出现了疾病的进展,应考虑二线抗HER2药物拉帕替尼联合内分泌或者化疗。
3.多线抗HER2方案的选择
本病例患者最后采用曲妥珠单抗+拉帕替尼联合靶向治疗,截至目前患者仍从抗HER2治疗中获益。在抗HER2的后线治疗方案选择中,曲妥珠单抗+拉帕替尼(HL)方案同样符合《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》的推荐。EGF104900研究[3]证实相对于拉帕替尼联合卡培他滨,单药T-DM1治疗有显著的PFS和OS获益,因此国际上标准的抗HER2二线治疗方案是T-DM1单药,目前T-DM1尚未在国内上市,可以鼓励患者通过临床研究,以取得最佳生存获益。
本病例治疗的经验
本病例中,患者虽然诊断为DCIS,但短时间内出现复发转移,值得临床警示。后续靶向治疗以及双靶治疗等全程管理治疗后,获得长期生存获益,效果非常显著,可见对于HER2阳性患者而言,更需要全程管理以及全程抗HER2治疗,此病例可作为此类患者治疗方案的借鉴。
1.Siziopikou Kalliopi P,Anderson Stewart J,Cobleigh Melody A et al. Preliminary results of centralized HER2 testing in ductal carcinoma in situ (DCIS): NSABP B-43.[J] .Breast Cancer Res. Treat., 2013, 142: 415-21.
2. Extra J M , Antoine E C , Vincent-Salomon A , et al. Efficacy of Trastuzumab in Routine Clinical Practice and After Progression for Metastatic Breast Cancer Patients: The Observational Hermine Study[J]. The Oncologist, 2010, 15(8):799-809
3. Blackwell KL, Burstein HJ, Storniolo AM, et al. Randomized study of Lapatinib alone or in combination with trastuzumab in women with ErbB2-positive, trastuzumab-refractory metastatic breast cancer[J]. J Clin Oncol, 2010, 28(7):1124-1130.












 苏公网安备32059002004080号
苏公网安备32059002004080号


