我们知道TMB(肿瘤突变负荷)可能影响肿瘤患者免疫治疗的疗效,这基于一些研究假说比如新抗原理论,之后近年来,又被越来越多的临床研究结果所证实。
ctDNA检测TMB预测免疫治疗疗效
今年7月,在《NatureMedicine》上发表了一篇II期研究结果,针对61名经pembrolizumab (Merck,Keytruda)治疗的胃癌患者,观察免疫疗效与一系列因素的关系,包括微卫星不稳定性(MSI),PD-L1表达,及TMB,本研究的TMB检测由Guardant's 360平台进行血液检测ctDNA,结果显示和组织标本的TMB检测结果响应预测一致。
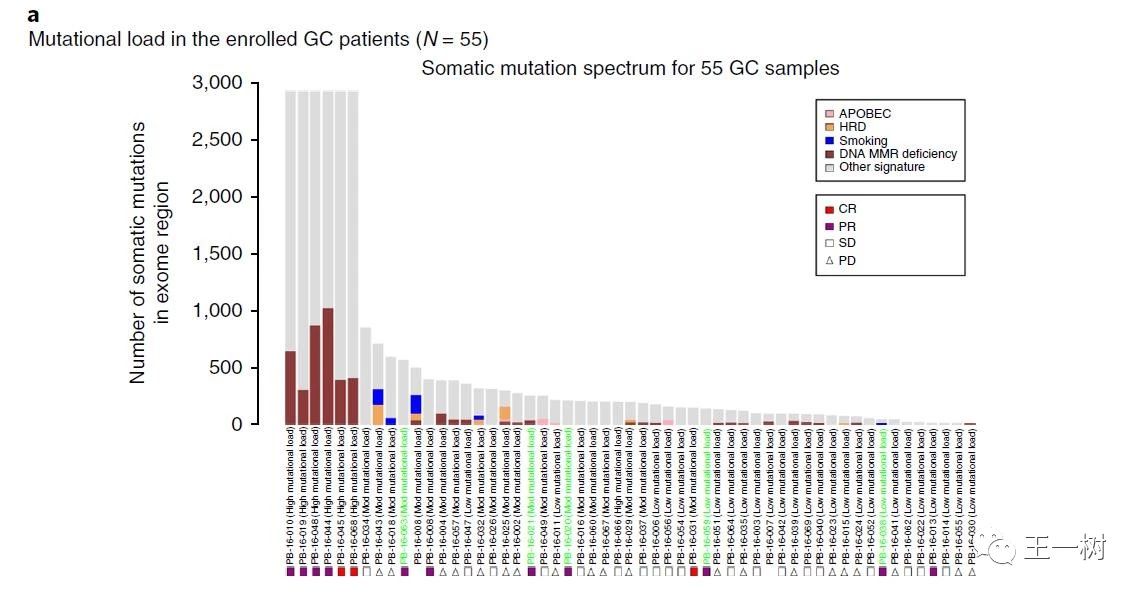
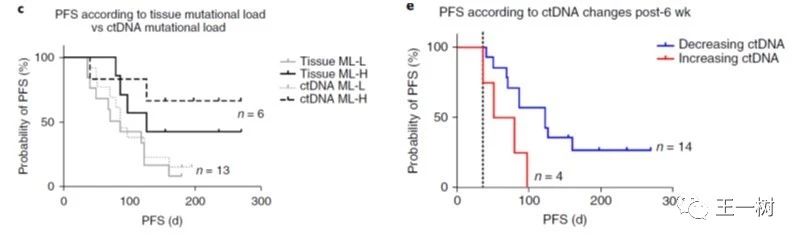 结果显示:进行ctDNA检测TMB与患者对Pembro响应相关;根据组织标本检测TMB和根据ctDNA检测结果一致,无论组织还是ctDNA检测高表达都与更长的PFS相关;治疗6周后,ctDNA的升高或降低会影响患者PFS。
结果显示:进行ctDNA检测TMB与患者对Pembro响应相关;根据组织标本检测TMB和根据ctDNA检测结果一致,无论组织还是ctDNA检测高表达都与更长的PFS相关;治疗6周后,ctDNA的升高或降低会影响患者PFS。
对患者的价值和血液检测商业化的机会
Samsung大学的作者说到:“ctDNA检测的肿瘤突变负荷分数和放射学反应有很好的相关性。从事后探索性分析中,显示出使用ctDNA检测TMB至少能够和组织检测TMB具有同等的预测免疫治疗PFS的效应。基于此,对于不能或者不愿意接受侵入性组织活检的患者,ctDNA检测突变负荷是一个可行的选择,或者至少是一个补充检测方法。”
TMB是基于肿瘤基因变化的考量,目前有跟多公司在以NGS方法进行对TMB检测的商业化,目前基于组织标本进行TMB检测已经相当成熟,诸多NGS公司现在全力攻克对血液标本进行TMB检测及商业化。
Guardant并未对其平台技术进行阐述,甚至没有可以去做自己和其他NGS竞争公司产品的区隔。目前Guardant公司也拒绝对TMB商业化进程发表评论,也拒绝对本月发表的这项由韩国Samsung大学发表的胃癌研究结果发表评论。该研究的作者也拒绝披露进一步的想法与信息。
在这项研究中,除了评估已知的免疫治疗反应生物标记物如MSI和PD-L1之外,该报告还包括来自血液和组织测序结果的患者的一个子集的数据,结果表明Guardant's360平台可以和肿瘤组织外显子测序一样,具有准确地进行TMB检测能力。
回顾首个血检ctDNA与免疫治疗疗效相关研究
在去年10月发表于《Clinical Cancer Research》杂志的一项研究证实使用血液检测ctDNA突变来观察患者免疫治疗疗效,这是首个发表的针对血检ctDNA与免疫治疗疗效相关的研究。血液NGS检测有望成为免疫治疗可实现的无创预测标志物。
这是美国UCSDMoores癌症中心的一项回顾性研究,观察了69名使用了免疫治疗的患者疗效与使用NGS技术血检ctDNA(54-70基因)的疗效关联,疗效观察包括治疗应答(CR,PR),PFS及OS,基于检测VUS(不明意义突变)的数目及突变总数。该研究使用了Guardant Health的检测平台进行NGS测序分析。
结果可以看到,突变率高(VUS突变〉3的患者对比VUS〈3 的患者)ORR,PFS及OS均显著提升。其中SD 6 months/PR/CR 45% 对比15%,P=0.014;PFS 3.82个月对比2.07个月,p=0.019;OS 尚未达到对比10.72个月,p=0.042。观察总突变高低(Cut off值为6)也得到和VUS一致的结果。
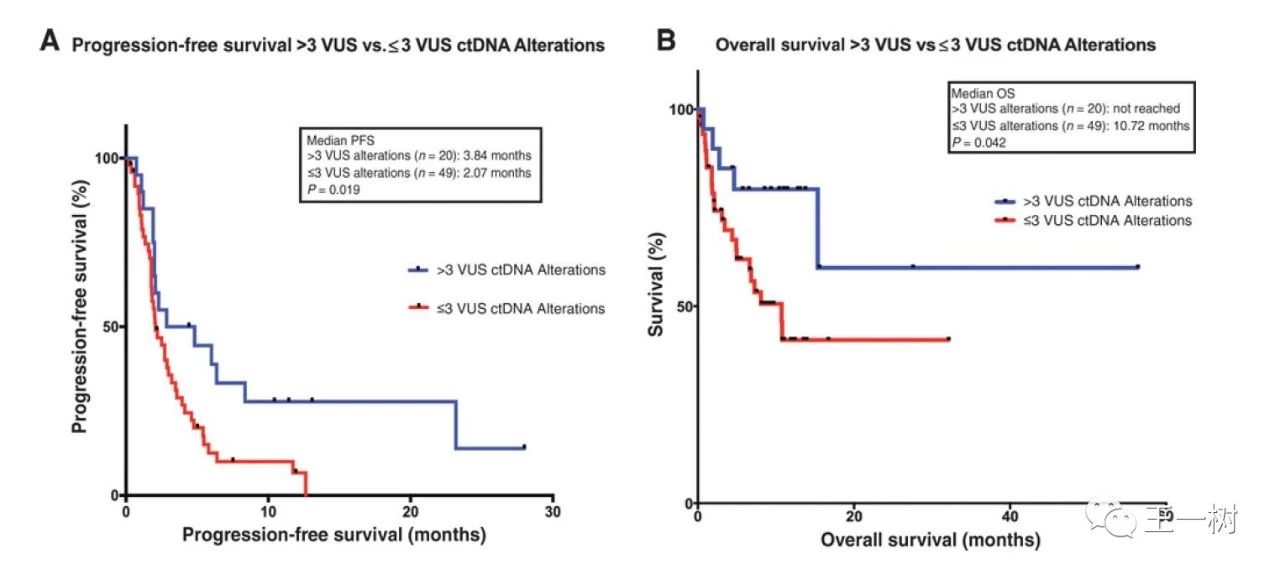 一句话总结,就是进行血液检测NGS观察ctDNA突变,可能能够作为免疫治疗的预测标志物。
一句话总结,就是进行血液检测NGS观察ctDNA突变,可能能够作为免疫治疗的预测标志物。
研究存在的问题及解决办法
样本量太小仅纳入69例患者的回顾性研究,后续要扩大样本量进行观察。UCSD团队表示他们已经着手进行一项400例患者的扩大研究。
目前使用的ctDNA进行NGS检测的Panel比较小,仅54-70的基因侧检测,可能需要观察更大panel来比对。
血检ctDNA是否能够替代组织TMB进行NGS检测来预测免疫治疗疗效还需要进行验证性研究。
血液检测ctDNA对肿瘤免疫治疗的意义
免疫治疗如火如荼的今天,进行肿瘤治疗被寄予很高期望,我们都知道PD-L1可能未必是最合适的标志物,找寻合适的标志物尤为重要。
组织检测TMB是很高潜的预测标志物,但其有创及昂贵的价格也存在一定的局限性。
血检必将是探索的方向,方便、无创、价格更低,如果能有合适的检测及结果,必将有广阔的市场。
血检很火热,各个公司都在做
本研究虽然是个小样本研究,却是首个发表的针对血检ctDNA与免疫治疗疗效相关的研究。各大检测公司都在积极开发血检平台,以期预测免疫治疗疗效。
FoundationMedicine已经验证性观察到其组织检测TMB的有效性,观察了这些标本对315个基因Panel检测TMB与对WES检测TMB的一致性,发现两者高度一致(R2=0.98),也就是说该CGP方法可替代WES检测。
罗氏公司在去年ESMO和今年ASCO都报道了血检bTMB进行免疫治疗预测"【NGS+IO】Foundation Medicine的血检TMB将作为免疫治疗一线伴随诊断"的研究结果。bTMB的检测前瞻性用于一线治疗NSCLC患者的国际多中心研究BFAST,旨在比较抗PD-1治疗与基于铂类的化疗。在OAK和POPLAR的研究的783例患者也回顾性的用到了bTMB检测,比较Atezo与多西他赛标准治疗的OS获益。结果显示bTMB的表达和Atezo疗效呈强关联。
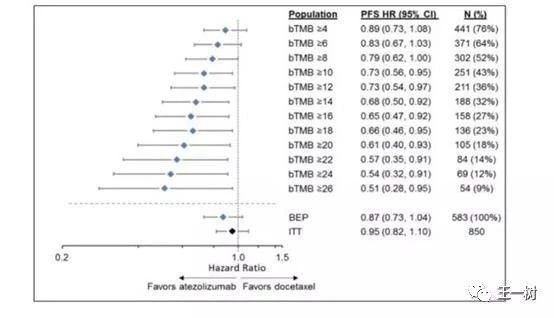
bTMB是不同于FoundationOne新推出的另一平台,进行血液394个基因的体细胞突变的检测来分析bTMB。罗氏公司计划推进将bTMB作为Atezolizumab的伴随诊断。
PersonalGenome Diagnostics(PGDx)公司也在推进一项名为MutatorDETECT的无创NGS血检平台,检测cfDNA来进行患者TMB分析,该平台基因数可能会小一些,但公司尚未透漏细节。
Johns Hopkins医院和 Memorial Sloan Kettering医院,是首先发表了TMB与免疫治疗反应预测的机构之二,Johns Hopkins在今年二月也宣布和Memorial SloanKettering达成IP协议共同开发组织检测和血液检测TMB的平台。
这么多家公司在做,存在的问题和需要规范的地方在哪里?
平台一致性的规范化和血检TMB验证性
NGS市场化推进的今天,我们需要去验证这些平台TMB检测的有效性和对临床指导的有效性,同时对于不同平台的一致性进行评估。目前有两家独立评估机构美国的Friends肿瘤研究中心,和德国的QuIP(Quality Assurance Initiative Pathology)。

Friends机构旨在评估不同厂家TMB平台的一致性,并于TCGA数据库的WES检测TMB进行比对。在2018年5月10日,他们召开了会议来探索TMB作为生物标志物的标准化及共识。包括了Foundation Medicine,Personal Genome Diagnostics, Thermo Fisher Scientific, Illumina, GuardantHealth, NeoGenomics Laboratories, Qiagen, 以及 MemorialSloan Kettering Cancer Center,这些都是著名的NGS公司或者开展NGS富有经验的医院检测。
项目的下一阶段将TMB检测应用于标准化的人肿瘤细胞系,并于exome数据库进行比对,第三阶段将回顾临床样本与患者治疗数据bingtansuo 临床检测数值变化,可能相关TMB的cut off值得问题。最终目标是比对不同平台TMB的检测结果,实现标准化,例如一位患者使用了Foundation Medicine的平台检测出TMB=12,他能够换算出如果使用PGDx的话,TMB的表达是多少。
Quip包含了德国和瑞士11家TMB检测机构和药厂,Foundation Medicine; ThermoFisher Scientific; Qiagen; Illumina; Siemens Healthineers 下属的Neo New Oncology,和一些学术实验室。这个项目的目的是了解各家评估方式并与TCGA数据库WES标准数据的TMB进行比对。和Friends一样,了解不同NGS平台之间的相互转化及关联。
Friends和QuIP发起的研究是了解不同平台之间的表现,深入了解其检测结果。不仅与标准化TCGA数据库WES的TMB结果比对,实现标准化;还进行平台间比对,实现一致性。将为临床应用带来更便捷的帮助。
临床应用之路
此次Guardant的血检结果是一个临床有效性和验证性的证据的开始,将会有更多指导临床药物的研究及结果出现。
例如前两天BENEFIT研究发表于Lancetrespiratorymedicine,是一项基于ctDNA中EGFR突变决策晚期肺腺癌一线治疗的前瞻性研究,为血液基因检测指导个体化靶向治疗提供了循证医学证据。结果显示检测cDNA中EGFR突变是一种有效的方法来识别可能受益于一线吉非替尼治疗的患者,进一步分析EGFR突变和伴随的基因变异的动态变化可以预测吉非替尼的耐药性。












 苏公网安备32059002004080号
苏公网安备32059002004080号


