第二届“35 under 35”CSCO-良医汇2018优秀青年肿瘤医师风采大赛评选活动”报名及筛选阶段已正式结束!在众多参与报名筛选的医生中,有100位优秀青年医生脱颖而出!他们将在近期进行三轮PK,展示青年医生风采!第一轮为ASCO最新摘要解读,候选人在主办方指定的2018ASCO口头报告专题中自由选择一份口头报告进行点评(如:背景,结果的评价,对临床的意义,和其他研究的对照,优点和不足等等),目前100位青年医生在规定的时间内已将解读提交,解读很精彩,现展示出来,供各位品读!欢迎转发,让更多的医生同道看到青年力量!欢迎评论,发表您的见解,与青年医师同台论道!

ASTRRA研究:他莫昔芬+卵巢功能抑制在化疗后未绝经/月经复潮的激素敏感性乳腺癌的辅助内分泌治疗中的角色(2018 ASCO abstract 502)
背景:对于新辅助或辅助化疗后未达到永久绝经的乳腺癌患者,在他莫昔芬(Tamoxifen,TAM)的基础上增加卵巢功能抑制(Ovarian function suppression,OFS)的疗效尚不确定。目的:在接受了(新)辅助化疗后仍未绝经或卵巢功能恢复的女性患者中比较他莫昔芬(5年)+OFS(2年)与他莫昔芬(5年)的5年DFS和OS的差异。
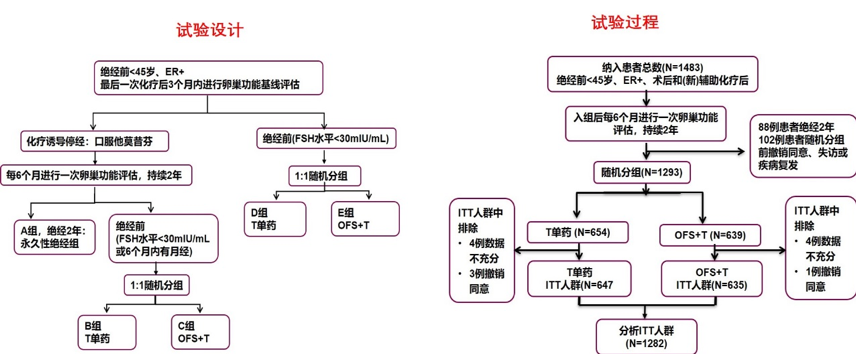
结果:卵巢监测2年期间有约95%的患者卵巢功能恢复,随访63个月后, TAM+OFS和TAM单药组5年的DFS分别为91.1%和87.5%,HR 0.686(95%CI=0.483 - 0.972,P=0.033);TAM+OFS组和TAM单药组的OS分别为99.4%和97.8%,HR:0.310 (95% CI=0.102-0.941, P=0.029)。
结论:化疗后卵巢功能需要监测至少24个月以评估是否符合行卵巢功能抑制,对于化疗后仍为绝经前状态和化疗后月经恢复的患者,他莫昔芬联合两年的卵巢功能抑制与单药他莫昔芬相比显著提高了患者的DFS和OS。
解读:
60-75%的乳腺癌是激素受体阳性的,雌激素是这类乳腺癌细胞存活增殖的根本,内分泌治疗是其主要治疗手段之一。卵巢功能抑制(Ovarian function suppression, OFS)是内分泌治疗的一种策略,已有100余年的历史,随着TEXT和SOFT临床研究结果公布,OFS再次成为乳腺癌内分泌治疗的热点,2018年ASCO大会上ASTRRA研究结果发布,同时TEXT和SOFT研究也进行了新的结果更新,现通过梳理OFS的历史以更清楚的了解ASTRRA研究。
1896年Beatson首次通过切除患者的卵巢在乳腺癌的治疗上获得成功,开启了乳腺癌内分泌治疗的序幕。20世纪70年代他莫昔芬(Tamoxifen,TAM)在乳腺癌的内分泌治疗上取的成功,其后第三代芳香化酶抑制剂(Aromatease inhibitor,AI)取得了优于他莫昔芬的疗效。雌激素受体和孕激素受体检测的普及,以及其在内分泌治疗疗效预测中的价值被证实,让我们认识到乳腺癌的异质性及不同分子分型之间生物学行为的差异,这也促使内分泌治疗慢慢地向精准化(给恰当的病人,在恰当的时间,使用恰当的方法)迈进。内分泌治疗手段的增多促使临床医生开始思考“如何合理组合不同的内分泌治疗手段以提高疗效”。OFS在进展期乳腺癌中的疗效确切,但在乳腺癌术后辅助治疗中的疗效一直很有争议。
1987年开始的ZIPP研究是第一个含单药TAM组和TAM+OFS组的III期随机对照研究,研究中纳入了绝经前或小于50岁的I-II期乳腺癌患者,分为对照组(476人),TAM单药组(879人),OFS+TAM组(882人)和单独OFS组(469人),研究结果在2006年公布,结果显示:OFS+TAM与TAM单药相比,DFS和OS的差异均无统计学意义[1]。当时的CMF方案是主流的化疗方案,其对卵巢功能抑制很强,这也可能导致了单药TAM治疗组患者的卵巢功能受损,从而造成了偏倚,由于当时尚不明确ER表达水平与内分泌疗效的关系,入组时并未考虑患者激素受体的表达状态,而且内分泌治疗的时间仅为2年,另外对患者月经状态的评估亦不严格。
1993年启动的ABC(OSA)研究,比较了术后辅助内分泌治疗应用TAM单药与TAM+OFS疗效的差异,患者入组时也没有考虑ER的表达情况。结果在2007年公布,虽然统计时对年龄、淋巴结状态和ER状态进行了校正,但是OFS+TAM(1063人)与单药TAM(1081人)相比RFS和OS差异均无统计学差异。在进行亚组分析时发现,在小于40岁的ER阳性,且未接受化疗的亚组中联合OFS后OS有获益的趋势[2]。该研究的缺陷在于患者月经状态的评估标准为:要求乳腺癌手术前的12个月内患者有规律的月经,研究者并未考虑之后的辅助化疗对患者月经状态的影响。
1994年开始进行的E-3193研究限制了入组的患者需为ER和/或PR阳性、无淋巴结转移,且不需要化疗,入组前6个月患者有规律的月经或雌激素水平符合绝经前状态。研究比较TAM(171人)5年与TAM+OFS(174人)5年疗效的差异,很遗憾由于入组太慢,试验提前终止,随访9年后的结果分析显示OFS并未带来DFS和OS的获益[3]。本研究入组患者均不需要化疗,复发风险比较低,当我们回过头来看时会发现,该研究最初设计的纳入标准就注定了其失败的命运。
2003年SOFT研究在悄无声息中开始,要求入组的患者必须在入组前6个月内有规律的月经或激素水平符合绝经前状态,在入组前已经完成化疗的患者要求激素水平必须符合绝经前状态。2014年研究结果首次公布,虽然没有得到整体的阳性结果,但亚组分析显示,在小于35岁的亚组中,5年无乳腺癌复发率,OFS+TAM和TAM分别为78.9%和67.7%,在需要化疗的患者中,OFS+TAM的OS显著优于TAM单药[4]。2017年SOFT/TEXT经过延长随访时间的联合分析显示:OFS+TAM和OFS+AI的DFS均优于TAM单药,但在OS方面,只有OFS+TAM优于TAM单药,OFS+AI与TAM单药相比,OS的差异并没有统计学意义[5]。
本届ASCO大会上SOFT和TEXT研究再次公布(503号摘要)了无远处转移间期(DRFI,这也是最有可能转化为OS的指标)的结果[6],显示对于HR(+)/HER-2(-)的绝经前患者,如果通过临床病理特征评估为高复发风险的,OFS+AI与OFS+TAM或TAM相比,其8年DRFI可获得10-15%的改善,对于低复发风险的患者OFS带来的8年DRFI获益只有4-5%,总人群中OFS+AI较OFS+TAM的DRFI绝对获益3%,但OFS+AI对OFS+TAM在远处转移方面的优势是否真的能转变为后期随访的OS优势尚需等待。因此对于高危的患者应用OFS+AI也许是最优选择,但若患者依从性差或不耐受AI,OFS+TAM也是一个不错的选择。
通过回顾历史,我们可以看到OFS研究的进步,研究的设计在不断改进,入组时由最初对激素受体状态的不作要求,到后来对ER、PR的严格限制,由最初对月经状态的模糊要求到后来对月经状态的严格评估,卵巢抑制的措施越来越人性化,研究结果逐步让我们意识到什么样的患者需要应用OFS,OFS应该联合AI还是TAM,但何时开始OFS一直存在争议。已有研究证实在激素受体阳性的绝经前乳腺癌中化疗诱导的停经可改善患者的预后。化疗后月经状态的改变与患者的年龄以及所用化疗药物的卵巢毒性(含烷基药物)相关。本次ASCO大会上韩国学者报道了ASTRRA研究的结果(502号摘要)[7]。该研究2009年5月启动,2015年12月完成,限制入组患者必须为ER阳性,年龄小于45岁,而且对于化疗后停经的患者在化疗结束后通过监测患者的月经情况和FSH水平对患者的月经状态进行了2年的严格评估,若患者符合绝经前状态则随机分为OFS+TAM或单药TAM组,OFS使用时间为2年,TAM使用时间为5年,结果显示OFS+TAM的DFS和OS均优于单药TAM[8]。虽然该研究的OFS仅使用了2年,但患者的DFS和OS仍然显著获益。本研究结果提示如果患者依从性差或对OFS的耐受性差,应用两年OFS也可获益。但本研究的“化疗后卵巢功能必须监测至少两年才可评估是否符合应用OFS”这个结论很牵强,本研究若能增加一个“化疗后停经的患者不监测月经状态及FSH而直接给与OFS”的研究组,才可以回答,“化疗后停经的小于45岁的患者直接给予卵巢功能抑制疗效好,还是监测2年后再给予卵巢功能抑制疗效好”。另外,本研究中95%的患者在2年内月经都得到了恢复,提示小于45岁的乳腺癌患者的卵巢恢复功能很强大,可能化疗结束后就应该开始给予OFS,长时间的检测可能会耽误患者应用OFS的最佳时机。我们可能需要进一步研究化疗导致患者永久绝经与暂时停经患者的内在差异,找到新的marker,以确定最需要进行监测的人群,使监测更精准,避免延误OFS开始的时间。另外该研究结果也告诉了我们,即使患者化疗结束后未及时给予OFS,2年后开始OFS也是获益的。该研究给了我们一个启发:部分化疗后停经的患者在应用OFS前可能需要监测卵巢功能一段时间,但哪个年龄段的患者合并多大复发风险才需要监测,监测多长时间比较合适,这需要更进一步设计严谨的试验进行探索。
OFS已从晚期患者的解救治疗迈向了术后的辅助治疗,而且符合术后辅助OFS的患者群体越来越精准化,越来越多的数据也在指导着我们到底是联合应用TAM还是联合AI,何时开始应用OFS也在不断的探索中,相信不久的将来OFS可能迈进乳腺癌患者的新辅助治疗阶段,而且可能出现新的Biomarker预测OFS的疗效和开始时间。
【温馨提示】:如果您觉得闫顺朝医生解读的好,请在下方为他点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!
1. Baum M, Hackshaw A, Houghton J, et al. ZIPP International Col-laborators Group. Adjuvant goserelin in pre-menopausal patients with early breast cancer: Results from the ZIPP study. Eur J Cancer. 2006;42(7):895-904.
2.The Adjuvant Breast Cancer Trials Collaborative Group. Ovarian ablation or suppression in premenopausal early breast cancer: results from the international adjuvant breast cancer ovarian ablation or suppression randomized trial. J Natl Cancer Inst. 2007;99(7):516–525.
3. Tevaarwerk AJ, Wang M, Zhao F, et al. Phase III comparison of tamoxifen versus tamoxifen plus ovarian function suppression in premenopausal women with node-negative, hormone receptor-positive breast cancer (E-3193, INT-0142): a trial of the Eastern Cooperative Oncology Group. J Clin Oncol. 2014;32(35):3948–3958.
4. Francis PA, Regan MM, Fleming GF. Adjuvant ovarian suppression in premenopausal breast cancer. N Engl J Med. 2015;372(5):436–446.
5. Francis, P. A., et al. "Abstract OT3-02-03: Long-term follow-up of TEXT and SOFT trials of adjuvant endocrine therapies for premenopausal women with HR+ early breast cancer." (2017): OT3-02.
6. Regan, Meredith M., et al. "Absolute improvements in freedom from distant recurrence with adjuvant endocrine therapies for premenopausal women with hormone receptor-positive (HR+) HER2-negative breast cancer (BC): Results from TEXT and SOFT." (2018): 503-503.
7. Noh, Woo Chul, et al. "Role of adding ovarian function suppression to tamoxifen in young women with hormone-sensitive breast cancer who remain premenopausal or resume menstruation after chemotherapy: The ASTRRA study." (2018): 502-502.
8. Kim HA, Ahn SH, Nam SJ, et al. The role of the addition of ovarian suppression to tamoxifen in young women with hormone-sensitive breast cancer who remain premenopausal or regain menstruation after chemotherapy (ASTRRA): study protocol for a randomized controlled trial and progress. BMC Cancer. 2016;16:319.
41本,27种肿瘤,63万字的【肿瘤患者指南丛书】,赶紧扫描或识别下方二维码,即可免费拥有!











 苏公网安备32059002004080号
苏公网安备32059002004080号


