2018年6月27日,美国国家综合癌症网络(NCCN)发布了2018年第五版非小细胞肺癌(NSCLC)临床实践指南。基于2018年ASCO上报道的KEYNOTE-407数据,新增“帕博利珠单抗(Pembrolizumab,Keytruda) +卡铂+紫杉醇”用于晚期鳞状非小细胞肺癌患者一线治疗。同时基于IMpower-150试验数据结果,新增了“Atezolizumab+联合化疗±血管抑制剂治疗”作为晚期非鳞NSCLC患者的一线治疗选择。

2018 V5版指南更新要点
EGFR敏感突变阳性患者的一线治疗(NSCL-18)
EGFR突变患者的一线治疗:推荐奥希替尼的证据等级由2A类提升为1类。
腺癌、大细胞癌、组织学亚型不明确(NOS)非小细胞肺癌患者的初始治疗和后续治疗(NSCL-27)
PS评分为0-2,初始接受“帕博利珠单抗+顺铂(或卡铂)+培美曲塞” 联合治疗后,肿瘤评估缓解或稳定的患者,在总共完成4-6周期治疗后,如果评估肿瘤继续缓解或稳定,新增“帕博利珠单抗+培美曲塞”作为继续维持治疗(1类证据)。
PS评分为0-2,初始接受“Atezolizumab+卡铂+紫杉醇+贝伐单抗”联合治疗后,肿瘤评估缓解或稳定的患者,在总共完成4-6周期治疗后,如果评估肿瘤继续缓解或稳定,新增“Atezolizumab和/或贝伐单抗”作为一个继续维持治疗的选择(1类证据)。
鳞状细胞癌患者的初始治疗和后续治疗 ( NSCL-28)
PS评分为0-2,初始接受“帕博利珠单抗+卡铂+紫杉醇”联合治疗后,肿瘤评估缓解或稳定的患者,在总共完成4-6周期治疗后,如果评估肿瘤继续缓解或稳定,新增“帕博利珠单抗”作为一个继续维持治疗的选择(2A类证据)。
晚期或转移性肿瘤的全身治疗(NSCL-J)
PS评分为0-1,腺癌、大细胞肺癌、组织学亚型不明确的非小细胞肺癌患者初始治疗
“帕博利珠单抗+顺铂(或卡铂)+培美曲塞”推荐的证据等级由2A类提升为1类。
新增“Atezolizumab+卡铂+紫杉醇+贝伐单抗”作为一个一线治疗选择(1类证据)
注:基于IMpower-150研究数据。
PS评分为0-1的鳞状细胞癌患者初始治疗
新增“帕博利珠单抗+卡铂+紫杉醇”作为一线治疗选择(2A类证据)。
注:基于KEYNOTE-407研究数据。
IMpower-150研究
背景
贝伐单抗会通过抑制VEGF免疫反应和提升T细胞对肿瘤的渗透性从而提升免疫治疗疗效。IMpower-150研究(NCT02366143)是一项非鳞癌mNSCLC患者一线治疗的随机对照III期临床试验,对比Atezolizumab(抗PD-L1)+化疗(CP,carboplatin [C] + paclitaxel [P])±贝伐单抗(bev)与bev+ CP的疗效。无论PD-L1表达水平如何,相比于CP + bev ,Atezolizumab + CP + bev组均显示PFS获益。此次报道是IMpower-150研究无进展生存PFS的最终分析和总体生存OS的中期分析结果。
方法
这项III期临床研究中,1202患者1:1:1随机分配至接受Atezolizumab加卡铂加紫杉醇(ACP组),或Atezolizumab加贝伐单抗加卡铂加紫杉醇(ABCP组)或贝伐单抗加卡铂加紫杉醇(BCP组)。随机化分层因素包括性别,基线时是否存在肝转移和PD-L1表达(通过免疫组织化学分析评估)。共同主要研究终点为ITT-WT(EGFR或ALK野生型患者)和Teff-high WT(Teff-high,T效应基因高表达)人群中的PFS以及ITT-WT人群中的OS。
结果
主要终点分析:无进展生存PFS
截至数据锁库时间(2017年9月15日),最短随访时间为9.5个月(WT人群随访时间中位数,ABCP组为15.4个月,BCP组为15.5个月)。WT人群中ABCP组和BCP组692个患者中,517个(74.7%)发生疾病进展或死亡。ABCP组的PFS显著长于BCP组(中位PFS:8.3个月vs. 6.8个月;HR=0.62,95%CI=0.52-0.74; P <0.001)。6个月PFS率ABCP组高于BCP组(66.9%比56.1%); 12个月PFS率分别为36.5%和18.0%。
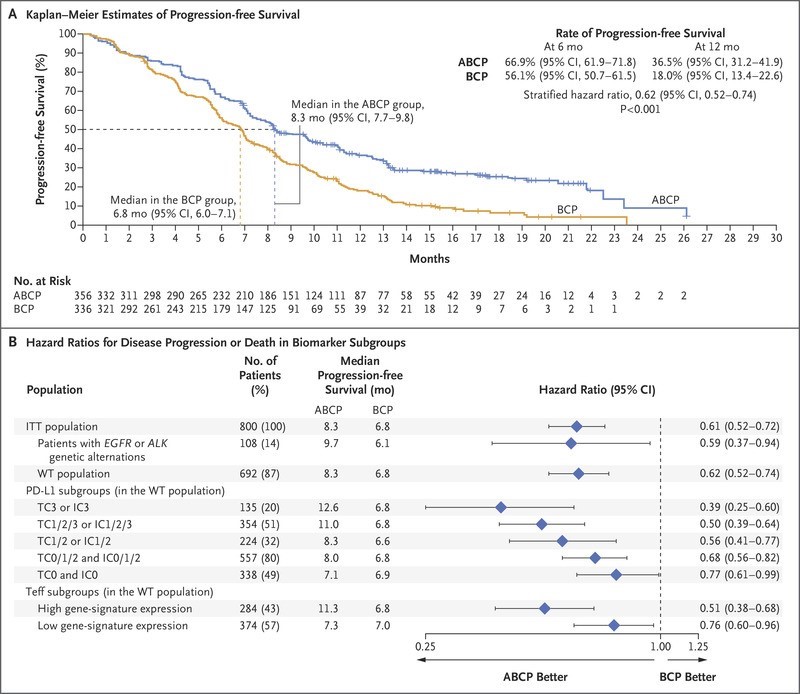
图1 ABCP组和BCP组研究者评估的无进展生存PFS分析
在Teff-high WT人群中,ABCP组和BCP组的284个患者中发生200例(70.4%)疾病进展或死亡。ABCP组的PFS显著长于BCP组(中位PFS :11.3个月vs. 6.8个月;HR=0.51, 95%CI=0.38-0.68; P <0.001)。6个月 ABCP组PFS率为71.7%,BCP组为57.0% 12个月PFS率分别为46.0%和18.0%。
中期分析:总生存OS
对WT人群总生存进行中期分析时ABCP和BCP组696例患者中总共376例死亡(54.0%),数据截止日期为2018年1月22日,最短随访时间约为14个月,中位随访时间约为20个月。 ABCP组的总生存期明显长于BCP组(中位OS:19.2个月 VS 14.7个月;HR=0.78, 95%CI=0.64-0.96; P = 0.02)。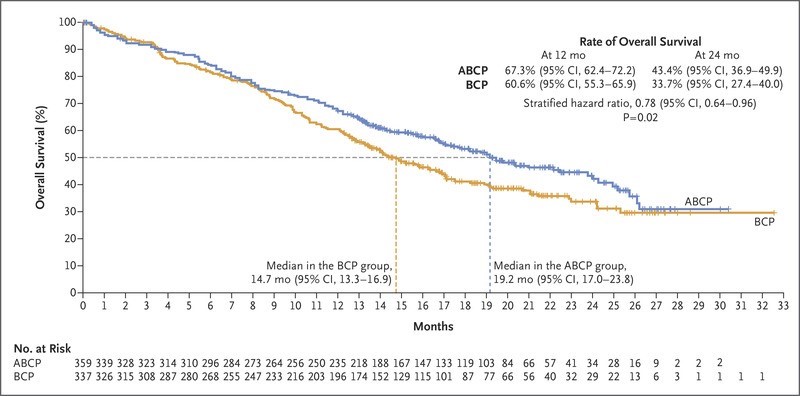
图2 ABCP组和BCP组总生存OS中期分析
结论
IMpower-150研究中,对比bev+ CP,Atezo+bev+CP的一线治疗方案可显著提升NSCLC患者的OS,且未观察到新的安全事件。
KEYNOTE-407研究
背景
帕博利珠单抗(pembrolizumab)联合培美曲塞卡铂治疗初治的非鳞癌非小细胞肺癌患者取得了可观的ORR(客观缓解率),PFS(无进展生存时间)和OS(总生存)。帕博利珠单抗在治疗肺鳞癌的疗效较好,因此,化疗联合使用帕博利珠单抗是我们要考虑的下一种治疗方式。
方法
KEYNOTE-407 (NCT02775435)是一个随机、安慰剂对照的全球研究,该研究计划入组560例初治的晚期肺鳞癌患者,ECOG评分为0-1分。分层因素包括紫杉醇类型、PD-L1表达水平(TPS<1%vs≥1%)和地域(东亚与其他)。患者随机分为2组,一组接受4周期卡铂(6mg/ml/min)+紫杉醇(200mg/m^2,每三周一次)或白蛋白紫杉醇(100mg/m^2,每周一次)联合帕博利珠单抗;另一组使用4周期化疗+安慰剂对照。4周期联合治疗后继续使用帕博利珠单抗/安慰剂维持治疗,总疗程为35次。根据RECIST1.1进行疗效评估。研究的主要终点为PFS和OS。研究已于2017年年底完成招募。
结果
在第一次中期分析时,共204例患者完成随机,其中101例接受化疗+帕博利珠单抗治疗,103例接受化疗;中位随访时间为7.7月(范围:0.4-13.9月)。入组患者中78%为男性,48%的患者年龄<65岁,28%的患者ECOG PS评分为 0分。35%的患者PD-L1为TPS<1%。32%的患者使用白蛋白紫杉醇。帕博利珠单抗+化疗和单纯化疗的ORR为58.4%和35.0%,p=0.0004。65.8%接受帕博利珠单抗+化疗的患者的中位缓解时间≥6m持续时间为65.8%,单纯化疗为45.6%。帕博利珠单抗+化疗组和单纯化疗组的3-4级的AE发生率分别为64.4%和74.5%。
结论
使用化疗+帕博利珠单抗治疗初治晚期肺鳞癌患者的ORR几乎增加一倍。化疗+帕博利珠单抗的安全耐受。第二次中期分析的结果将在会议之前公布。临床试验编号:NCT02775435.
点评
联合免疫治疗已经成为晚期NSCLC一线治疗的研究热点。免疫检查点抑制剂联合化疗具有协同作用机理,因此,联合化疗可以进一步免疫检查点抑制剂的疗效。在今年的AACR会议上,联合免疫治疗用于晚期非鳞NSCLC或NSCLC一线治疗的三项重磅研究公布:KEYNOTE-189研究,IMPower-150研究和CheckMate-227研究,上述3项研究中的KEYNOTE-189和IMPower-150仅入组晚期非鳞NSCLC。
在即将召开的2018年ASCO大会上,联合免疫治疗用于晚期鳞癌一线治疗的两项III期重磅研究也将公布:KEYNOTE-407研究和IMPower-131研究。KEYNOTE-407研究评估了卡铂紫杉醇/白蛋白紫杉醇联合或不联合帕博利珠单抗用于晚期鳞癌一线治疗;IMPower-131研究评估了卡铂紫杉醇/白蛋白紫杉醇联合或不联合atezolizumab用于晚期鳞癌一线治疗,目前两个研究的结果均已经递交FDA,哪一个联合方案将被最新获批,值得期待。
与帕博利珠单抗联合化疗用于晚期非鳞NSCLC一线治疗的KEYNOTE-189研究结果相似(联合组和化疗组的ORR分别为47.6%和18.9%,P <0.001),帕博利珠单抗联合化疗用于晚期鳞癌一线治疗,可以提高接近1倍的ORR(联合组和化疗组的ORR分别为58.4%和35.0%,p=0.0004)。
此外,与帕博利珠单抗单药用于PD-L1高表达的NSCLC患者一线治疗结果相比(KEYNOTE-024研究中帕博利珠单抗单药的ORR为44.8%),帕博利珠单抗联合化疗可以进一步提高ORR达58.4%。
2018 V5版NCCN指南下载链接:https://www.nccn.org/
Socinski M, Jotte R, Cappuzzo F, et al. Atezolizumab for first-line treatment of metastatic nonsquamous NSCLC. N Engl J Med 2018;378:2288-2301.
Paz-Ares L. Luft A, Tafreshi A, et al. Phase 3 study of carboplatin-paclitaxel/nab-paclitaxel (Chemo) with or without pembrolizumab for patients with metastatic squamous non-small cell lung cancer [abstract]. J Clin Oncol 2018;36(suppl): Abstract 105.















 苏公网安备32059002004080号
苏公网安备32059002004080号


