
专业文字|非专业慎点
一、奥希替尼一线应用

ORR-objective response rate;DOR-duration of response;AEs-adverse events
旨在分析Osimertinib在EGFR突变型NSCLC患者中一线应用的有效性和安全性。
纳入60名患者,Osimertiniba剂量80mg/d及160mg/d各30名。
疗效:
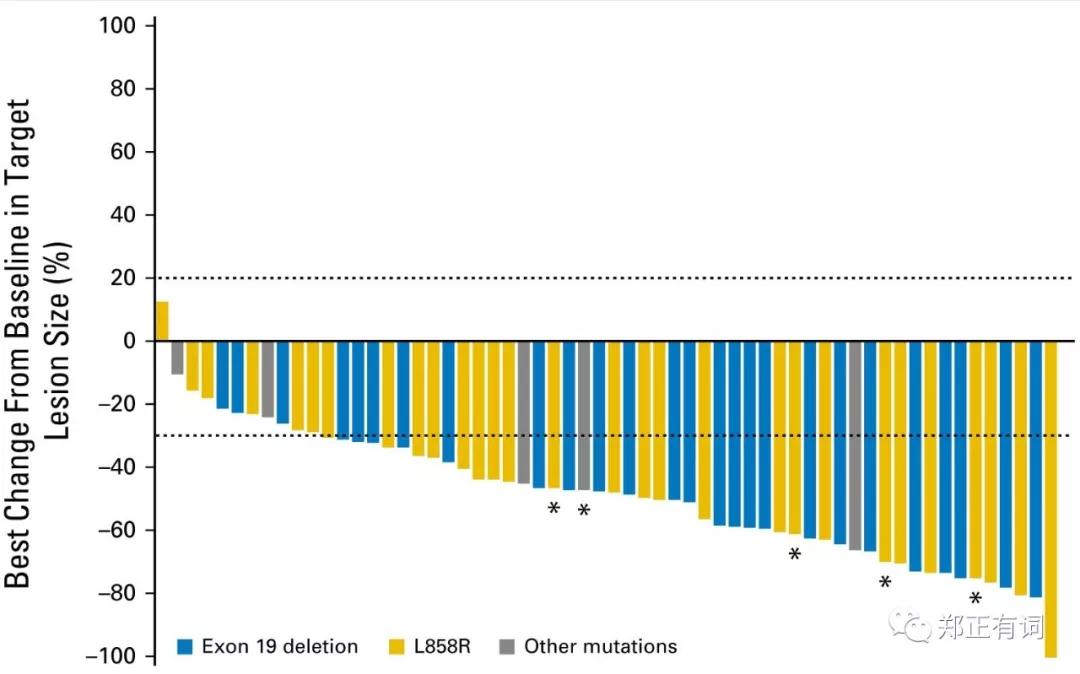
80mg组,ORR 67%、PFS 22.1m、DOR 19.3m。
160mg组,ORR 87%、PFS 19.3m、DOR 16.7m。
汇总,ORR 77%、PFS 20.5m、DOR 18.0m。
研究显示,两组患者的PFS并无显著差异。
进展机制:
38名进展患者留取血标本。
19名未测到肿瘤cDNA。
余19名检测到肿瘤cDNA的患者中,有9名发现潜在耐药机制,包括MET扩增(n=1)、EGFR及KRAS扩增(n=1)、MEK1突变(n=1)、KRAS突变(n=1)、PIK3CA突变(n=1)、EGFR C797S突变(n=2)、JAK2突变(n=1)、HER2 20号外显子插入(n=1)。
EGFR T790M突变未检测到。
安全性检测发现,80mg组药物安全性更高。
Osimertib作为不可逆性EGFR-TKI,既往多用于EGFR突变且T790M耐药的那部分人群。
因为有研究指出,EGFR突变且一线接受诸如吉非替尼、厄洛替尼等EGFR-TKI药物并发生耐药者,有约60%为T790M突变。
一项meta分析指出,在EGFR突变患者中,一线予吉非替尼/厄洛替尼,其中位PFS 11.0月,而一线化疗中位PFS 仅仅5.6月。因此,该研究所得到的20.5月的中位PFS证实了Osimertinib更优的治疗效果。
在该研究中,38名进展的患者中,有19名检测出肿瘤cDNA成分,其中又有9名检出潜在耐药机制。针对未检测出的那10名患者,作者指出其耐药机制可能是那些无法通过液体活检检出的机制(比如小细胞转化)。
结论:EGFR突变患者一线给予Osimertiniba可以获得很好的ORR及较长的PFS。
点评:一项证实在EGFR突变型NSCLC一线使用Osimertinib有效性的RCT研究,I级临床证据。
相关话题持续发酵,没有人怀疑Osimertinib的有效性,目前讨论的重点是,接受Osimertinib并发生进展的患者中,没有发现T790M的突变。
因此有学者认为其较长的生存时间可能为伪优势,因为如果采用传统TKI,虽然PFS较短(11月),但是其中60%可出现T790M突变,从而再接受Osimertinib则可再获得中位约10.1月的PFS。

二、非小细胞肺癌肾上腺寡转移

寡转移:转移病灶<5枚
同时性寡转移:原发肺癌确诊后6月内出现的寡转移
异时性寡转移:原发肺癌确诊后6月后出现的寡转移
这是一项囊括法国多家医疗中心的回顾性研究,纳入对象为既往接受根治性手术切除的非小细胞肺癌患者,同时后续发生了肾上腺转移(认定为寡转移)并予积极手术切除的患者。
采用相对准确的评估方法,包括支气管镜+全身PET/CT+脑MRI。
在2004.1~2014.12间,总共有59名患者满足此标准从而被纳入研究。
患者具体信息:
同时转移 26名、异时转移 33名;
同侧转移 22名、对侧转移 34名、双侧转移 3名;
原发肺癌 N0 22名、N1 15名、N2 19名。
最终此人群中位生存时间77月,5年生存率59%。
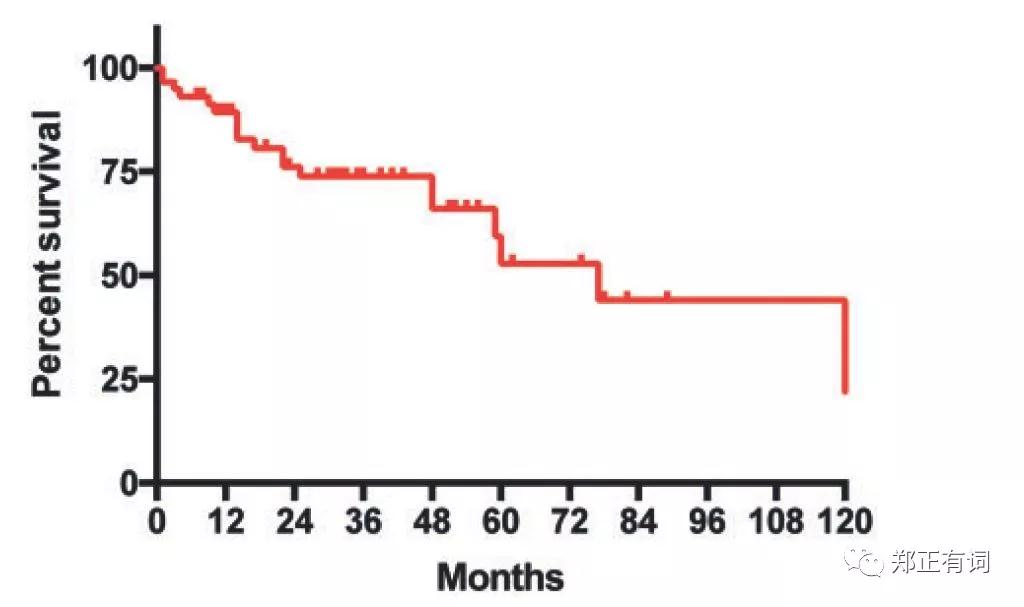
经过多因素分析发现,对预后有独立影响的因素有原发瘤纵隔淋巴结转移(N2)及病理鳞癌。
而转移时限性(同时性/异时性)、肾上腺切除后的辅助治疗(是否接受放疗/化疗)、原发肿瘤的切除方式(叶切/扩大叶切/全肺切)以及转移形式(单侧/对侧转移)均对预后无显著影响。
结论:接受过彻底的检查而确定为寡肾上腺转移的患者,接受手术能够获得较好的治疗效果。
点评:针对寡肾上腺转移开展的多中心回顾性临床研究,证据级别IIB。
进一步确定经过仔细筛选确定的寡转移状态的患者,可以经过激进的局部治疗获得较好的疗效。但是,文中关于寡转移切除后无需加用放疗/化疗的结果,我保留我的态度。

三、新辅助治疗对食管癌生存质量的影响

PF-physical functioning;EA-eating problems;GQOL-global quality of life;
EM-emotional problem; FA-fatigue; nCRT-neoadjuvant chemoradiotherapy
食管癌新辅助治疗(CROSS研究)的进一步随访结果,分析新辅助治疗对远期生存质量的影响。
纳入363名患者,新辅助治疗177例,单纯手术186例。
新辅助治疗方案为(卡铂+多西他赛+41.4Gy)。
生活质量问卷量表为欧洲癌症研究和治疗组织生活质量调查问卷系列的核心30题(C-30)及食管癌专项24题(OES-24)。
所有患者均接受术后3/6/9/12月的常规问卷;此外,新辅助治疗组患者还有一次术后一周的额外问卷。
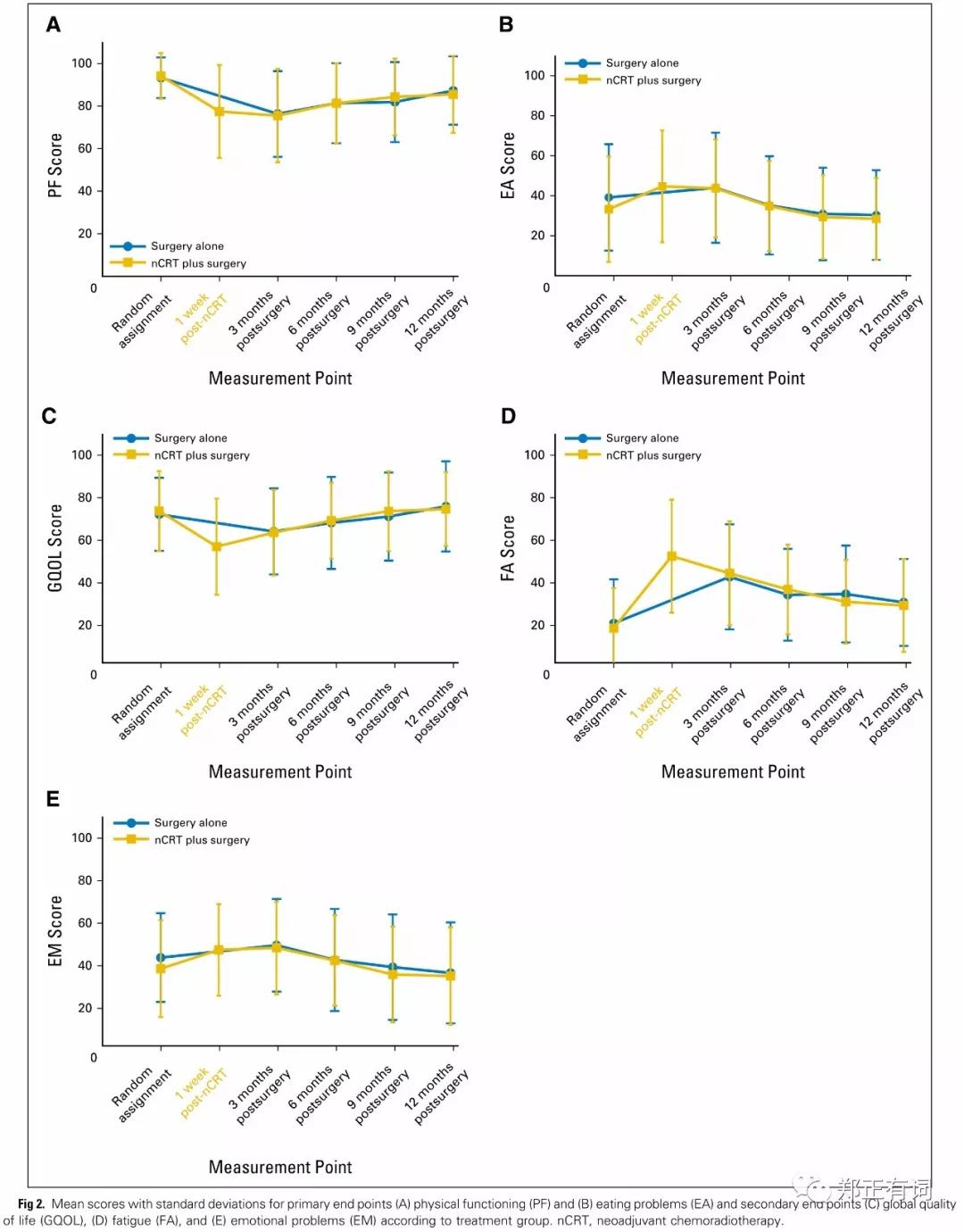
如上所示,术后生活质量相关分析指标有体力状态、吞咽问题、总体生存质量、疲乏及情绪问题。
比较单纯手术组与新辅助治疗组发现,治疗方案的选择并未对术后生活质量造成显著影响。
不同的指标在术后随访过程中,均表现为先江后升的过程,即均在3月出现一个显著下降,而后逐步回升,但是指标不同,回升速度及所达高度也不一样:
体力状态,术后3月下降以后开始逐步回升,半年趋于稳定,但无法达到术前基线水平;
吞咽问题,术后3月上升以后开始逐步下降,半年后达到术前基线水平;
总体生存质量,术后3月下降后开始逐步回升,9月达到术前基线水平;
疲乏感,术后3月下降以后开始逐步回升,半年后趋于稳定,但无法达到术前基线水平;
情绪问题,术后3月上升后开始逐步下降,9月达到术前基线水平。
结论:新辅助治疗并不会对食管癌术后生活质量造成显著影响。
点评:赫赫有名的CROSS研究先后出了3篇大paper,2012年的NEJM(短期随访及完全缓解)、2015年的Lancet Oncology(长期随访)及今天这篇JCO(生活质量)。研究发现新辅助治疗对生活质量无明显不良影响。I类临床证据。
有了这项研究,将来临床医生在管理临床患者时,针对患者的术后恢复,应该有一个大概的时间判断了。无法达到术前状态的是体力状态和疲乏感,除此之外,吞咽问题、总体生存质量以及情绪问题都能在6-9月以后达到基础水平。

四、肺上沟瘤15年治疗经验总结

该研究为位于意大利米兰的欧洲肿瘤研究所所报道。
旨在总结该中心从1998-2013年期间的肺上沟瘤的治疗经验,总共纳入研究对象94名。
对全部患者采用肿物与胸壁的en-bloc切除。
手术路径的选择基于肿瘤部位,其中肿瘤侵犯前方大血管时选用前入路、肿瘤侵犯后侧胸壁时选择后入路、联合入路适用于位于中部或前部的肿瘤。
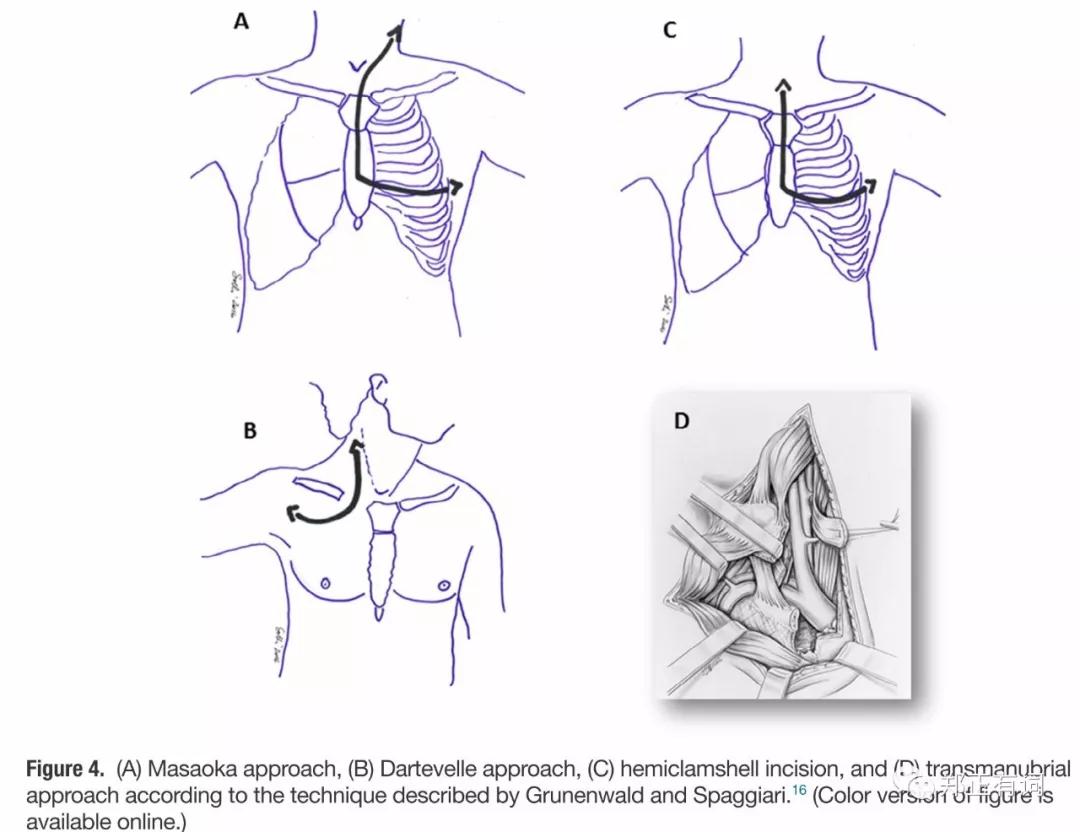
有48名患者接受术前诱导治疗。
手术路径选择,前路径 46名、后路径35名、联合路径13名。
肺叶切除方式,叶切78名、全肺切除3名、气管重建6名、楔形切除7名。
中位肋骨切除数2(1-5根);42名接受胸壁重建,21名接受相应的血管重建。
85名患者实现根治性切除(90.4%);90天死亡率9.6%。
在末次随访时,有32名患者存活,4例患者出现复发。
其2-y、5-y、10-y总生存率分别为51%、35%及23%。
生存分析显示,前入路、完全切除、新辅助质量后完全缓解及淋巴结状态阴性患者治疗效果好。
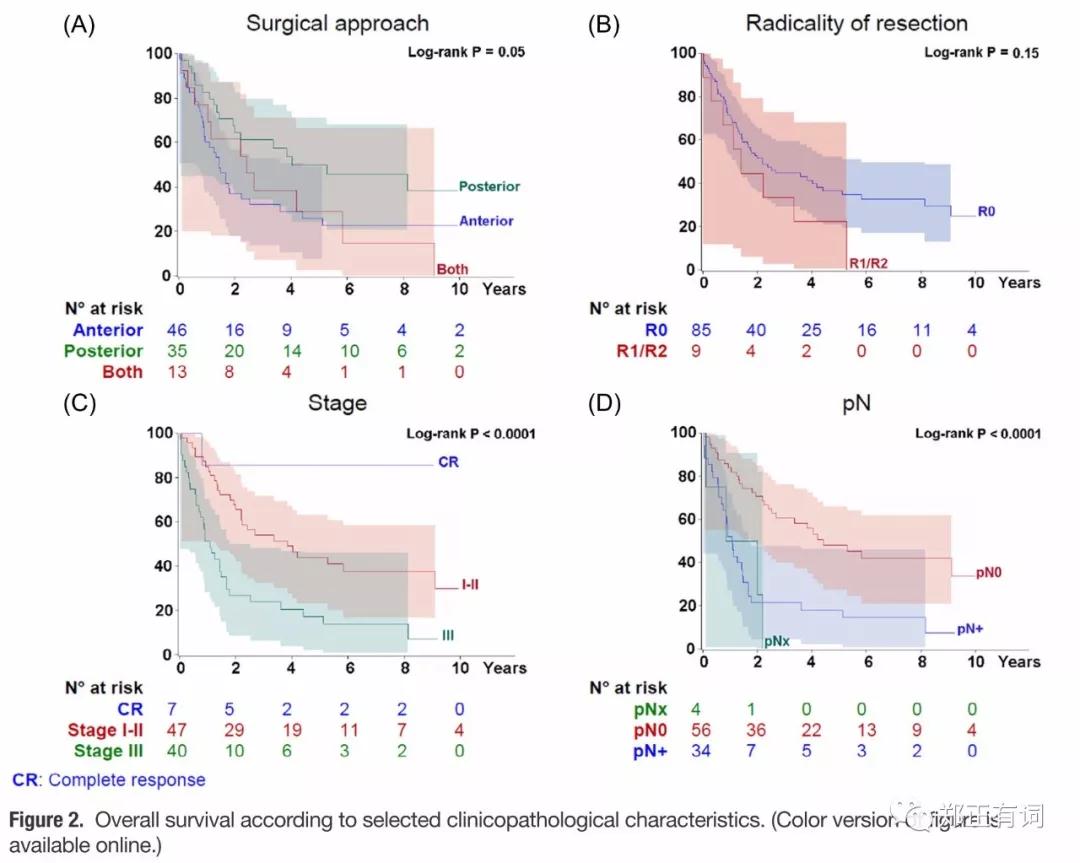
诱导治疗组尽管5年生存率较高(43% vs 26%),但未达到统计学意义(p=0.24).
多因素分析中,则仅仅只有淋巴结状态保持统计学意义,并被确定为独立预后风险因素。
结论:肺上沟瘤是一种严重的疾病,但是经过谨慎的选择及处理仍然可以获得较好的治疗效果。其中,淋巴结浸润、不完全切除、血管浸润是最重要的不良预后因素。新辅助治疗可能有助于疗效改善。
点评:单中心、长时间的回顾性分析。IIB类临床证据。
该研究中,适于推广的数据是肺上沟瘤的预后因素,比如淋巴结状态、完全切除等。因为手术路径的选择与肿瘤部位有关,因此应该对手术路径的选择的预后意义进行审慎评估,不能粗鲁地定性为前路径患者能够获得较好的效果。
上沟瘤是一种难治性肿瘤,对主刀者手术技巧要求很高,因此其生存率在不同中心、乃至不同的主刀医生之间应该是存在显著的差异的,因此,该研究中的生存率仅供参考,并不适用于其他医疗中心。多说一句,意大利米兰欧洲肿瘤研究所好强呀,虽然病例并不多。
专家介绍:

作者微信公众号:












 苏公网安备32059002004080号
苏公网安备32059002004080号


