【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!
 100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
患者病史摘要
性别:女
年龄:28岁
主诉:胰腺脂肪肉瘤术后6月余,4周期化疗后。
体能状态评分:KPS评分:80分
既往史:平素健康,否认“高血压”、“糖尿病”、“冠心病”等疾病史,否认肝炎、疟疾等传染病史,2015年6月19日行胰腺体尾切除术,否认其他手术史,否认外伤史,否认输血史,否认药物、食物过敏史,预防接种随当地进行。
家族史:无与患者疾病类似病史。父母、兄弟、姐妹健在。无遗传病史,无高血压等家族遗传倾向疾病。无肿瘤家族史
入院查体:上腹沿肋缘下可见长30cm横切口,愈合良好; 左腹部膨隆,可触及肿块;
入院实验室检查:
CRP :265.4mg/L↑; PCTQ :0.185ng/ml↑ 超敏C反应蛋白测定:195.0mg/L↑;离子紊乱: 血清钾测定 3.28mmol/L;肿瘤标志物正常;
影像学检查
入院时胸、腹、盆腔等影像学检查及CT/MRI片子

病理及免疫组化结果
病理结合免疫组化结果:恶性间叶源性肿瘤;免疫组化结果显示:C6:CK(-)、Vimentin(+)、CD34(+)、CD117(±)、S-100(局部+)、Dog-1(±)、CD68(散在+)、Desmin(-)、MyoD1(灶状+)、Bcl-2(+)、Beta-Catenin(-)、Ki67(25%)
外院病理会诊提示:梭形细胞恶性肿瘤,去分化脂肪肉瘤可能性大;
 HE染色结果
HE染色结果
同时,患者对去分化脂肪肉瘤的非特异性生物标志物MDM2的增殖表达的FISH检测结果如下:
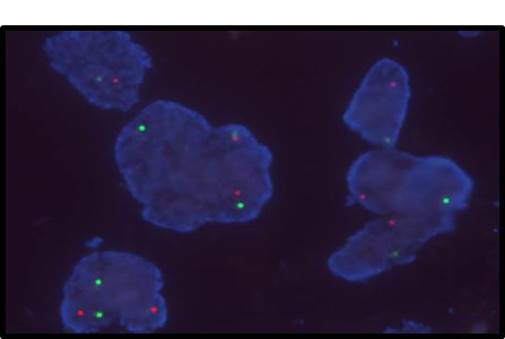
MDM2的增殖表达的FISH检测结果
入院前治疗史
此前是否经过手术? 术式?术后病理,淋巴结转移情况
2015年6月因胰腺占位就诊于中国医科大学附属第一医院胰腺外科行胰腺体尾切除术,术中见肿瘤位于胃后方,胰腺上缘,左侧达脾门,20cm×15cm×10cm,将肿物,胰体尾部,脾脏整块切除。
病理示:恶性间叶源性肿瘤,考虑为去分化脂肪肉瘤。免疫组化结果显示:C6:CK(-)、Vimentin(+)、CD34(+)、CD117(±)、S-100(局部+)、Dog-1(±)、CD68(散在+)、Desmin(-)、MyoD1(灶状+)、Bcl-2(+)、Beta-Catenin(-)、Ki67(25%);后腹膜腔可见数个淋巴结影。
是否曾接受术前或术后放疗? 时间、方式、总量?(常规放疗/伽马刀?)
未接受术前或术后放疗。
是否曾接受术前或术后化疗(是否同步放疗?是否放疗后辅助?化疗的方案、剂量,疗程?)
2015年7月27日于中国医科大学附属第一医院肿瘤内科行4个周期术后辅助化疗;
方案:表阿霉素联合异环磷酰胺方案;
具体:剂量:
表阿霉素 55 mg vd d1-2,
异环磷酰胺 1.8 g vd d1-5,
美司钠 360 mg vd d1-5 21days/cycle
2016年7月疾病进展后行甲磺酸阿帕替尼联合紫杉醇单药治疗;
具体:
甲磺酸阿帕替尼 500 mg PO 1/d,
紫杉醇 210 mg VD d1, 21days/cycle
既往放/化疗治疗转归(RECIST标准):
2015年12月(术后六个月)患者出现左侧腹腔巨大实性占位性病变,直径约112mm×76mm,符合脂肪肉瘤复发,给予阿帕替尼靶向治疗。
2016年2月22日口服阿帕替尼2个月后复查CT,病灶由146.1mm缩小到85.3mm,病灶缩小41.78%,疗效评价为:PR。
2016.2-2016.6月患者规律服用阿帕替尼并定期复查CT,提示病灶稳定SD。
2016年7月患者于当地医院复查CT提示患者腹腔出现新增病灶,疗效评价PD。
经多学科会诊及查阅相关文献,阿帕替尼可增加紫杉醇敏感性,故于2016年7月行甲磺酸阿帕替尼联合紫杉醇单药治疗, 2周期后(2016年9月18日)复查CT提示:病灶较前缩小3.4%,疗效评价为SD
2016年11月03日4周期后复查CT,提示肿瘤较9月份缩小7.61%,较7月份缩小32.9%总体疗效评价PR。
2016年11月至今,定期复查,疗效评价SD。
PFS:
术后复发:2015年06月-2015年12月 PFS: 6个月;
疾病进展:2015年12月-2017年7月 PFS:19个月;
入院诊断
患者入院诊断:胰腺脂肪肉瘤术后
1) 病灶(复发)出现时间:2015年12月
2) 病灶部位(复发?播散?转移?)
CT检查提示:左侧腹腔巨大实性占位性病变,直径约112mm×76mm,临近多发结节灶,周围胃壁及肠壁受累可能,符合脂肪肉瘤复发;后腹膜腔可见数个淋巴结影。
对症治疗
改善离子紊乱状态,血清钾测定 4.03mmol/L
经规范化止痛治疗,NRS评分降为0分;
鉴于患者发热且感染指标升高,在抽血培养之后给予抗炎治疗,3天后患者体温降至正常,感染指标下降;
患者体力及精神状态明显好转,KPS评分80分。
一线治疗方案(如果含靶向药物)
靶向药物:阿帕替尼
开始使用靶向药物时间: 2015 年 12 月 31 日
用法用量:500 mg PO 1/d
临床症状好转距首次用药时间 :1个月
用药持续时间:7个月
有无剂量调整,如何调整:无
剂量调整的原因:无
一线治疗疗效评估——概述
治疗一个周期后:术后复发后,给予患者阿帕替尼抗肿瘤血管生成剂靶向治疗后复查病灶缩小41.78%,疗效评价为:PR。
治疗两个周期后:2016.2-2016.6月患者规律服用阿帕替尼并定期复查CT,提示病灶稳定SD。
一线治疗后的转归及下一步治疗策略
疾病缓解
疾病首次进展:2016年07月
治疗策略:准备给予甲磺酸阿帕替尼联合紫杉醇单药治疗
当疗效为疾病首次进展(二线治疗)
进展时间:2016年07月
进展时影像学图片:2016年7月患者于当地医院复查CT提示患者腹腔出现新增病灶,疗效评价PD。
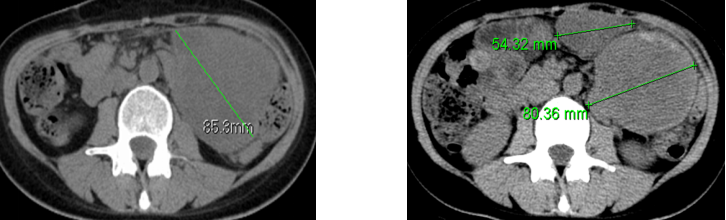
(2016.2) (2016.7)
诊断:胰腺脂肪肉瘤术后
二线治疗方案选择
方案组成:甲磺酸阿帕替尼联合紫杉醇单药治疗
是否含靶向药物?含有靶向药物阿帕替尼
开始时间: 2016年 7 月 13 日
用法用量:甲磺酸阿帕替尼 500 mg PO 1/d, 紫杉醇 210 mg VD d1,
21days/cycle
治疗周期数:4周期
疗效评估情况:PR
方案是否调整,如何调整:无
二线治疗方案—化疗
化疗方案:紫杉醇单药
化疗药物用法用量:紫杉醇 210 mg VD d1, 21days/cycle
开始时间:2016年 7 月 13 日
化疗周期数:4周期
有无剂量调整,如何调整:无
剂量调整的原因:无
二线治疗方案(如含靶向药物)
靶向药物:甲磺酸阿帕替尼
开始使用靶向药物时间: 2016 年 7 月13日
用法用量:甲磺酸阿帕替尼 500 mg PO 1/d,
临床症状好转距首次用药时间 :一个月
用药持续时间:至今
有无剂量调整,如何调整:无
剂量调整的原因:无
二线治疗疗效评估
恢复或转归情况(RECIST):PR
PFS时间:12个月
PS评分:1分
后续治疗
方案组成:阿帕替尼单药维持
是否有靶向药物:有
开始时间: 2016 年 12 月
用法用量:甲磺酸阿帕替尼 500 mg PO 1/d
治疗周期数:7个月
疗效评估情况:SD
方案是否调整,如何调整:无
整体治疗疗效评估—影像学检查
(1)术前可见左侧腹腔巨大软组织肿块影,密度不均,与胰腺分布不清,术后无肉眼可见病灶。
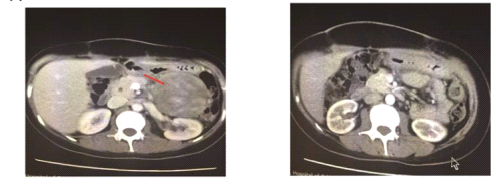
手术前(2015.06.04) 手术后(2015.06.22)
(2)术后6个月(2015.12.30)CT提示复发:左侧腹腔巨大实性占位性病变,直径约112mm×76mm,临近多发结节灶,后腹膜腔可见数个淋巴结影。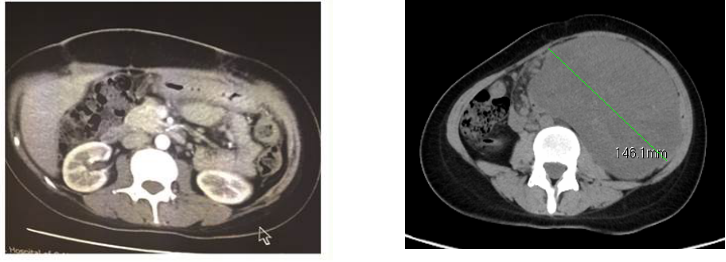
手术后(2015.06.22) 术后复发(2015.12.30)
(3)患者既往行表阿霉素联合异环磷酰胺术后辅助化疗,化疗相关不良
反应较重,对化疗十分抵触,复发后拒绝更换方案一线化疗。经过pubmed检索,Oncotargets and Therapy (IF 2.5)报道。阿帕替尼单药治疗转移性纤维组织肉瘤一例,PFS达到10个月。遂给予患者阿帕替尼抗肿瘤血管生成剂靶向治疗,2个月后复查病灶缩小41.78%,疗效评价为:PR。
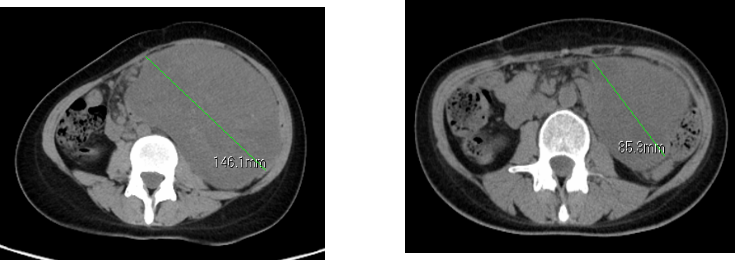
阿帕替尼治疗前(2015.12.30) 阿帕替尼治疗后(2016.2.26)
(4)2016.2-2016.6月患者规律服用阿帕替尼并定期复查CT,提示病灶稳定SD。

(2016.2.26) (2016.5.15)
(5) 2016年7月患者于当地医院复查CT提示患者腹腔出现新增病灶,疗效评价PD。
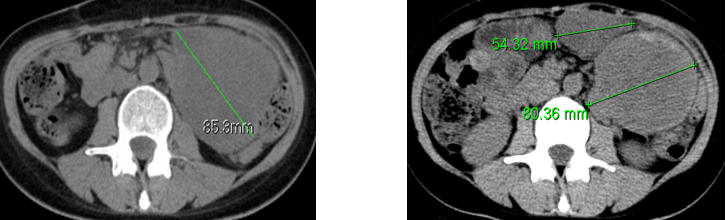
(2016.2) (2016.7)
(6) 2016年7月行甲磺酸阿帕替尼联合紫杉醇单药治疗,2周期后复查CT提示:病灶较前缩小3.4%,疗效评价为SD。
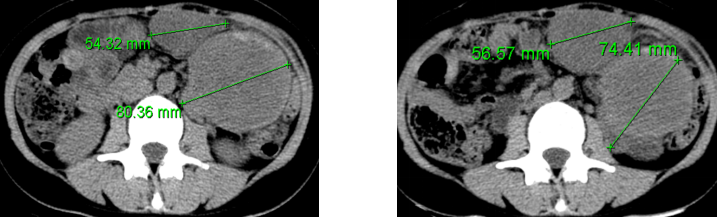
(2016.7.11) (2016.9.18)
(7)4周期后复查CT,提示肿瘤较9月份缩小27.61%,较7月份缩小32.9%总体疗效评价PR。
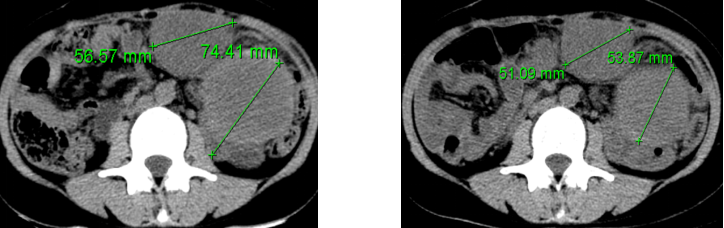
(2016.9.18) (2016.11.03)
治疗疗效评估——肿瘤标志物

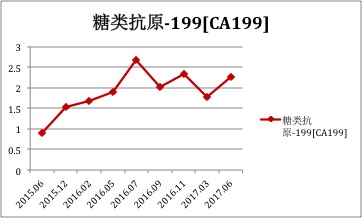
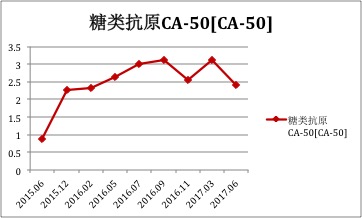
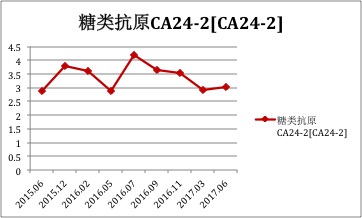
总结:患者治疗策略一览

治疗转归
目前患者情况 疾病稳定,阿帕替尼已治疗获益19个月,疗效显著,远高于复发性脂肪肉瘤的平均生存期,不良反应可控,患者耐受性良好。
问题:若患者再次复发,下一步的治疗意见
放疗+阿帕替尼?or 更改化疗方案? or 再次行基因检测,选择靶向治疗药物?or 其他(比如放射性粒子植入)?
此病例共有1位入围选手点评:63-章琦。病例提供作者为:31-韩涛,详情如下:
点评医生简介:63-章琦

点评内容分享:
胰腺脂肪肉瘤是罕见的胰腺恶性肿瘤,对于脂肪肉瘤本身来说,发生在胰腺也非常少见。该例去分化脂肪肉瘤邻近胰体尾部,故起病隐匿,患者首次就诊时肿瘤已十分巨大。因未发现远处转移或大血管侵犯,手术切除是应当首先考虑的。然而,脂肪肉瘤往往存在多中心起源,且肿瘤边缘境界不甚清晰,术后复发频繁。患者术后6月即出现复发,且肿瘤已超过10cm,提示肿瘤对术后辅助化疗方案(表阿霉素联合异环磷酰胺)敏感性有限。因免疫组化提示VEGFR阳性,尝试性地使用了阿帕替尼(VEGFR2抑制剂),取得了非常好的疗效。脂肪肉瘤血供较丰富,且该病例恰有VEGFR2在肿瘤细胞中过表达[1],阿帕替尼的使用应该说有一定理论支撑。在VEGFR2高表达的其它类型脂肪肉瘤中,阿帕替尼也有成功的报道[2],可见VEGFR2对肉瘤细胞自身的生存和增殖存在一定作用。作为一种口服抗血管靶向药,阿帕替尼最初在胃癌中应用,但近年来已有许多临床试验或病例报道将其尝试于肺癌、胶质瘤等其它实体瘤。但不论是在胃癌还是肺癌中,阿帕替尼的中位PFS仅为5个月左右;而本例患者在阿帕替尼单药获益6个月的前提下,通过联合紫杉醇再次实现4个月左右的疾病控制期,并以阿帕替尼单药维持至今。阿帕替尼整体获益近19个月,并可能继续延长,疗效不可谓不惊人。首先,阿帕替尼单药在6个月后出现进展,提示巨大胰腺去分化脂肪肉瘤在对阿帕替尼的敏感性上可能与其它实体瘤类似;但更大的获益实际上来源于阿帕替尼的跨线应用,并将其作为紫杉醇的增敏剂。当然,从后面阿帕替尼再次单药维持获得半年以上的临床稳定期,也有可能紫杉醇的应用克服了肿瘤对阿帕替尼的耐药。无论如何,作为第一个阿帕替尼应用于胰腺脂肪肉瘤的成功病例报告,该病例充分提示了个体化靶向治疗在未来肿瘤综合治疗中的价值,也提醒肿瘤医生对目前已具有现实干预方法的靶点进行筛查的重要性。
由于肿瘤的异质性,靶向治疗迟早会出现耐药,后续治疗永远是肿瘤科医生需要预先考虑的。患者目前尚无远处转移证据,可行PET-CT,若排除远处转移,患者仍有手术机会,在一般情况允许的条件下可考虑再次手术切除病灶。因患者对紫杉醇+阿帕替尼方案较敏感,复发可继续沿用此方案。若方案失效,可考虑新药曲贝替定或艾日布林,并跨线联用阿帕替尼。后由于脂肪肉瘤通常对放化疗和免疫治疗均不敏感[3],术后辅助治疗在脂肪肉瘤的综合治疗中贡献有限。参考《腹膜后脂肪肉瘤诊断和治疗专家共识(2016)》,针对基因变异的试验性治疗是值得尝试的。在征得患者首肯的前提下可行基因检测,若提示存在可使用的靶向药物,亦可作为后期备选方案。
--------------------------------------
病例提供作者简介:31-韩涛

病例提供作者自评:
脂肪肉瘤是肉瘤的异质体,主要发生在软组织、四肢和腹膜后腔,其中去分化脂肪肉瘤5年生存率为15-30%,且存在远处转移风险。由于其病灶生长隐匿,且大部分患者早期无明显症状,所以在诊断、治疗等方面存在一定难度。该患者脂肪肉瘤原发于胰腺,术中得以完整切除,术后病理明确诊断,但其存在较为年轻(28岁)、肿瘤巨大(最长径> 15厘米)、肿瘤位于腹膜后位及手术切缘存在肿瘤细胞等提示不良预后的高危因素,引起我们的重视。
术后辅助化疗、解救化疗是软组织肉瘤预防复发转移的重要手段。目前,软组织肉瘤专家共识推荐阿霉素或异环磷酰胺为辅助化疗用药。但胰腺脂肪肉瘤的相关报道甚少,尚无明确的诊疗方案,急需探究更为个体化的有效治疗手段。2016年04月刊登在Medicine杂志上的一篇报道显示阿帕替尼对转移性腹腔、盆腔圆细胞脂肪肉瘤疗效显著,引起学者对脂肪肉瘤抗血管生成靶向治疗的广泛关注。
阿帕替尼为特异性表皮生长因子VEGFR2的拮抗剂,具有抗血管生成和抗肿瘤细胞增殖双重作用。本例患者一线治疗过程中免疫组化结果示VEGFR (+),提示抗血管生成有效,考虑患者因经济原因无法承受静脉抗血管生成药物的高昂费用,且口服给药依从性较高,故选择甲磺酸阿帕替尼做为本例去分化脂肪肉瘤患者的一线靶向治疗用药。单药阿帕替尼500mg PO 1/d 2个月后复查CT疗效评价为PR,患者一般状态显著改善,生活质量明显提高。但2016年7月复查CT结果提示PD。查阅相关文献显示阿帕替尼可以逆转紫杉醇耐药性,增强紫杉醇疗效,遂给予患者阿帕替尼跨线治疗并联合紫杉醇化疗,这是阿帕替尼在脂肪肉瘤中首次进行的跨线用药,且4周期后得到了积极的疗效评价,结果为PR,周期性化疗结束后继续口服阿帕替尼维持治疗,定期复查,疗效评价为稳定,PFS 11个月。至今,患者口服阿帕替尼获益19个月,显著高于脂肪肉瘤报道的中位生存期。
胰腺脂肪肉瘤属于软组织肉瘤的一种,极为罕见,而对于复发的软组织肉瘤治疗目尚无明确的治疗原则,放化疗的有效率均不理想。鉴于肉瘤富血供的生物学特征,抗血管生成治疗具有潜在的治疗价值,而在本病例中体现了阿帕替尼抗血管生成治疗对特殊部位巨大软组织肉瘤的积极疗效,进一步利用阿帕替尼跨线治疗并增强紫杉类药物的疗效,为患者带来极大的生存获益,达到了长期带瘤生存。现今精准治疗理念越来越被人们所认可,靶向治疗药物及其应用方式的扩展必将在肿瘤精准治疗的征途中得到更完美的诠释与发展。
--------------------------------------
以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!
以上所有点评参考文献略。
版权声明














 苏公网安备32059002004080号
苏公网安备32059002004080号


