【35 under 35】风采展示第二轮已经开始啦!本轮正经名叫“病例实战分析”,不正经名叫“互相伤害”,哈哈哈~100位入围选手每人提交一个有意思的病例,并就病例提出一个问题,形成一个病例库!然后100位入围选手从病例库中任意选择一个非自己提供的病例进行解读并回答问题!最后,我们将呈现病例+别人的点评+病例提供者自己的点评,同步展示!
 100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
100位小伙伴已将自己的病例提交,并提出了问题,让我们一起先阅读下精彩病例吧!
患者男性,62岁,“因痰中带血1周”于外院行胸部CT提示“右肺占位”,于2015年8月27日收入院。
入院评估:
一般情况及体格检查:PS评分0分,血压120/75mmHg。皮肤巩膜无黄染,浅表淋巴结未触及肿大;右中肺局部呼吸音减低,余双肺呼吸音清,心脏听诊、叩诊无异常;腹平软,未及明显肿块,无压痛及反跳痛,肝脾下界未触及。
既往史:高血压病史20余年,最高血压150/95mmHg,目前口服“尼群地平”、“阿替洛尔”,血压可控制在110-120/70-80mmHg。
入院检查:血、尿、粪常规,肝肾功能,凝血功能,传染病未见明显异常。肺癌相关肿瘤标志物CEA 3.68ng/ml、NSE 19.98ng/ml、CY211 12.77ng/ml。
胸部增强CT:右肺中叶肿块,最大横截面106*76mm,考虑肺癌;右肺散在结节,考虑转移;右
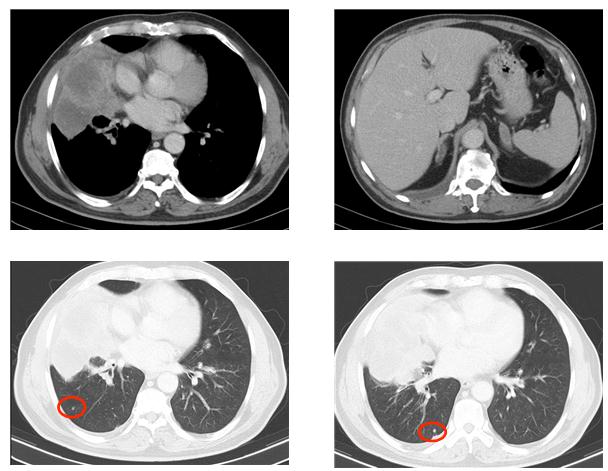
侧肾上腺增粗,左肾上腺见肿块影,最大横截面37*15mm,考虑转移。
脑部平扫+增强MRI:左侧颞叶,右侧顶叶斑点影,考虑缺血性改变;右侧额叶静脉畸形;两侧筛窦、上颌窦炎症。
腹部彩超:未见异常。
锁骨上及颈部淋巴结彩超:无肿大淋巴结。
全身骨ECT:右前第5、6、7肋骨,胸12和腰3椎体骨质代谢活跃。
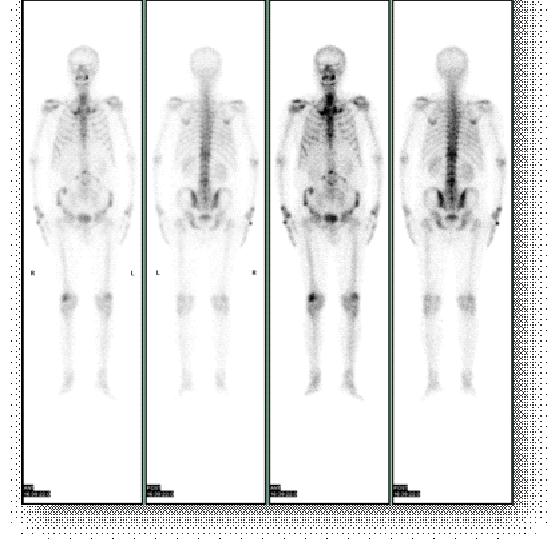

胸腰椎MRI:1.胸腰椎退行性变;2.胸12椎体压缩性骨折;3.腰4-骶1椎间盘变性、膨出。
CT引导下肺穿刺活检病理结果:(右肺)低分化腺癌。免疫组化CK+,Vim-,CK5/6-,P40-,CK7+,TTF-1+,Ki-67+约50%。
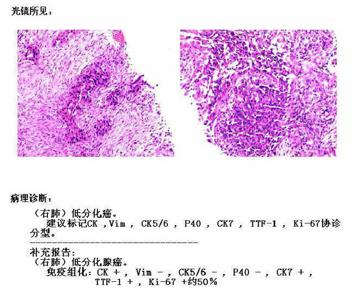
肺癌八基因NGS检测(包含EGFR、KRAS、ALK、ROS1、BRAF、RET、ERBB2、MET):EGFR 21外显子L858R突变,突变丰度 45.1%;MET基因拷贝数扩增,CN=4.7 。
问题:该患者下一步应该选择何种治疗?依据是什么?
此病例共有2位入围选手点评,分别为50-邵宜、58-吴芳;病例提供作者为:26-张国伟。详情如下:
点评医生简介:50-邵宜
 点评内容分享:
点评内容分享:
根据患者病史、影像学及病理检查结果,IV期肺腺癌诊断明确。首先进行基因检测寻找可能的治疗靶点,二代测序结果显示,患者具有EGFR 21外显子L858R突变,并且检测出MET基因拷贝数增加。
上世纪90年代,肺癌中MET通路异常得以发现。近年来,MET 14外显子突变和MET扩增被认为是NSCLC具有驱动性的基因改变。MET拷贝数增加有两种不同的途径:染色体多体型和真正的基因扩增,前者主要来自于7号染色体的多拷贝,不属于癌基因改变,而真正的扩增来自于局灶或区域基因的复制,因此不同于染色体多体型,MET扩增才是真正的驱动癌基因活化。随着荧光免疫杂交技术(FISH)的应用,MET和7号染色体着丝点部分(CEP7)比值(MET/CEP7)可用来鉴别染色体多体型和真正的扩增[1],因此,此病例应行FISH检测MET情况,以明确患者是否具有真正的MET扩增。尽管MET/CEP7≥1.8就可说明存在MET扩增,但进一步分析显示,高水平的MET扩增(MET/CEP7)较少出现和其他基因共突变情况,并和MET抑制剂疗效相关,因此,“MET扩增阳性”通常被定义为FISH MET/CEP7≥5[2]。
MET扩增和一代EGFR TKI的获得性耐药相关[3],15%-20%获得性耐药是通过MET扩增作为旁路活化机制,通过ERBB3依赖的PI3K途径,绕过EGFR抑制而产生。联合抑制EGFR和MET治疗获得性耐药EGFR突变NSCLC的试验已在进行,一项MET抑制剂INC280联合吉非替尼治疗一/二代EGFR TKI耐药的MET阳性(IHC 3+,或IHC 2+且基因拷贝数≥5)患者的Ib/II期研究中,65名评估疗效患者,ORR 18%,DCR 80%,表现出较好的临床活性[4]。
而原发的MET扩增发生于约3%EGFR突变患者,可导致EGFR TKI原发性耐药[5]。一些个案报道和初步临床试验证实联合EGFR和MET抑制似乎也可克服MET导致的EGFR TKI原发性耐药。JTO上曾报道一例肺癌患者,基因检测示EGFR 21外显子突变, FISH确定MET扩增(MET/CEP7>15),患者使用厄洛替尼4周后进展,改为厄洛替尼+克唑替尼治疗。由于之前I期研究表明同时给予克唑替尼时,厄洛替尼血液浓度增加,因此给厄洛替尼100 mg Qd+克唑替尼250 mg Qd减量治疗,5周后评估病灶反应显著,不良反应只有1度皮疹和腹泻。今年ASCO的壁报公布了一项厄洛替尼联合MET抗体emibetuzumab(Emi)一线治疗EGFR突变NSCLC的随机II期研究,141名患者随机接受厄洛替尼+Emi或厄洛替尼单药治疗,中位PFS分别是9.3 vs 9.5个月,而亚组分析显示,MET高表达患者,PFS是15.3个月,中位OS分别是未达到vs 20.6个月[ASCO 2017 摘要9019]。MET蛋白高表达和高水平扩增相关[02],因此对于具有EGFR和MET基因共改变患者,EGFR和MET的联合抑制可能有效。
综上,对此患者建议行FISH明确有无真正的MET扩增。如果没有,可行EGFR TKI单药治疗;如果同时存在MET扩增,可能存在EGFR TKI原发耐药,可考虑行EGFR和MET的联合抑制治疗,或行化疗。
点评医生简介:58-吴芳
 点评内容分享:
点评内容分享:
治疗策略
一、一线治疗首选一代或二代EGFR-TKI,如:吉非替尼,厄洛替尼,埃克替尼,阿法替尼。如在充分取得患者的理解下,也可EGFR-TKI联合METi(克唑替尼)作为一线治疗。
二、若单用EGFR-TKI,则一月后复查,同时可通过动态血检来监测EGFR突变及MET扩增的丰度变化,若疗效评价为CR、PR或SD则可以继续单药EGFR-TKI,若PD则EGFR-TKI联合METi(克唑替尼)治疗或培美曲塞+铂类化疗+/-贝伐珠单抗。
三、双膦酸盐药物如唑来膦酸抑制骨转移,若靶向治疗及唑来膦酸处理后骨痛仍难以缓解,可考虑骨转移灶的放疗。
治疗依据
患者62岁男性,临床诊断为:原发性支气管肺癌(右中肺 周围型 低分化腺癌 T4NxM1c IV期 L858R突变/MET扩增)并肺、骨、肾上腺转移。
一、首选EGFR-TKI的依据
基于IPASS、First-SIGNAL、NEJ002、WJTOG-3405、OPTIMAL、EURTAC、LUX-Lung 3、LUX-Lung 6、CONVIENCE等研究,目前NCCN指南及CSCO指南均一类证据推荐EGFR敏感性突变的晚期NSCLC首选一代或二代EGFR-TKI治疗。
二、EGFR-TKI联合METi的依据
1、MET扩增是EGFR-TKI获得性耐药的机制之一
EGFR敏感性突变如19del和L858R,对EGFR-TKI具有很有的反应。但1年左右往往会出现耐药。目前已知的主要分子机制有EGFR二次突变,肺癌表型改变,旁路激活等。大量研究证实MET扩增是导致第一代或第三代EGFR-TKI继发性耐药的旁路激活机制之一[1],约占继发性耐药的5%-20%,对于这类患者,若要克服耐药,需要采用EGFR-TKI联合 MET TKI的治疗策略,相关临床试验见后。
2、原发性MET扩增可能是EGFR-TKI原发性耐药的机制之一
原发性MET扩增见于1-3%的晚期肺腺癌中,同时出现EGFR敏感性突变和MET扩增的病例非常罕见,目前仅有个案报道,尚无相关临床研究。Nemoto等[2]2015年在ICCJ上报道了一例EGFR L858R突变伴MET扩增的肺癌病例,76岁肺腺癌,吉非替尼治疗40天PD,换厄洛替尼20天后疾病进展,患者死于呼吸功能衰竭,提示EGFR-TKI对于伴有MET扩增的EGFR敏感性突变患者疗效差。Gainor等[3]2016年在JTO上报道了一例EGFR突变伴MET扩增的肺腺癌病例,采用厄洛替尼150mg Qd,4周后评价疗效PD,改为厄洛替尼100mg Qd+克唑替尼250mg Qd,6天后患者咳嗽完全缓解,5周复查CT,评价疗效PR。Bahcall等[4]2016年在Cancer Discov上报道了一例EGFR 19del突变晚期肺腺癌,对一代及二代EGFR-TKI均原发耐药,基因检测提示同时存在MET扩增,采用三代EGFR-TKI联合I型METi(Savolitinib),肿瘤显著缩小,8个月后出现耐药,基因检测提示新发的METD1228V突变,换用一代EGFR-TKI联合II型METi(Cabozantinib)后再次有效。而在本团队的在近期的肺癌诊疗过程中也遇到过一例血检L858R突变(丰度4.12%)伴MET(CN=2.31)扩增的肺癌患者,埃克替尼一线治疗20天后即出现疾病进展,再次血检提示L858R突变(丰度17.44%)伴MET(CN=3.53)扩增,建议患者埃克替尼联合METi克唑替尼,患者坚决拒绝继续口服埃克替尼,单药克唑替尼,一月后评价疗效PR。虽然目前对于原发性MET扩增与EGFR敏感性突变的相互作用还并不完全清楚,但从有限的证据提示:原发性MET扩增可能也是EGFR-TKI原发性耐药的机制,但此时EGFR 通路仍然活跃,所以,EGFR-TKI与METi的联合治疗可能是这类患者很好的选择。但由于目前尚缺乏MET扩增引起EGFR TKI原发耐药患者的临床研究,而我国目前上市的METi仅有克唑替尼,临床研究已证实其用于MET扩增NSCLC的有效性,但在我国尚未获批治疗MET阳性NSCLC患者,同时价格昂贵,所以采用联合治疗作为一线治疗必须与患者充分沟通并取得其理解。
3、EGFR-TKI与METi联合治疗的相关研究
目前主要集中在EGFR-TKI继发性耐药的患者中。NCT01610336研究中METi(INC280)联合吉非替尼用于TKI治疗后的EGFR敏感性突变伴MET扩增晚期NSCLC患者。NCT1866410研究中为cabozantinib联合厄洛替尼。NCT01900652研究为LY2875358联合厄洛替尼。
病例提供作者简介:26-张国伟
 病例提供作者自评:
病例提供作者自评:
该患者属于EGFR敏感突变的晚期NSCLC,按道理来讲治疗毫无悬念——首选EGFR TKI。但偏偏,NGS检测发现了同时存在的另一个基因改变:MET基因扩增。
MET是一种发现于1984年的原癌基因,位于7号染色体的长臂,编码同名跨膜蛋白,其配体为肝细胞生长因子(HGF),HGF/MET信号通路信号通路是调节细胞增殖、分化和运动的重要通路,其异常的激活可导致多种肿瘤的发生和发展。目前认为在肺癌中MET的活化形式可能包括MET 14外显子跳跃突变、MET扩增、MET过表达,这三种情况可能存在内在联系——比如突变和扩增可能会导致过表达,但也可能各自独立。
着眼于该病例,我们暂时撇开其他,着重来谈一谈MET扩增。笔者将MET扩增可能出现的情境归纳为3种:1、在EGFR TKIs继发性耐药时检测出的MET扩增:这种情况约占EGFR TKIs继发性耐药机制的20%(仅次于T790M);2、单独出现的原发性(de novo)MET扩增,这种情况不同文献报道发生率在2%-20%;3、与其他驱动基因同时出现的de novo MET扩增,主要是与EGFR突变同时出现——也就是本病例的情况,发生率约3%。
MET扩增的界定目前还没有一个统一的方法和标准:检测方法包括FISH、基于PCR的方法、NGS等;所取cut-off值从GCN(Gene copy number)>1.31到GCN>5不等【1】。而在克唑替尼治疗原发性MET扩增的I期临床试验中采取了这样一种界定方式【2】:1.8≤MET/CEP7≤2.2为低度扩增, 2.2≤MET/CEP7≤5称为中度扩增,MET/CEP7>5为高度扩增。什么意思呢?所谓MET/CEP7是MET拷贝数和7号染色体计数的比值,MET的扩增可能由两种情况引起(见下图)【1】:其一是7号染色体数目的增加(也就是多倍体)、其二是单纯的该基因位点的拷贝数增加,也就是真性扩增。有观点认为多倍体形式的GCN增加,并非真正的驱动基因,而这种情况反而占了所谓“扩增”的多数。因此采用MET/CEP7比值可以排除多倍体的影响,甄别出真正的扩增。
(图片来源:Kawakami H, Cancers, 2014)
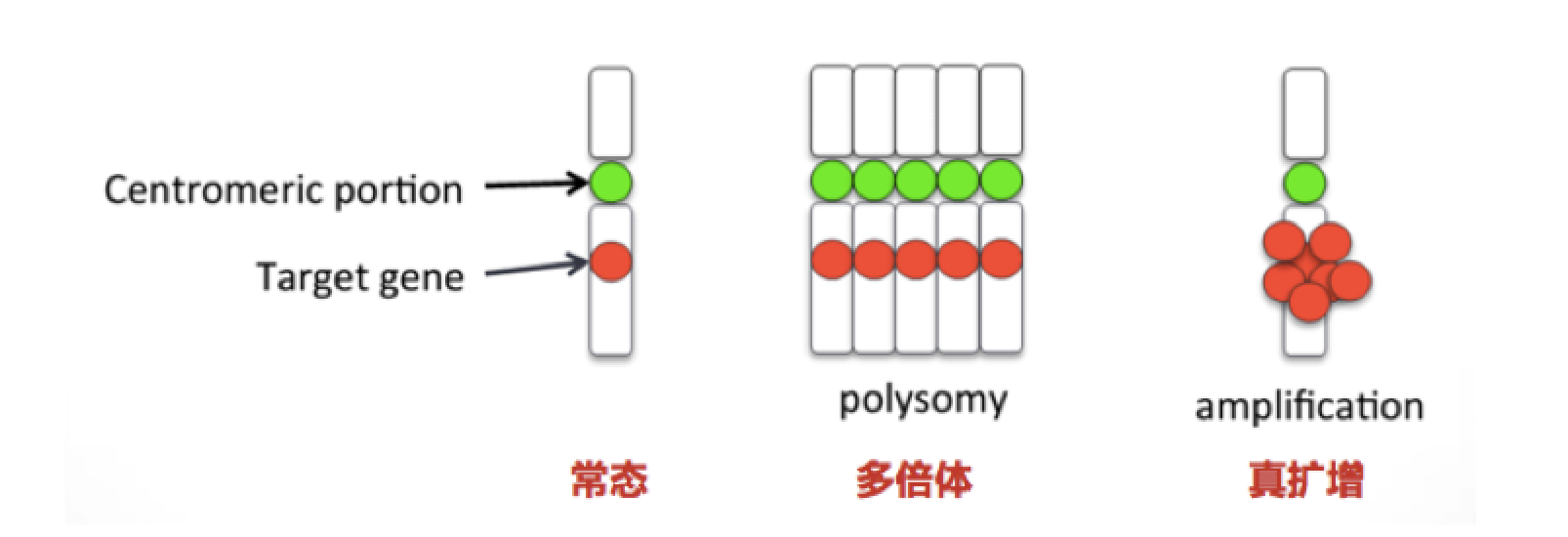
从以上回归到我们的病例当中,该患者MET的GCN为4.7,这个数值究竟属于低度、中度、还是高度扩增?另外NGS并不能区分该拷贝数的增加是来自于多倍体还是真性扩增,它在该患者肿瘤的发生发展中是否起到驱动基因的作用?这是我们所不明确的。
另外,在以上MET扩增出现的3种情境中,我们有前瞻性的证据表明de novo扩增MET抑制剂有效[2]、MET扩增导致的EGFR TKIs耐药者应用EGFR TKI联合MET抑制剂有效[3],但唯独在本例的情况中,并无证据。吴一龙教授团队2015年在ASCO发表的一篇摘要中[4],回顾性分析了原发性MET过表达与EGFR敏感性突变同时存在时EGFR TKI的疗效,同时用FISH做了MET扩增,其中仅有的2例MET扩增合并EGFR突变的患者中,1例PR,1例SD。
综上所述,笔者认为对于该患者我们有几个不确定如下:
MET扩增GCN=4.7究竟如何界定:低、中、高扩增?多倍体?真扩增?
原发性MET扩增与EGFR突变同时存在EGFR TKIs有效与否?
MET抑制剂在这类患者中的疗效如何?
因此,再综合对于EGFR+MET抑制剂联合治疗不良反应的担心、以及经济方面的考量,笔者认为先选择EGFR TKI应用,并密切观察症状和影像学变化,若无效,则联合MET抑制剂克唑替尼;若有效,则用至病情进展后重新行组织或血液的NGS检测,若MET扩增仍然存在,则于该时联合克唑替尼。
以上为【35 under 35】的观点,您怎么看?欢迎广大肿瘤医生在下方留言发表您的观点!














 苏公网安备32059002004080号
苏公网安备32059002004080号


