编译: 血液科那条鱼
1. 前言
过去 20 年里,AML治疗最巨大的进展可谓是采用维甲酸和三氧化二砷(ATO)治疗急性早幼粒细胞白血病(APL)。虽然新的靶向药物的研究迅速,如FLT3-IDH抑制剂的研发,但非APL患者的治疗现状并不乐观,治疗手段缺乏创新性,只能依赖于调整标准化疗剂量或改进造血干细胞移植(HSCT)的技术。
年轻患者完全缓解率(CR)可达80%以上,5年总生存率(OS)40%左右。老年患者AML治疗仍是一个难题,去甲基化药物能提高老年患者的中、短期生存率,但治愈率仍然处于令人失望的低值。本文总结近期有效的临床试验数据和用经批准的药物的研究,为临床AML常规治疗提供理论基础。
2. 一线诱导治疗
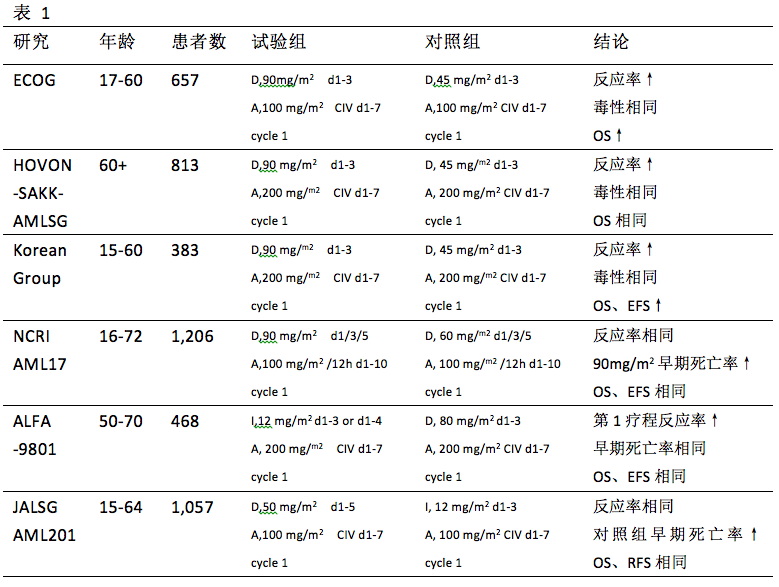
阿糖胞苷联合蒽环类药物仍然是AML诱导治疗的标准方案,俗称7 + 3方案,1-7天输注阿糖胞苷100或200 mg/m2·d,1-3天柔红霉素60mg/m2·d。近期的临床试验(表1)对更高剂量的蒽环类或阿糖胞苷或对诱导方案中添加另一药物均做了对比。然而,由于一些关键参数和诱导疗程等因素不同,研究结果直接可比性较差。
蒽环类药物
其中4项研究评估了高剂量柔红霉素。ECOG试验纳入患者为60岁以下,European trial纳入荷兰、比利时、德国、瑞士患者的年龄在60岁以上,研究对比了“7+3”方案当中的“3”部分,45 mg/m2·d vs 90 mg/m2·d。研究结果显示高剂量柔红霉素与较高的CR率相关,在平均年龄较低的ECOG试验中,OS是在90 mg/m2·d明显延长,包括FLT3-ITD突变和NPM1、DNMT3A基因突变的患者的OS均受益。然而在老年人群(60-65岁)的试验中,OS的提高很有限,CBF-AML也获益甚少。
该结果说明,柔红霉素45 mg/m2·d并非65岁以下年龄段患者的最佳选择,然而剂量提高至90mg/m2·d是否妥当尚不确定,毕竟该剂量已经超过2010年国际指南的60 mg/m2·d。最近英国NCRI AML17试验解决了这个问题,在第1疗程比较了剂量60和90mg/m2·d,患者在第2疗程接受剂量改为50 mg/m2·d剂量,中期分析发现90mg/m2/d组的60天死亡率显着增加,OS无受益,至于亚组中的生存获益与否仍需更长时间的随访。
急性白血病法国协会(ALFA)9801研究比较了柔红霉素和去甲氧基柔红霉素,结果未能体现80 mg/m2柔红霉素优于标准剂量12 mg/m2的去甲氧柔红霉素。日本急性白血病研究组(JALSG)的AML201研究报告中有类似结果。
总而言之,60或90mg/m2·d柔红霉素与12 mg/m2·d去甲氧柔红霉素抗白血病活性相似。
阿糖胞苷
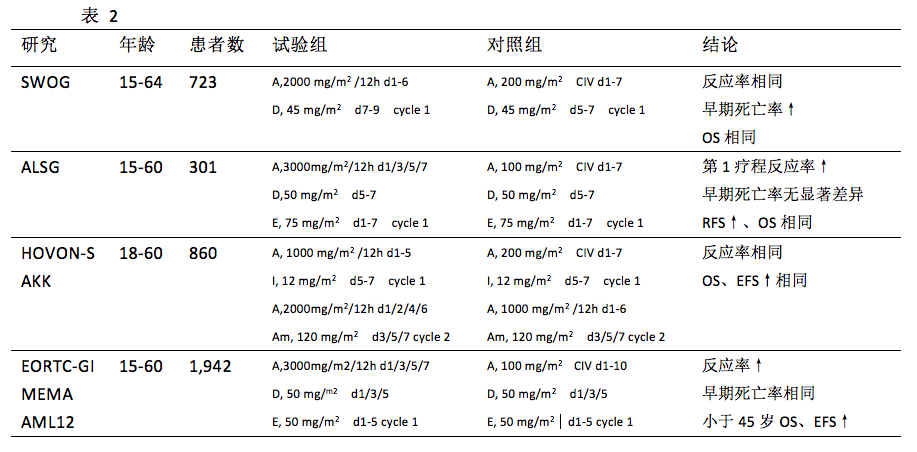
表2总结了近期探索AML诱导方案中阿糖胞苷的剂量和疗程的临床试验。西南肿瘤组(SWOG)和澳大利亚白血病研究组(ALSG)的结果显示更高剂量阿糖胞苷剂量的临床疗效未能获益,反而增加了毒性。另外两项研究解决了该问题,一是应用去甲氧柔红霉素或安吖啶,另一是使用较低剂量依托泊苷。
在比利时-荷兰合作血液疾病试验组(HOVON)和临床肿瘤研究瑞士组(SAKK)中患者随机分配,分别接受第1疗程阿糖胞苷200 mg/m2·d加第2疗程1000 mg/m2·12h持续使用6天,和第1疗程高剂量(HIDAC)1000 mg/m2·12h持续5天加第2疗程第1、2、4、6天2000mg/m2/12h。两组CR率、无事件生存率(EFS),和OS均相似,高剂量组毒性大。
EORTC和GIMEMA 白血病组进行将患者随机分配,阿糖胞苷10天100 mg/m2·d,或HIDAC组第1疗程第1、3、5、7天3000 mg/m2·12h。研究结果显示HIDAC组CR率高,并且年龄低于45岁患者OS延长有统计学意义。最后,在德国人群研究显示“常规剂量”“中剂量”“高剂量”三组间OS无显著差异。因此,在IDAC或HIDAC方案中增加阿糖胞苷剂量是否能使患者受益尚无定论。
“剂量密集型”方案
另一种增加诱导强度的方法是通过调整二次化疗时间,通常提前进行二次化疗(在第7天和第14天)。然而,近期“剂量密集型”方案研究均表明,剂量密集型方案并不优于标准的7+3方案,特别是否定了高剂量柔红霉素的使用。
三药联合
有6项研究评估了联合3或6 mg/m2吉妥单抗在诱导方案中的作用。即使SWOG S0106将柔红霉素降低到45mg/m2·d,但仍由于早期死亡率高而提前终止试验,同时FDA也要求将其撤出。另4项研究显示联用吉妥单抗用于诱导或巩固治疗疗效都显著,但也会导致严重肝损和持续性血小板减少。
EORTC/GIMEMA 组同样观察到毒性增加和临床获益甚少的情况。最终分析,对该药的临床疗效的评价是否定。吉妥单抗的临床反应可能受CD33表达水平影响,白血病克隆程度和药物外排强度等相关因素都由AML遗传学决定,因此低中等风险的异常基因包括FLT3-ITD的患者对吉妥单抗反应良好,不良核型疗效较差。总而言之,吉妥单抗的使用需要改进,至少目前用于部分亚型患者身上反应并不理想。
嘌呤类似物
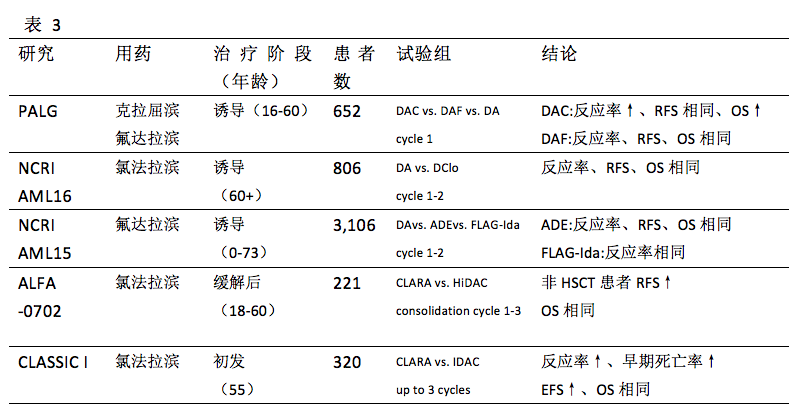
在表3中总结了嘌呤类似物的相关研究。在波兰急性白血病组(PALG)研究中,虽然克拉屈滨的结果并非最理想,但其延长OS。有趣的是,克拉屈滨不仅使高危患者获益,不良核型的50岁以上患者也能获益。单药使用氯法拉滨或与阿糖胞苷联用都表现出显著的抗白血病活性。
然而,British AML16 trial显示嘌呤类似物与柔红霉素联用疗效不佳,其他与7+3方案的研究成果也即将公布,我们十分期待。在British AML15 trial年轻组的研究显示,氟达拉滨、阿糖胞苷、粒细胞集落刺激因子(G-CSF)和去甲氧基柔红霉素(FLAG-Ida)带来的缓解率更高,且减少了复发风险。
索拉非尼
索拉非尼是一种FLT3-ITD AML的多激酶抑制剂。德国白血病研究联盟(SAL)的AML试验评估了索拉非尼联合标准诱导方案和IDAC巩固方案用于老年患者的疗效,结果显示索拉非尼不能有效改善EFS和OS。
亚组分析也有类似结果,如FLT3-ITD阳性亚组,索拉非尼的诱导治疗结果差——早期死亡率高和CR率较低。另一研究将索拉非尼联合7 + 3诱导方案和HiDAC巩固,初步结果显示,CR率没有最显著差异,然而索拉非尼组EFS和复发存活率(RFS)显著提高。FLT3-ITD阳性亚组显示,EFS无显著差异,索拉非尼的RFS和OS有延长趋势。
3. 缓解后治疗
HiDAC巩固治疗
对于不接受HSCT的年轻患者而言,HiDAC巩固治疗是首选,第1、3、5天用阿糖孢苷3g/m2每日两次。目前阿糖胞苷最佳剂量是确定的,但使用周期还有待研究。HiDAC和IDAC方案适合联合其他靶向和非靶向药,ALFA-0702/CLARA发现相比HiDAC巩固方案,氯法拉滨联合IDAC可延长RFS。
异基因造血干细胞移植(HSCT)
治疗AML最重要的决策之一是评估患者第1次缓解时异基因造血干细胞移植相关的疗效/风险。移植是防止AML复发的最好手段,但目前治疗相关发病率和死亡率(TRM)仍较高,尤其是老年患者。对于AML风险低的患者,复发的风险要足够低而救治率高至足以推迟HSCT——该策略已应用于多种研究。
在这些研究中,大多数患者接受同胞供者的骨髓移植,HSCT获益年龄通常小于40,采用完全相合的无血缘关系供体和相合有血缘关系的供体,两者结果是相似的,中高危的AML年轻患者通常在第1次缓解后考虑采用同胞异基因造血干细胞移植或完全相合的无血缘关系供体移植。
分子标记或白血病相关的异常免疫表型是评估微小残留病灶(MRD)的有力工具,用于预测患者是否应进行异基因造血干细胞移植。MRD已是ALL最终是否进行造血干细胞移植的决策因素,以取代遗传因素。但早期不良MRD是否进行 HSCT还有待考究。
4. 靶向治疗AML亚型
核心结合因子相关性急性髓细胞白血病(CBF-AML)
吉妥单抗联合强化化疗能使CBF-AML年轻群体OS获益。最近的研究已经评估了KIT抑制剂——达沙替尼潜在CBF-AML中的效益,这部分患者常有KIT突变或KIT受体过度表达效益。在法国的一项研究中,通过强化巩固化疗的患者如有持续MRD或分子生物学复发,但又不合适进行HSCT,可有资格进行12个月达沙替尼的化疗,目前正在进行III期临床试验。
FLT3 基因突变的AML
FLT3-ITD突变是AML最常见的一种预后不良的突变,至少在年轻和复发的患者中是如此。 MRC AML15 trial显示来他替尼(Lestaurtinib)相关化疗未能改善复发/难治性FLT3-ITD AML患者预后。目前已有大型国际III期临床试评估米哚妥林联合7+3方案用于初诊FLT3-ITD阳性患者疗效。
正如此前提及,目前为止还没有明确的证据表明索拉非尼联合强化化疗能使FLT3-ITD阳性患者获益。在一项II期临床试验中也表明索拉非尼联合强化化疗用于FLT3突变的AML老年患者疗效也有限。另一方面,FLT3-ITD阳性患者在HSCT后使用索拉非尼可见一定疗效。在早期的试验中发现第一、二代抑制剂FLT3选择耐药突变已成为一个普遍现象。
NPM1基因突变的AML
大约30%的CN-AML患者有NPM1基因突变,与FLT3-ITD基因突变不同的是,NPM1基因突变多数情况下早期出现。多项用全反式维甲酸(ATRA)治疗非APL的研究结果不一致。在大型MRC试验发现,另加ATRA无显著疗效。
另一方面,德国两个AML研究组报道ATRA使NPM1突变AML患者获益。产生研究矛盾的结果的原因目前尚未明确。最近,临床前研究显示三氧化二砷(ATO)对NPM1突变的AML有效,强调ATO对于该亚型患者的益处。通过大量的临床研究才确立ATO治疗APL的地位,因此ATO治疗NPM1基因突变阳性AML患者或许也得依赖大量的临床实验。
IDH突变的AML
在AML中,大约有10-15%的患者异柠檬酸脱氢酶1、2基因突变。关于IDH1、IDH2突变抑制剂在早期临床试验的结果令人印象深刻,III期临床研究也将复发IDH2突变的患者开始研究。
具有不良遗传学特征的AML
在难治性AML群体中,改善早期缓解率仍然是重要的临床终点,尤其是及时考虑HSCT。在PALG克拉屈滨研究中,不良细胞遗传学亚组的患者反应良好。同样的,与大型单中心临床试验的7+3方案相比,克拉屈滨联合阿糖胞苷、G-CSF和米托蒽醌(CLAG-M)治疗高危AML患者效果好。然而,非靶向药氨萘非特(amonafide)联合阿糖胞苷产生效益未能超过7+3方案。
5. 治疗老年AML
与年轻患者相比,老年AML患者总体预后差——CR率较低,很少有长期存活,因此研发老年的抗白血病药一直是该领域的热点。即使短期疗效可见,但极少老年患者随访生存超过两年。在老年患者中,年龄本身不是主要的影响因素,预后还受患者本身和AML相关的因素左右,一般健康状况和器官功能障碍影响强化化疗耐受性。
治疗老年AML的最重要的临床决策仍然是评估强化化疗的利益/风险。至于是否推荐第1次缓解时HSCT,目前没有唯一的指南。根据ELN分类,低风险AML老年患者可能从标准治疗中获益。两大国际试验显示,低甲基化地西他滨联合阿扎胞苷疗效好,LDAC生存期延长1年,但长期生存患者的比例无显著改变,具有不良细胞遗传学和骨髓增生异常相关变化的患者对阿扎胞苷反应良好。
到目前为止,研究结果显示替吡法尼、ATO、吉妥单抗、vosaroxin联合LDAC疗效不佳。Quizartinib、ganetespib、tosedostat、selinexor联合LDAC目前正在研究中。单药sapacitabine或氯法拉滨的疗效同样没能超越LDAC。已有II期临床试验开展关于Polo样激酶抑制剂Volasertib联合LDAC或vosaroxin联合地西他滨,这些研究由于老年患者的耐受性较差而不能对疗效进行评价。
6. 复发/难治性AML治疗
复发/难治性AML的治疗仍不明确。简单临床表现和疾病参数,如年龄,第1次完全缓解持续时间、细胞遗传学特征和HSCT均是用于评价复发的有用参数。大多数AML亚型(非APL)临床治疗主要目的是作为患者HSCT的桥梁,无论是靶向治疗如FLT3抑制剂或对能耐受的患者开展强化化疗,中危和高危的AML患者同种异体移植结果受初发时情况的影响。
最佳的化疗方案组合、药物剂量和疗程仍然悬而未决,例如除蒽环类药物之外的阿糖胞苷以及阿糖胞苷的剂量目前仍无定论。日前,两家大型公司赞助的研究评估了氯法拉滨或vosaroxin联合IDAC,研究结果显示氯法拉滨增加55岁以上的患者的反应率,增加患者HSCT率,但同时也增加毒性和早期死亡率,但未能改善OS。
结论
总之,成人AML的治疗研究有所进展,但许多问题有待解决。尽管许多新的药或治疗方案在飞速发展,但大多数成人AML患者的远期疗效不佳,应大力鼓励将他们纳入到前瞻性临床试验。此外,标准化临床试验程序和合理的对照组将有助于对比的试验结果,并提高未来的治疗建议的可行性。
(本文为肿瘤资讯原创,转载须授权且注明出处)
欲了解更多血液肿瘤、淋巴瘤相关资讯,与全国各地血液肿瘤、淋巴瘤医生交流与讨论,请扫描以下二维码,添加肿瘤资讯小助手-Dinna微信,备注“血液肿瘤”!
参考文献:
An update of current treatments for adult acute myeloid leukemia
http://www.bloodjournal.org/content/early/2015/12/10/blood-2015-08-604520.long?sso-checked=true















 苏公网安备32059002004080号
苏公网安备32059002004080号


