外周T细胞淋巴瘤(PTCL)是一组来源于成熟T 细胞和NK细胞的具有高度异质性的非霍奇金淋巴瘤(NHL)[1]。流行病学数据显示,PTCL 的发病率存在显著的地域差异,在亚洲国家中PTCL 占NHL 的15%~25%,在我国PTCL 占NHL 的25%~30%,高于西方国家的10%~15%[1]。PTCL 的异质性使其在临床治疗进展中面临复杂且棘手的难题[2] 。
中国一项回顾性多中心研究 [3],收集了从 2014 年 1 月至 2022 年 3 月期间,中国南方 21 家医疗中心 1031 例 PTCL 患者的临床资料,研究结果不仅揭示了中国 PTCL 的临床特征、治疗模式及预后评估关键信息,更凸显了 CD30 在PTCL诊疗和预后全程管理中的临床价值,为临床实践提供了重要参考。
多维临床特征:亚型分布与疾病特点差异显著
亚型分布:共收集 1031 例 T 细胞淋巴瘤患者,排除 94 例前驱 T 淋巴母细胞淋巴瘤患者。在 937 例成熟 T 细胞或 NK 细胞淋巴瘤患者中,结外 NK/T 细胞淋巴瘤(ENKTL,鼻型)占比最高(35.5%),其次为血管免疫母细胞性 T 细胞淋巴瘤(AITL,21.6%)和外周 T 细胞淋巴瘤 - 非特指型(PTCL-NOS,20.1%),系统性间变性大细胞淋巴瘤(sALCL,含 ALK + 和 ALK - 亚型)合计占 15.7%。
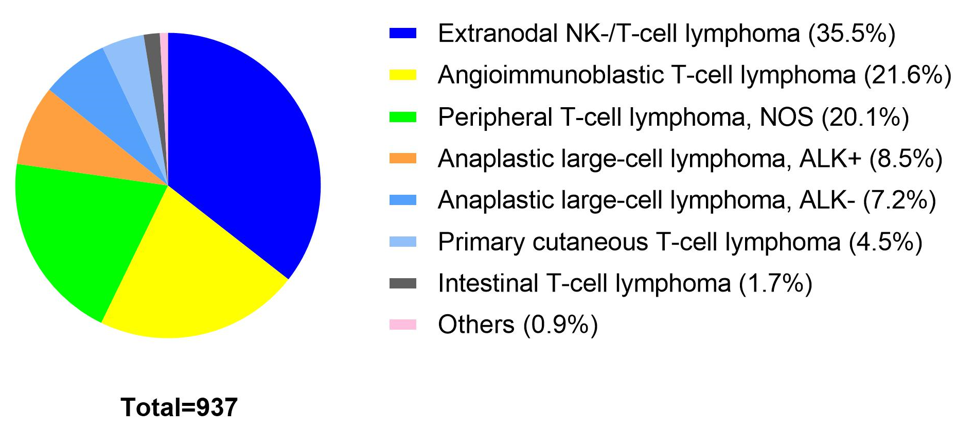
男性占比 66.3%;初始诊断时中位年龄为 52 岁(范围:14-103 岁),其中 ALK+ ALCL 组患者中位年龄最小,为 33 岁(范围:14-85 岁)。
多数患者确诊时处于 Ann Arbor III-IV 期(70.5%),且存在多个(≥1 个)结外侵犯部位(77.1%);ENKTL、PTCL-NOS、AITL 亚型患者更易出现高危 IPI 评分(45.7%-64.1%)。
44.7% 的患者存在 LDH 升高,42.5% 的患者存在 β2M 升高,21.0% 的患者存在骨髓侵犯,且 AITL 亚型中上述指标异常的发生率最高。
67 例(8.3%)患者接受了造血干细胞移植(HSCT),其中 57 例(7.1%)接受自体造血干细胞移植(auto-HSCT),10 例(1.2%)接受异基因造血干细胞移植(allo-HSCT)。
病毒感染发生率相对较高:其中 HBsAg 阳性患者占 11.4%,既往 HBcAb 阳性患者占 42.9%。
治疗方案与生存结局:揭示 PTCL 未满足的临床需求
治疗方案
一线治疗方案:以蒽环类药物为基础的化疗(48.0%)最为常用,其次为含培门冬酶的方案(28.5%)。含培门冬酶的方案在 ENKTL 亚型中应用更为广泛(72.1%),而以蒽环类药物为基础的化疗则是其他亚型的首选方案。所有患者中,PD-1 抑制剂和西达本胺单药的使用率较低;其中,PD-1 抑制剂在 ENKTL 亚型中使用率相对较高(12.4%),西达本胺单药在 AITL 亚型中使用率相对较高(8.3%)。2.9% 的患者接受了含CD30靶向药物的治疗方案。
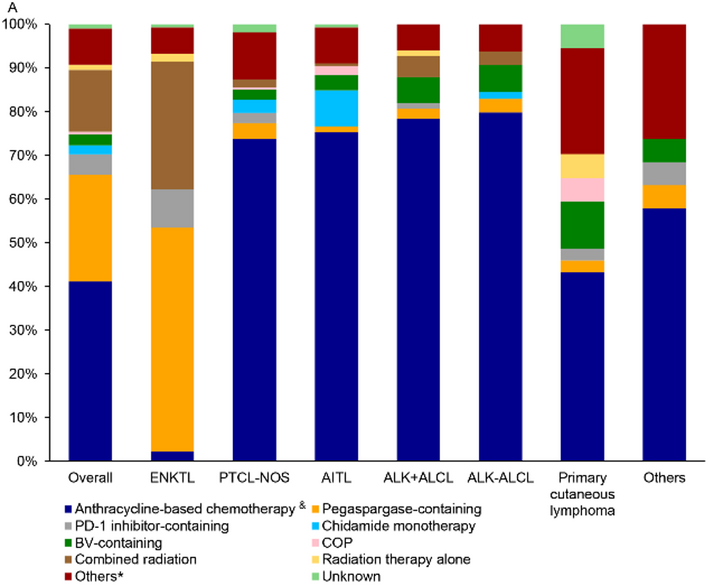
二线治疗:在 230 例(28.6%)接受二线治疗的患者中,最常用的方案为含吉西他滨的方案(23.9%)和含西达本胺的方案(24.3%)。含吉西他滨的方案在 ALK- ALCL(59.1%)和 ALK+ ALCL(35.7%)亚型中应用更频繁,而含西达本胺的方案在 ENKTL、PTCL-NOS、AITL 亚型中更常用。与一线治疗相比,二线治疗中含 PD-1 抑制剂的方案使用率(10.9%)有所上升。
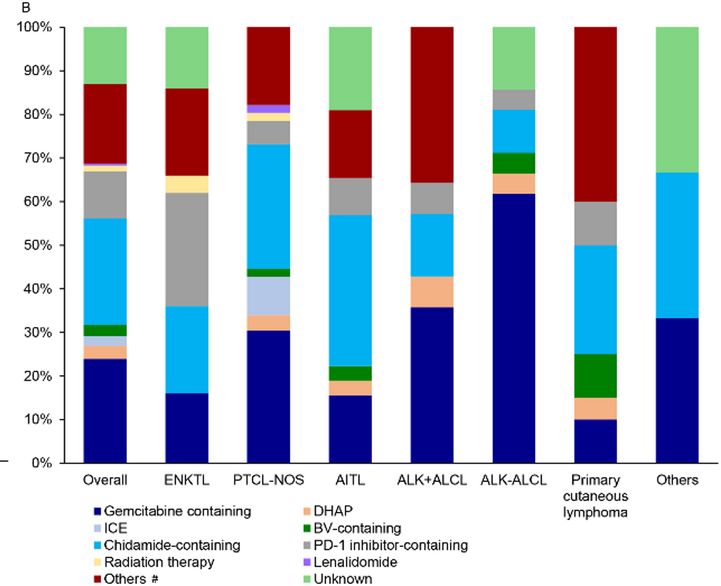
治疗结局 & 预后影响因素
OS:中位随访时间为 25.9 个月(范围:1.0-107.6 个月)。在 804 例患者中,259 例(32.2%)死亡,中位 OS 为 83.8 个月(95% CI:未达到 [NR]-NR),预估 5 年 OS 率为 56.6%(95% CI:54.10%-60.00%)。5 种最常见亚型间的 OS 存在显著差异(P<0.01)。对 PTCL 中 3 种更常见亚型(PTCL-NOS、AITL、ALK- ALCL)的生存分析显示,其中位 OS 为 29.9 个月(95% CI:19.73-40.07 个月),5 年 OS 率为 35.9%(95% CI:30.00%-42.00%)。
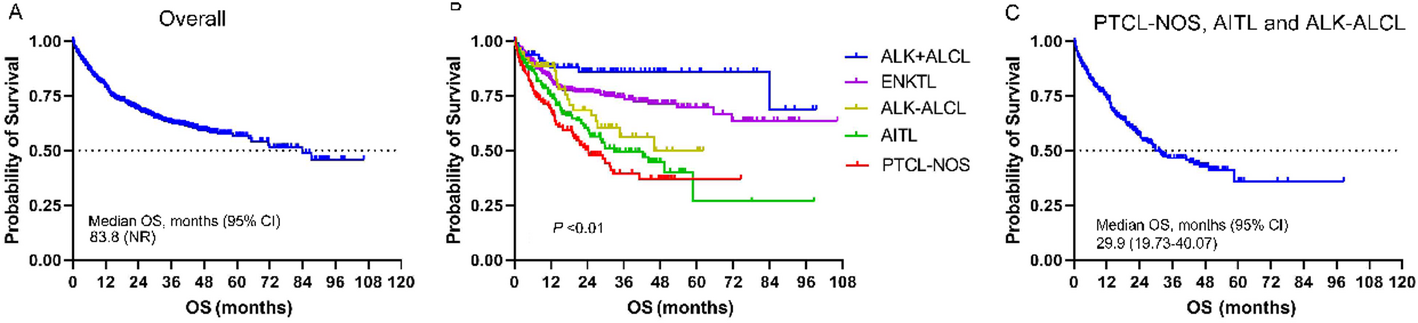
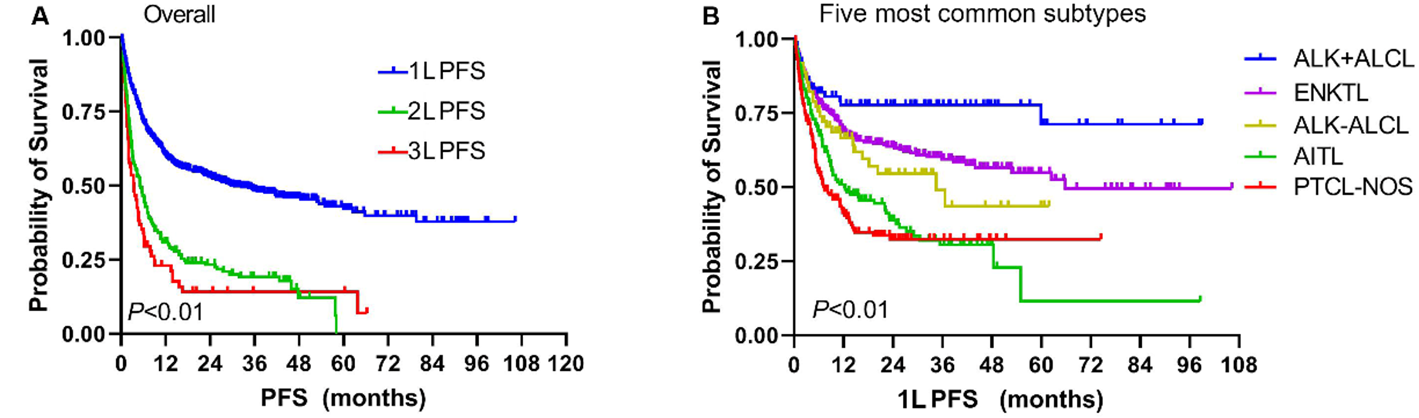
PFS:在所有患者中,376 例(46.8%)出现疾病进展或复发。PFS Kaplan-Meier 曲线显示,一线 PFS 与二线 / 三线 PFS 曲线早期即出现明显分离且持续存在差异,从一线治疗到三线治疗,中位 PFS 显著下降(30.5 个月 vs 5.2 个月 vs 3.5 个月,P<0.01)。在 5 种最常见亚型中,仅一线 PFS 存在显著差异(P<0.01);除ALK+ ALCL 患者外,其他亚型患者预后较差。
独立预后因素:多因素分析证实,年龄、乳酸脱氢酶(LDH)水平、β₂微球蛋白(β₂M)水平、ECOG 体力状态评分及组织学亚型均为总生存期(OS)和一线无进展生存期(PFS)的独立预后因素。
CD30 表达:贯穿 PTCL 诊疗及预后全程的关键标志物
CD30 表达在 PTCL 各亚型中存在差异:
在 436 例可评估 CD30 表达的患者中,53.9%(235 例)为 CD30 阳性(CD30 ≥10%)。不同亚型的 CD30 阳性率存在显著差异(P<0.001):ALK+ ALCL(98.0%)、ALK- ALCL(95.7%)、AITL(54.9%)、PTCL-NOS(41.8%)、ENKTL(37.8%)。
CD30 表达与临床病理特征显著相关:
CD30 表达水平在组织学亚型(P<0.01)、骨髓受累(P<0.01)、EBV‑DNA 阳性及结外受累(P=0.02)方面差异均具有统计学意义。在包含 ENKTL、PTCL‑NOS 和 AITL 的亚组人群(n=317)中,CD30 阴性患者的骨髓受累情况与 CD30 阳性患者存在显著差异(P=0.01);其中在 ENKTL 亚型中,CD30 阴性患者的骨髓受累率更高(84.0% vs 16.0%)。
CD30 表达潜在获益人群广泛,但靶向药物应用不足:
该研究显示, 53.9% 的 PTCL 患者为 CD30 阳性,这意味着超过一半的患者可能从 CD30 靶向治疗中获益,然而CD30 靶向药物的应用率较低(2.9%),其临床价值尚未得到充分挖掘。
CD30 表达与生存预后:
与 CD30 阳性患者相比,CD30 阴性患者呈现出总生存期(OS)更优、无进展生存期(PFS)更长的趋势(中位 OS:71.5 vs 25.0 个月,P=0.10;中位一线 PFS:13.7 vs 9.1 个月,P=0.14)。在 AITL 亚型患者中,CD30 阴性状态与更佳预后显著相关(中位 OS:32.8 [95% CI:NR‑NR] vs 15.0 [95% CI:6.14–23.86] 个月,P=0.02;中位一线 PFS:11.0 [95% CI:0.21–21.79] vs 5.2 [95% CI:1.47–8.93] 个月,P<0.01)。
CD30 作为 T 细胞淋巴瘤中的重要免疫标志物,其表达差异对PTCL患者的诊断分型、治疗选择及预后评估具有重要指导意义。《淋巴瘤 CD30 免疫组织化学检测及结果判读规范》中指出,对于肿瘤细胞普遍高水平表达 CD30 的淋巴瘤类型,可直接报告CD30 阳性(即默认 100% 的肿瘤细胞阳性),而其他类型淋巴瘤的染色结果则推荐半定量判读整张切片中的阳性细胞所占比例[4]。关于阳性细胞占比的计算和报告,共识推荐以 10% 为递升,低于 10% 者设 5% 和 < 5% 两档[4]。不过,共识并未对CD30 阳性界定值作出统一规定。不同研究或医院之间对 CD30 阳性的界定值标准不一,不仅导致不同研究间的疗效数据难以横向对比,更让临床治疗决策陷入标准不一的困境。在临床实践中已观察到部分CD30低表达(1~10%)PTCL患者仍可获益于靶向治疗[5]。此外,NCCN 最新指南表明,在CD30 低表达阳性的患者中仍可观察到CD30靶向治疗应答,任何水平的 CD30 阳性均可接受CD30靶向治疗为基础的方案治疗 [6],这为更多 PTCL 患者,尤其是 CD30 低表达患者,打开了靶向治疗的大门。目前,CD30阳性判定阈值不一,在一定程度上制约了临床实践的规范化,为PTCL患者的精准诊疗带来挑战。
小结
本项多中心真实世界研究揭示了中国PTCL患者的临床特征、治疗现状、生存结局及 CD30 表达价值。我国 PTCL 发病率高于西方国家[1],疾病高度异质性显著,以 ENKTL、AITL、PTCL‑NOS 为主要亚型[3]。治疗上,一线以蒽环类化疗为主,二线常用吉西他滨及西达本胺方案,新型药物应用有限,CD30 靶向药物使用率仅 2.9%。生存方面,整体预后欠佳,3 种常见亚型中位 OS 29.9 个月,且 PFS 随治疗线数显著下降,未满足临床治疗需求突出。CD30 在 中国PTCL 患者中阳性率达 53.9%,其表达与亚型、临床特征及预后相关,但临床价值未被充分挖掘。综上,本研究提示中国 PTCL 患者临床负担重、新型药物应用不足,CD30 有望为优化诊疗、填补未满足需求提供方向。
1. 中国临床肿瘤学会(CSCO)淋巴瘤专家委员会,中华医学会血液学分会淋巴细胞疾病学组. 淋巴结外周T细胞淋巴瘤诊断与治疗中国专家共识(2025年版)[J]. 中华血液学杂志,2025,46(12):1094-1104.
2. Ma H, Marchi E, O’Connor OA. The peripheral T-cell lymphomas: an unusual path to cure. Lancet Haematol. 2020;7:e765–71.
3. Huang L, Yang Y, Zhao Z, et al. Clinical characteristics, treatment patterns, and survival outcomes of 1031 patients with peripheral T cell lymphoma in china: a multicenter, real-world study. Discov Oncol. 2025 Jul 2;16(1):1252.
4. CD30阳性淋巴瘤病理专家组.淋巴瘤CD30免疫组织化学检测及结果判读规范[J].中国癌症杂志,2023,33(3):228-234.
5. Swaminathan Padmanabhan Iyer et al. Frontline brentuximab vedotin and CHP (A+CHP) in patients (pts) with peripheral T-cell lymphoma with less than 10% CD30 expression: Results from the phase 2 SGN35-032 study. J Clin Oncol 42, 7069-7069(2024).
6. NCCN Clinical Practice Guidelines in Oncology: T-Cell Lymphomas(Version 2.2025).
审批编号:VV-MEDMAT-135351
获批日期:2026年4月
排版编辑:肿瘤资讯-LWT
本资讯提供的信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。如该等信息被用于了解资讯以外的目的,本平台、作者及武田不承担相关责任。











 苏公网安备32059002004080号
苏公网安备32059002004080号


