福建省抗癌协会癌痛专业委员会和福建省抗癌协会中西医整合肿瘤专委会青年委员会主办的【十邑论坛】开播啦!论坛于每周二推出,带您用中文听原汁原味的国际学术会议研究。本期由三明市第二医院杨兰芳教授进行分享,内容源自日本爱知县癌症中心医院 Kei Muro教授在2026 ASCO-GI会议上的学术报告。深度解析了免疫治疗在胃食管癌(G/GEJC)领域的角色与价值,为临床精准决策带来指导和参考。
三明市第二医院 肿瘤科 主治医师
HER2阴性转移性胃食管癌免疫治疗的现状与证据
胃食管癌的治疗研发长期聚焦于肿瘤相关分子靶点及免疫检查点抑制剂。回顾过去十余年的发展历程,2010年ToGA研究确立了曲妥珠单抗联合化疗作为HER2阳性转移性胃癌的一线标准治疗。此后很长一段时间内,该领域未见能够突破这一方案的新靶向药物,直到2021年CheckMate 649研究问世,开启了免疫检查点抑制剂治疗的新纪元。随后,KEYNOTE-811研究进一步证实了曲妥珠单抗联合帕博利珠单抗及化疗在HER2阳性患者中的疗效。
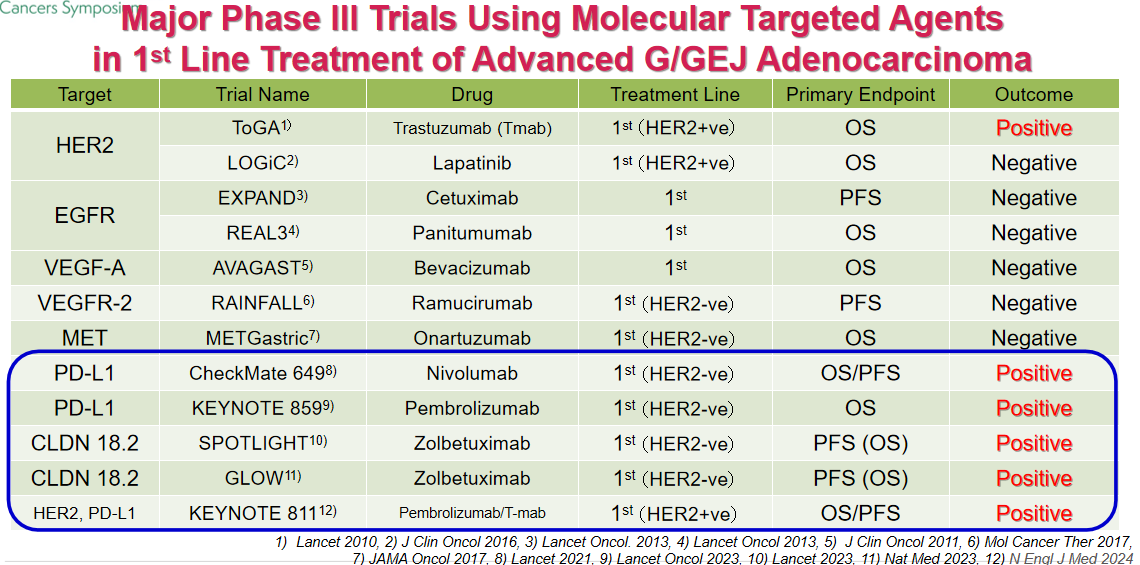
目前,胃癌治疗依赖于多种生物标志物的检测。核心难点在于,这些检测主要通过免疫组织化学(IHC)染色实现,这对标本的保存和前期质量控制提出了高要求,同时也考验病理医师的诊断专业能力。此外,临床中需警惕多生物标志物之间可能存在的共表达重叠现象。基于此,日本胃癌协会于2024年4月正式发布了《晚期胃食管癌生物标志物检测指南》,强烈建议在转移性胃食管癌一线治疗前,完成HER2、CLDN18.2、MSI/MMR及PD-L1四项关键检测。
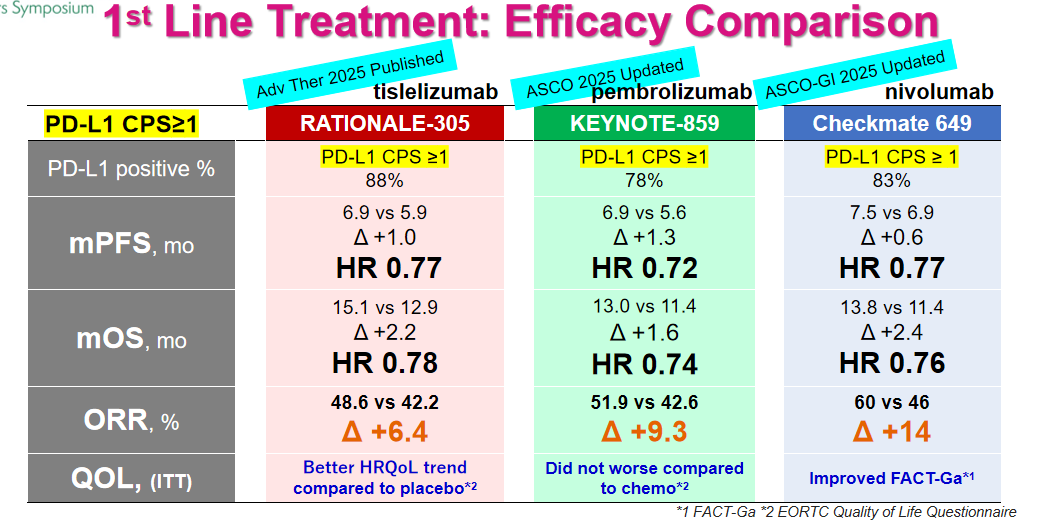
对比替雷利珠单抗、帕博利珠单抗及纳武利尤单抗用于晚期胃食管癌一线治疗的随机临床研究可以发现,这三种免疫检查点抑制剂在无进展生存期(PFS)和总生存期(OS)方面的疗效相当,客观缓解率(ORR)也表现出高度相似性。
通过对CheckMate 649、KEYNOTE-859、SPOTLIGHT、GLOW四项研究生存曲线的分析可见,纳武利尤单抗在提升4年生存率方面表现突出,帕博利珠单抗与佐妥昔单抗在长期生存结局上相似。根据CheckMate 649和KEYNOTE-859研究中按PD-L1 CPS分层的OS风险比(HR)数据,生存获益与CPS表达水平密切相关。当CPS<1时,免疫治疗的生存获益极低;而当CPS≥1,特别是CPS≥10时,生存改善显著。
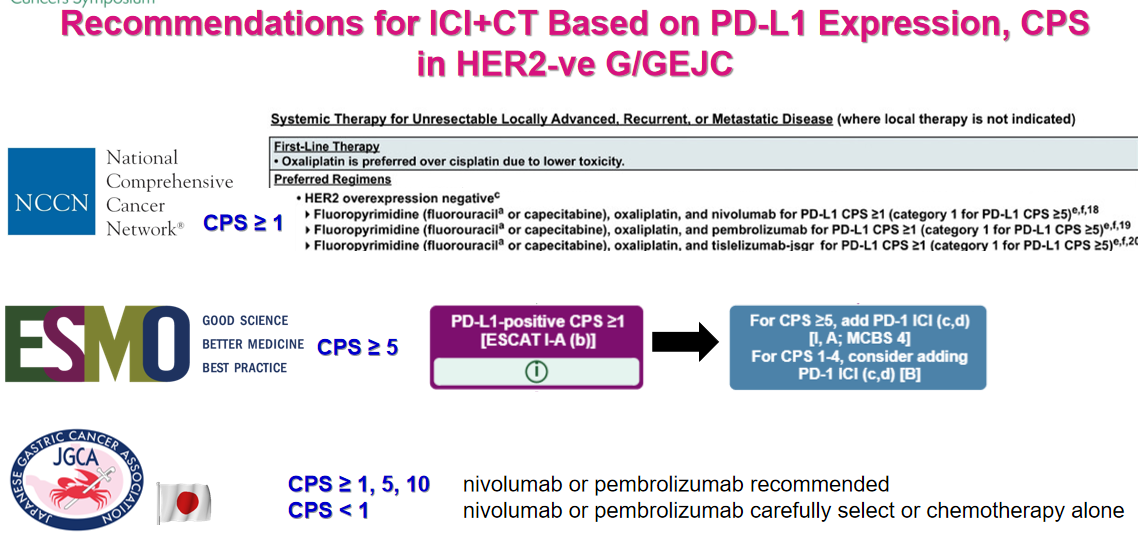
目前全球主流指南对免疫检查点抑制剂联合化疗的推荐存在细微差异:NCCN指南对于CPS≥1的患者给予优选推荐;ESMO指南推荐用于CPS≥1的患者,并强调CPS≥5时获益更优;日本指南基本推荐纳武利尤单抗或帕博利珠单抗用于 CPS≥1的群体;对于CPS<1的患者,选择免疫治疗需审慎。
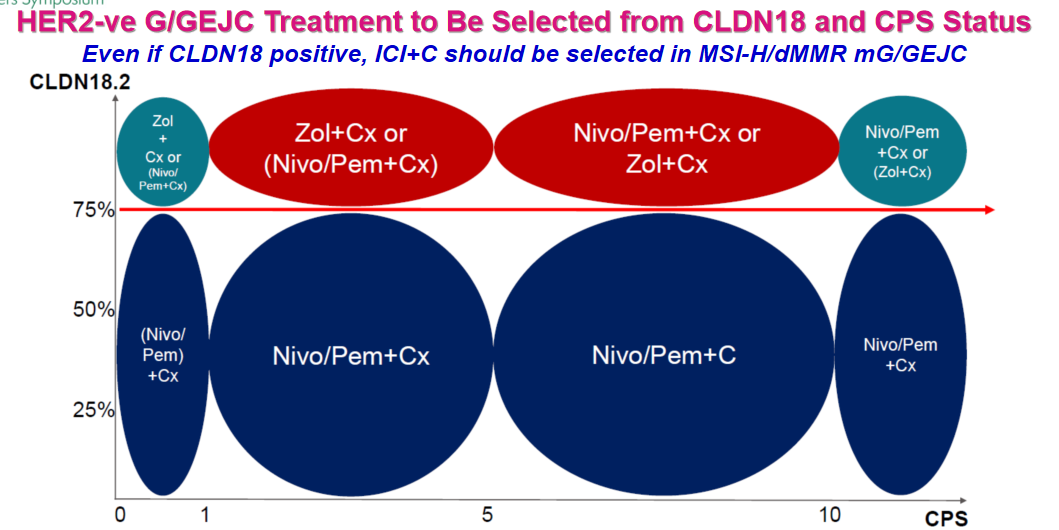
个人观点认为,在HER2阴性且CLDN18.2阳性的患者中,若CPS<1,则优先考虑佐妥昔单抗;若CPS≥10,则考虑采用免疫检查点抑制剂。对于CPS介于1~10之间的患者,一般考虑佐妥昔单抗,但最终需进行个体化权衡。此外,若患者确诊为MSI-H型,无论CLDN18.2表达如何,均应选择免疫检查点抑制剂联合化疗。
总结而言,虽然KEYNOTE-811奠定了HER2阳性胃癌的标准方案,但对于HER2阴性患者,治疗决策需基于MSI/MMR、CPS及CLDN18.2的检测结果,并综合考量病理特征、疾病负荷、肿瘤部位、后续序贯治疗空间以及患者对毒性的耐受性等进行决策,强烈建议通过MDT制定最优的个体化治疗策略。
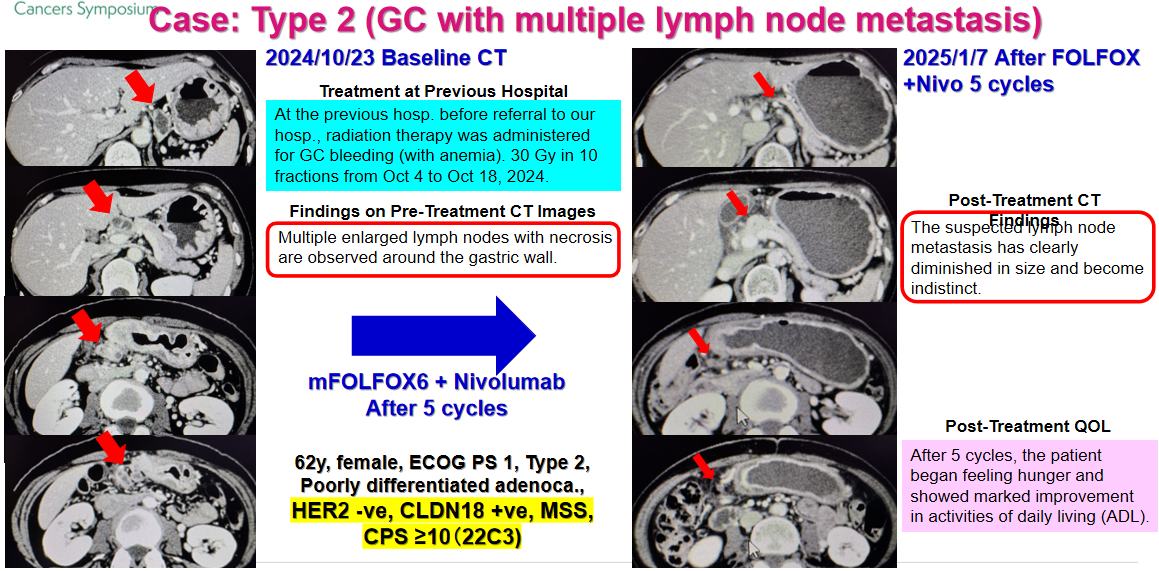
接下来分享的一例CLDN18.2和PD-L1均为阳性的胃癌病例,以期为临床实践带来参考。患者女性,62岁,确诊为II型胃癌伴多发淋巴结转移。ECOG 1分,病理提示为低分化腺癌。关键检测显示:HER2阴性、CLDN18.2阳性、MSS型、PD-L1 CPS≥10。
因胃原发灶出血伴贫血,患者先行30Gy局部放疗。CT显示胃周存在多发且伴坏死的肿大淋巴结。针对该病例,虽然CLDN18.2呈阳性,但考虑到CPS≥10的强效免疫获益指征,最终选择了mFOLFOX6联合纳武利尤单抗方案。经过5个周期治疗,影像学显示转移灶显著缩小,患者食欲恢复,日常生活能力明显改善。值得一提的是,前期放疗可能通过免疫调节产生协同效应(参考食管鳞癌的 SKYSCRAPER-07研究),这进一步支持了在化疗基础上联合纳武利尤单抗的决策。
HER2阳性、MSI-H/dMMR转移性胃食管癌及可切除胃食管癌围手术期免疫治疗新进展
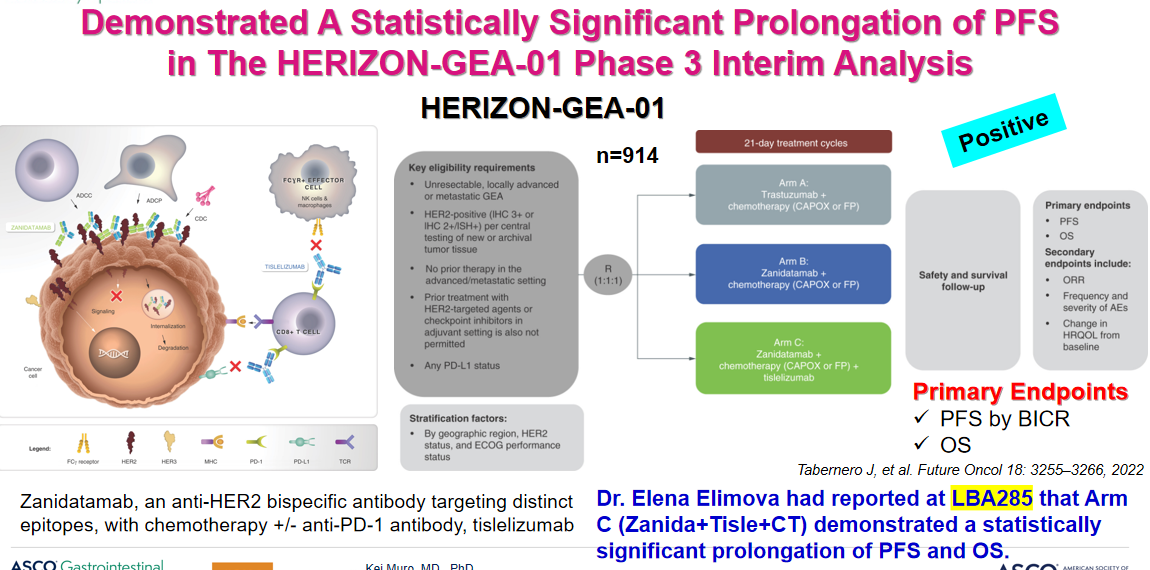
在HER2阳性领域,KEYNOTE-811研究已确立了化疗联合曲妥珠单抗及帕博利珠单抗方案的标准治疗地位,该研究在历次分析中均取得了进展,从首次中期分析的ORR显著提升,到第二次中期分析的PFS差异,至最终分析确认了OS的阳性结果。而HERIZON-GEA-01研究的成功也为临床带来了新选择。该研究证实,泽尼达妥单抗联合化疗及替雷利珠单抗在PFS和OS上均有统计学意义的获益,有望成为新的标准方案。
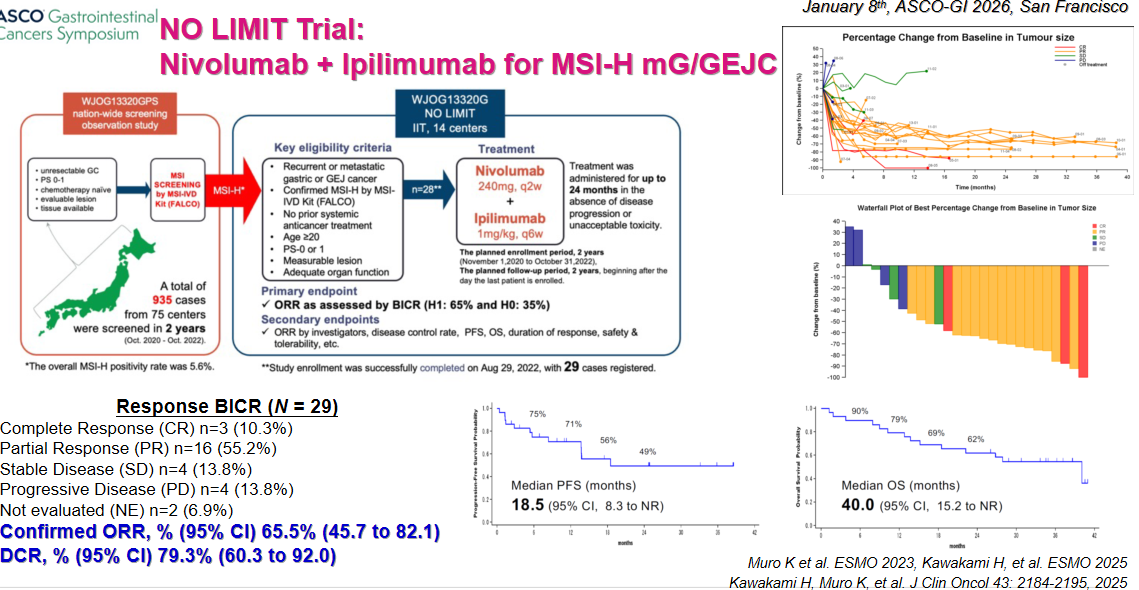
针对MSI-H患者,NO LIMIT研究中纳武利尤单抗联合伊匹木单抗方案展现了令人振奋的数据:客观缓解率(ORR)达66%,疾病控制率(DCR)约80%,更有10%的患者达到完全缓解(CR)。从瀑布图中可以看到,这类患者能获得长期、持久且深度的缓解,PFS与OS显著延长。
围手术期证据(如MAGIC研究和CLASSIC研究)均显示,MSI-H型患者单纯手术的效果往往优于手术联合化疗,这提示该亚型对化疗反应不佳。与之类似,TMB-H患者同样能从免疫治疗中获得更优获益。
在局部晚期胃癌领域,随机对照试验中,KEYNOTE-585的OS和无事件生存期(EFS)为阴性结果,但MATTERHORN研究则在病理完全缓解(pCR)率和OS方面均获得阳性结果。对于可切除的MSI-H患者,法国的NEONIPIGA、意大利INFINITY及德国DANTE试验结果高度一致:pCR率均在60%左右,TRG 1a+1b率约65%。这表明新辅助免疫治疗可诱导MSI-H型胃癌产生较高且持续的病理缓解。

鉴于多塔利单抗等药物在dMMR肿瘤中观察到的极高缓解率,我们正积极探讨MSI-H型胃癌实现“非手术管理”的可能性。尽管目前胃癌达到完全缓解并转入非手术观察的难度稍大,但相关探索已成为行业前沿的热点。
胃食管癌免疫治疗的未来展望与挑战
尽管免疫治疗已取得诸多进展,但近期多项临床研究的阴性结果提示,联合方案仍面临重重挑战。例如,LEAP-015 研究探讨了仑伐替尼联合帕博利珠单抗及化疗的方案,虽然达到了PFS的阳性终点,但在OS这一主要终点上为阴性结果。此外,在2026 ASCO GI上公布的ATTRACTION-06 研究显示,伊匹木单抗联合纳武利尤单抗及SOX方案对比单纯SOX方案的试验结果也为阴性。同时,抗TIGIT抗体联合抗PD-1抗体及化疗对比纳武利尤单抗联合化疗的STAR-221研究,同样未能观察到预期的生存获益。
在新兴靶点的探索中,EP4拮抗剂展现了极具潜力的应用前景。研究表明,EP4信号通路的激活会在肿瘤微环境中诱导免疫抑制状态,进而导致免疫治疗耐药。作为一种EP4拮抗剂,ONO-4578有望通过抑制PGE2-EP4信号通路来逆转肿瘤免疫抑制,从而增强PD-1抗体的疗效。此外,化疗联合佐妥昔单抗与纳武利尤单抗的探索性数据也令人振奋,而针对CLDN18.2与PD-L1 CPS双阳性胃癌的 LUCERNA研究正在进行中。双特异性T细胞衔接器如ASP2138联合帕博利珠单抗及化疗的方案也在探索阶段,尽管样本量较少,但已显示出深度缓解趋势,非常具有前景。

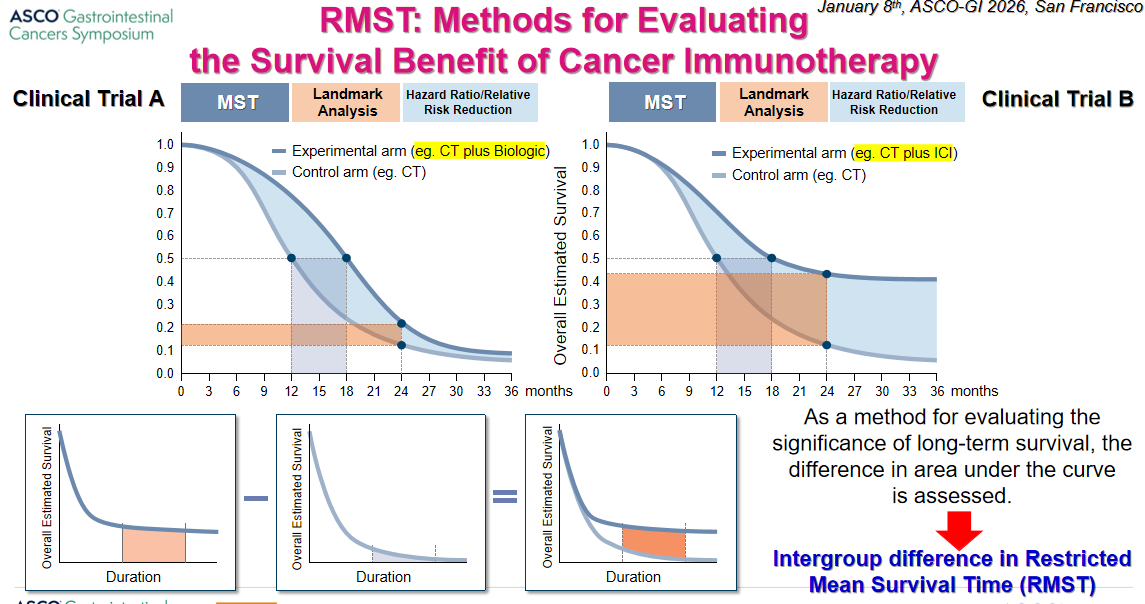
从长远来看,免疫治疗的核心挑战在于如何体现长期生存获益。正如KM生存曲线所展示的,免疫联合组与单纯化疗组的曲线差异往往随随访时间延长而持续扩大,呈现出特征性的“长期拖尾效应”。由于这种非比例风险的曲线特征无法通过传统的Log-rank检验进行准确评估,临床上亟需引入新的评价方法。例如,限制性平均生存时间(RMST)通过比较生存曲线下的面积,能更科学地衡量免疫治疗的临床价值。构建这些新型评估体系,将是评价未来免疫治疗价值的重要方向。
排版编辑:肿瘤资讯-YXD











 苏公网安备32059002004080号
苏公网安备32059002004080号


