复发/难治性(R/R)淋巴瘤,尤其是合并中枢神经系统受累或化疗耐药的患者,临床治疗难度较大,传统单一治疗手段往往难以实现长期生存。造血干细胞移植(HSCT)作为淋巴瘤巩固治疗的经典手段,与CAR-T细胞治疗、脐带血干细胞输注等新型疗法的联合应用,已成为优化淋巴瘤治疗结局、突破治疗瓶颈的重要研究方向。
2026年第52届欧洲血液与骨髓移植学会(EBMT)年会公布了多项HSCT联合治疗淋巴瘤的创新研究,为临床探索更高效的联合治疗模式提供了关键循证依据。【肿瘤资讯】特此整理其中三项重点研究,系统梳理自体造血干细胞移植(ASCT)联合CAR-T细胞治疗、ASCT联合脐带血干细胞输注等模式的疗效与安全性,以飨读者。
ASCT联合CAR-T细胞治疗:桥接治疗有效后R/R CNSL的优选方案,显著延长PFS
R/R中枢神经系统淋巴瘤(CNSL)患者的临床管理极具挑战性。CAR-T细胞疗法虽展现出一定疗效,但患者的无病生存期及长期结局仍不理想,ASCT与CAR-T细胞治疗的联合治疗模式能否进一步提升疗效尚未明确。
一项单中心回顾性研究(摘要号OS02-03)纳入2019年9月至2025年9月接受CAR-T细胞治疗的153例R/R CNSL患者,其中男性占51%,中位年龄56岁(范围19~79岁)。原发中枢神经系统淋巴瘤(PCNSL)占53%,继发性中枢神经系统淋巴瘤(SCNSL)占47%,SCNSL最常见的组织学类型为弥漫大B细胞淋巴瘤(DLBCL,n=55)。83例患者既往接受≥3线治疗。
根据IELSG(PCNSL)或IPI(SCNSL)评分,低危、中危、高危患者分别占27%、59%、14%。85%的患者对大剂量甲氨蝶呤(HD-MTX)耐药,58%的患者在CAR-T细胞治疗前6个月内接受过MTX治疗,64%存在BTK抑制剂耐药,18%既往ASCT治疗失败。74%的患者为脑实质受累,8%为脑脊液受累,18%为两者均受累。
患者接受中位2周期(0~5周期)桥接治疗,客观缓解率(ORR)达71%(完全缓解[CR] 84例,部分缓解[PR] 24例)。根据桥接治疗疗效,将患者分为桥接有效组(BE,CR/PR)和桥接无效组(BI,SD/PD)。其中BE组108例患者中,49%(53/108)接受ASCT联合CAR-T细胞治疗,55例接受单纯CAR-T细胞治疗。
研究结果显示,所有患者3个月ORR为79%,CR率为69%。桥接治疗疗效对CAR-T细胞治疗结局影响显著。BE组3个月ORR(91% vs 56%)和CR率(87% vs 33%)均显著高于BI组。中位随访26个月,BE组中位无进展生存期(PFS)为49个月,显著长于BI组的6个月(P<0.0001);BE组中位总生存期(OS)未达到,BI组为13个月(P<0.0001)。生存数据显示,BE组1年OS率(93% vs 57%,P<0.01)、1年PFS率(75% vs 27%,P<0.01)、2年OS率(78.5% vs 29%,P<0.01)、2年PFS率(67% vs 14%,P<0.01)均显著优于BI组。
安全性方面,任意级别细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)发生率分别为69%(105/153)和14%(21/153),其中≥3级CRS和ICANS发生率分别为6%和24%,治疗毒性整体可控。
针对BE组的亚组分析显示,ASCT联合CAR-T细胞治疗的患者中位PFS为57.11个月,显著长于单纯CAR-T细胞治疗的27.35个月(P=0.001);两组中位OS均未达到(P=0.053);且两组间CRS和ICANS发生率无统计学差异,联合治疗未增加毒性风险。
该研究结论指出,有效的桥接治疗可显著提升CAR-T细胞治疗R/R CNSL的疗效。在桥接治疗有效的基础上,采用ASCT联合CAR-T细胞的治疗模式,能进一步显著延长患者PFS,且不增加治疗相关毒性,为R/R CNSL的临床治疗提供了优化的联合治疗方案。
ASCT联合脐带血干细胞输注:R/R DLBCL治疗的新型移植模式,生存获益显著且移植重建良好
ASCT缺乏异基因造血干细胞移植(allo-HSCT)的移植物抗肿瘤(GVT)效应,对于微小残留病(MRD)阳性或化疗耐药的R/R DLBCL患者,复发率高达50%~60%。人脐带血干细胞(hUCBSCs)具有免疫原性低、免疫重建能力强、生物安全性好的特点,有望成为实现ASCT与allo-HSCT双重疗效的潜在选择。
一项单臂前瞻性临床试验(摘要号A187),纳入国内三甲医院确诊的R/R DLBCL患者,患者在ASCT后第2天接受无关供者hUCBSCs输注。研究主要终点为2年OS率、无复发生存率(RFS)和PFS率;次要终点为中性粒细胞和血小板植入时间。
2023年9月27日至2023年11月27日,研究共纳入44例患者,中位年龄37岁(18~65岁),其中男性20例,女性24例;复发患者23例(55.6%),难治患者21例(44.4%)。移植后90天,患者外周血中无关供者hUCBSCs来源细胞比例持续低于0.01%。中位中性粒细胞植入时间为11天(10~21天),中位血小板植入时间为14天(12~31天),造血重建效果良好。
生存结局显示,患者2年OS率达90.9%,2年PFS率达86.3%,中位生存时间未达到,展现出显著的长期生存获益。
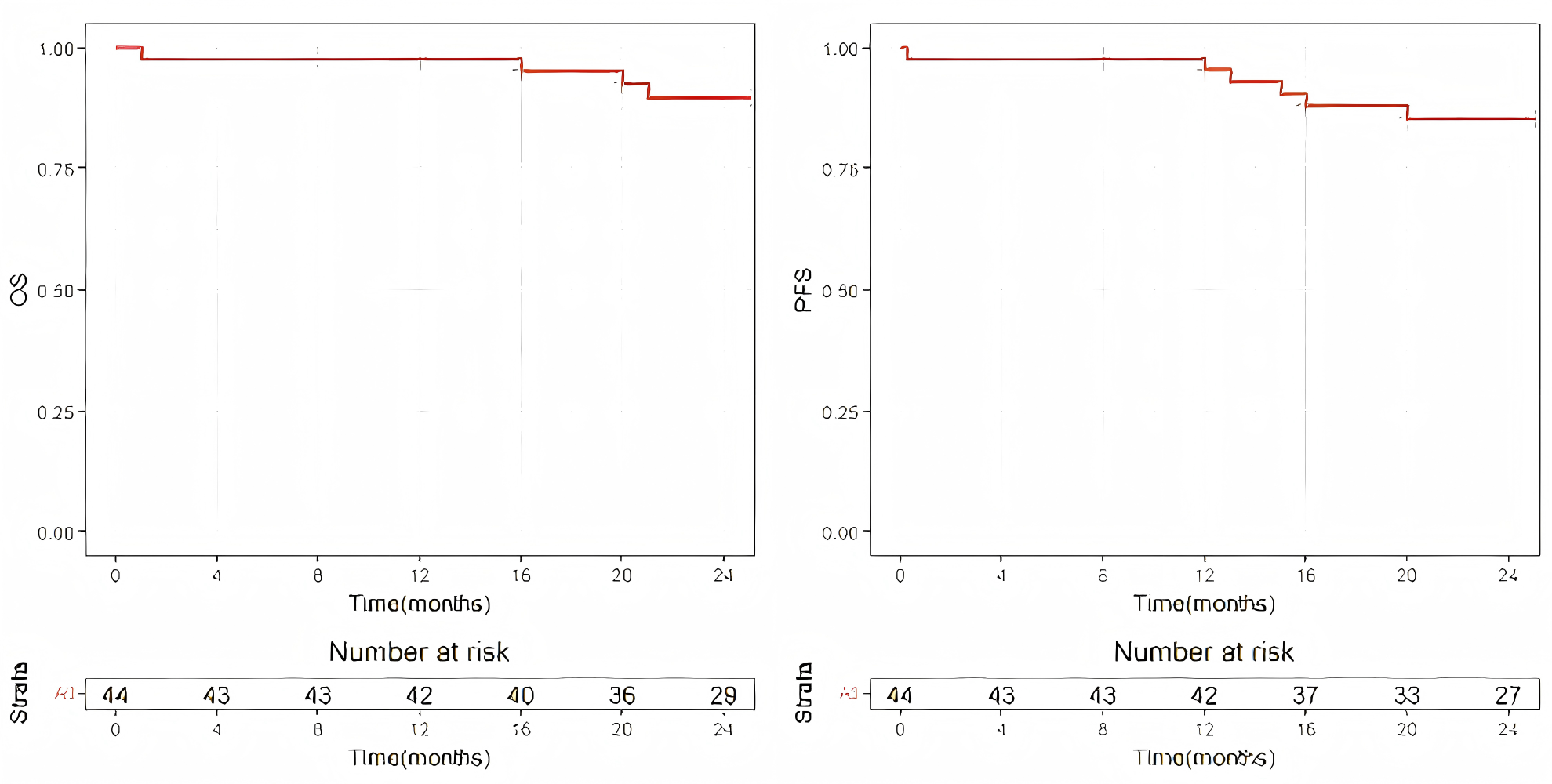
该研究结论表明,ASCT联合无关供者hUCBSCs输注的新型移植模式,能显著改善R/R DLBCL患者的生存结局,且造血重建顺利,安全性良好。该方案的可行性仍需扩大样本量、延长随访时间进一步验证,为R/R DLBCL的移植治疗提供了新的创新思路。
ASCT联合CAR-T细胞治疗:R/R侵袭性B细胞淋巴瘤的潜在优化方案,生存结局呈改善趋势
抗CD19 CAR-T细胞疗法已获批用于至少二线治疗失败的R/R大B细胞淋巴瘤。ASCT与CAR-T细胞的联合治疗对多亚型R/R大B细胞淋巴瘤有效,但该联合模式与单纯CAR-T细胞治疗的疗效对比仍需更多循证证据。
一项倾向评分匹配(PSM)队列研究(摘要号A049)纳入64例R/R非霍奇金淋巴瘤患者,根据10项基线特征将患者分为ASCT联合CAR-T细胞组(32例)和单纯CAR-T细胞组(32例),排除既往接受过CAR-T细胞或ASCT治疗的患者。两组基线特征经匹配后均衡可比,适用于结局对比分析。两组患者均接受CD19 CAR-T细胞治疗。
研究结果显示,联合治疗组和单纯CAR-T细胞组3个月治疗有效率分别为68.8%和55.2%(P=0.302),其中CR率分别为62.5%和41.4%(P=0.127)。中位随访38.4个月,总体人群3年PFS率为51.58%,3年OS率为63.73%。联合治疗组患者生存结局呈改善趋势,3年PFS率为60.66% vs 44.20%(P=0.082),3年OS率为74.22% vs 52.22%(P=0.082)。
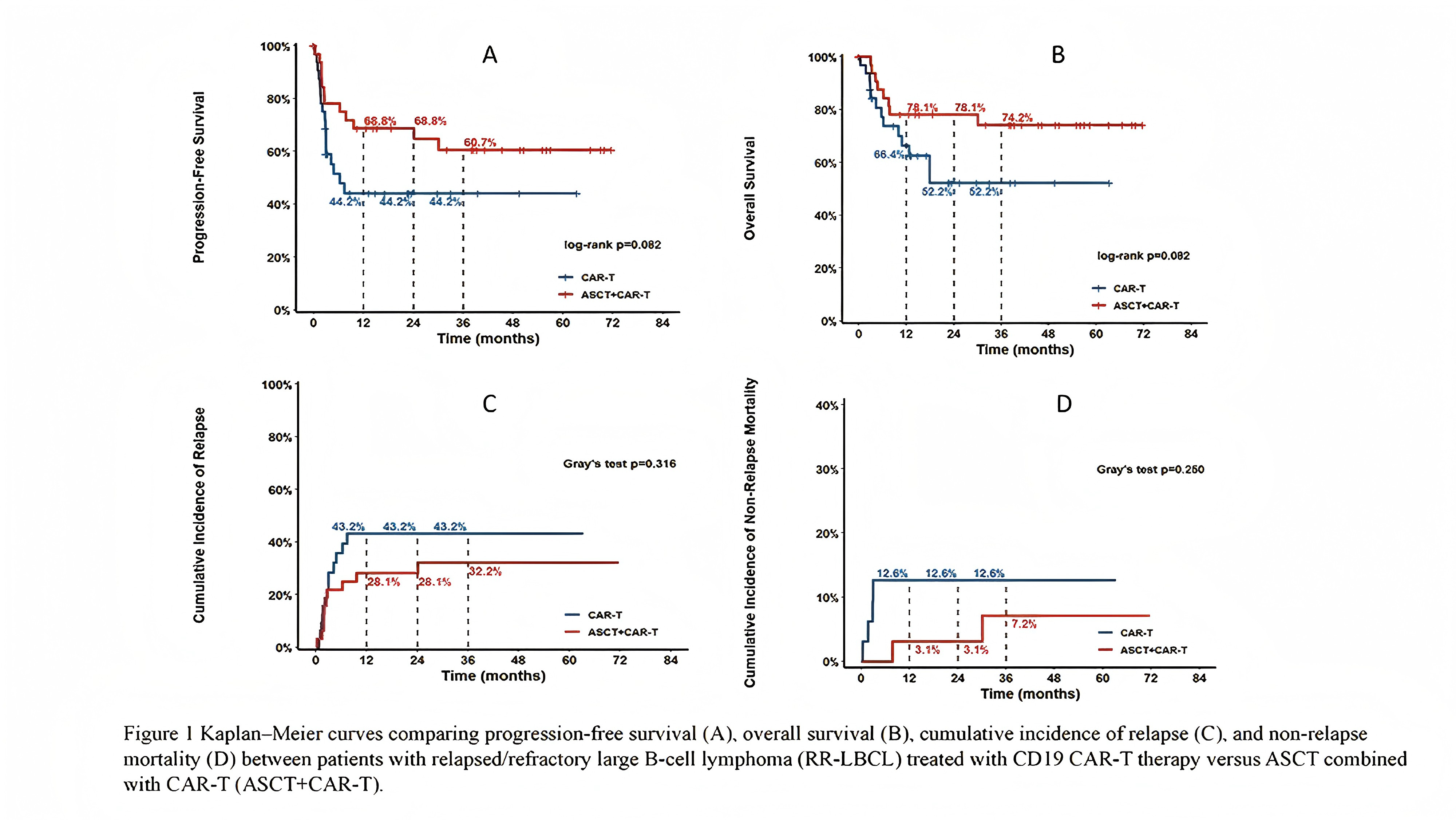
复发及非复发死亡(NRM)分析显示,联合治疗组3年复发/疾病进展发生率为32.17%,低于单纯CAR-T细胞组的43.15%(P=0.316);联合治疗组3年NRM率为7.17%,低于单纯CAR-T细胞组的12.65%(P=0.250)。
毒性方面,联合治疗组和单纯CAR-T细胞组≥3级CRS发生率分别为12%和6.8%,≥3级ICANS发生率分别为0和1.4%,两组严重毒性发生率无显著差异,联合治疗未增加神经毒性风险。
该研究结论指出,与单纯CAR-T细胞治疗相比,ASCT联合CAR-T细胞治疗在R/R侵袭性B细胞淋巴瘤患者中展现出生存结局改善的趋势,且未显著增加治疗相关毒性,但该结论仍需更大样本量的研究进一步验证。
综合来看,三项研究均基于中国临床数据,聚焦淋巴瘤治疗的临床痛点,所探索的联合治疗模式均具有临床可操作性,且未显著增加治疗相关毒性,符合临床“高效低毒”的治疗需求。其中,ASCT与CAR-T细胞治疗的联合成为核心研究方向,两项研究均证实该模式的有效性,且明确了桥接治疗疗效是影响联合治疗结局的关键因素,为临床筛选联合治疗获益人群提供了重要依据。此外,ASCT联合脐带血干细胞输注的模式,则为不适合接受CAR-T细胞治疗或CAR-T细胞治疗失败的R/R DLBCL患者提供了新的思路。
当前,HSCT与新型疗法的联合治疗仍处于探索阶段,现有研究尚存在样本量有限、部分研究为回顾性设计等局限性。未来,亟需开展大样本量、多中心、前瞻性随机对照研究,进一步验证各联合治疗模式的长期疗效与安全性,同时探索疗效预测标志物,明确不同联合模式的最佳适用人群、治疗序贯及剂量方案,推动HSCT联合治疗淋巴瘤的模式向更精准、更高效的方向发展,最终让更多R/R淋巴瘤患者从联合治疗中获益。
https://ebmt2026.abstractserver.com/programme/#/programme/1/list
排版编辑:Grady











 苏公网安备32059002004080号
苏公网安备32059002004080号


