近年来,针对人表皮生长因子受体(HER2)双靶向治疗的全面普及显著提升了HER2阳性早期乳腺癌的治愈率,随之而来的另一个问题是:如何在保证疗效的前提下通过“降阶梯”策略降低化疗毒性?尽管我国临床指南已基于部分证据,将不含卡铂的THP方案(紫杉类+曲妥珠单抗+帕妥珠单抗)纳入治疗HER2阳性患者的推荐范畴,但该方案长期缺乏与全球标准方案TCbHP(紫杉类+卡铂+双靶)直接“头对头”对比的确证性证据。由广东省人民医院王坤教授团队牵头开展的neoCARHP研究,作为首个头对头对比THP与TCbHP的大型多中心Ⅲ期随机非劣效试验,成功填补了这一关键的循证医学空白,为HER2阳性乳腺癌患者提供了更安全的新辅助治疗选择。

研究背景
在肿瘤临床诊疗中,一个不可忽视的逻辑是:指南虽有初步推荐,但并不代表该方案的循证医学证据已完善,也不意味着其临床应用不存在争议。neoCARHP研究的启动,正是为解决现阶段临床实践中亟待明确的三大关键问题:
指南推荐仍需高级别循证证据确证
长期以来,TCbHP方案(含卡铂)依托TRYPHAENA等研究奠定的证据基础,始终是国际权威指南中HER2阳性早期乳腺癌新辅助治疗的首选标准方案。此前国内指南对THP方案的推荐,其证据主要来源于研究数据的间接交叉对比或特定人群的小样本研究。例如,NeoSphere研究的核心目的是评估帕妥珠单抗的附加治疗价值,并未将THP与TCbHP进行直接对比;而WSG ADAPT等研究不仅为1-2周短疗程的Ⅱ期试验设计,且入组人群高度筛选,难以充分证实两种方案在全人群中的等效性。在循证医学体系中,间接数据的交叉对比无法完全替代预设非劣效界值、“头对头”直接对比的Ⅲ期确证性试验。填补中国人群专属的临床数据空白
既往HER2阳性乳腺癌新辅助治疗的核心循证数据多源自欧美人群,但中国患者的发病年龄、肿瘤生物学特征及化疗耐受性均与欧美人群存在差异。尤为值得关注的是,中国患者卡铂相关骨髓抑制、感染发生率在真实世界中较高,真实世界临床实践中,因无法耐受卡铂毒性导致治疗中断、剂量下调或严重感染的比例较高。因此,开展基于中国本土患者的大样本临床试验,对优化国内HER2阳性乳腺癌诊疗规范具有重要的现实意义。缓解高危患者“去卡铂”疗效折损的临床顾虑
即便指南已推荐THP方案,临床医师在面对淋巴结阳性、激素受体(HR)阴性等高危患者时,仍存在省略卡铂是否会导致疗效下降的疑虑。这一争议的根源在于,既往不同研究对卡铂的治疗价值结论不一(如TRYPHAENA研究显示含卡铂方案的pCR率更高,而GeparSixto等研究未观察到卡铂带来的额外获益)。为此,neoCARHP研究在严格的临床试验框架下,旨在通过大样本数据明确卡铂在HER2阳性乳腺癌新辅助治疗中是否存在不可替代的临床价值,从而完善“降阶梯”治疗的证据链闭环。
研究方法
neoCARHP研究是一项在我国15家医疗中心开展的多中心、开放标签、随机、Ⅲ期非劣效性临床试验。研究纳入18周岁及以上、既往未接受过任何系统性抗肿瘤治疗、经组织学确诊为Ⅱ期或Ⅲ期HER2阳性浸润性乳腺癌的女性患者。符合入组标准的患者按1:1比例集中随机分配至THP组或TCbHP组,并根据激素受体(HR)状态和淋巴结状态进行分层。THP组患者接受研究者选择的紫杉类药物(多西他赛、紫杉醇或白蛋白结合型紫杉醇)联合曲妥珠单抗、帕妥珠单抗(不含卡铂),每3周给药1次,共6个周期;TCbHP组患者接受同类型紫杉类药物(其中多西他赛剂量在两组保持一致,卡铂按标准AUC给药)联合卡铂及曲妥珠单抗、帕妥珠单抗,给药频率同THP组。新辅助治疗完成后6周内择期行手术治疗。
该研究的主要研究终点为改良意向治疗(mITT)人群(即所有随机分配且至少接受1剂研究治疗的患者)的乳腺及腋窝病理完全缓解(pCR)率;次要研究终点包括客观缓解率、保乳手术率、无事件生存期(EFS)、无浸润性疾病生存期(iDFS)、总生存期(OS)及安全性。研究预设-10%的非劣效界值——若两组pCR率差异的95%置信区间(CI)下限大于-10%,即可证实THP方案非劣效于TCbHP方案。
研究结果
2021年4月30日至2024年8月27日期间,研究共筛查809例患者,其中766例患者至少接受1次研究治疗并纳入mITT人群分析(THP组382例,TCbHP组384例)。两组患者基线特征均衡,中位年龄约51-52岁,约64%的患者为淋巴结阳性,超四分之一为Ⅲ期患者。
1. 疗效非劣效,“去卡铂”不影响整体及关键亚组的pCR率
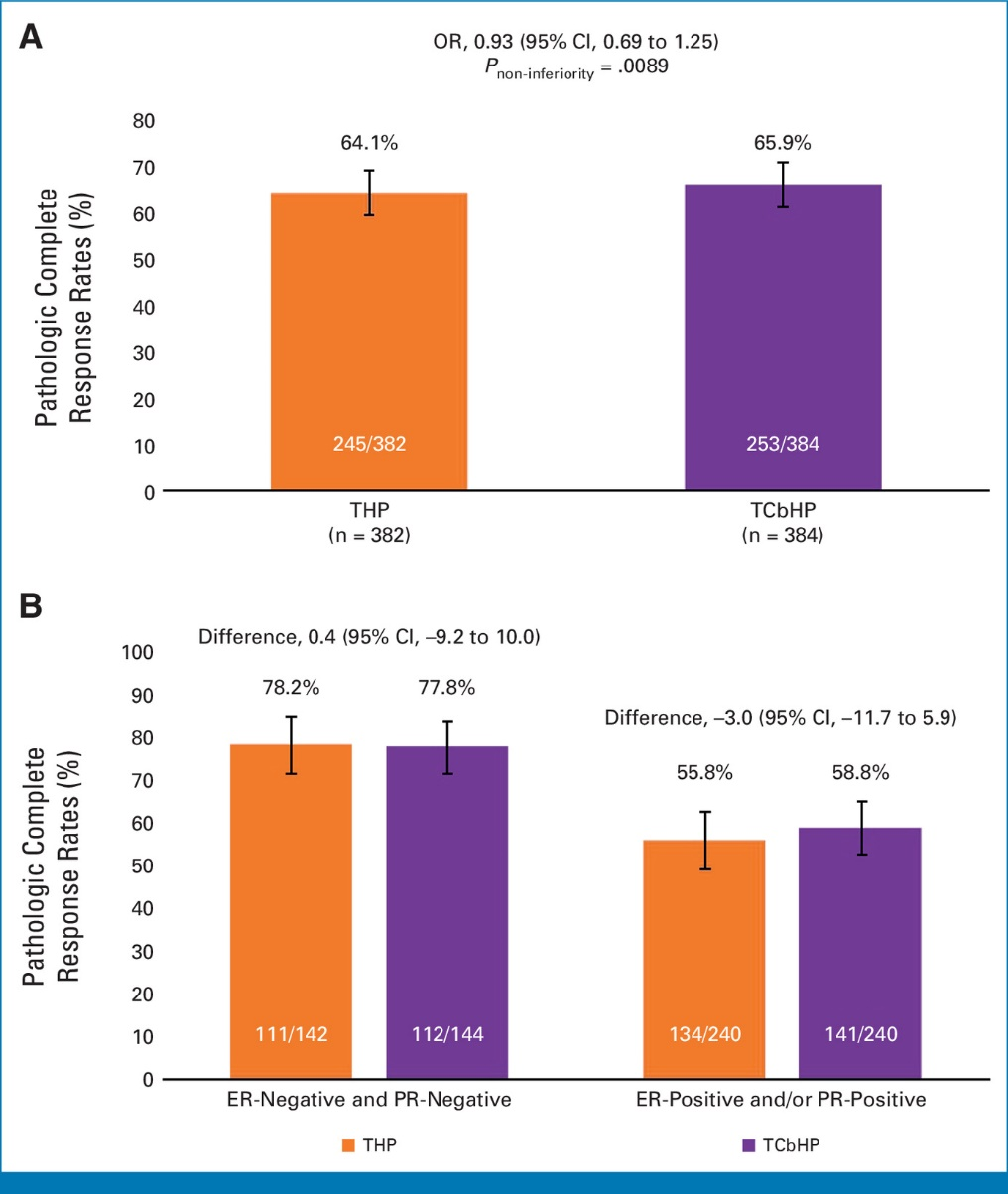
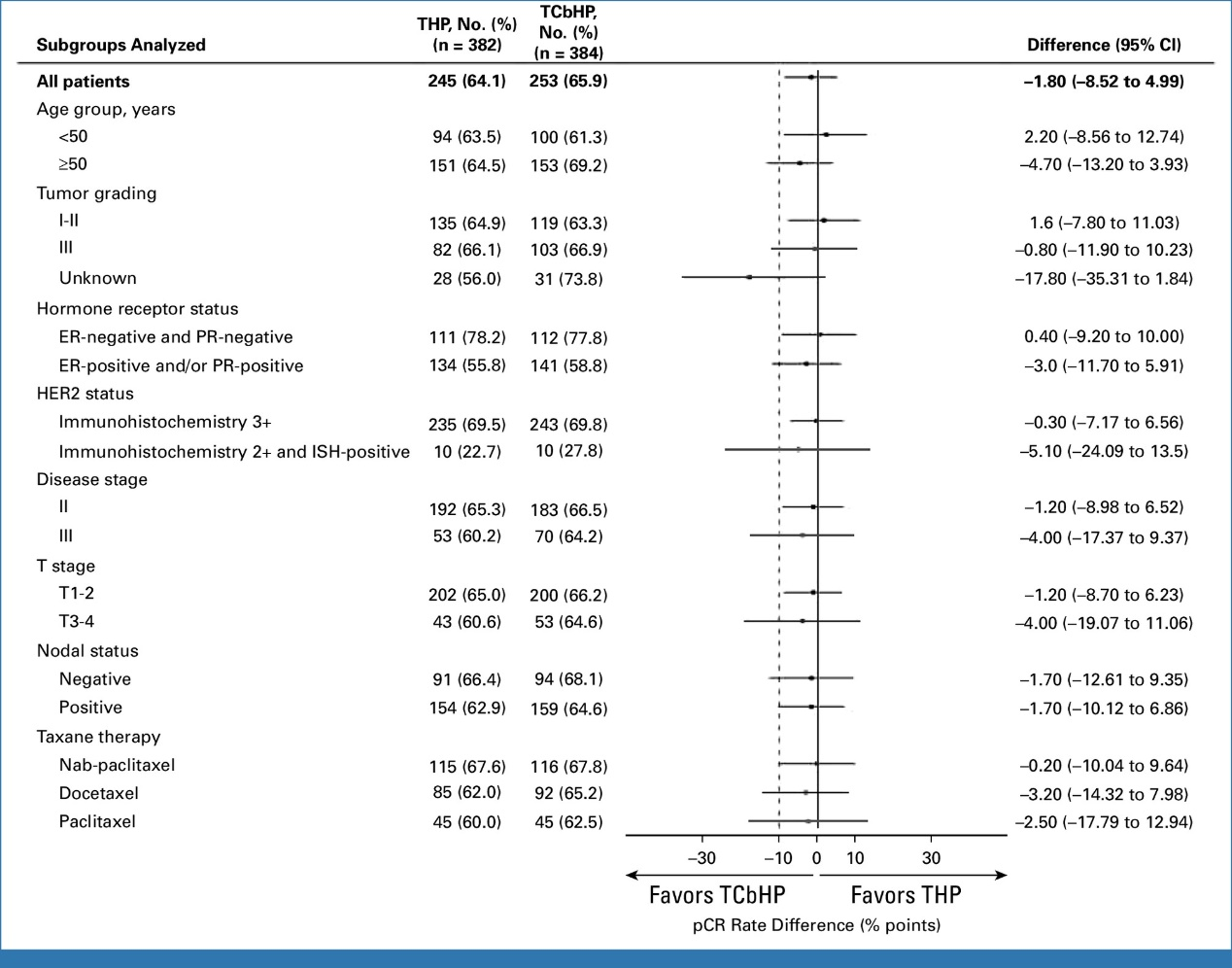
总体pCR率达到非劣效标准:mITT人群中,THP组总体pCR率为64.1%(95%CI 59.1~69.0),TCbHP组为65.9%(95%CI 60.9~70.6);两组绝对差异仅为-1.8%(95%CI -8.5~5.0),非劣效性检验P=0.0089,研究证实THP方案整体非劣效于TCbHP方案。
HR阴性高危人群疗效高度一致:HR阴性高危亚组中,THP组pCR率达78.2%,与TCbHP组的77.8%持平。
HR阳性及其他亚组获益稳定:HR阳性人群中,THP组与TCbHP组pCR率分别为55.8%和58.8%;此外,无论患者淋巴结转移状态如何,或研究者选择何种紫杉类药物,THP方案均展现出一致的非劣效获益。
2. 安全性显著提升,核心毒副反应大幅降低
THP组3级及以上不良事件发生率仅为20.7%,显著低于TCbHP组的34.6%;严重不良事件(SAE)发生率从TCbHP组的4.7%降至THP组的1.3%。骨髓抑制相关毒性方面,THP组3-4级中性粒细胞减少发生率为6.8%(TCbHP组16.4%),3-4级白细胞减少发生率为5.5%(TCbHP组14.8%);非血液学毒性方面,THP组3-4级腹泻发生率降至2.6%(TCbHP组4.2%)。
3. 治疗依从性改善,剂量调整需求明显减少
THP组仅8.1%的患者需下调紫杉类药物剂量,而含卡铂的TCbHP组高达25.3%的患者需进行剂量调整。
讨论
neoCARHP研究结果不仅从统计学层面证实THP与TCbHP方案疗效相当,更从循证医学角度进一步巩固了HER2阳性早期乳腺癌新辅助治疗的降阶梯策略,为指南推荐THP方案提供了高级别证据支撑,使其成为临床实践中更可靠的首选方案之一。在评估neoCARHP研究的临床价值时,可与另一项我国重磅研究HELEN-006共同分析。
1. 严格单变量控制,直击“卡铂是否必需”的核心问题
HELEN-006研究首次通过优效性设计证实,每周白蛋白结合型紫杉醇+曲帕双靶方案的pCR率优于传统TCbHP方案(59.3% vs 45.9%)。然而,HELEN-006研究对照组为“每3周给药的多西他赛+卡铂+曲帕双靶”,存在药物种类与给药周期双重变量,难以单独确证“去除卡铂”的独立效应。相比之下,neoCARHP研究实现了更严格的单变量控制:两组均采用每3周给药模式,紫杉类药物选择完全一致,有效排除混杂因素,研究结果直接证实“卡铂在双靶方案中并非必需”这一核心结论。
2. 规避神经毒性叠加,实现更优耐受性
HELEN-006研究虽规避了卡铂所致骨髓抑制,但高强度每周白蛋白结合型紫杉醇方案导致试验组3-4级周围神经病变发生率较高(13.1%,对照组仅0.5%),一定程度上限制了其在神经毒性敏感患者中的应用。而neoCARHP研究采用标准每3周给药方案,THP组3-4级周围神经病变发生率仅为0.3%,在保持高pCR率的同时,妥善规避了高频给药带来的神经毒性风险,实现了疗效与安全性的更优平衡。
3. 贴合常规诊疗节奏,临床落地性较高
HELEN-006研究使用的每周给药模式要求患者治疗期间频繁就诊,可能增加部分患者的交通与时间成本;而neoCARHP研究的每3周给药方案完全契合我国绝大多数医院的常规化疗流程,既降低了患者就医负担,也便于各级基层医院推广应用。
总体而言,HELEN-006研究为追求高pCR率且能耐受周疗的患者提供了优效选择,而neoCARHP研究则面向更广泛的普通乳腺癌人群,证实常规每3周给药场景下省略卡铂仍具备疗效保障,且整体安全性更优。
结论
neoCARHP研究凭借高质量的“头对头”Ⅲ期循证医学证据证实,对于Ⅱ期、Ⅲ期HER2阳性早期乳腺癌患者,每3周1次的THP方案新辅助治疗,其pCR率非劣效于经典的TCbHP标准方案,同时可有效降低严重不良事件发生率及治疗期间的剂量调整风险。该研究进一步确立了THP方案作为该人群更安全、便捷且高效的标准新辅助治疗方案的地位,为未来精准降阶梯治疗奠定了坚实的循证基础。
1. Gao HF, Ye GL, Lin Y, et al. Neoadjuvant Taxane Plus Trastuzumab and Pertuzumab With or Without Carboplatin in Human Epidermal Growth Factor Receptor 2-Positive Breast Cancer: The Randomized Noninferiority Phase III neoCARHP Trial. J Clin Oncol.
2. Schneeweiss A, Chia S, Hickish T, et al. Pertuzumab plus trastuzumab in combination with standard neoadjuvant anthracycline-containing and anthracycline-free chemotherapy regimens in patients with HER2-positive early breast cancer: a randomized phase II cardiac safety study (TRYPHAENA). Ann Oncol. 2013;24(9):2278-2284.
3. Gianni L, Pienkowski T, Im YH, et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomised multicentre, open-label, phase 2 trial. Lancet Oncol. 2012;13(1):25-32.
4. Nitz U, Gluz O, Graeser M, et al. De-escalated neoadjuvant pertuzumab plus trastuzumab therapy with or without weekly paclitaxel in HER2-positive, hormone receptor-negative, early breast cancer (WSG-ADAPT-HER2+/HR-): survival outcomes from a multicentre, open-label, randomised, phase 2 trial. Lancet Oncol. 2022;23(5):625-635.
5. von Minckwitz G, Schneeweiss A, Loibl S, et al. Neoadjuvant carboplatin in patients with triple-negative and HER2-positive early breast cancer (GeparSixto; GBG 66): a randomised phase 2 trial. Lancet Oncol. 2014;15(7):747-756.
6. Chen XC, Jiao DC, Qiao JH, et al. De-escalated neoadjuvant weekly nab-paclitaxel with trastuzumab and pertuzumab versus docetaxel, carboplatin, trastuzumab, and pertuzumab in patients with HER2-positive early breast cancer (HELEN-006): a multicentre, randomised, phase 3 trial. Lancet Oncol. 2025;26(1):27-36.
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


