坏疽性脓皮病(Pyoderma Gangrenosum, PG)是一种罕见的自身炎症性中性粒细胞性皮肤病,以快速进展的疼痛性溃疡性皮损为典型表现,病变边缘常呈紫罗兰色、潜行性破坏,好发于下肢。其发病多与系统性疾病相关,最常见于炎症性肠病、未明意义的单克隆丙种球蛋白病(MGUS)等自身免疫性或血液系统疾病,但与淋巴浆细胞淋巴瘤(LPL)及其亚型华氏巨球蛋白血症(WM)相关的病例极为罕见。WM是一种B细胞淋巴增殖性疾病,以骨髓中淋巴浆细胞浸润(比例>10%)和过量IgM单克隆球蛋白产生为特征,可引发高黏滞血症、终末器官损伤等一系列表现。本文报道1例以坏疽性脓皮病为首发表现的WM病例,结合文献探讨其临床特点、诊断思路及潜在发病机制,为临床医生提供参考。

病例介绍:典型皮损为首发,复杂病史藏隐忧
基本情况与既往史
患者女性,72岁,因“双小腿疼痛性皮损数周”就诊于初级保健科。患者既往病史复杂,有30-包-年吸烟史,曾患左前臂鳞状细胞癌(14年前)、基底细胞癌(具体不详)、蕈样肉芽肿(8年前,活检证实),近期有脑卒中、复发性肺炎、慢性低钠血症及肠易激综合征病史,存在多次跌倒史。
体格检查
双小腿可见3处疼痛、脆嫩、血性浆液性瘀斑样皮损,最大皮损位于右小腿内侧,大小约6cm×5cm×0.1cm(面积33.5cm²,体积3.35cm³),符合坏疽性脓皮病典型表现,临床高度怀疑合并感染(图1)。
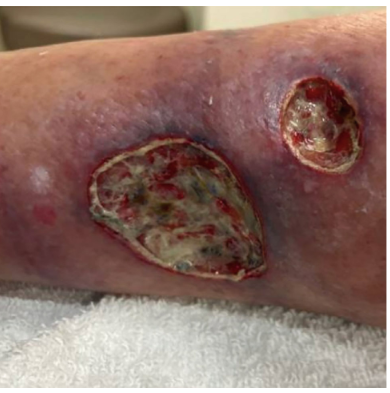
辅助检查
感染及风湿免疫相关检查:快速血浆反应素(RPR)、甲肝/乙肝/丙肝抗体、红细胞沉降率(ESR)、C反应蛋白(CRP)、钙卫蛋白均为阴性;抗核抗体、抗中性粒细胞胞浆抗体、类风湿因子等自身抗体检测均无异常,初步排除感染及常见自身免疫性疾病。
免疫分型及血液学检查:血清蛋白电泳示IgM显著升高(746.8mg/dL,正常范围33.0-293.0mg/dL),伴单克隆峰(0.5g/dL);血清κ/λ游离轻链比值升高至2.83(正常范围 0.26-1.65),α1球蛋白(0.41g/dL)及γ球蛋白(1.73g/dL)水平升高。复查电泳及免疫分型显示,κ/λ游离轻链比值进一步升至3.00,IgM(649.8mg/dL)及单克隆峰(0.38g/dL)持续升高。
影像学及病理检查:¹⁸F -氟脱氧葡萄糖正电子发射断层显像(¹⁸F-FDG PET)示食管胃交界处、胃窦、十二指肠近端及右肺下叶小结节存在异常放射性摄取,后者可疑恶性;右髂骨骨髓活检示50%~60%骨髓被克隆性淋巴浆细胞浸润,符合淋巴浆细胞淋巴瘤诊断,骨髓涂片可见铁储备减少及散在伴胞浆空泡形成的红系前体细胞。
其他检查:患者去世后尸检发现EB病毒(EBV)衣壳抗原IgG及核抗原抗体显著升高(分别>750.0U/mL、>600.0U/mL)。
治疗经过:抗感染抗炎收效微,病情急转终致命
患者初始皮损分泌物需氧培养示大肠埃希菌生长,予复方磺胺甲恶唑治疗1周后无改善,疑诊铜绿假单胞菌感染,调整为左氧氟沙星联合多西环素(100mg,每日2次,共7天)广谱抗感染治疗,同时予泼尼松25mg口服针对皮损治疗。
1个月后,因创面愈合不佳入院,创面培养示耐抗生素粪肠球菌、大肠埃希菌及弗氏柠檬酸杆菌生长,血培养无细菌生长。予头孢吡肟(1g,每6小时静脉输注)联合利奈唑胺静脉抗感染,感染科会诊后建议出院后予厄他培南(每日1次静脉输注,经PICC管给药)联合利奈唑胺(每日2次口服)治疗2周,同时由创面护理团队予Santyl药膏及加压包扎处理,皮肤科会诊后监督泼尼松逐渐减量,并计划出院后行皮损活检。期间感染控制略有改善,但皮损外观无明显好转。
出院8天后,患者出现咽痛(诊断为鹅口疮),予克霉唑口服治疗,随后出现剧烈头晕、腹部锐痛及恶心。用药5天后出现意识改变,急诊就诊时表现为心动过缓、低血压及严重低血糖(血糖<20mg/dL),转运途中予10%葡萄糖输注,随后心跳骤停,予心肺复苏及肾上腺素注射,入院时口咽部可见血性分泌物,最终因心跳呼吸骤停死亡,距初始皮损出现仅2个月。
寻根溯源:罕见关联揭真相,诊疗困境析缘由
病例核心矛盾与诊断突破
本例患者以典型坏疽性脓皮病皮损为首发表现,初始治疗聚焦于抗感染及抗炎,但创面愈合不佳且反复出现耐药菌感染,提示存在非感染性基础病因。通过系统检查排除感染、常见自身免疫性疾病后,免疫分型发现的IgM单克隆丙种球蛋白病成为关键线索,最终经骨髓活检确诊华氏巨球蛋白血症,揭示了皮肤病变与潜在血液系统恶性肿瘤的关联。
坏疽性脓皮病与华氏巨球蛋白血症的罕见关联
坏疽性脓皮病与血液系统疾病的关联在65岁以上人群中更为密切,其中最常见的相关血液系统疾病为未明意义的单克隆丙种球蛋白病(MGUS),发生率最高可达27%。但现有文献中,坏疽性脓皮病与IgM型单克隆丙种球蛋白病相关的报道极少,与WM相关的病例更为罕见——一项纳入340例坏疽性脓皮病合并血液系统恶性肿瘤的系统综述中,仅3例与WM相关,且无单独病例报道。
WM的皮肤表现多与副蛋白血症、副蛋白相关自身免疫病或肿瘤细胞皮肤浸润相关,直接由IgM沉积于小血管导致的溃疡已有少量报道,但本例患者临床表现更符合坏疽性脓皮病,虽未完成皮损组织病理学确诊,但结合典型临床表现及排除其他病因后,高度支持该诊断。
发病机制与治疗困境
坏疽性脓皮病的发病机制与先天及适应性免疫调节紊乱相关,表现为TNF-α、IL-17、IL-23等促炎细胞因子升高,且存在“皮肤外伤后皮损诱发”的皮肤过敏现象。对于合并单克隆丙种球蛋白病的坏疽性脓皮病患者,其皮损复发率更高、对标准治疗反应更差,推测与单克隆免疫球蛋白通过激活中性粒细胞但抑制其功能,进而阻碍皮肤愈合相关,其中IgA亚型最常见,IgM亚型的作用机制尚不清楚。
本例患者治疗效果不佳的核心原因在于未及时针对潜在WM进行治疗——现有证据表明,仅控制坏疽性脓皮病症状无法实现皮损根治,需同时治疗基础单克隆丙种球蛋白病。此外,患者存在的高黏滞血症(可能被复杂基础病史掩盖)、恶性肿瘤相关免疫抑制及长期使用糖皮质激素导致的感染风险增加,共同促成了病情快速恶化。
关键临床启示
坏疽性脓皮病患者需常规完善血液系统疾病筛查,尤其是单克隆丙种球蛋白病相关检查,即使无血液系统疾病典型症状,也需警惕罕见淋巴增殖性疾病的可能。
对于合并单克隆丙种球蛋白病的坏疽性脓皮病患者,若标准抗炎、抗感染治疗效果不佳,应及时评估基础血液疾病活动性,尽早启动针对性治疗。
WM等惰性血液系统恶性肿瘤可能以自身炎症性皮肤病为首发表现,且可导致患者病情快速进展,临床需避免因“惰性肿瘤”认知而延误治疗。
坏疽性脓皮病患者出现创面耐药菌感染时,除调整抗感染方案外,需重点排查基础病因,避免过度聚焦感染而忽视潜在恶性疾病。
小结
本例报道了1例以坏疽性脓皮病为首发表现的WM病例,凸显了罕见血液系统恶性肿瘤与自身炎症性皮肤病之间的特殊关联。临床工作中,对于表现为坏疽性脓皮病的患者,需警惕潜在系统性疾病,尤其是血液系统疾病的可能,及时完善相关筛查,避免漏诊误诊。对于合并单克隆丙种球蛋白病的患者,应重视基础疾病的评估与治疗,以改善皮损预后及患者生存。此外,本例患者快速进展的临床病程提示,即使是惰性血液系统肿瘤,也可能在自身炎症性疾病背景下导致严重后果,需采取积极的诊断与治疗策略。
以下关于坏疽性脓皮病(PG)与华氏巨球蛋白血症(WM)的关联及临床管理,说法正确的是:
A. 坏疽性脓皮病最常见的相关血液系统疾病为华氏巨球蛋白血症,发生率约 27%
B. 合并单克隆丙种球蛋白病的坏疽性脓皮病患者,皮损对标准抗炎治疗反应良好,复发率低
C. 华氏巨球蛋白血症的皮肤表现可包括因 IgM 沉积于小血管导致的溃疡,与坏疽性脓皮病需注意鉴别
D. 坏疽性脓皮病患者若创面愈合不佳,仅需强化抗感染治疗,无需排查血液系统疾病
E. 华氏巨球蛋白血症为高度侵袭性肿瘤,其合并的坏疽性脓皮病皮损多在肿瘤确诊后出现
上一期《【寻根溯源】嗜酸性粒细胞持续增多背后的致命隐患:一例慢性嗜酸性粒细胞白血病的诊疗启示》的答案为C
Laya Krishnan et al; A Rare Case of Pyoderma Gangrenosum Pointing to Waldenström Macroglobulinemia;https://onlinelibrary.wiley.com/doi/10.1155/crom/5443156.
排版编辑:Mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


