2025年,激素受体阳性/人表皮生长因子受体2阴性(HR+/HER2-)早期乳腺癌(EBC)的辅助治疗领域迎来重要循证医学里程碑。随着NATALEE研究5年随访数据的重磅发布,细胞周期蛋白依赖性激酶4/6(CDK4/6)抑制剂瑞波西利在早期辅助治疗中的长期疗效获得确证性证据。结合多项真实世界研究(RWE)结果、国际指南更新及市场准入,瑞波西利的应用范围已明确覆盖高复发风险HR+/HER2-全人群。本文将从最新循证医学数据、真实世界复发风险、指南与准入及临床实践意义四个维度,对2025年瑞波西利的临床进展进行年度盘点。
NATALEE研究的创新设计
HR+/HER2-是乳腺癌最常见的亚型,约占所有乳腺癌的70%以上。尽管辅助内分泌治疗(ET)的规范应用显著改善了患者预后,但临床数据显示,约20%-30%的早期乳腺癌患者在治疗期间或治疗结束后仍面临复发风险,该风险具有长期持续性,最长可延伸至确诊后20年[1]。尤其对于中高危患者,如何进一步降低复发率、延长无病生存期,是当前临床实践中的核心挑战。
CDK4/6抑制剂在HR+/HER2-晚期乳腺癌治疗中已确立标准地位,显著改善了患者的无进展生存期和总生存期,这为其向早期辅助治疗领域的探索奠定了基础。NATALEE研究在此背景下应运而生,其设计具有鲜明的临床导向性与创新性:与既往CDK4/6抑制剂早期乳腺癌临床试验相比,该研究不仅纳入了淋巴结阳性(N+)患者,而且将伴有高危因素的淋巴结阴性(N0)患者纳入研究人群[2],具体包括:①N0合并肿瘤大小T3-T4;②N0且肿瘤大小T2,合并高位复发因素(G3,或G2且Ki-67指数≥20%,或G2且多基因检测提示高风险)的患者。在给药方案上,NATALEE研究采用400mg/d的瑞波西利起始剂量(低于晚期治疗常用的600mg/d剂量),并将给药时长延长至3年,旨在通过更长周期的细胞周期抑制清除微小残留病灶,诱导肿瘤细胞进入不可逆衰老状态,在保障良好耐受性的前提下最大化治疗获益。此外,研究允许患者在辅助内分泌治疗启动后12个月内入组,提供了更宽泛的治疗窗口,提升了临床实践的可操作性。

NATALEE研究5年随访数据揭示长期疗效
2025年欧洲肿瘤内科学会(ESMO)年会上,NATALEE研究的5年随访数据以最新突破性摘要(LBA)形式发布[3]。所有入组患者均已停止瑞波西利治疗中位时间达2年,该时间节点数据能够客观反映药物停药后的长期疗效维持效应及对患者预后的持续影响。
主要终点:iDFS获益持续且具统计学显著性
截至2025年5月28日,研究中位随访时间达55.4个月。在意向治疗(ITT)人群中,瑞波西利联合非甾体芳香化酶抑制剂(NSAI)组对比单独NSAI组的5年无浸润性疾病生存率(iDFS)分别为85.5%和81.0%,绝对获益幅度从3年时的2.7%提升至5年时的4.5%。瑞波西利组较对照组显著降低28.4%的复发或死亡风险(HR=0.716,95% CI:0.618-0.829,P<0.0001),提示在停止瑞波西利治疗2年后,治疗组与对照组的生存曲线(Kaplan-Meier曲线)仍保持分离趋势,证实其疗效具有长期[3]。
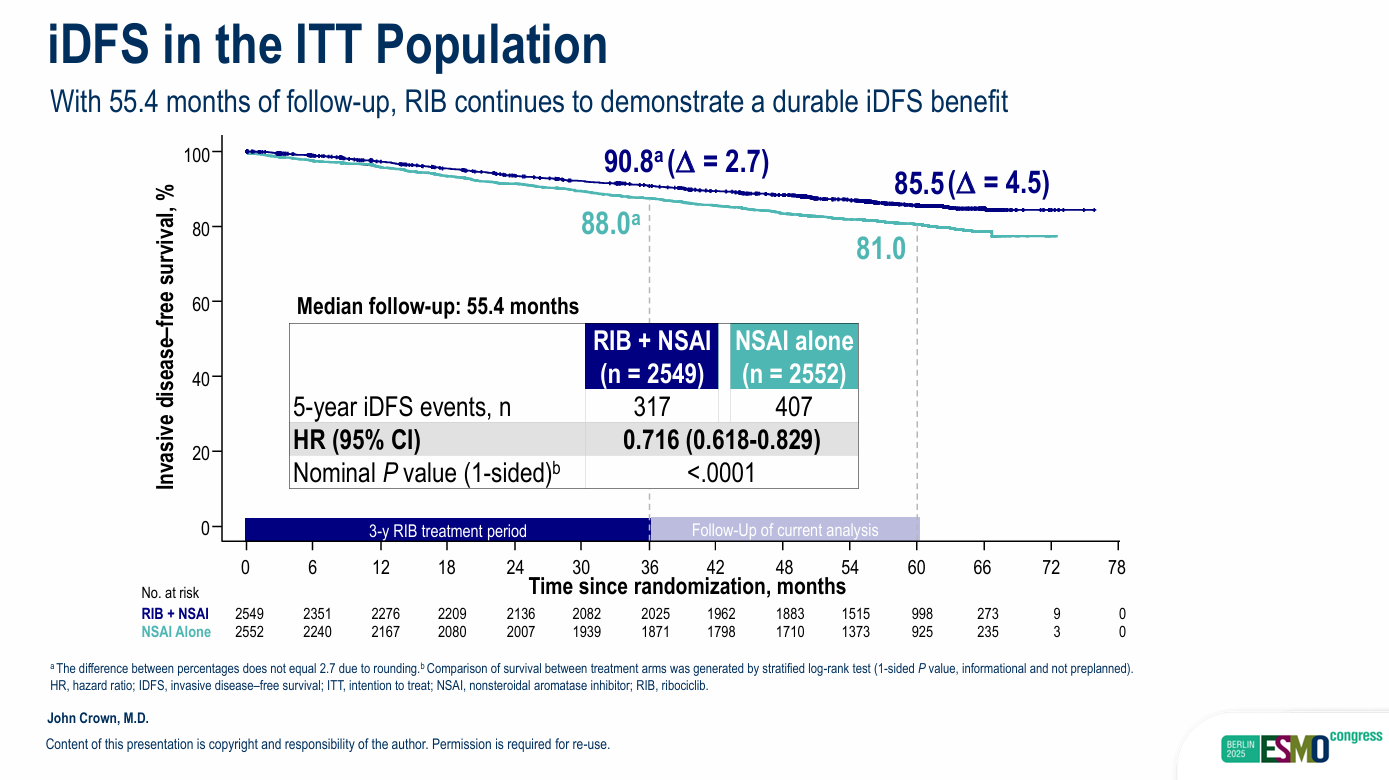
次要终点:DDFS数据更新证实长期远处转移风险降低
2025年圣安东尼奥乳腺癌研讨会(SABCS)上,NATALEE研究公布了更新的无远处疾病生存期(DDFS)5年随访数据。远处转移是乳腺癌患者的主要致死原因,且一旦发生通常被认为不可治愈,因此降低远处复发风险具有重要临床意义。数据显示,在所有患者停用瑞波西利中位时间达2年时,瑞波西利联合NSAI组相较于NSAI单药组,仍展现出持续、稳健的远处复发风险降低获益。ITT人群中,瑞波西利联合NSAI组的DDFS显著改善,HR为0.749(95% CI 0.623-0.900,双侧名义P=0.0020)。
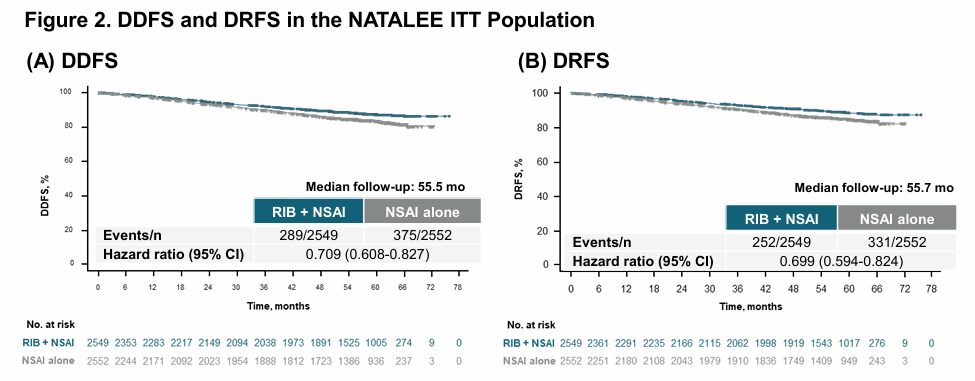
具体而言,乳腺癌最常见的远处复发部位依次为骨、肝脏、肺/胸膜及远处淋巴结。数据表明,瑞波西利联合NSAI组在上述所有部位的复发事件数均少于NSAI单药组。该结果充分证实,3年瑞波西利辅助治疗方案不仅可延缓疾病复发,更能有效减少致死性远处转移事件的发生。随着随访时间延长,两组生存曲线持续分离,进一步强化了“延继效应”的临床证据——即停药后较长时间内,患者仍可持续从早期强化治疗中获益,这为改善患者长期生存奠定了坚实基础。
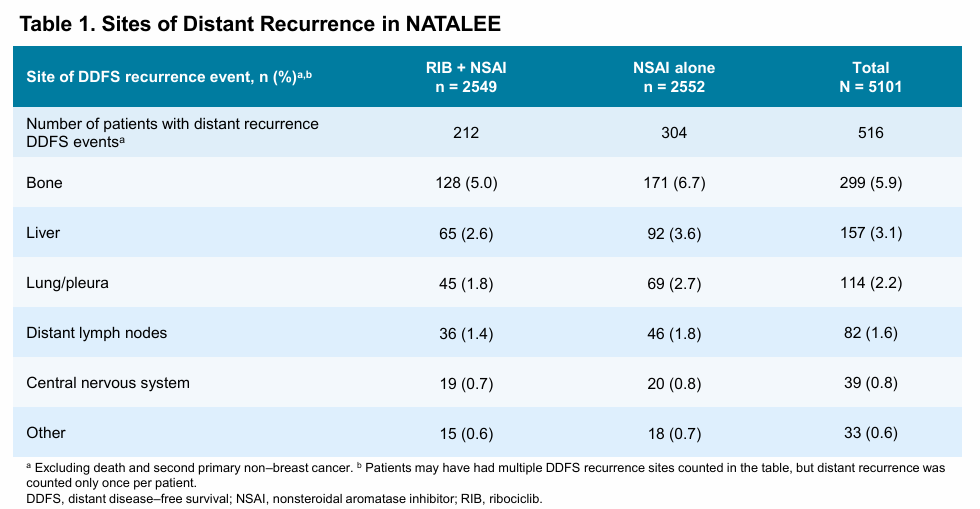
真实世界研究证据验证高复发风险人群治疗需求
除随机对照临床试验数据外,2025年发表的一项真实世界研究进一步佐证了NATALEE研究人群定义的临床合理性,同时凸显了强化治疗的必要性。
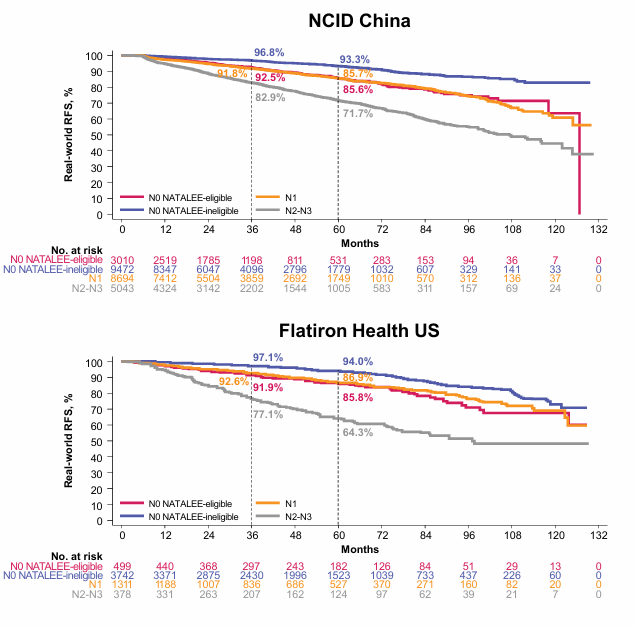
2025年ESMO大会公布的一项联合大样本回顾性分析(摘要号:438eP),基于中国国家癌症中心(NCC)数据库与美国Flatiron Health电子健康记录数据库构建,为早期乳腺癌风险分层提供了关键真实世界证据[5]。该研究纳入2013-2022年确诊的近3.5万例Ⅰ-Ⅲ期HR+/HER2-乳腺癌患者(中国28,623例、美国5,930例),旨在评估符合NATALEE研究入组标准人群的长期预后。
结果显示,无论中国还是美国人群,符合NATALEE研究入组标准的患者均存在客观的高复发风险。在接受标准手术联合传统辅助治疗后,该人群5年无复发生存(RFS)事件风险仍高达19%,5年无远处转移生存(DRFS)事件风险约为15%。该数据打破了既往对部分早期患者“低危”的传统认知。
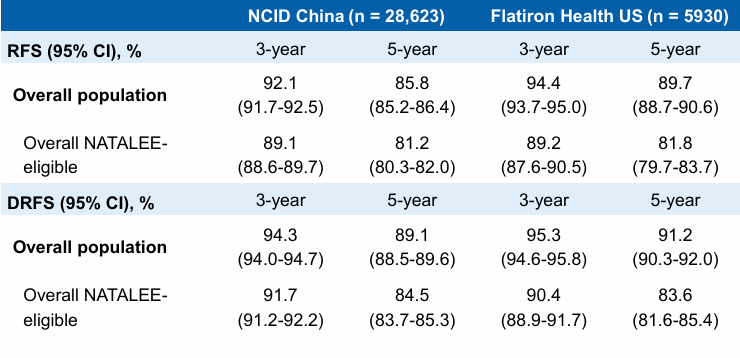
此外,该研究进一步对比不同淋巴结状态患者的预后差异,发现淋巴结阴性伴高危因素(N0高危)患者的复发风险与淋巴结阳性(N1)患者相当。这一结果从真实世界数据层面,有力佐证了对N0高危人群实施强化辅助治疗的必要性,同时验证了NATALEE研究纳入该人群的科学性——临床医生不应仅依据淋巴结阴性状态就忽视患者潜在复发风险,而瑞波西利强化治疗方案对填补这一临床未满足需求具有重要价值。
指南更新与临床获批
基于临床试验与真实世界证据的持续积累,瑞波西利在2025年获得全球主要指南推荐及临床广泛批准,确立了其在早期乳腺癌辅助治疗中的标准地位。
国际指南地位提升
2025年v5版《美国国家综合癌症网络(NCCN)乳腺癌临床实践指南》将瑞波西利联合AI方案列为HR+/HER2-早期乳腺癌辅助治疗的1级推荐(优选方案),推荐范围明确覆盖淋巴结阳性及高危淋巴结阴性患者[6]。基于NATALEE研究,瑞波西利同时获得欧洲肿瘤内科学会临床获益量表(ESMO-MCBS)A级评分,该评级代表辅助治疗领域的最高等级临床获益,使瑞波西利成为目前唯一在早期及晚期HR+/HER2-乳腺癌领域均获得ESMO-MCBS最高评分的CDK4/6抑制剂,充分体现其全程治疗价值[7]。
中国指南同步更新
《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2025版)》紧跟国际前沿,基于NATALEE研究数据首次基于NATALEE入组人群特征对HR+/HER2-早期乳腺癌患者复发风险分层重新定义,推荐瑞波西利联合AI用于NATALEE全人群的辅助强化治疗(Ⅱ级推荐,IB类证据)[8]。
《中国抗癌协会乳腺癌诊疗指南(2026版)》对HR+/HER2-早期乳腺癌的辅助内分泌治疗策略进行了重要更新[9]:
对于淋巴结阳性的患者,瑞波西利联合AI 均作为其辅助内分泌治疗最高级别推荐方案。
对于淋巴结阴性伴高危因素患者,指南推荐评估复发风险及治疗敏感性,同时新增瑞波西利联合内分泌治疗作为“考虑”方案。
这一更新标志着中国权威指南正式认可瑞波西利在NATALEE全人群中的核心治疗价值,为临床规范化应用提供了强有力的指导。
2025年5月14日,中国国家药品监督管理局(NMPA)正式批准瑞波西利新增早期乳腺癌辅助治疗适应症,适用范围覆盖NATALEE研究全人群,成为中国首个且唯一获批用于广泛II-III期HR+/HER2-早期乳腺癌辅助治疗的CDK4/6抑制剂。2025年12月,瑞波西利早期乳腺癌辅助适应症也已被纳入国家医保目录,将于2026年1月1日正式落地执行。
2025年是瑞波西利在HR+/HER2-早期乳腺癌辅助治疗领域的里程碑之年。NATALEE研究5年随访数据不仅确立了其在中高危全人群中的疗效基石地位,更通过真实世界证据验证与全球指南更新,将循证医学获益转化为标准化临床实践。这标志着HR+/HER2-早期乳腺癌治疗已迈入"精准分层、高危强化"的新阶段,为更多患者带来长期生存希望,助力实现乳腺癌治愈的终极目标。
[1] Burstein HJ, Lacchetti C, Anderson H, et al. Adjuvant Endocrine Therapy for Women With Hormone Receptor-Positive Breast Cancer: ASCO Clinical Practice Guideline Focused Update. J Clin Oncol. 2019;37(5):423-438.
[2] Hortobagyi GN, Lacko A, Sohn J, et al. A phase III trial of adjuvant ribociclib plus endocrine therapy versus endocrine therapy alone in patients with HR-positive/HER2-negative early breast cancer: final invasive disease-free survival results from the NATALEE trial. Ann Oncol. 2025;36(2):149-157.
[3] Adjuvant ribociclib (RIB) plus nonsteroidal aromatase inhibitor (NSAI) in patients (pts) with HR+/HER2− early breast cancer (EBC): NATALEE 5-year outcomes.2025 ESMO LBA14.
[4] Five-Year Analysis of Distant Disease-Free Survival Across Key Subgroups From The Phase 3 NATALEE Trial of Ribociclib Plus a Nonsteroidal Aromatase Inhibitor in Patients with HR+/HER2− Early Breast Cancer 2025 SABCS. Poster PS3-09-08.
[5] Real-world characteristics, treatment patterns, and outcomes in patients (pts) with HR+/HER2− early breast cancer (EBC) from China and the US. 2025 ESMO 438eP.
[6] National Comprehensive Cancer Network. (2025). NCCN Clinical Practice Guidelines in Oncology (Version 5.2025).
[7] Loibl S, André F, Bachelot T, et al. Early breast cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol. 2024;35(2):159-182.
[8] 中国临床肿瘤学会. CSCO乳腺癌诊疗指南(2025版)[EB/OL]. (2025-04-12)[2025-11-19]. https://www.csco.org.cn
[9] 中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2025年版)[EB/OL]. (2024-12-21) [2025-11-19]. https://cacaguidelines.cacakp.com
排版编辑:肿瘤资讯-李鑫











 苏公网安备32059002004080号
苏公网安备32059002004080号


