激素受体(HR)阳性/人表皮生长因子受体2(HER2)阴性乳腺癌是乳腺癌中最常见的亚型。近年来,CDK4/6抑制剂联合内分泌治疗已成为该亚型晚期患者的标准一线方案,显著改善了患者的无进展生存期。然而,部分患者,特别是携带PIK3CA等特定基因突变的患者,可能出现快速耐药,预后不佳,其后续治疗策略充满挑战。
本期【PIK TALK】专栏分享一例由中山大学孙逸仙纪念医院龚畅医生团队诊治的一例复杂的HR+/HER2-双侧乳腺癌。该患者肿瘤负荷巨大,合并肝、骨等多处转移,且携带PIK3CA p.H1047R热点突变。虽经标准一线CDK4/6抑制剂联合内分泌治疗一度获益,但在短短6个月后即出现疾病进展。面对棘手的快速耐药局面,临床医生基于精准的基因检测结果,果断采用以PI3Kα抑制剂及突变体降解剂伊那利塞(Inavolisib)为核心的三联靶向方案,成功逆转了病情进展。为深入剖析诊疗策略与临床启示,本专栏特邀龚畅教授和曾银朵教授进行专业点评。
诊疗报告
基本信息与初诊(2024年9月)
1.基本情况:患者女,46岁,未绝经,因“发现左乳肿物1年余,伴皮肤红肿4月余”就诊。无肿瘤家族史及其他基础疾病史。
影像学评估:初诊时影像学检查(乳腺MR、肝脏MR、PET-CT)提示病情严重。
原发灶:双侧乳腺均可见巨大癌灶,左乳最大肿块约 53×32mm,右乳约 23×16mm,均已侵犯胸壁。
转移灶:存在广泛的多处、多器官转移,包括左侧腋窝及锁骨上淋巴结、肝脏(最大病灶达 80×62mm)、以及全身多发骨骼(脊椎、骨盆、肋骨、胸骨等)。
2.病理及免疫组化:经多部位穿刺活检,病理结果证实:
双侧乳腺及肝转移灶均为HR阳性/HER2阴性浸润性导管癌。左乳Ki-67指数为40%,肝转移灶为20%。
3.基因检测(NGS):为指导后续治疗,对肿瘤组织进行了二代测序,结果显示:
检出关键的PIK3CA基因p.H1047R体细胞热点突变,突变丰度达33.54%。
同时伴有TP53突变、CCND1扩增等多个基因变异。
4.最终诊断:双侧HR+/HER2-乳腺癌,初诊IV期(骨、肝、淋巴结多发转移),PIK3CA突变型。
晚期一线治疗:短暂缓解后快速进展(PFS: 6个月)
该患者于2024年10月中旬开始接受一线治疗,方案为:瑞波西利联合依西美坦、戈舍瑞林 。整个评估过程动态地反映了治疗初期肿瘤的显著退缩和后期的快速反弹。
1.疗效评估:
初期显著缓解(治疗后2个月):评效为部分缓解(PR)。影像学显示肝脏最大病灶由80×62mm 缩小至 27×25mm;乳腺原发灶亦显著缩小。肿瘤标志物CA153从734 U/mL骤降至57.8 U/mL。
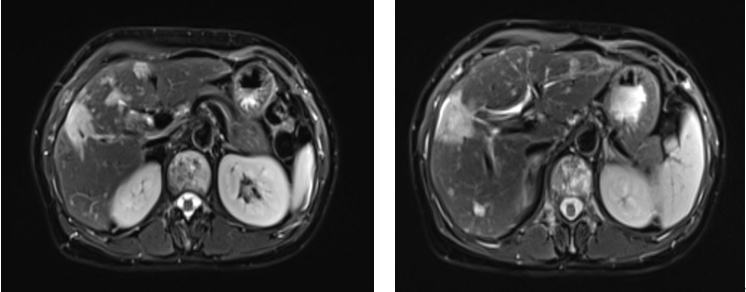
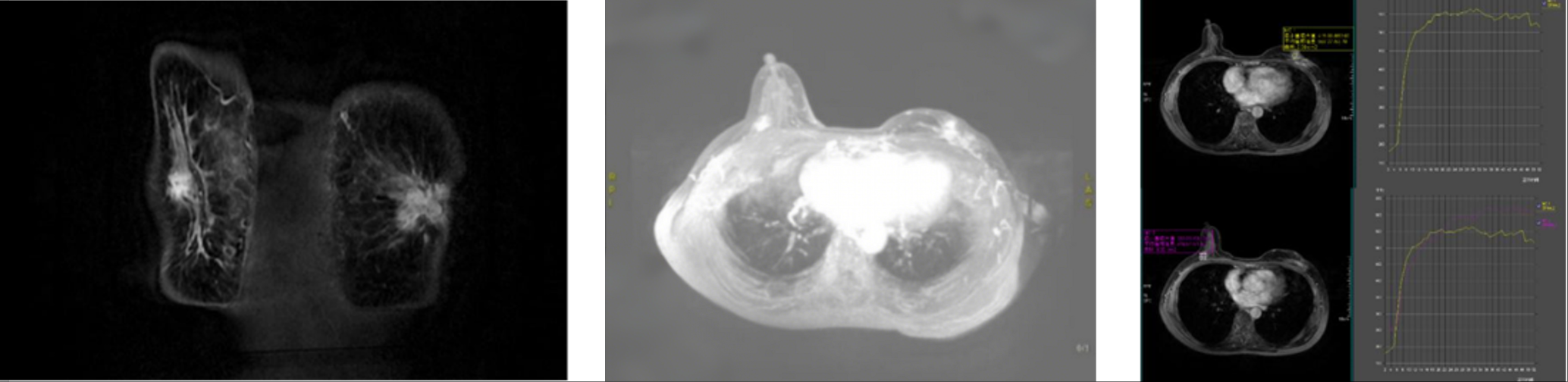
乳腺MR
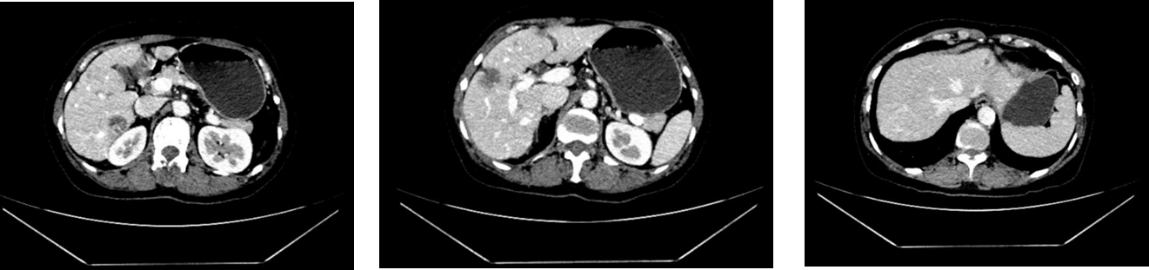
出现进展信号(治疗后5-6个月):2025年4月,CEA指标由最低点6.6 ng/mL反弹至14.6 ng/mL。至5月,CEA进一步升至21.9 ng/mL,影像学复查证实肝脏病灶较前增大(最大 23×29mm)。
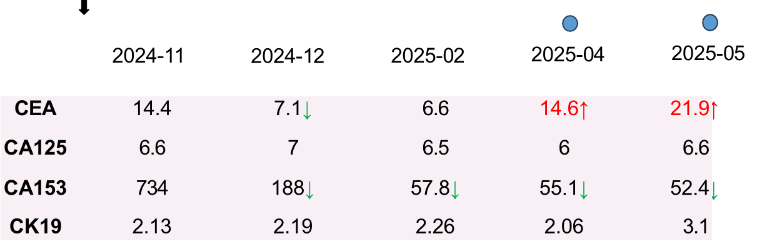
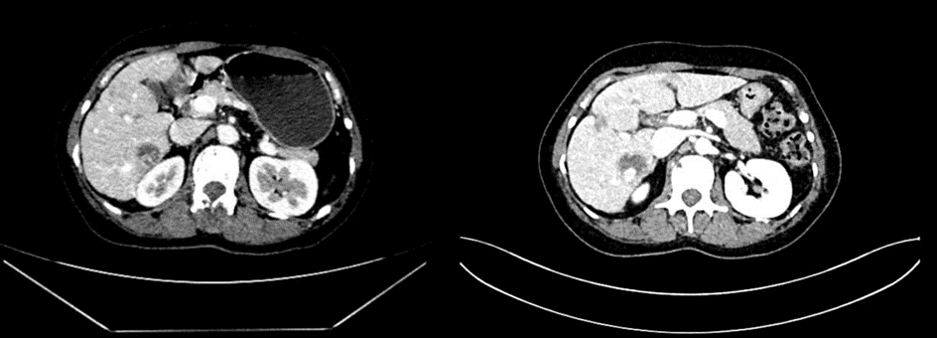
2.一线治疗结局:评效为疾病进展(PD),一线治疗的无进展生存期(PFS)仅为6个月。
晚期二线治疗:精准靶向,力挽狂澜
1.治疗决策:基于明确的PIK3CA突变及一线快速耐药,团队决定采用以PI3Kα抑制剂为核心的精准靶向治疗。于2025年5月底启动二线方案:伊那利塞(PI3Kαi)+ 哌柏西利(CDK4/6i)+氟维司群(SERD),并继续支持治疗。
2.初步疗效评估(治疗后1个月):2025年6月底复查CT显示:
双乳原发灶及肝内转移灶均显著缩小。
评效为PR。
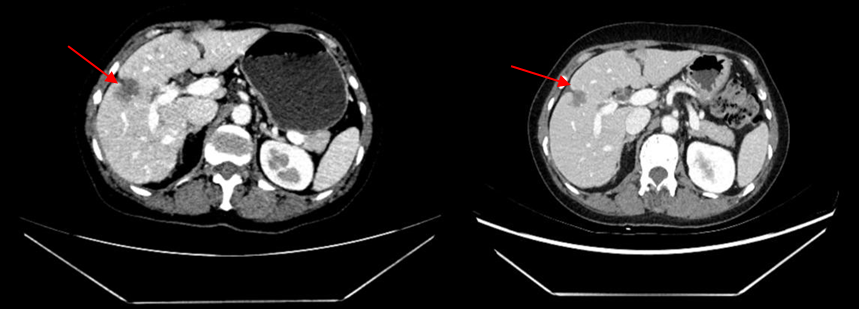
腹部CT (左边为二线治疗开始前(2025年5月) vs. 右边为伊那利塞三联方案靶向治疗1个月后(2025年6月)
3.不良反应管理:
治疗期间出现了可预期的口腔溃疡及轻度粒细胞缺乏,经对症处理后均好转。
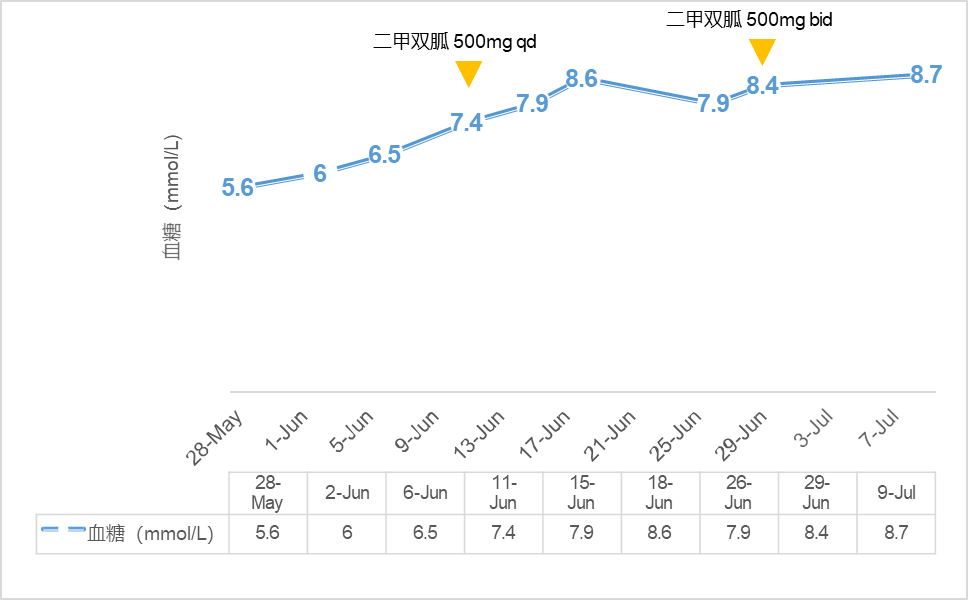
用药后21天出现空腹血糖升高(最高8.6 mmol/L),立即启动二甲双胍口服治疗,并根据血糖监测结果将剂量从每日一次调整至每日两次,血糖被平稳控制在安全范围内,患者耐受性良好,治疗未受影响。
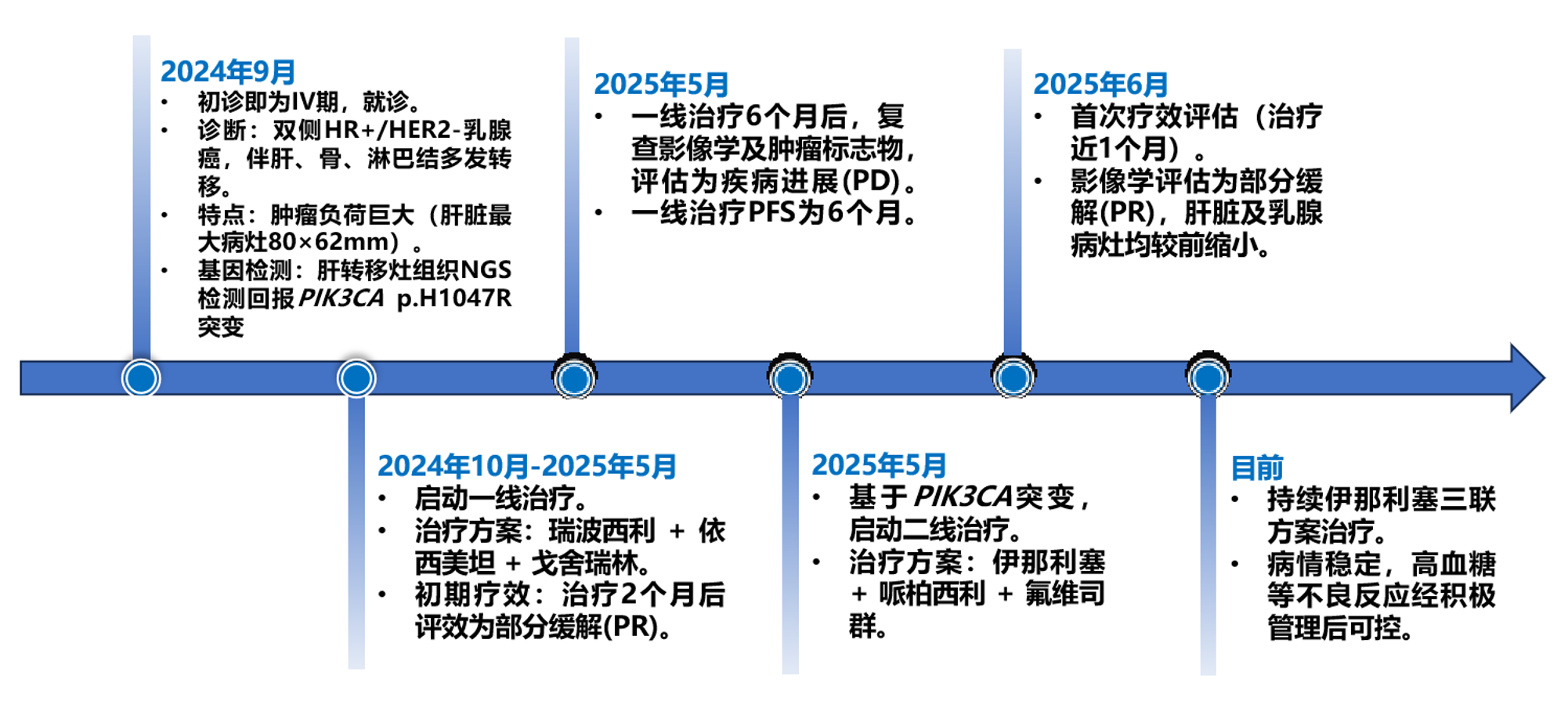
诊疗过程总结
专家点评
专家介绍
中山大学孙逸仙纪念医院逸仙乳腺肿瘤医院
乳腺外科教授三级/二级主任医师 外科学博士 博士生导师
乳腺诊断专科主任 乳腺肿瘤中心第二职工党支部书记
中国抗癌协会乳腺癌整合防筛专委会常委
中国抗癌协会乳腺癌专委会委员
中国女医师协会乳腺专委会 常委
中国女医师协会临床肿瘤专委会 委员
中国医师协会医学遗传医师分会肿瘤医学学组组员
广东省医师协会乳腺专科医师分会副主委
广东省精准医学应用分会癌症早筛早诊分会副主委
广东省抗癌协会癌症筛查与早诊早治专委会副主委
广东省临床医学学会泛家族遗传性肿瘤防控专委会副主委
广东省临床医学学会乳腺癌专委会副主委
广东省医学会乳腺病学分会常委
主持科技部国家重点研发计划(课题组长)1项、国家科技创新20230(课题组长)1项,国家自然科学基金7项,省部级基金7项。CSCO基金2项。入选科技部、教育部、广东省杰青等人才项目5项。主编人卫出版社专著《组织标记在乳腺疾病精准诊疗中的应用》。研究成果获广东省科技进步二等奖(第一完成人),获专利12项。以通讯(含共同)在BMJ,Cell Reports Medicine,Med, Molecular Cancer,Advanced Science,等发表论文35篇,总引用2771次,高被引论文4篇。
专家介绍
中山大学孙逸仙纪念医院 乳腺内科
广东省胸部肿瘤防治研究会乳腺肿瘤内科专业委员会,主任委员
中国医药卫生事业发展基金会乳腺肿瘤学组,常委兼秘书长
广东省药学会第二届肿瘤全程管理专家委员会,副主任委员
广东省卫生信息网络协会智慧肿瘤研究分会,副会长
广东省临床医学学会泛家族遗传性肿瘤防控专业委员会,常委
广东省胸部肿瘤防治研究会胸部肿瘤脑转移专业委员会委员
广东省抗癌协会乳腺癌专业委员会委员
中国抗癌协会肿瘤分子医学专业委员会委员
中国抗癌协会肿瘤标志专业委员会会员
主持国家自然科学基金青年基金1项
主持中山大学5010培育项目1项
主持逸仙临床研究培育项目1项
参加编写《临床肿瘤内科学》和《乳腺癌保乳治疗》
英国卡迪夫大学访问学者
参加多项国际及国内多中心临床研究
龚畅教授:本例患者的完整诊疗历程,为携带PIK3CA突变的HR+/HER2-晚期乳腺癌(MBC)在一线CDK4/6抑制剂治疗快速进展后的管理,提供了重要的临床启示和范例。新方案迅速起效,仍需动态监测患者后续影像学与临床指标,以进一步确定疗效的持续性。
患者一线选用“瑞波西利+依西美坦”方案,符合国内外指南(如2025 CBCS指南)推荐的HR+/HER2-晚期乳腺癌一线标准治疗策略[1]。该类方案的疗效已在多项大型III期临床研究(如MONALEESA系列、PALOMA-2, MONARCH-3等)中得到充分验证,通常能带来超过2年的中位无进展生存期(PFS)。然而,本例患者的PFS仅为6个月,提示其肿瘤存在原发性耐药,其内在生物学机制是决策后续治疗的关键。
NGS检测发现的PIK3CA p.H1047R高丰度突变,是解释这一现象的核心。PI3K/AKT/mTOR信号通路是独立于细胞周期(Cyclin D-CDK4/6-Rb)通路的另一条关键促癌通路 。PIK3CA基因的激活型突变(H1047R为最常见的热点突变之一)可导致PI3Kα激酶亚基的持续活化,从而绕过上游生长因子受体的调控,持续驱动下游AKT/mTOR信号,促进肿瘤细胞增殖与存活 。当CDK4/6抑制剂有效阻断细胞周期通路时,这条被持续激活的PI3K通路便构成了强大的“旁路逃逸机制”,导致治疗失效。一项针对CDK4/6抑制剂联合内分泌治疗的大型荟萃分析数据显示,携带PIK3CA突变的患者,其中位总生存期(mOS)缩短了超过10个月,这明确了PIK3CA突变是该疗法的不良预后因素[2]。因此,该患者的短暂PFS,是其肿瘤内在基因型(PIK3CA突变)在外在临床表型上的直接体现。
面对一线治疗的失败,二线决策充分体现了以分子分型为基础的精准治疗, 其成功建立在坚实的理论依据、高级别的循证支持和规范的安全性管理之上:
理论依据:HR+乳腺癌的耐药网络涉及ER、CDK4/6和PI3K三大核心通路,它们之间存在复杂的信号串扰,互为耐药机制 。临床前证据显示,同时阻断PI3K和CDK4/6通路可能延缓或阻止内分泌治疗耐药的发生 。因此,在已确认存在PI3K通路异常激活的情况下,采用伊那利塞(PI3Kαi)+ 哌柏西利(CDK4/6i)+ 氟维司群(SERD)的三联方案,旨在同时对这三条关键通路进行垂直、深度阻断,理论上能最大程度地克服耐药。
循证支持:该方案的决策源于高级别的循证医学证据——全球III期临床研究INAVO120 。该研究入组了HR+/HER2-、PIK3CA突变晚期乳腺癌中预后差、亟待更优一线治疗的人群,即:未进行针对局晚/转移性疾病的系统治疗,辅助内分泌治疗期间或治疗完成后12月内复发的患者[3]。结果显示,与“安慰剂+哌柏西利+氟维司群”的标准治疗相比,伊那利塞三联方案将中位PFS从7.3个月显著延长至17.2个月,实现了超双倍的临床获益 。疾病进展或死亡风险大幅降低58%(HR=0.42) 。值得注意的是,该研究中,伊那利塞在亚洲人群(HR=0.40)、原发内分泌耐药人群(HR=0.39)等多个高危亚组中均展现出一致甚至更优的获益 。本例患者的临床特征与INAVO120研究的获益人群高度吻合,其治疗一个月后即获得PR的快速响应,正是该研究结果在真实世界临床实践中的有力印证。
曾银朵教授:在临床实践中,对治疗出现相关不良反应的有效管理是确保患者从创新疗法中最大化获益的关键。PI3K通路是胰岛素信号传导的重要介质,其抑制剂会阻断AKT信号,进而影响葡萄糖转运蛋白GLUT4向细胞膜的定位,减少葡萄糖摄取,因此,抑制PI3Kα带来的高血糖是一种机制相关的“中靶效应”[4]。有效管理高血糖是确保患者能够从治疗中持续获益的前提。
诊疗中的血糖管理堪称典范,严格遵循了临床研究中验证的规范化流程:治疗前评估空腹血糖及糖化血红蛋白,治疗启动后进行规律的血糖监测(如第一周每3天检测,后续每周或每两周) 。在发现血糖升高后(如空腹血糖≥140 mg/dL),立即启动二甲双胍作为首选药物进行干预,为了更好的控制血糖在两周后逐步增加二甲双胍剂量从500mg qd到500mg bid,减少胃肠道不适。患者的血糖在二甲双胍的调整下得到了良好控制,并未对治疗造成影响。二甲双胍是治疗PI3K通路相关高血糖的首选药物,它可以通过改善外周组织对胰岛素的敏感性来有效降低血糖,且不影响PI3K抑制剂的抗肿瘤活性。
值得强调的是,伊那利塞的安全性特征具有高度的可预测性。INAVO120研究数据显示,其关键不良事件,如高血糖(中位发生时间7天)、口腔炎(13天)等,均集中在治疗的第一个月内,且大多数(约80%)为可逆性。这提示我们,通过在治疗初期进行重点监测和前瞻性干预,可以有效控制大部分不良反应,平稳度过AE高风险期。
新一代PI3Kα抑制剂伊那利塞在安全性上相较于前代药物已实现显著优化。INAVO120研究中,伊那利塞组≥3级高血糖的发生率仅为6.8%。且更优的耐受性直接转化为了更低的治疗中断率,因不良反应导致治疗中止的患者比例仅为6.8%。此外,INAVO120研究的生活质量(HRQoL)数据显示,联合伊那利塞治疗并未对患者的身体功能、角色功能及整体生活质量造成额外的不利影响,患者的生活质量始终维持在基线水平。本例患者的成功管理,再次证实了该方案在临床实践中的安全性与可行性。
总体而言,全程诊疗清晰地展示了:对于初诊即为晚期、高肿瘤负荷且携带PIK3CA突变的HR+/HER2-乳腺癌患者,应警惕其对一线标准治疗快速耐药的风险。NGS基因检测在制定全程管理策略中具有不可或缺的价值。新一代高选择性PI3Kα抑制剂伊那利塞为核心的三联靶向方案,能够有效克服PIK3CA驱动的耐药,为患者带来快速、深度的缓解,且安全性可控,为这类棘手患者的后续治疗树立了新的标杆。
案例整理专家
中山大学孙逸仙纪念医院/乳腺肿瘤医院 外科主治医师
加拿大多伦多大学联合培养外科学博士
中山大学孙逸仙纪念医院完成博士后
广东省健康科普促进会甲状腺乳腺分会常委
广东省医院协会乳腺科管理专业委员会委员
广东省临床医学学会乳腺癌专业委员会委员
广东省呼吸与健康学会临床研究专业委员会委员
《中国普外基础与临床》杂志青年编委
主持国家级及省级基金多项,发表相关学术论文20余篇,其中第一作者论文10余篇
1.中国抗癌协会乳腺癌专业委员会. 中国抗癌协会乳腺癌诊治指南与规范(2025版).
2.Fillbrunn M, et al. PlK3CA mutation status, progression andsurvival in advanced HR+/HER2- breastcancer: a meta-analysis of publishedclinical trials BMC Cancer.2022;22(1):1002.
3.Turner NC, Oliveira M, Howell SJ, et al.Inavolisib-Based Therapy inPIK3CA-Mutated Advanced Breast Cancer. N Engl J Med. 2024; 391:1584-1596.
4.Tankova T et al,Cancers 2022;14:1598
本文仅为个人观点分享,具体诊断方案需结合实际情况判断;本文仅作为对医疗专业人士的个例分享,具体诊断方案需由医疗专业人士结合实际情况判断。
排版编辑:肿瘤资讯-Delia











 苏公网安备32059002004080号
苏公网安备32059002004080号


