对于晚期驱动基因阴性非小细胞肺癌(NSCLC),免疫治疗联合化疗已成为一线治疗标准。另外,根据现有循证证据,对于携带部分基因突变的晚期NSCLC,在靶向治疗失败后同样可以采用免疫联合化疗进行二线治疗。广州医科大学附属第一医院沈盼晓医生分享了一例MET扩增NSCLC患者经靶向治疗失败后接受舒格利单抗联合化疗获得持续缓解的病例,【肿瘤资讯】整理了其中内容,并邀请广州医科大学附属第一医院秦茵茵教授进行点评,以飨读者。
广州医科大学附属第一医院 广州呼吸健康研究院
呼吸与危重症医学科主治医生博士研究生
广东省呼吸与健康学会呼吸肿瘤慢病化管理专业委员会秘书
广东省胸部疾病学会呼吸肿瘤全程管理专业委员会秘书
广东省呼吸与健康学会肿瘤专委会委员
广东省胸部疾病学会健康管理专委会委员
广东省胸部疾病学会胸膜纵隔疾病专业委员会委员
广东省胸部肿瘤防治研究会肺癌多学科治疗专委
参与编写书籍:《喘息样发作疾病鉴别诊断》、《嗜酸性粒细胞相关疾病鉴别诊断》、《胸膜与纵隔疑难少见病例精解》
病例信息
患者男,61岁。
现病史
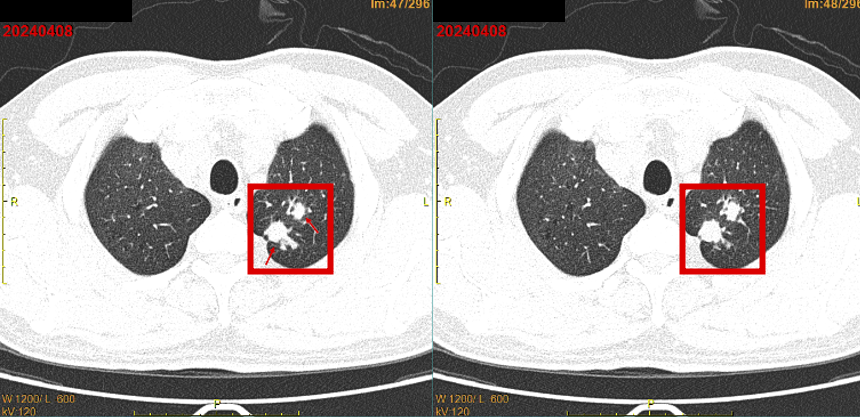
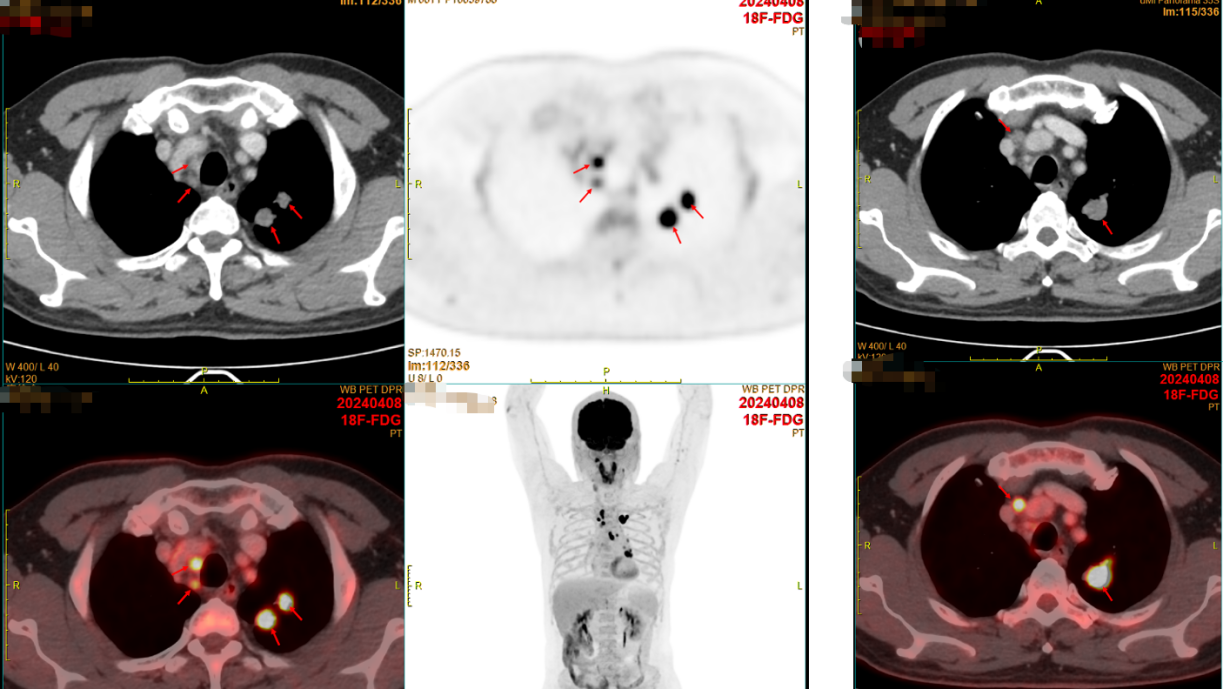
患者2024年2月感冒后出现咽痛、咳嗽、咳黄色粘痰,偶有痰中带血(7-8次/天,晨起明显),伴胸闷、活动后稍气促,偶有头晕、盗汗,未重视。2024年3月因咯血增多于当地医院就诊,胸CT提示肺占位。2024-04-08我院全身PET/CT示:
1.左肺上叶尖后段高代谢实性结节(2个结节融合),考虑周围型肺癌;
2.左侧肺门、纵隔(2R、3A、4L、6组)多发淋巴结转移;
3.左侧肾上腺结合部增粗,代谢增高,考虑转移瘤。
4.自患病以来,神清,精神可,胃纳、睡眠可,二便正常,近期体重减轻约2kg。
其余信息
既往史:平素体健,无传染病史、食物或药物过敏史。
手术史:2019年因左手骨折行手术治疗,恢复可。
个人史:无外地/疫区居住史。
吸烟史:40年,20支/日,未戒烟。
婚育史:已婚已育。
家族史:无肿瘤、传染性、遗传性疾病史。
查体
体温36℃,脉搏71次/分,呼吸20次/分,血压116/65mmHg,体重64kg,身高162cm。
头颅正常,颈软无抵抗;心界不大,律齐,未闻及杂音,无心包摩擦音;双肺呼吸音清、对称,未闻及干湿啰音及胸膜摩擦音;肝脾未触及肿大,肝区无叩击痛;腹软,无压痛,无反跳痛,无包块,移动性浊音呈阴性,肠鸣音正常;四肢关节活动可,无红肿,无杵状指(趾) ,双下肢无水肿。
辅助检查
肺肿瘤六项(2024-04-06):糖类抗原153 28.8U/mL↑,细胞角蛋白19片段4.98ng/mL↑,CEA 4.38ng/mL(正常)。
血常规、肝肾功能、凝血功能、大小便常规、诱导痰、痰涂片+培养:未见异常。
18F-FDG全身显像:左肺上叶尖后段高代谢实性结节(较大1.9×1.8×2.4cm),考虑周围型肺癌;左侧肺门、纵隔多发淋巴结转移;左侧肾上腺结合部稍粗,代谢增高,考虑转移瘤。
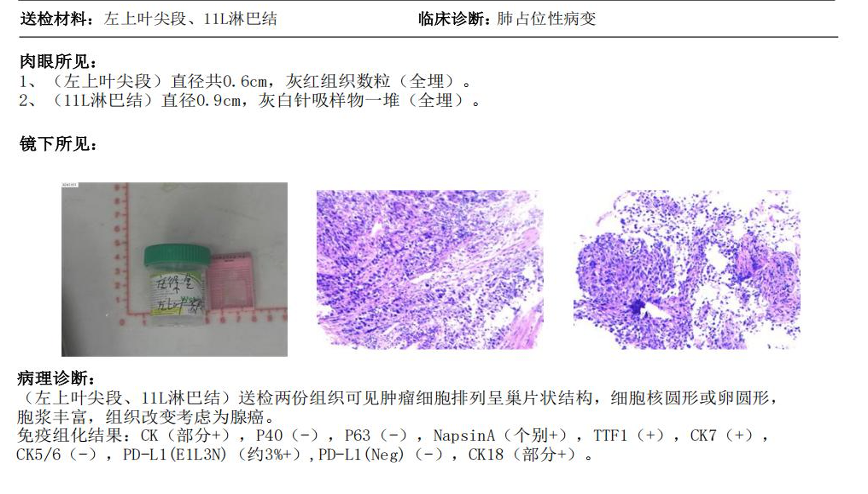
病理活检(2024-04-09):腺癌,PD-L1(E1L3N)约3%+。
基因检测(2024-04-22):MET扩增(3.8%)。
肺功能(2024-04-09):FEV1/FVC 68.49%,FEV1 77.56%,提示轻度阻塞性肺通气功能障碍。
睡眠监测(2024-04-10):轻度阻塞性睡眠呼吸暂停低通气综合征并轻度夜间低氧血症。
临床诊断
左肺腺癌(T1cN2M1b 肾上腺 IVA期),ECOG PS 1分,MET扩增,PD-L1(3%+),慢性阻塞性肺疾病,轻度阻塞性睡眠呼吸暂停低通气综合征并夜间低氧血症,鼻窦炎,双肺肺气肿并多发肺大泡,肝囊肿。
治疗方案
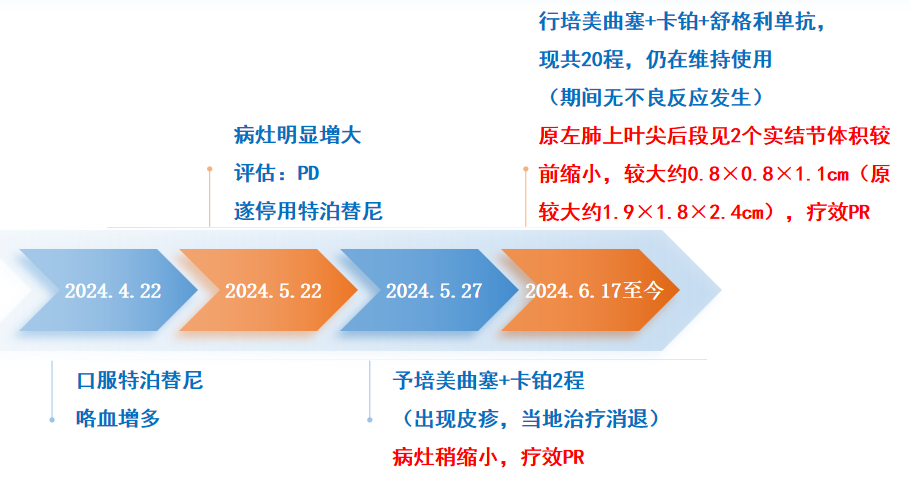
1. 2024.4.22:口服特泊替尼450mg(2片)每日一次。
2.2024.5.22复查:咯血增多,胸部CT示病灶明显增大,评估疾病PD,停用特泊替尼。
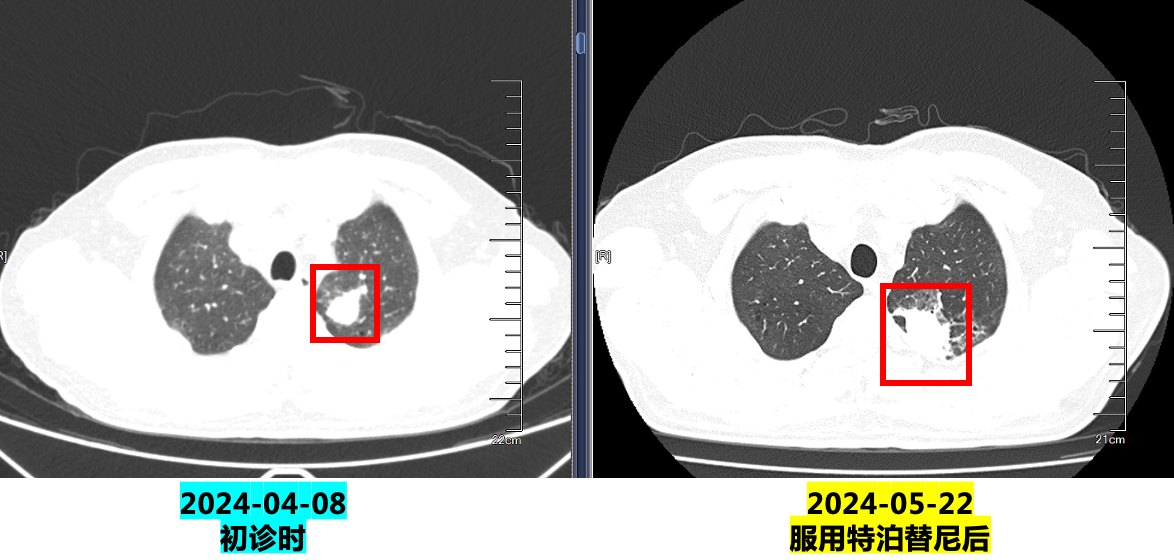
3. 2024.5.27:予培美曲塞+卡铂化疗,出现皮疹(口服氯雷他定片后4-5天消退)。
4. 2024.6.17至今:行培美曲塞二钠0.8g + 卡铂400mg + 舒格利单抗1200mg(共20程,维持治疗中,无不良反应)。
临床随访影像对比
2024-04-08(初诊)vs 2025-03-07(复查)PET/CT:
左肺上叶尖后段实性结节体积缩小(较大约0.8×0.8×1.1cm vs 原1.9×1.8×2.4cm);
左肺门、纵隔多发淋巴结转移瘤体积缩小;
左侧肾上腺结合部增粗程度减轻。
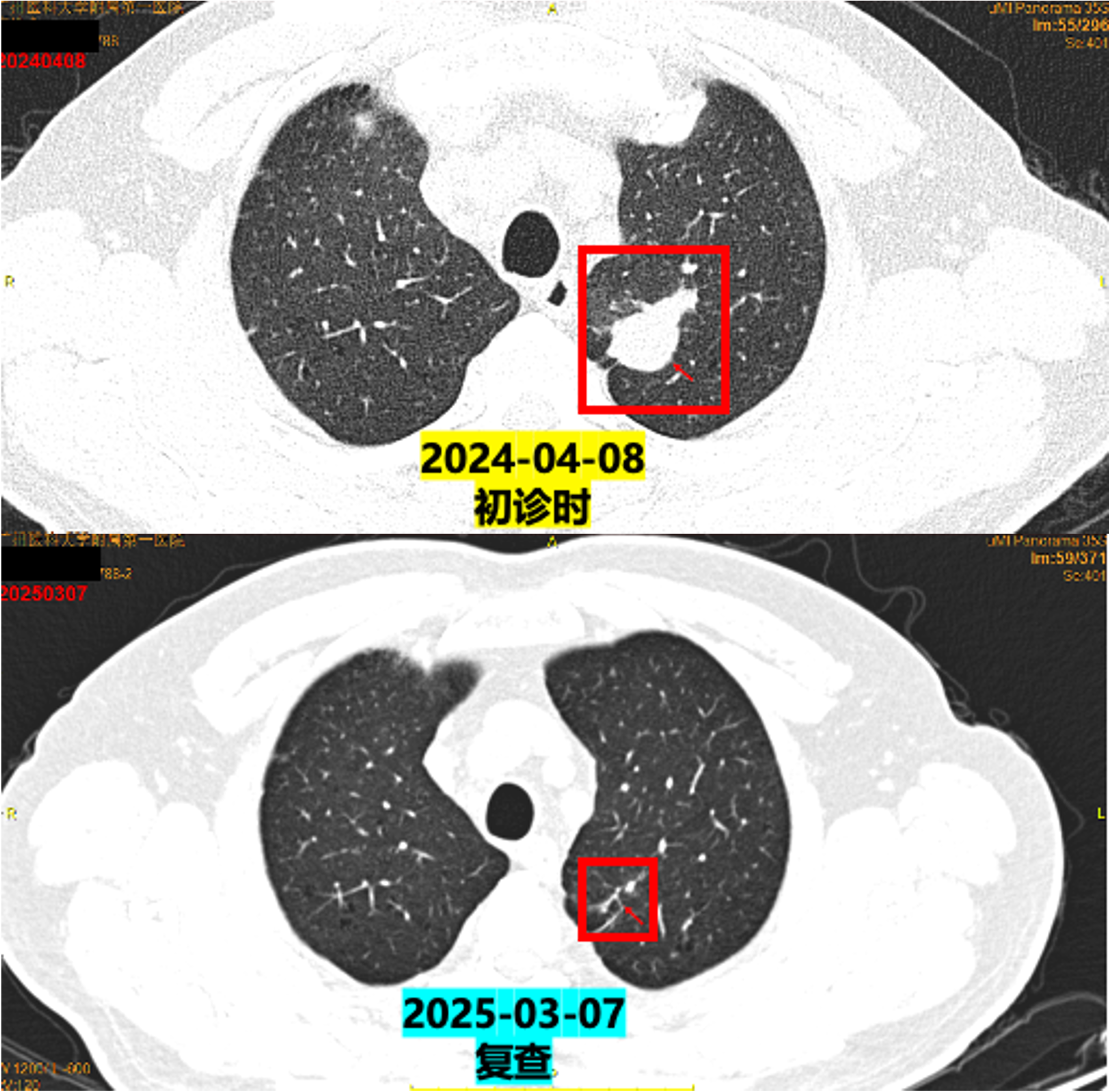
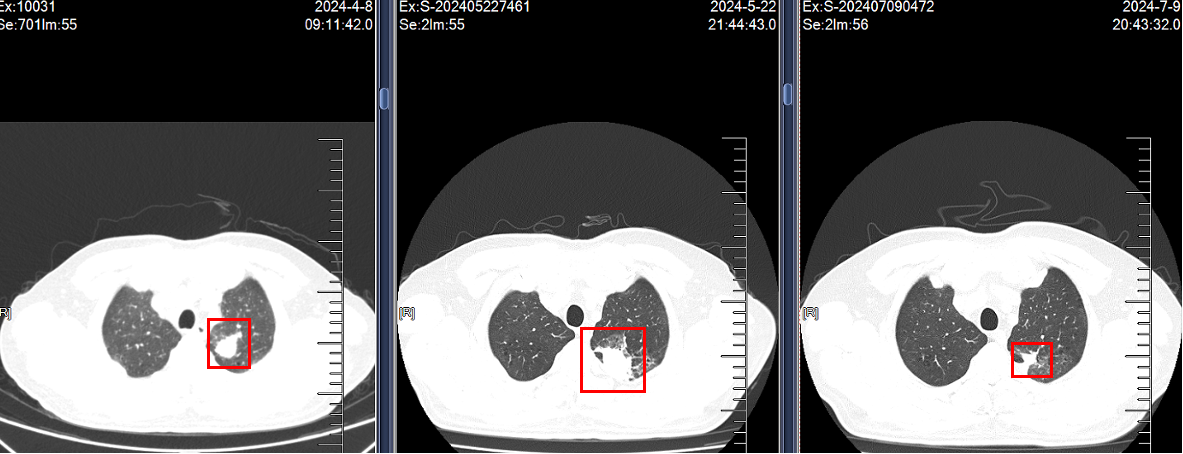
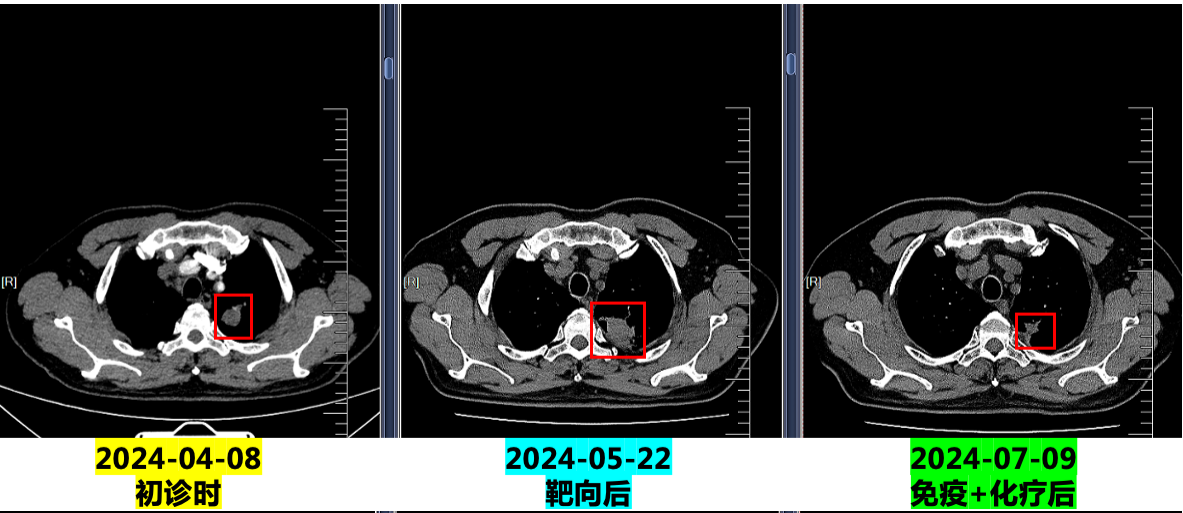
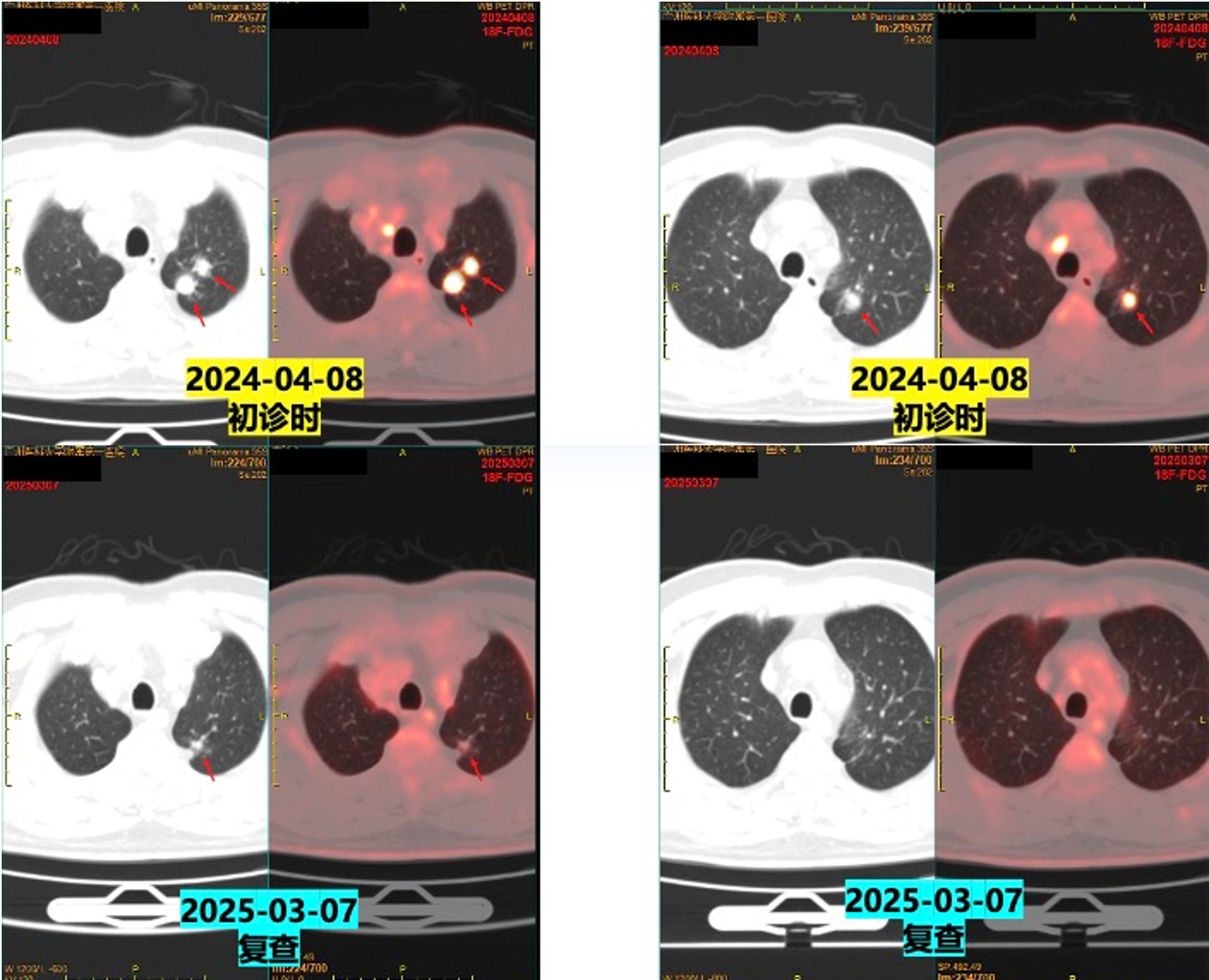
在2025年3月7日复查petCT后,建议患者行原发病灶或者肺门、纵隔淋巴结的放疗,但是患者家属自觉目前治疗疗效理想,患者体能状态良好,暂不愿意行放疗。
疗效评估:PR(部分缓解)。
广州医科大学附属第一医院广州呼吸健康研究院病区主任
主任医师医学博士 博导
呼吸疾病全国重点实验室PI广州国家实验室PI
全国高等学校临床医学规划教材《内科学》第10版副主编
国家卫健委“十三五”规划 临床医学第二轮器官-系统整合教材《呼吸系统与疾病》副主编
广东省第一批杰出青年医学人才
南粤优秀教师
广东医院最强科室之实力中青年医生
广州市高层次卫生重点人才
国家临床医学研究中心-中国呼吸肿瘤协作组青年委员会常委
广东省医学会肺部肿瘤学分会常务委员
广东省医师协会呼吸科医师分会间质病与肺癌专业组副组长
广东省胸部疾病学会呼吸肿瘤全程管理专业委员会主委
广东省呼吸与健康学会呼吸肿瘤慢病化管理专业委员会主委
广东省女医师协会肺癌专业委员会常务委员
师从我国著名呼吸内科专家钟南山院士, 擅长肺部肿瘤并COPD等“重症肺癌” 及各种疑难少见呼吸系统疾病的诊治
主持多项国家自然科学基金项目、省市科研及教学项目
病例点评
对于携带驱动基因突变的晚期非小细胞肺癌(NSCLC),靶向治疗无疑是首选。然而,无论是原发性耐药还是继发性耐药,都是临床常常面对的严峻挑战。当TKI治疗失败后,后续治疗方案的选择需要基于耐药机制、患者基因背景和身体状况进行综合考量,其策略主要包括针对耐药机制靶向治疗、化疗、抗血管生成治疗以及联合治疗等,其中化免联合治疗是主要策略之一。
尽管免疫治疗已成为无驱动基因NSCLC的标准治疗方案,也是驱动基因阳性NSCLC靶向治疗耐药后的可选方案,但由于MET变异在NSCLC中的罕见性,MET变异晚期NSCLC接受免疫治疗的疗效和安全性数据有限。为此,一项研究分析了免疫检查点抑制剂(ICI)单药治疗和联合治疗在MET变异NSCLC中的疗效和安全性,相关结果于2024年4月发表于Clin Transl Oncol杂志。结果显示1,在MET变异晚期NSCLC患者中,ICI联合化疗的疗效优于ICI单药治疗,可带来5个月左右的额外PFS获益。由此可见,免疫治疗是MET变异NSCLC患者潜在可选的治疗方案。
本例患者为MET扩增晚期肺腺癌,一线使用MET抑制剂特泊替尼后疾病快速进展,是典型的原发耐药,预后较差。更换为舒格利单抗联合培美曲塞和卡铂的方案后,患者获得了长达1年以上的持续部分缓解(PR),这充分展示了免疫联合化疗在这一挑战性人群中的价值。
舒格利单抗是一款全人源抗PD-L1单克隆抗体,GEMSTONE-302是一项多中心、随机、双盲III期临床试验,旨在探索舒格利单抗联合铂类化疗对比安慰剂联合化疗一线治疗转移性NSCLC的疗效和安全性。研究结果显示2, 在全人群中,舒格利单抗组和安慰剂组的中位无进展生存期(PFS)分别为 9.0个月 vs 4.9个月(HR 0.48),疾病进展或死亡风险降低52%。 在总生存期(OS)方面,舒格利单抗组和安慰剂组的中位OS分别为25.2个月 vs 16.9个月(HR 0.68),死亡风险降低32%。此外,舒格利单抗组的4年OS率达 32.1%,显著优于安慰剂组的17.3%。 安全性方面,舒格利单抗组的≥3级免疫相关不良事件(irAE)发生率仅 3.1%,安全性良好,可为合并肺部疾病的患者提供更优选择3。 本病例中,患者患有慢性阻塞性肺疾病,而舒格利单抗治疗期间无不良反应发生,体现了舒格利单抗良好的安全性以及其在合并呼吸系统疾病患者中的良好适用性。
GEMSTONE-302亚组分析结果显示2,舒格利单抗在不同PD-L1表达亚组人群中均有显著生存获益,在PD-L1低表达(1%<TPS ≤ 49%)人群中,舒格利单抗组中位OS为24.8个月,4年OS率达29.3%,近3成患者活过4年。 本病例中,患者PD-L1低表达,同样从舒格利单抗联合化疗治疗中明显获益,并且持续缓解近1年,体现了舒格利单抗不受限于PD-L1表达水平的良好疗效。
综上,GEMSTONE-302研究的长期生存数据为舒格利单抗一线应用提供了高级别循证支持,基于这些结果,2025CSCO非小细胞肺癌诊疗指南将舒格利单抗联合化疗列为IV期无驱动基因非鳞NSCLC一线治疗的I级推荐。本例IV期MET扩增肺腺癌患者在靶向治疗失败后经舒格利单抗联合化疗实现持续PR,印证了其在特殊驱动基因(MET扩增)、PD-L1低表达及合并COPD人群中的显著疗效与安全性优势。
1. Wang Y, Wei J, Xu M, et al. Efficacy and safety analysis of immunotherapy in non-small cell lung cancer patients with MET alterations. Clin Transl Oncol. 2024;26(10):2503-2512. doi:10.1007/s12094-024-03455-y
2. Zhou C, Wang Z, Sun M, et al. 1318P Four-year outcomes from GEMSTONE-302 study: First-line sugemalimab plus platinum-based chemotherapy in metastatic non-small cell lung cancer (NSCLC). Ann Oncol. 2024;35:S839. doi:10.1016/j.annonc.2024.08.1374
3. Zhou C, Wang Z, Sun M, et al. Interim survival analysis of the randomized phase III GEMSTONE-302 trial: sugemalimab or placebo plus chemotherapy as first-line treatment for metastatic NSCLC. Nat Cancer. 2023;4(6):860-871. doi:10.1038/s43018-023-00578-z
排版编辑:肿瘤资讯-展思懿











 苏公网安备32059002004080号
苏公网安备32059002004080号


