间变性淋巴瘤激酶(ALK)基因融合是非小细胞肺癌(NSCLC)中一个重要的治疗靶点。近年来,针对ALK的靶向治疗在晚期患者中取得了巨大成功,并逐渐向早期、可手术的NSCLC领域拓展。
2025年ASCO年会上,妙佑医疗国际(Mayo Clinic)的Kaushal Parikh教授总结和探讨了ALK阳性早期NSCLC患者围手术期的管理策略:在对早期可切除NSCLC患者使用新辅助或围手术期免疫治疗前,进行ALK融合检测是必要的;基于ALINA研究的突破性成果,阿来替尼已成为II期(≥4cm)至IIIA期ALK阳性NSCLC患者术后辅助治疗的标准方案;同时,ALK抑制剂的新辅助治疗研究也展现出令人鼓舞的早期结果,预示着该领域未来的发展方向。【肿瘤资讯】整理了其中精华内容,以飨读者。
ALK融合及其在肺癌中的生物学特性
患病率与人群:ALK融合存在于约1%-4%的早期NSCLC患者中。这类患者几乎均为腺癌 ,且通常为年轻、无吸烟史或轻度吸烟史的女性。
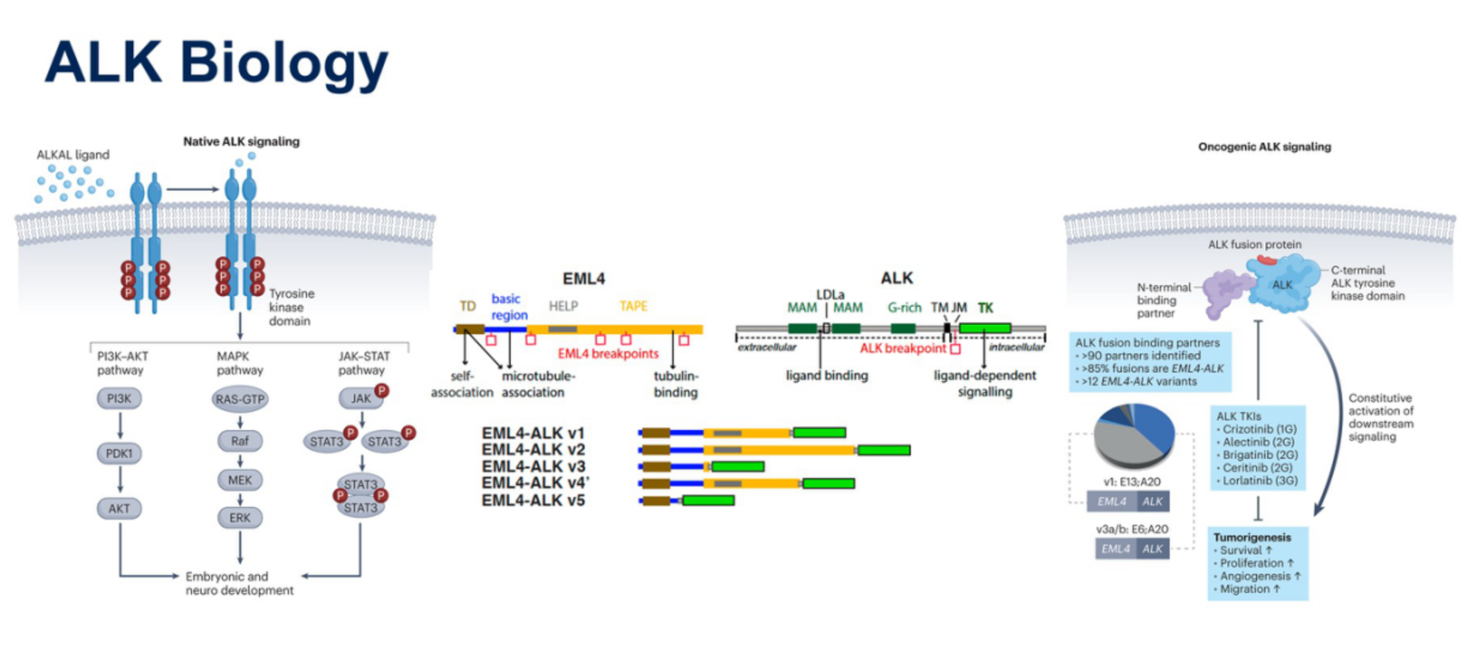
生物学机制:ALK基因编码一种受体酪氨酸激酶,其天然信号通路在胚胎和神经发育中至关重要。在肺癌中,ALK基因常与其它基因(最常见的是EML4)发生融合,形成异常的融合蛋白。这种融合蛋白会持续激活下游的PI3K-AKT、MAPK和JAK-STAT等信号通路,从而驱动肿瘤的发生和发展。EML4-ALK存在多种变体,其中变体1和变体3最为常见,各占约30%。
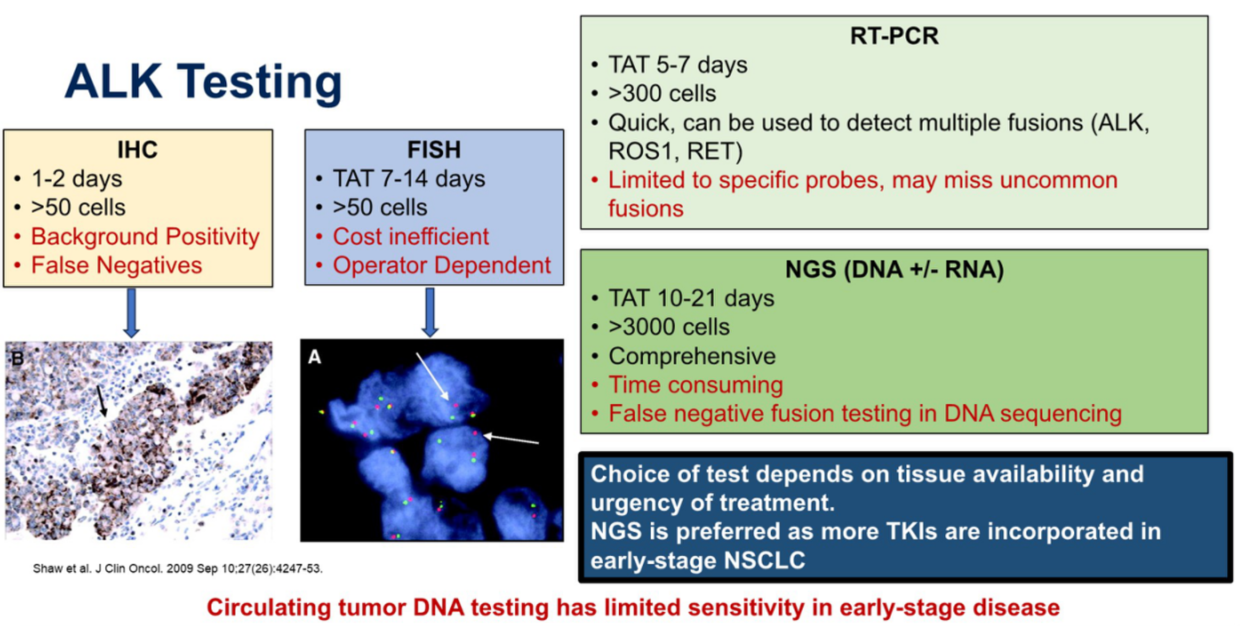
检测方法:
免疫组化 (IHC): 速度快,操作简便,但可能存在背景着色和假阴性的问题。
荧光原位杂交 (FISH): 曾被视为金标准,但成本高、依赖操作者经验,且周转时间较长(通常超过一周)。
逆转录PCR (RT-PCR):周转时间较短,可同时检测多种融合基因(如ALK、ROS1、 RET),但其局限性在于只能检测已知的特异性探针,可能漏掉不常见的融合类型。
二代测序 (NGS):是目前最全面的检测方法,但需要更多组织样本,检测周期长,并且在仅进行DNA测序时,偶尔会导致假阴性的融合检测结果。
最佳检测方法的选择取决于组织的可用性和治疗的紧迫性。随着更多靶向药进入早期治疗领域,NGS将成为更受青睐的选择。值得注意的是,循环肿瘤DNA(ctDNA)检测在早期疾病中的灵敏度有限,阴性结果需由组织检测来确认。
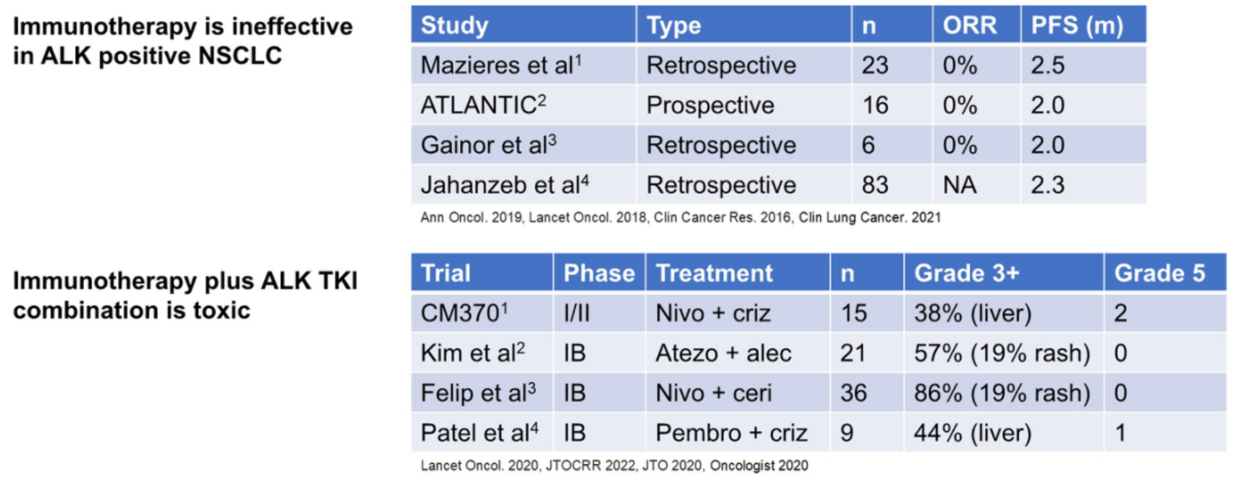
ALK融合阳性NSCLC免疫治疗可行吗?
尽管新辅助免疫联合化疗改善了早期NSCLC患者的生存,但免疫治疗在ALK阳性的晚期NSCLC中已被证明是无效的。回顾性和前瞻性研究均显示,ALK阳性患者接受免疫治疗的缓解率极低,无进展生存期(PFS)很短。此外,免疫治疗与ALK-TKI的联合使用与显著的毒性相关,特别是3级及以上的肝毒性,甚至导致5级事件。
在辅助治疗的KEYNOTE-091和IMpower010研究中,虽然纳入了ALK阳性患者,但KEYNOTE-091研究并没有提供具体的ALK相关结果,而IMpower010研究中ALK融合阳性患者的总生存期(OS)风险比(HR)为1.87。对于ALK阳性的患者,即使PD-L1高表达,也不应考虑辅助免疫治疗。
因此,在对早期可切除NSCLC患者实施任何包含免疫治疗的围手术期方案前,必须进行ALK融合检测。
辅助治疗——ALINA研究的里程碑意义
ALK抑制剂在晚期NSCLC中已证明了其疗效,这为在早期疾病中的探索提供了理论依据。
早期的回顾性研究显示,与化疗相比,克唑替尼显著改善了完全切除的IB-IIIA期ALK阳性NSCLC患者的无病生存期(DFS)和OS,但这需要前瞻性研究来证实。
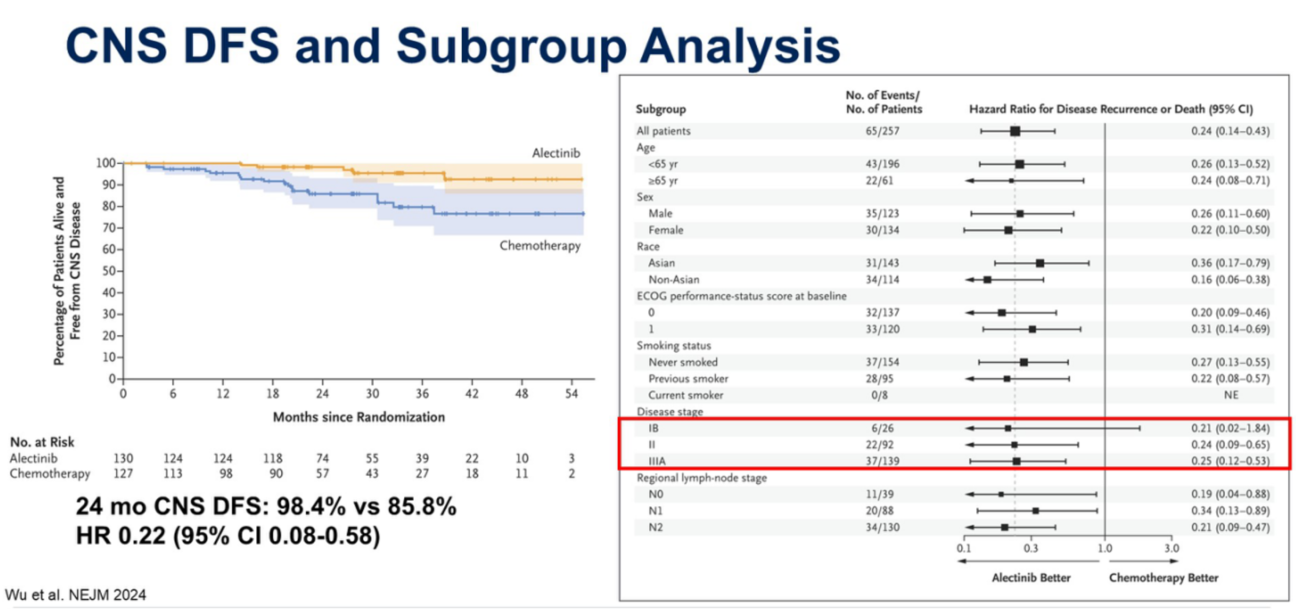
ALINA研究这项大型III期临床试验为辅助治疗设立了新的标准。纳入了257例已完全切除的IB期(≥4cm)至IIIA期ALK阳性NSCLC患者。患者被1:1随机分配,分别接受为期2年的阿来替尼口服治疗或4个周期的铂类双药化疗。研究达到了其主要终点,在II-IIIA期患者中,阿来替尼组的DFS尚未达到,而化疗组为44.4个月,HR为0.24,显示出巨大的统计学差异(p<0.001) 。在总意向治疗人群中,结果同样显著(HR 0.24)。
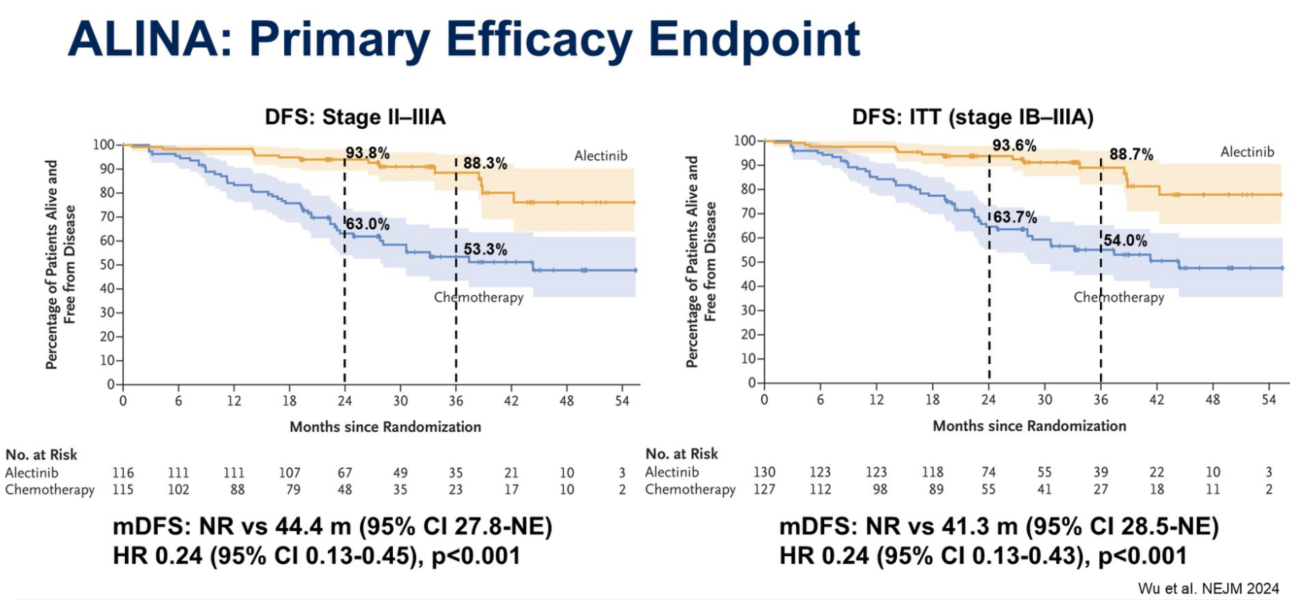
此外, 阿来替尼具有良好的血脑屏障穿透能力,其24个月的CNS DFS率高达98.4%,化疗组为85.8%(HR 0.22)。
亚组分析显示,无论疾病分期如何,所有亚组患者均能从阿来替尼治疗中获益。
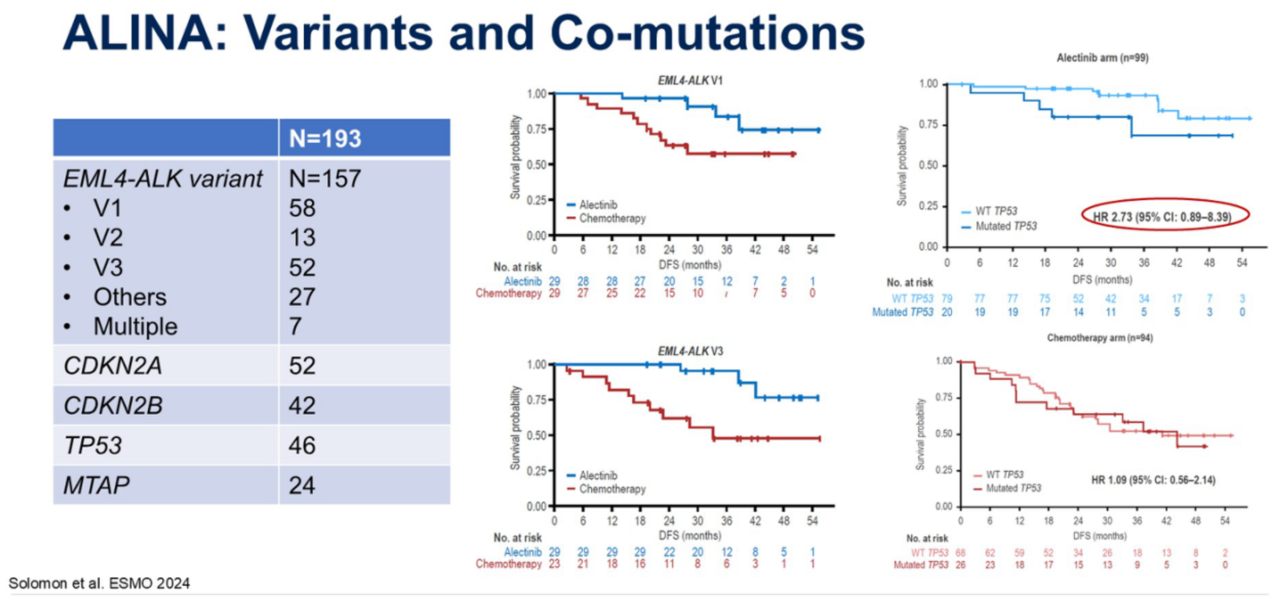
阿来替尼对EML4-ALK变体1和变体3均显示出显著的DFS改善。然而,数据显示,伴有TP53突变的患者在使用阿来替尼时,有预后较差的趋势,而化疗组则不受TP53状态影响。
ALINA研究的启示与待回答问题:
阿来替尼辅助治疗2年,已成为可切除的ALK融合阳性NSCLC(IB期-IIIA期,AJCC v.7,肿瘤≥4cm或淋巴结阳性)的标准治疗方案,且无需联合辅助化疗。
待回答问题:最佳治疗时长是多久?第三代TKI洛拉替尼甚至第四代药物的角色是什么?是否需要联合化疗?对于TP53共突变的患者应如何优化策略?ctDNA在监测和指导治疗决策中的作用是什么?
新辅助治疗——前景广阔的新兴领域
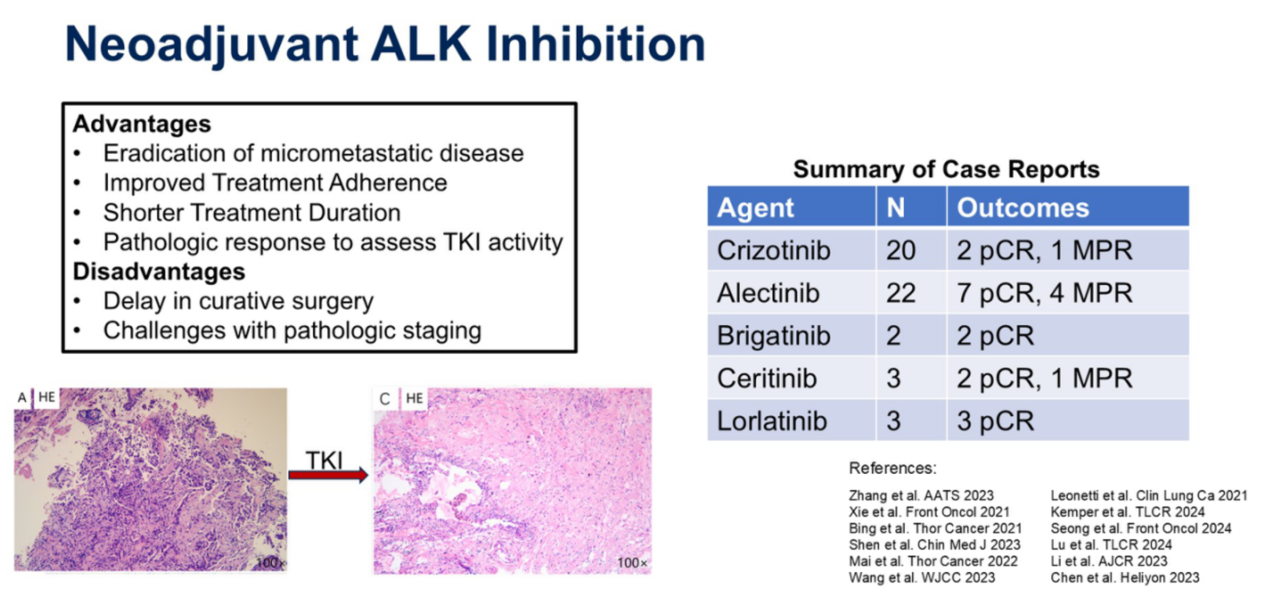
新辅助治疗具有根除微小转移灶、提高治疗依从性、缩短治疗持续时间以及评估药物活性等潜在优势,但有时会导致治愈性手术的延迟,并可能在病理分期方面带来挑战。
在针对ALK靶点的新辅助治疗领域,已有多项研究和病例报告展现了其应用潜力。既往的病例报告显示,第一、二、三代ALK-TKI在新辅助治疗中均表现出令人鼓舞的疗效,在实现主要病理缓解(MPR)或病理完全缓解(pCR)方面取得了积极成果。
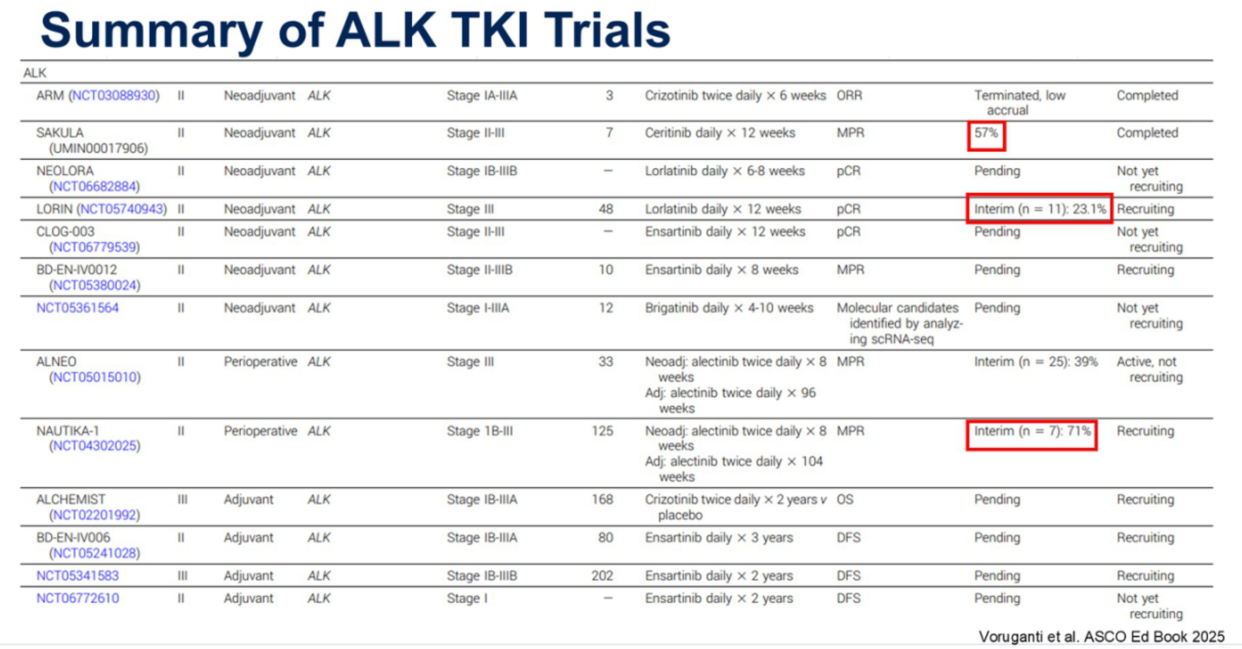
SAKULA研究是一项关于塞瑞替尼新辅助治疗的研究,取得了57%的MPR率。目前,NAUTIKA-1和LORIN等研究正在招募患者中,将为该领域提供更多数据。
 由Marcelo Tiseo博士在近期会议上公布的ALNEO研究是一项II期试验,专门针对可切除的、局部晚期的III期ALK阳性NSCLC患者。患者先接受2个周期的阿来替尼新辅助治疗,然后进行手术,术后再继续2年的阿来替尼辅助治疗。研究的主要终点是BICR评估的MPR。结果显示,MPR率达到了42%,其中12%的患者实现了pCR。这一结果比既往EGFR抑制剂在新辅助治疗中的数据更为鼓舞人心。
由Marcelo Tiseo博士在近期会议上公布的ALNEO研究是一项II期试验,专门针对可切除的、局部晚期的III期ALK阳性NSCLC患者。患者先接受2个周期的阿来替尼新辅助治疗,然后进行手术,术后再继续2年的阿来替尼辅助治疗。研究的主要终点是BICR评估的MPR。结果显示,MPR率达到了42%,其中12%的患者实现了pCR。这一结果比既往EGFR抑制剂在新辅助治疗中的数据更为鼓舞人心。
小结
1. 检测先行:在对早期可切除NSCLC患者使用围手术期免疫治疗前,进行ALK融合检测是强制性的,以避免无效甚至有害的治疗。
2. 辅助标准:对于已切除的II期(≥4cm)至IIIA期ALK阳性NSCLC,阿来替尼辅助治疗是目前的标准治疗方案。
3. 新辅助潜力:ALK抑制剂的新辅助治疗展现出巨大的应用前景,早期研究结果喜人,未来有望改变当前的治疗模式。
未来的研究将继续探索最佳治疗时长、新一代TKI的应用、联合治疗策略以及生物标志物(如TP53和ctDNA)在个体化治疗中的价值。
排版编辑:肿瘤资讯-TY












 苏公网安备32059002004080号
苏公网安备32059002004080号


