病史摘要:患者,女性,47岁。患者2022年9月因发现“左乳肿块进行性增大1月余”入院。
症状体征:患者2022年9月因发现“左乳肿块进行性增大1月余”至宁波市第一人民医院就诊,乳腺钼靶示:左乳外上象限局部致密团块,BI-RAD 4a级。2022年10月10日行腋窝来不及活检术:淋巴结内见腺癌组织浸润,润性乳头状癌,WHO Ⅲ级。免疫组化:浸润性癌表达ER(-),PR(-),Ki67(50%+),Her2(3+)。后患者至我院甲乳外科就诊,排除手术禁忌后,2022年10月19日行左乳癌的改良根治术,术后病理:左乳浸润性癌,部分为浸润性乳头状癌,同侧腋窝淋巴结5/15见癌转移,锁骨下淋巴结0/2未见癌转移。免疫组化:浸润性癌表达ER(-),PR(2%,+),Ki67(60%+),Her2(3+),P120(膜阳性)。2022年11月起予以AC×4—T×4(吡柔比星+环磷酰胺,多西他赛),2023年6月行乳腺癌术后辅助放疗(外院),2023年7月起予以曲妥珠单抗+帕妥珠单抗靶向维持治疗至今,化疗期间常规使用硫培非格司亭6mg预防性升白治疗,整个治疗过程未发生骨髓抑制。既往体健,家族史:父亲因“胃癌”去世,母亲因“宫颈癌”去世,哥哥因“鼻咽癌”去世。
诊断方法:2022年10月19日行左乳癌的改良根治术,术后病理:左乳浸润性癌,部分为浸润性乳头状癌,大小5cm×4cm,脉管内可见癌栓。基底切缘未见癌累及。同侧腋窝淋巴结5/15见癌转移,锁骨下淋巴结0/2未见癌转移。免疫组化:浸润性癌表达ER(-),PR(2%,+),Ki67(60%+),Her2(3+),P120(膜阳性)。
治疗方法:化疗期间使用硫培非格司亭6mg预防性升白治疗,降低患者骨髓抑制风险。
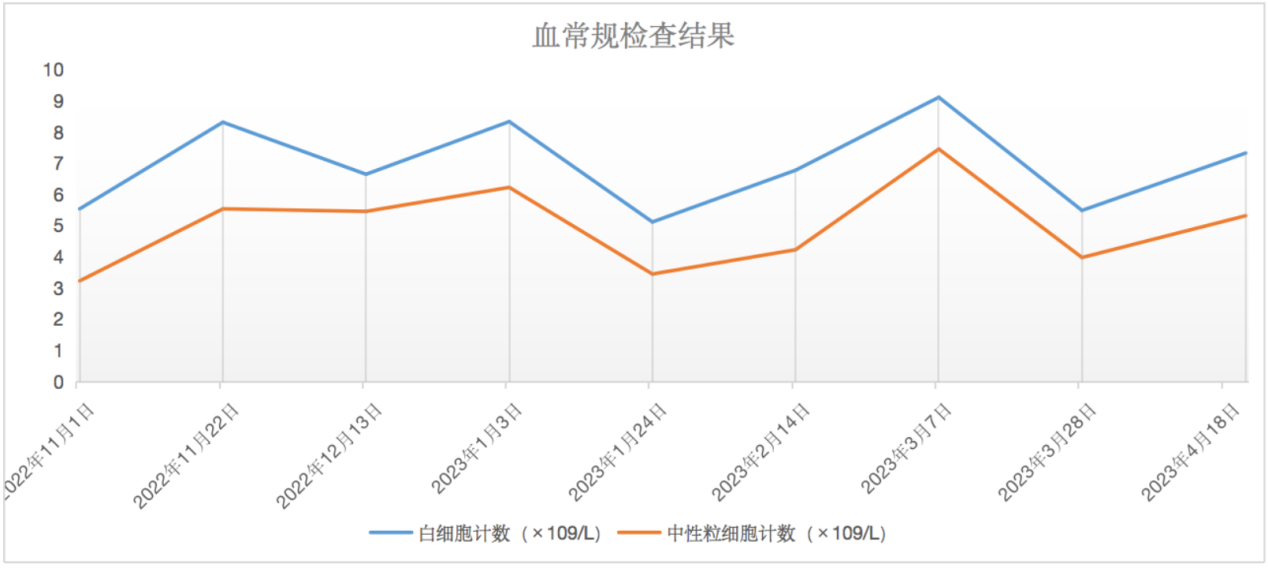
临床转归:患者化疗、放疗及靶向维持治疗过程顺利,第2周期后监测血常规提示白细胞及中性粒细胞未见明显下降。
适合人群:肿瘤科,乳腺外科,放疗科,化疗科
关键词:乳腺癌;放化疗;白细胞减少;升白治疗;一级预防
前言
乳腺癌目前已经成为全球女性发病率最高的恶性肿瘤,严重影响着女性的生命和健康[1]。化疗是乳腺癌主要的全身治疗手段之一,是利用药物杀死肿瘤细胞,抑制肿瘤细胞生长繁殖与促进肿瘤细胞分化的一种治疗方式。但化疗药物会引起许多不良反应,其中骨髓抑制是化疗的限制性不良反应。骨髓抑制常表现为白细胞及中性粒细胞减少[2],制约着化疗剂量强度和化疗周期的实现,影响肿瘤的缓解率与治愈率。当中性粒细胞数<0.5×109/L或<1.0×109/L,但预计在48 h后会下降至0.5×109/L以下及口测温度>38.3℃或≥38.0 ℃持续时间超过1 h称之为发热性中性粒细胞减少症(febrile neutropenia,FN)。这些不良反应的发生,使化疗后肿瘤患者极易发生感染甚至败血症,严重时可导致患者死亡[3]。近年来乳腺癌的化疗方案不断向较高剂量强度以及高剂量密度发展,因此预防化疗导致的中性粒细胞减少症对于保证化疗按期完成、保证疗效、提高患者生活质量具有重要意义。
临床资料
一般资料
患者2022年9月因发现“左乳肿块进行性增大1月余”至解放军东部战区海军医院就诊,查乳腺超声示:左乳外上象限见数个低回声结节,最大约2.6cm×2.0cm,BI-RAD 3级。后患者至宁波市第一人民医院就诊,乳腺钼靶示:左乳外上象限局部致密团块,BI-RAD 4a级。2022年10月10日行“左侧腋窝淋巴结穿刺活检术+左乳肿物微创旋切活检术”。活检病理:(左侧腋下淋巴结):淋巴结内见腺癌组织浸润,伴微乳头结构。(左侧乳腺结节穿刺活检标本):浸润性乳头状癌,WHO Ⅲ级(腺管形成3分,核级3分,核分裂像2分)。免疫组化:浸润性癌表达ER(-),PR(-),Ki67(50%+),Her2(3+)。后患者至我院甲乳外科就诊,排除手术禁忌后,2022年10月19日行左乳癌的改良根治术,术后病理:左乳浸润性癌,部分为浸润性乳头状癌,大小5cm×4cm,脉管内可见癌栓。基底切缘未见癌累及。同侧腋窝淋巴结5/15见癌转移,锁骨下淋巴结0/2未见癌转移。免疫组化:浸润性癌表达ER(-),PR(2%,+),Ki67(60%+),Her2(3+),P120(膜阳性)。
检查
乳腺超声示:左乳外上象限见数个低回声结节,最大约2.6cm×2.0cm,BI-RAD 3级。
乳腺钼靶示:左乳外上象限局部致密团块,BI-RAD 4a级。
行“左侧腋窝淋巴结穿刺活检术+左乳肿物微创旋切活检术”。活检病理:(左侧腋下淋巴结):淋巴结内见腺癌组织浸润,伴微乳头结构。(左侧乳腺结节穿刺活检标本):浸润性乳头状癌,WHO Ⅲ级(腺管形成3分,核级3分,核分裂像2分)。免疫组化:浸润性癌表达ER(-),PR(-),Ki67(50%+),Her2(3+)。
诊断与鉴别诊断
诊断:术后病理:左乳浸润性癌,部分为浸润性乳头状癌,大小5cm×4cm,脉管内可见癌栓。基底切缘未见癌累及。同侧腋窝淋巴结5/15见癌转移,锁骨下淋巴结0/2未见癌转移。免疫组化:浸润性癌表达ER(-),PR(2%,+),Ki67(60%+),Her2(3+),P120(膜阳性)。诊断明确,无需鉴别。
治疗
患者于2022年10月19日在我院甲乳外科完成左侧乳腺癌的改良根治手术。术后,从2022年11月起,患者接受了AC4—T4(吡柔比星+环磷酰胺,多西他赛)的化疗方案,这是一种专门针对乳腺癌的标准化疗方案,分为两个阶段,广泛适用于早期或晚期乳腺癌患者的辅助治疗。AC阶段涉及的药物组合包括吡柔比星(Adriamycin)和环磷酰胺(Cyclophosphamide)。吡柔比星作为蒽环类抗生素,通过插入DNA链并抑制拓扑异构酶活性来阻断癌细胞的分裂与增殖。环磷酰胺,一种烷化剂,通过损害癌细胞DNA,干扰其生长。该阶段通常包括4个治疗周期,每个周期间隔大约21天。T阶段则采用多西他赛(Docetaxel),一种紫杉醇类药物,通过干扰癌细胞微管的正常功能,抑制其分裂与增殖。此阶段也包含4个治疗周期,与AC阶段的治疗间隔相同。2023年6月,患者开始接受乳腺癌术后的辅助放疗。自2023年7月起,患者采用曲妥珠单抗和帕妥珠单抗进行靶向维持治疗,同时常规使用硫培非格司亭6mg进行预防性中性粒细胞减少症(CIN)治疗,以降低由化疗引发的潜在感染风险。
治疗结果、随访及转归
患者未诉特殊不适。2023年11月12日复查CT:乳腺癌治疗术后,未见明显复发转移征象。
治疗前后患者血常规检查结果见图1 。
讨论
乳腺癌是女性最常见的癌症。全世界每年有超过 130 万名癌症患者被诊断出患有癌症[4]。一些全身治疗方式被广泛用作早期乳腺癌的辅助治疗,例如内分泌治疗、化疗和人源化单克隆抗体曲妥珠单抗的抗 HER2 治疗。在内分泌治疗方面,最确定的辅助治疗是他莫昔芬用于绝经前和绝经后妇女。卵巢抑制和/或他莫昔芬是绝经前患者的公认疗法。第三代芳香化酶抑制剂应纳入绝经后妇女的辅助内分泌治疗。由多个周期的多化疗组成的辅助化疗是降低乳腺癌复发风险和提高生存率的重要策略,不仅在风险较高的女性中,而且在淋巴结阴性患者中也是如此。紫杉烷类药物的引入是传统烷基烷类和蒽环类药物治疗方案的重要进步。生物靶向药物曲妥珠单抗已被纳入 HER2 阳性肿瘤的辅助治疗,其治疗持续时间通常为 1 年。乳腺癌的辅助全身治疗是临床肿瘤学中一个快速发展的领域。基于紫杉烷的化疗、芳香化酶抑制剂在绝经后妇女辅助内分泌治疗中的应用,以及曲妥珠单抗作为辅助治疗的可用性,都显著改善了早期乳腺癌的预后[5]。
中性粒细胞减少是决定化疗剂量和疗程安排的关键因素之一。虽然中性粒细胞减少本身可能无明显症状,但它与患者的临床预后紧密相关,可显著提高感染风险和发热性中性粒细胞减少(FN)的发生率,从而影响肿瘤的控制效果和治愈可能性。特别地,严重的中性粒细胞减少甚至可能导致化疗周期的推迟[6]。对于接受蒽环类和紫杉类药物治疗的乳腺癌患者,若不采取支持性治疗措施,几乎所有人都会遭遇重度中性粒细胞减少(中性粒细胞绝对计数<0.5×109/L),且FN的发生率位于23%至34%之间,重度中性粒细胞减少的平均发生时间通常在首个治疗周期的3.8天内[7]。
研究显示,预防性使用硫培非格司亭(PEG-rhG-CSF)能够将FN的发生率显著降低,从20.0%降至1.7%,验证了其在减少FN发生率方面的有效性。在非霍奇金淋巴瘤、乳腺癌等多种恶性肿瘤治疗中,大量临床试验已证实,硫培非格司亭(PEG-rhG-CSF)能有效预防和治疗由化疗和骨髓抑制导致的白细胞及中性粒细胞减少。其作用机制主要包括减轻化疗引起的白细胞减少程度,降低严重白细胞减少和化疗后感染的风险,以及缩短中性粒细胞恢复的时间,因而,预防性使用硫培非格司亭(PEG-rhG-CSF)对于防止中性粒细胞减少至关重要[8-9]。
因此,硫培非格司亭(PEG-rhG-CSF)在预防和治疗乳腺癌化疗引发的骨髓抑制中扮演了核心角色。化疗后24至48小时内预防性地应用硫培非格司亭(PEG-rhG-CSF),可以有效减少白细胞和中性粒细胞计数的减少,缓解骨髓抑制的程度和持续时间,显著降低FN的风险。值得一提的是,硫培非格司亭(PEG-rhG-CSF)对血红蛋白和血小板的影响相对较小。因此,预防性应用硫培非格司亭(PEG-rhG-CSF)不仅有助于患者安全渡过化疗期间的高感染风险阶段,还助于保持化疗的连贯性和提高患者的生活质量。
在处理患者后续治疗中出现的骨髓抑制问题时,我们将继续运用我们丰富的临床经验,采取一系列细致的管理策略。这些策略的目标是保障患者的健康并最大化治疗效果。我们会持续跟踪患者的健康状况,根据他们的具体需求及时调整治疗计划。在适当的情况下,我们可能会重新考虑并实施化疗的常规剂量,以确保获得最理想的治疗效果。
本病例中,47岁女性患者的乳腺癌治疗过程充分体现了个性化医疗和综合治疗策略的重要性。患者经历了手术、化疗、靶向治疗、放射治疗和双靶治疗等一系列规范化治疗,同时在化疗前评估为中危发热性中性粒细胞减少症风险,并采取了预防性应用硫培非格司亭的措施,有效预防了化疗期间的粒细胞缺乏及发热性中性粒细胞减少症(FN)的发生。这一治疗过程不仅遵循了当前的治疗指南,而且通过精细的管理和适时的干预,确保了患者的安全和治疗效果的最大化。这种综合考虑多种因素的治疗策略,为临床医生提供了宝贵的经验和参考,特别是在处理具有相似病理特征的乳腺癌患者时,可以借鉴本病例的治疗思路和方法。同时,这也强调了在乳腺癌治疗中,多学科团队合作的重要性,以及在治疗过程中对患者进行密切监测和及时调整治疗方案的必要性。通过综合管理和个体化治疗,可以更好的提高患者的治疗效果和生活质量。
[1]Youlden D R, Cramb S M, Dunn N A M, et al. The descriptive epidemiology of female breast cancer: an international comparison of screening, incidence, survival and mortality[J]. Cancer epidemiology, 2012, 36(3): 237-248.
[2] Olivera, J, Finn. Cancer immunology[J]. New England Journal of Medicine, 2008.
[3] Vogel, C. L. First and subsequent cycle use of pegfilgrastim prevents febrile neutropenia in patients with breast cancer: a multicenter, double-blind, placebo-controlled phase III study [J]. Journal of Clinical Oncology Official Journal of the American Society of Clinical Oncology, 2005, 23(6):1178.
[4] Ghoncheh, Mahshid et al. “Disparities in Incidence and Mortality of Breast Cancer.” Iranian journal of public health vol. 45,2 (2016): 270-1.
[5] Boér K. A gyógyszeres kezelés szerepe a korai emlôrák kezelésében [Adjuvant chemotherapy of early stage breast cancer]. Orv Hetil. 2010 Feb 28;151(9):344-53. Hungarian. doi: 10.1556/OH.2010.28824. PMID: 20159750.
[6] Ozer H, Armitage J O, Bennett C L, et al. 2000 update of recommendations for the use of hematopoietic colony-stimulating factors: evidence-based, clinical practice guidelines. American Society of Clinical Oncology Growth Factors Expert Panel[J]. Journal of Clinical Oncology, 2000, 18(20):3558-3585.
[7] Giglio A D, Eniu A, Ganea-Motan D, et al. XM02 is superior to placebo and equivalent to Neupogen™ in reducing the duration of severe neutropenia and the incidence of febrile neutropenia in cycle 1 in breast cancer patients receiving docetaxel/doxorubicin chemotherapy[J]. BMC Cancer, 2008, 8(1):332.
[8] Kuderer N M, Dale D C, Crawford J, et al. Impact of primary prophylaxis with granulocyte colony-stimulating factor on febrile neutropenia and mortality in adult cancer patients receiving chemotherapy: a systematic review[J]. Database of Abstracts of Reviews of Effects (DARE): Quality-assessed Reviews [Internet], 2007.
[9]Teofili L, Izzi I, Nuzzolo E R, et al. Chemotherapy-Induced Neutropenia in HIV Positive Patients with Lymphoma: Comparison of Pegfilgrastim with Daily Filgrastim Administration[J]. Mediterranean Journal of Hematology and Infectious Diseases, 2012, 4(1).
排版编辑:肿瘤资讯-momo











 苏公网安备32059002004080号
苏公网安备32059002004080号


